第九单元金属测试题—2021-2022学年九年级化学鲁教版下册(word版 含答案)
文档属性
| 名称 | 第九单元金属测试题—2021-2022学年九年级化学鲁教版下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 129.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-01 00:00:00 | ||
图片预览

文档简介
第九单元金属2021-2022学年九年级化学鲁教版下册测试题
一、单选题
1.下列物质为纯净物的是
A.氯化钠 B.空气 C.不锈钢 D.碘酒
2.下列金属中,金属活动性最弱的是
A.金 B.银 C.铜 D.铁
3.下列观点正确的是( )
A.生铁是混合物,钢是很纯的铁是纯净物
B.“真金不怕火炼”说明金具有熔点高的物理性质
C.常见金属的治炼难易程度和应用的先后顺序与金属活动性顺序无关
D.铜在空气中久置后表面生成铜绿[Cu2(OH)2CO3],说明铜的锈蚀可能与空气中的氧气、水蒸气和二氧化碳有关
4.垃圾分类投放已成为新时尚。某同学清理教室时收集到如下垃圾:
①废纸 ②铝制易拉罐 ③废口罩 ④矿泉水瓶 ⑤废电池,应投入图1所示标志垃圾箱的是
A.①②④
B.①②③④
C.①②③⑤
D.①②③④⑤
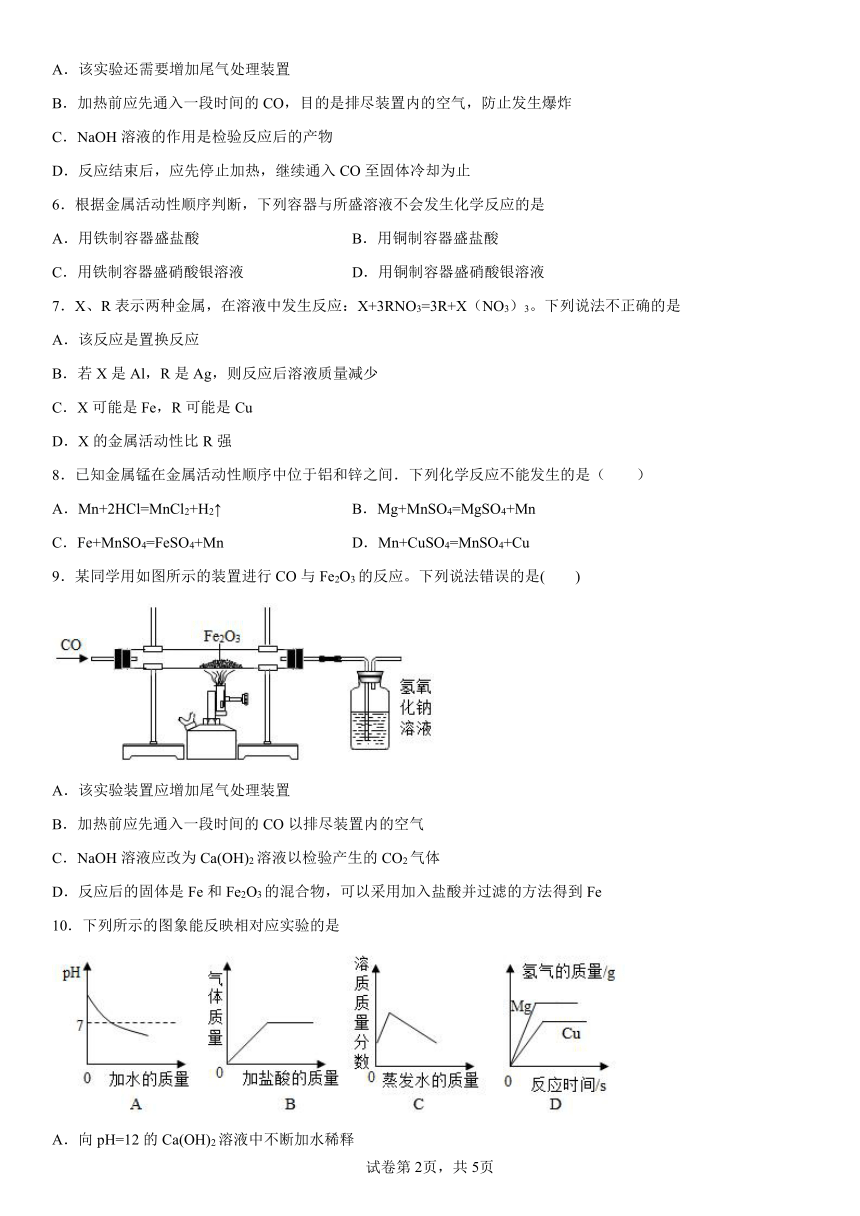
5.钢铁厂会利用焦炭产生的还原性气体来炼铁,某同学用此原理按如图装置进行实验,下列说法不正确的是( )
A.该实验还需要增加尾气处理装置
B.加热前应先通入一段时间的CO,目的是排尽装置内的空气,防止发生爆炸
C.NaOH溶液的作用是检验反应后的产物
D.反应结束后,应先停止加热,继续通入CO至固体冷却为止
6.根据金属活动性顺序判断,下列容器与所盛溶液不会发生化学反应的是
A.用铁制容器盛盐酸 B.用铜制容器盛盐酸
C.用铁制容器盛硝酸银溶液 D.用铜制容器盛硝酸银溶液
7.X、R表示两种金属,在溶液中发生反应:X+3RNO3=3R+X(NO3)3。下列说法不正确的是
A.该反应是置换反应
B.若X是Al,R是Ag,则反应后溶液质量减少
C.X可能是Fe,R可能是Cu
D.X的金属活动性比R强
8.已知金属锰在金属活动性顺序中位于铝和锌之间.下列化学反应不能发生的是( )
A.Mn+2HCl=MnCl2+H2↑ B.Mg+MnSO4=MgSO4+Mn
C.Fe+MnSO4=FeSO4+Mn D.Mn+CuSO4=MnSO4+Cu
9.某同学用如图所示的装置进行CO与Fe2O3的反应。下列说法错误的是( )
A.该实验装置应增加尾气处理装置
B.加热前应先通入一段时间的CO以排尽装置内的空气
C.NaOH溶液应改为Ca(OH)2溶液以检验产生的CO2气体
D.反应后的固体是Fe和Fe2O3的混合物,可以采用加入盐酸并过滤的方法得到Fe
10.下列所示的图象能反映相对应实验的是
A.向pH=12的Ca(OH)2溶液中不断加水稀释
B.向碳酸钙固体中逐滴加入稀盐酸至过量
C.在40℃,将饱和的硝酸钾溶液恒温蒸发水分至有白色晶体析出
D.分别向等质量Mg和Cu中加入足量等质量、等浓度的稀硫酸
二、简答题
11.(1)金属资源面临枯竭,保护金属资源的有效途径之一就是回收再利用,请说出回收废旧金属的好处.(答一点即可)
(2)除回收再利用外,你还知道保护金属资源的有效途径有哪些?(答两点即可)
12.现有①赤铁矿(主要成分是Fe2O3)②磁铁矿(主要成分是Fe3O4)③黄铁矿(主要成分是FeS2),请你从经济效益和环境保护的角度分析三种矿石哪种不适合用来炼铁?为什么?
13.请你判断,下列家庭小实验“能”或“不能”达到预期目的,并说明其理由。
(1)“品尝”:鉴别厨房中的白糖和食盐________________。
(2)“加食醋”:鉴别苏打和食盐___________________________。
(3)“观察”:鉴别黄铜和黄金___________________________。
三、推断题
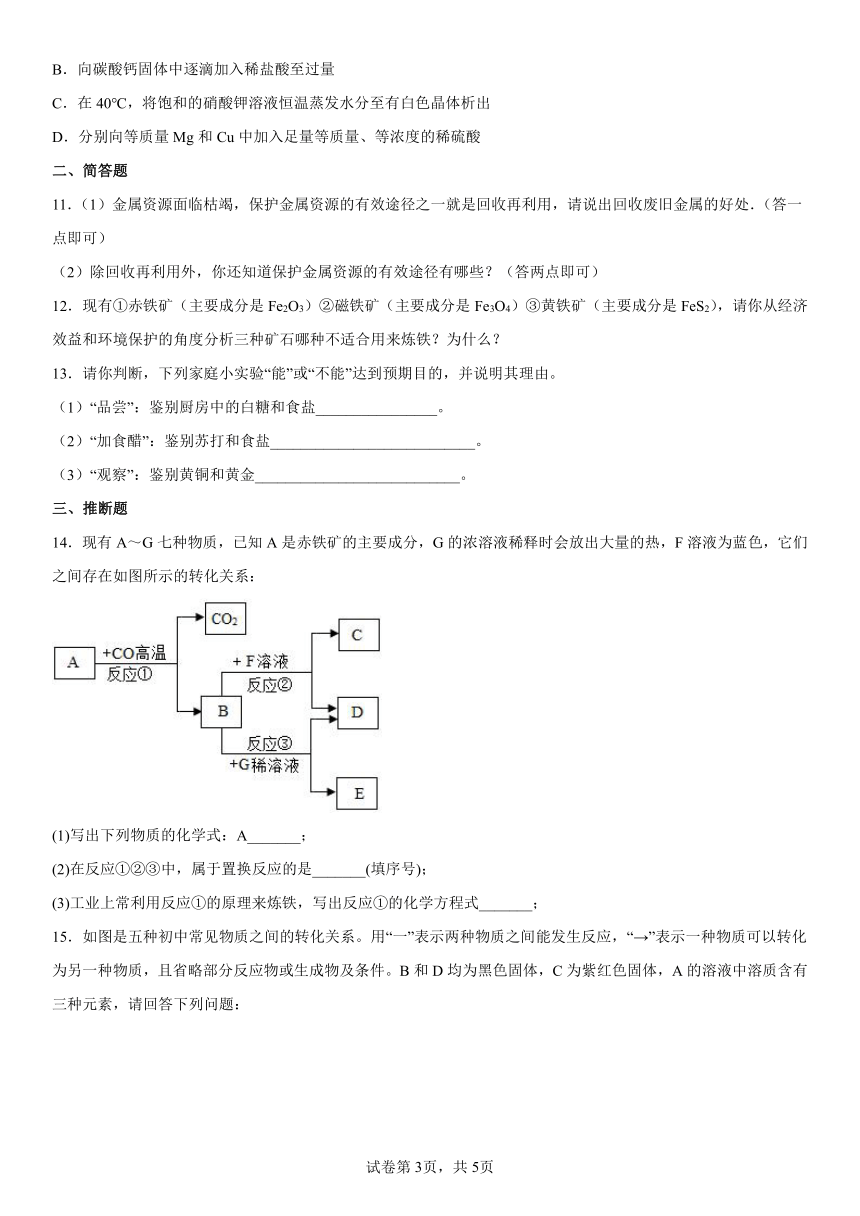
14.现有A~G七种物质,已知A是赤铁矿的主要成分,G的浓溶液稀释时会放出大量的热,F溶液为蓝色,它们之间存在如图所示的转化关系:
(1)写出下列物质的化学式:A_______;
(2)在反应①②③中,属于置换反应的是_______(填序号);
(3)工业上常利用反应①的原理来炼铁,写出反应①的化学方程式_______;
15.如图是五种初中常见物质之间的转化关系。用“一”表示两种物质之间能发生反应,“→”表示一种物质可以转化为另一种物质,且省略部分反应物或生成物及条件。B和D均为黑色固体,C为紫红色固体,A的溶液中溶质含有三种元素,请回答下列问题:
(1)请写出C和E两种物质的化学式C_____、E_____;
(2)请写出D转化C的化学方程式_____;
(3)请写出B与足量A反应的实验现象_____。
四、实验题
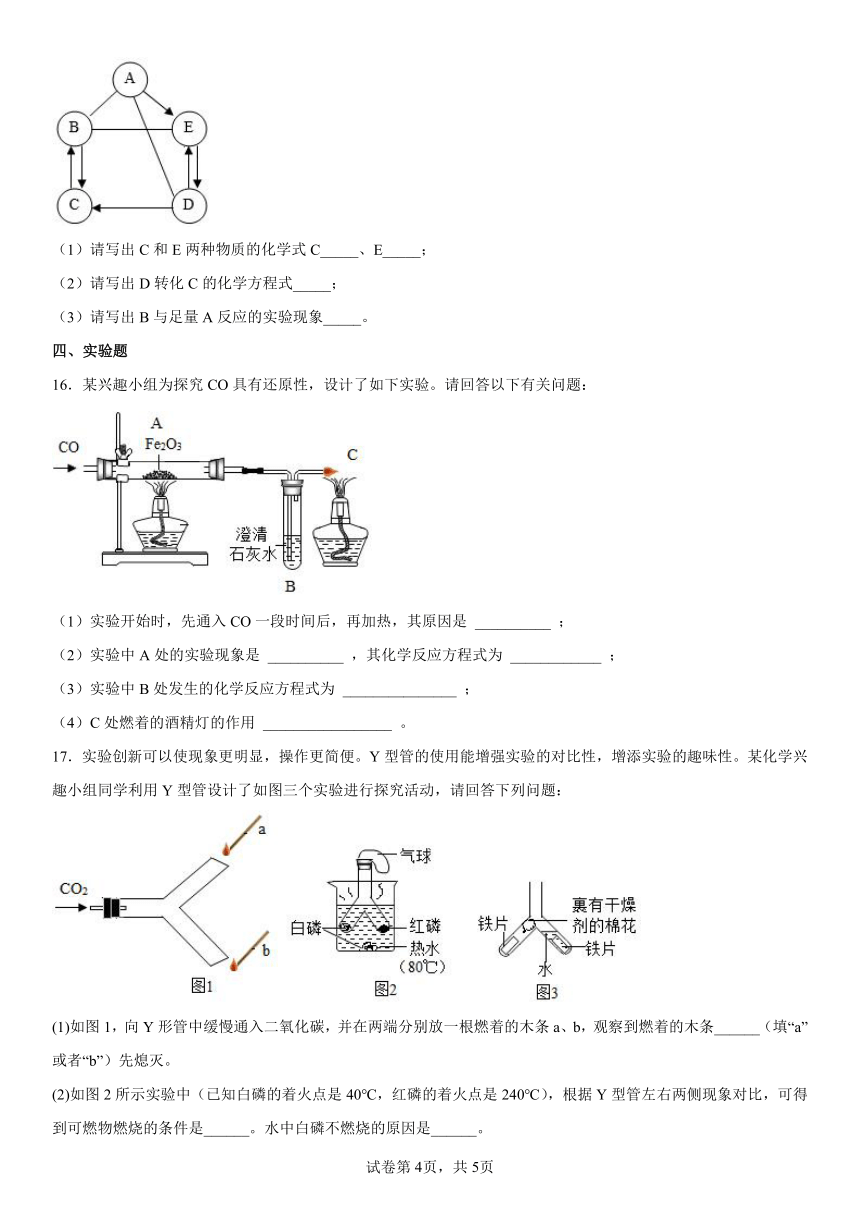
16.某兴趣小组为探究CO具有还原性,设计了如下实验。请回答以下有关问题:
(1)实验开始时,先通入CO一段时间后,再加热,其原因是 __________ ;
(2)实验中A处的实验现象是 __________ ,其化学反应方程式为 ____________ ;
(3)实验中B处发生的化学反应方程式为 _______________ ;
(4)C处燃着的酒精灯的作用 _________________ 。
17.实验创新可以使现象更明显,操作更简便。Y型管的使用能增强实验的对比性,增添实验的趣味性。某化学兴趣小组同学利用Y型管设计了如图三个实验进行探究活动,请回答下列问题:
(1)如图1,向Y形管中缓慢通入二氧化碳,并在两端分别放一根燃着的木条a、b,观察到燃着的木条______(填“a”或者“b”)先熄灭。
(2)如图2所示实验中(已知白磷的着火点是40℃,红磷的着火点是240℃),根据Y型管左右两侧现象对比,可得到可燃物燃烧的条件是______。水中白磷不燃烧的原因是______。
(3)如图3所示实验中,一段时间后,Y形管______(填“左”或“右”)侧铁片生锈,由此可得出结论:______是铁生锈的必要条件。
18.氢气是一种还原性气体。
①装置A 开始反应,锌粒表面的现象为______,该反应的化学方程式为______。充分反应后,可以观察到氧化铜表面的现象为______,说明氢气具有还原性,该反应的化学方程式为______。
②装置 B 的实验操作顺序如下:
I.制氧化铜:打开低压加热器,加热铜丝,发现铜丝表面变黑后停止加热,此时铜丝表面反应的化学方程式为______。
II.制氢气:必须待铜丝冷却至室温,才能倾斜装置使稀硫酸流入锌粒,开始反应,理由是______。
III.反应:应先对产生的气体进行______操作后,再打开低压加热器,加热铜丝,直至铜丝表面黑色物质消失后停止加热,取出铜丝,停止反应。
③请选择一套合适的装置______,并从实验装置和药品的角度阐述你的理由______。
五、计算题
19.黄铜的主要成分是铜锌合金,将10g黄铜与足量稀硫酸反应,生成0.1g氢气,求该黄铜中铜的质量分数。
20.锌和稀硫酸反应生成硫酸锌和氢气。实验室常用此反应来制取氢气,小敏想制取8克氢气,请你帮她算算最少需要消耗多少克的金属锌?
21.工业上用600t含氧化铁80%的赤铁矿石冶炼生铁。
(1)600t赤铁矿石中氧化铁的质量为___________t。
(2)上述赤铁矿石理论上冶炼出含铁96%的生铁多少吨?(请根据化学方程式计算,写出计算过程)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.A
3.D
4.A
5.C
6.B
7.C
8.C
9.D
10.B
11.(1)节约金属资源; (2)防止金属锈蚀;有计划、合理开采金属矿物。
12.FeS2;因为FeS2的含铁量少,而且在冶炼的过程中,会产生二氧化硫而污染空气
13. 能,白糖有甜味,食盐有咸味 能,食醋中的醋酸与苏打中的碳酸钠能反应有气泡冒出,醋酸与食盐中的氯化钠不反应,没有气泡冒出; 不能,黄铜和黄金都呈黄色。
14. Fe2O3 ②③
15. Cu H2 Fe+CuSO4=Cu+FeSO4(合理即可) 黑色固体逐渐减少至消失,溶液有无色变为蓝色。
16. 排出装置中的空气,防止爆炸(意思正确可给分) 红色固体变黑色 Ca(OH)2+CO2=CaCO3↓+H2O 防止污染空气
17.(1)b
(2) 温度达可燃物着火点 未与氧气接触
(3) 右 水 H2O
18. 产生大量气泡 由黑色变成红色 防止氢气与装置中的空气混合加热发生爆炸 验纯 B 装置简单,操作方便,药品用量少
19.解:锌的质量为x
答:黄铜中铜的质量分数为67.5%。
20.最少需要消耗金属锌质量为260g。
21.(1)480
(2)解:设:上述赤铁矿石理论上冶炼出含铁96%的生铁质量为x。
x=350t
答:上述赤铁矿石理论上冶炼出含铁96%的生铁质量为350t。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列物质为纯净物的是
A.氯化钠 B.空气 C.不锈钢 D.碘酒
2.下列金属中,金属活动性最弱的是
A.金 B.银 C.铜 D.铁
3.下列观点正确的是( )
A.生铁是混合物,钢是很纯的铁是纯净物
B.“真金不怕火炼”说明金具有熔点高的物理性质
C.常见金属的治炼难易程度和应用的先后顺序与金属活动性顺序无关
D.铜在空气中久置后表面生成铜绿[Cu2(OH)2CO3],说明铜的锈蚀可能与空气中的氧气、水蒸气和二氧化碳有关
4.垃圾分类投放已成为新时尚。某同学清理教室时收集到如下垃圾:
①废纸 ②铝制易拉罐 ③废口罩 ④矿泉水瓶 ⑤废电池,应投入图1所示标志垃圾箱的是
A.①②④
B.①②③④
C.①②③⑤
D.①②③④⑤
5.钢铁厂会利用焦炭产生的还原性气体来炼铁,某同学用此原理按如图装置进行实验,下列说法不正确的是( )
A.该实验还需要增加尾气处理装置
B.加热前应先通入一段时间的CO,目的是排尽装置内的空气,防止发生爆炸
C.NaOH溶液的作用是检验反应后的产物
D.反应结束后,应先停止加热,继续通入CO至固体冷却为止
6.根据金属活动性顺序判断,下列容器与所盛溶液不会发生化学反应的是
A.用铁制容器盛盐酸 B.用铜制容器盛盐酸
C.用铁制容器盛硝酸银溶液 D.用铜制容器盛硝酸银溶液
7.X、R表示两种金属,在溶液中发生反应:X+3RNO3=3R+X(NO3)3。下列说法不正确的是
A.该反应是置换反应
B.若X是Al,R是Ag,则反应后溶液质量减少
C.X可能是Fe,R可能是Cu
D.X的金属活动性比R强
8.已知金属锰在金属活动性顺序中位于铝和锌之间.下列化学反应不能发生的是( )
A.Mn+2HCl=MnCl2+H2↑ B.Mg+MnSO4=MgSO4+Mn
C.Fe+MnSO4=FeSO4+Mn D.Mn+CuSO4=MnSO4+Cu
9.某同学用如图所示的装置进行CO与Fe2O3的反应。下列说法错误的是( )
A.该实验装置应增加尾气处理装置
B.加热前应先通入一段时间的CO以排尽装置内的空气
C.NaOH溶液应改为Ca(OH)2溶液以检验产生的CO2气体
D.反应后的固体是Fe和Fe2O3的混合物,可以采用加入盐酸并过滤的方法得到Fe
10.下列所示的图象能反映相对应实验的是
A.向pH=12的Ca(OH)2溶液中不断加水稀释
B.向碳酸钙固体中逐滴加入稀盐酸至过量
C.在40℃,将饱和的硝酸钾溶液恒温蒸发水分至有白色晶体析出
D.分别向等质量Mg和Cu中加入足量等质量、等浓度的稀硫酸
二、简答题
11.(1)金属资源面临枯竭,保护金属资源的有效途径之一就是回收再利用,请说出回收废旧金属的好处.(答一点即可)
(2)除回收再利用外,你还知道保护金属资源的有效途径有哪些?(答两点即可)
12.现有①赤铁矿(主要成分是Fe2O3)②磁铁矿(主要成分是Fe3O4)③黄铁矿(主要成分是FeS2),请你从经济效益和环境保护的角度分析三种矿石哪种不适合用来炼铁?为什么?
13.请你判断,下列家庭小实验“能”或“不能”达到预期目的,并说明其理由。
(1)“品尝”:鉴别厨房中的白糖和食盐________________。
(2)“加食醋”:鉴别苏打和食盐___________________________。
(3)“观察”:鉴别黄铜和黄金___________________________。
三、推断题
14.现有A~G七种物质,已知A是赤铁矿的主要成分,G的浓溶液稀释时会放出大量的热,F溶液为蓝色,它们之间存在如图所示的转化关系:
(1)写出下列物质的化学式:A_______;
(2)在反应①②③中,属于置换反应的是_______(填序号);
(3)工业上常利用反应①的原理来炼铁,写出反应①的化学方程式_______;
15.如图是五种初中常见物质之间的转化关系。用“一”表示两种物质之间能发生反应,“→”表示一种物质可以转化为另一种物质,且省略部分反应物或生成物及条件。B和D均为黑色固体,C为紫红色固体,A的溶液中溶质含有三种元素,请回答下列问题:
(1)请写出C和E两种物质的化学式C_____、E_____;
(2)请写出D转化C的化学方程式_____;
(3)请写出B与足量A反应的实验现象_____。
四、实验题
16.某兴趣小组为探究CO具有还原性,设计了如下实验。请回答以下有关问题:
(1)实验开始时,先通入CO一段时间后,再加热,其原因是 __________ ;
(2)实验中A处的实验现象是 __________ ,其化学反应方程式为 ____________ ;
(3)实验中B处发生的化学反应方程式为 _______________ ;
(4)C处燃着的酒精灯的作用 _________________ 。
17.实验创新可以使现象更明显,操作更简便。Y型管的使用能增强实验的对比性,增添实验的趣味性。某化学兴趣小组同学利用Y型管设计了如图三个实验进行探究活动,请回答下列问题:
(1)如图1,向Y形管中缓慢通入二氧化碳,并在两端分别放一根燃着的木条a、b,观察到燃着的木条______(填“a”或者“b”)先熄灭。
(2)如图2所示实验中(已知白磷的着火点是40℃,红磷的着火点是240℃),根据Y型管左右两侧现象对比,可得到可燃物燃烧的条件是______。水中白磷不燃烧的原因是______。
(3)如图3所示实验中,一段时间后,Y形管______(填“左”或“右”)侧铁片生锈,由此可得出结论:______是铁生锈的必要条件。
18.氢气是一种还原性气体。
①装置A 开始反应,锌粒表面的现象为______,该反应的化学方程式为______。充分反应后,可以观察到氧化铜表面的现象为______,说明氢气具有还原性,该反应的化学方程式为______。
②装置 B 的实验操作顺序如下:
I.制氧化铜:打开低压加热器,加热铜丝,发现铜丝表面变黑后停止加热,此时铜丝表面反应的化学方程式为______。
II.制氢气:必须待铜丝冷却至室温,才能倾斜装置使稀硫酸流入锌粒,开始反应,理由是______。
III.反应:应先对产生的气体进行______操作后,再打开低压加热器,加热铜丝,直至铜丝表面黑色物质消失后停止加热,取出铜丝,停止反应。
③请选择一套合适的装置______,并从实验装置和药品的角度阐述你的理由______。
五、计算题
19.黄铜的主要成分是铜锌合金,将10g黄铜与足量稀硫酸反应,生成0.1g氢气,求该黄铜中铜的质量分数。
20.锌和稀硫酸反应生成硫酸锌和氢气。实验室常用此反应来制取氢气,小敏想制取8克氢气,请你帮她算算最少需要消耗多少克的金属锌?
21.工业上用600t含氧化铁80%的赤铁矿石冶炼生铁。
(1)600t赤铁矿石中氧化铁的质量为___________t。
(2)上述赤铁矿石理论上冶炼出含铁96%的生铁多少吨?(请根据化学方程式计算,写出计算过程)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.A
3.D
4.A
5.C
6.B
7.C
8.C
9.D
10.B
11.(1)节约金属资源; (2)防止金属锈蚀;有计划、合理开采金属矿物。
12.FeS2;因为FeS2的含铁量少,而且在冶炼的过程中,会产生二氧化硫而污染空气
13. 能,白糖有甜味,食盐有咸味 能,食醋中的醋酸与苏打中的碳酸钠能反应有气泡冒出,醋酸与食盐中的氯化钠不反应,没有气泡冒出; 不能,黄铜和黄金都呈黄色。
14. Fe2O3 ②③
15. Cu H2 Fe+CuSO4=Cu+FeSO4(合理即可) 黑色固体逐渐减少至消失,溶液有无色变为蓝色。
16. 排出装置中的空气,防止爆炸(意思正确可给分) 红色固体变黑色 Ca(OH)2+CO2=CaCO3↓+H2O 防止污染空气
17.(1)b
(2) 温度达可燃物着火点 未与氧气接触
(3) 右 水 H2O
18. 产生大量气泡 由黑色变成红色 防止氢气与装置中的空气混合加热发生爆炸 验纯 B 装置简单,操作方便,药品用量少
19.解:锌的质量为x
答:黄铜中铜的质量分数为67.5%。
20.最少需要消耗金属锌质量为260g。
21.(1)480
(2)解:设:上述赤铁矿石理论上冶炼出含铁96%的生铁质量为x。
x=350t
答:上述赤铁矿石理论上冶炼出含铁96%的生铁质量为350t。
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
