第九单元金属综合训练---2021-2022学年九年级化学鲁教版下册(word版 含答案)
文档属性
| 名称 | 第九单元金属综合训练---2021-2022学年九年级化学鲁教版下册(word版 含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 175.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-01 08:51:10 | ||
图片预览


文档简介
第九单元金属2021-2022学年九年级化学鲁教版下册综合训练
一、单选题
1.下列物质的用途中,利用其化学性质的是( )
A.赤铁矿用于炼铁 B.氦气用于飞艇
C.干冰用作制冷剂 D.铜用于制作导线
2.下列物质不属于合金的是
A.生铁 B.青铜 C.钢 D.铝
3.世界每年因锈蚀而损失的金属数量巨大,防止金属锈蚀以成为科学研究中的重大问题。下列有关金属锈蚀与保护措施中不正确的是
A.铁锈蚀的实质是铁与空气中的氧气、水蒸气等发生了化学变化
B.同样的铁制品在海南比在兰州更易锈蚀
C.在铁表面刷油漆可以防止铁锈蚀
D.铝的抗锈蚀性能比铁强,生活中可用钢丝球洗刷铝锅
4.有X、Y、Z三种金属片,分别放入稀硫酸中,X、Z表面有气泡产生,Y没有明显现象,X放入ZCln溶液,没有明显现象。判断这三种金属的活动性由强到弱的顺序是
A.X>Y>Z B.Z>X>Y C.X>Z>Y D.Y>X>Z
5.锰和镍(Ni)都是重要的金属,将镍丝插入MnSO4溶液中,无明显现象,插入CuSO4溶液中,镍丝表面有红色固体析出。则Mn、Ni、Cu三种金属的活动性由强到弱的顺序是( )
A.Mn、Ni、Cu B.Mn、Cu、Ni
C.Ni、Mn、Cu D.Cu、Mn 、Ni
6.在一密闭容器中加入a、b、c、d四种物质,测得反应前后各物质的质量如下表。
物质 a b c d
反应前质量/g 5.6 10 0 20
反应后质量/g 0 16.4 15.2 x
下列说法正确的是A.x等于36
B.b可能是单质
C.该反应一定为置换反应
D.a与b的相对分子质量之比为7:8
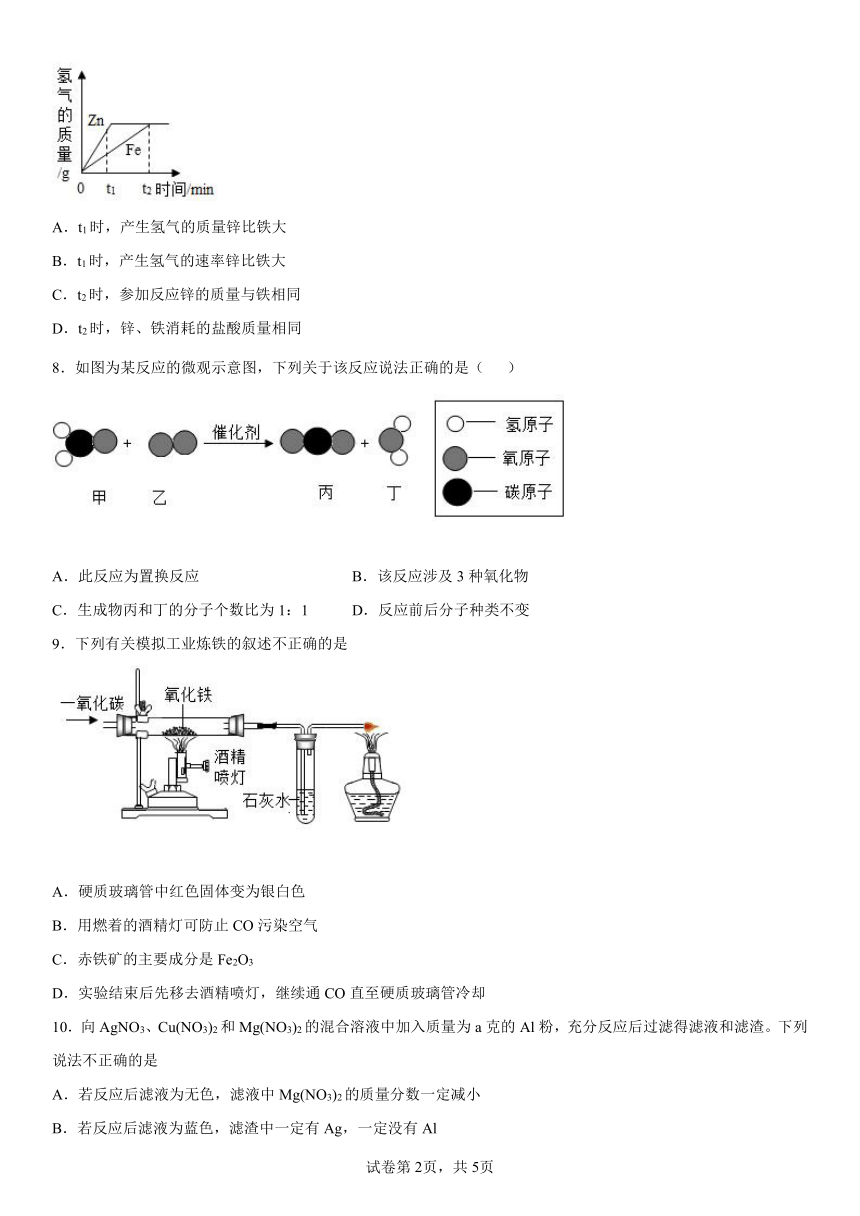
7.一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,下列说法不正确的是
A.t1时,产生氢气的质量锌比铁大
B.t1时,产生氢气的速率锌比铁大
C.t2时,参加反应锌的质量与铁相同
D.t2时,锌、铁消耗的盐酸质量相同
8.如图为某反应的微观示意图,下列关于该反应说法正确的是( )
A.此反应为置换反应 B.该反应涉及3种氧化物
C.生成物丙和丁的分子个数比为1:1 D.反应前后分子种类不变
9.下列有关模拟工业炼铁的叙述不正确的是
A.硬质玻璃管中红色固体变为银白色
B.用燃着的酒精灯可防止CO污染空气
C.赤铁矿的主要成分是Fe2O3
D.实验结束后先移去酒精喷灯,继续通CO直至硬质玻璃管冷却
10.向AgNO3、Cu(NO3)2和Mg(NO3)2的混合溶液中加入质量为a克的Al粉,充分反应后过滤得滤液和滤渣。下列说法不正确的是
A.若反应后滤液为无色,滤液中Mg(NO3)2的质量分数一定减小
B.若反应后滤液为蓝色,滤渣中一定有Ag,一定没有Al
C.若向滤渣中加盐酸无气泡,则滤渣质量一定大于3a克
D.若反应后滤液为无色,则滤液中一定有Mg(NO3)2、Al(NO3)3
二、简答题
11.2018年10月,江西省第十五届省运会火炬传递活动在景德镇举行,陶瓷火炬赢尽喝彩。
(1)火炬的主要材料为陶瓷,下列陶瓷制作工艺中发生化学变化的是_______。
A 混合 B 成型
C 晾干 D 烧结
(2)火炬的灭火方法为用灭火盖盖灭,它的灭火原理为__________________________。
(3)体育场的建设中采用了大量的金属材料,为防止钢铁制品锈蚀,采取的方法有________________(任写一种)。
(4)2018年世界环境日主题是“塑战速决”,塑料制品的使用方便了人类的生活,但大量废弃塑料带来的____________异常严重,作为一名中学生,要有意识的减少塑料制品的使用,保持赛场的清洁。
(5)为了保证运动员能够发挥出应有的水平,食堂阿姨们将榨好的蔬菜汁放到面粉中,做成口味独特、营养丰富的蔬菜馒头,这种馒头提供的营养素主要有______________(任写一种)。
12.归纳与比较,是学习化学的重要方法之一,对比CO和CO2 , 它们的组成元素 ________(填“相同”或“不同”,下同),但它们的化学性质 ________:工业上CO可用来炼铁,请写出反应的化学方程式 ________,废气不能随意排放,处理方法是 ________
13.有①Cu﹣Zn ②Cu﹣Ag 两种貌似黄金的合金,它们都有其特殊的用途,但一些骗子常用它们做成饰品冒充真黄金欺骗消费者.对此,化学科学有责任加以揭露.
(1)现有上述两种合金制成的假黄金饰品各一件,小明同学只用稀盐酸和必要的实验仪器就鉴别出其中一种饰品是假黄金,它是合金 (填写代号);若要证明另一种饰品也是假黄金,可选用一种盐溶液来验证,这种盐可以是 (写一种盐的名称或化学式);
(2)取与上述用稀盐酸鉴别出的同种合金10g,放入烧杯中,再向其中加入93.7g某稀盐酸恰好完全反应后,测得烧杯内剩余物质的质量共为103.5g.
①上述过程中变化的质量10g,+93.7g﹣103.5g=0.2g是 (填物质的名称或化学式)的质量;
②10g,该合金中铜的质量是多少?已知反应后的溶液中溶质全部溶解,求该溶液中溶质的质量分数是多少?
三、推断题
14.已知A、B为两种黑色粉末,D为红色单质。A、B、C、D、E五种物质之间的转化关系如下图所示。
请回答下列问题:
(1)E的化学式为_______;
(2)D的一种用途______;
(3)反应①的化学方程式为_______。
15.已知A、B、C、D、E分别是稀盐酸、氢氧化钠溶液、硫酸铜溶液、氧化铁和一氧化碳中的一种,E是实验室一种常见溶液,它们之间的关系如图所示,“─”两端的物质在一定条件下可以反应.请回答:
(1)C的一种用途是 ______ ;D、E反应的化学方程式为 ______ .
(2)上述各物质间的反应均可用“甲+乙→丙+丁”表示,其中不属于四种基本反应类型,但能用上式表示的一个化学方程式是 ______ .
(3)若B、C、D、E都不变,五种物质之间的关系也不变,A还可能是 ______ .
四、实验题
16.根据图回答问题:
(1)由实验1得到的结论是 ______________________________ 。为确保实验成功,操作时需注意的问题是 ________________________________________________ 。
(2)实验2的目的是 _________________________________ 。
(3)实验3中发生反应的化学方程式为 ____________________________ ,当观察到溶液由红色变为无色后,小明想知道反应后溶液中除NaCl外,是否还含有其它溶质(不考虑酚酞),于是他向反应后的溶液中加入一种试剂,从而得出了结论。小明加入的试剂可能是 _____________________ 。
17.金属冶炼历史悠久。
(1)火法炼铜—Cu2S在高温下与氧气反应的部分转化关系如下图:
①从环境保护的角度分析,火法炼铜的弊端______;
②《天工开物》中记载:“凡红铜(纯铜)升黄(黄铜)而后熔化造器”由此可知,黄铜的熔点比纯铜______(填“高”或“低”)。
(2)《浸铜要略序》中记载:“山麓有胆泉(硫酸铜),土人汲以浸铁,锻炼成铜”,反应的化学方程式为______。
(3)现行的铝冶炼方法是1886年美国的霍耳和法国的埃鲁发明的冰晶石—氧化铝熔盐电解法,其原理是氧化铝在通电条件下分解,反应的化学方程式为______。
18.金属材料广泛应用于生产生活中。
(1)生铁和______是两种常见的铁合金。用赤铁矿(主要成分是Fe2O3)冶炼铁的化学方程式为______。铁制品锈蚀,是铁与空气中的______发生了化学反应:防止铁锅锈蚀的一种方法是______。
(2)铝的抗腐蚀性很强,是因为铝在空气中能生成一层______,该反应的化学方程式为______。
五、计算题
19.锌与盐酸(HCl)反应生成氢气和氯化锌,实验室里用3.25g锌与足量的盐酸反应,可制得多少g氢气?
20.学校课外活动小组为了测定某钢铁厂生铁样品中铁的质量分数,在实验室称取生铁样品5.8g放入烧杯中(烧杯的质量为30g).然后再加入50g稀硫酸,使之充分反应后,称量,烧杯及烧杯中物质的总质量为85.6g(已知该反应中稀硫酸恰好完全反应,杂质不参与反应).请计算:
(1)产生氢气的质量是_____.
(2)该生铁样品中铁的质量分数?_____(精确到0.1%)
21.金属锰大量用于制造锰钢。地壳中含锰的矿石有软锰矿,软锰矿的主要成分是二氧化锰。金属锰可用软锰矿跟铝反应来制取,其反应为3MnO2+4Al2Al2O3+3Mn。
(1)用100t含MnO278.3%的软锰矿石,可冶炼出多少t锰(准确至0.1t,下同)。
(2)实际冶炼出的锰是含有5%杂质的粗锰,则实际得到多少t粗锰。
试卷第1页,共3页
试卷第2页,共2页
参考答案:
1.A
2.D
3.D
4.B
5.A
6.B
7.C
8.C
9.A
10.A
11. D 使可燃物与氧气隔绝 刷漆(合理即可) 白色污染 糖类(或维生素)
12. 相同; 不同; 3CO+Fe2O3 3Fe+3CO2; 回收利用或点燃
13.(1)①;硝酸银 (2)①氢气 ②3.6%
14.(1)CaCO3
(2)导线等
(3)
15. 除铁锈
C或H2
16. 二氧化碳不燃烧也不支持燃烧,密度比空气大 沿蜡烛对面一侧烧杯内壁缓缓倾倒二氧化碳 探究反应物的状态对反应速率的影响 紫色石蕊溶液(或锌等活泼金属或碳酸钠溶液等)
17.(1) 产生SO2造成大气污染(合理答案均可) 低
(2)
(3)
18.(1) 钢 水和氧气 洗完后保持铁锅干燥(合理即可)
(2) 致密氧化铝薄膜
19.解:设生成氢气质量为x
答:生成氢气质量为0.1g。
20. 0.2g 96.6%
21.(1)49.5t;(2)52.1t
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列物质的用途中,利用其化学性质的是( )
A.赤铁矿用于炼铁 B.氦气用于飞艇
C.干冰用作制冷剂 D.铜用于制作导线
2.下列物质不属于合金的是
A.生铁 B.青铜 C.钢 D.铝
3.世界每年因锈蚀而损失的金属数量巨大,防止金属锈蚀以成为科学研究中的重大问题。下列有关金属锈蚀与保护措施中不正确的是
A.铁锈蚀的实质是铁与空气中的氧气、水蒸气等发生了化学变化
B.同样的铁制品在海南比在兰州更易锈蚀
C.在铁表面刷油漆可以防止铁锈蚀
D.铝的抗锈蚀性能比铁强,生活中可用钢丝球洗刷铝锅
4.有X、Y、Z三种金属片,分别放入稀硫酸中,X、Z表面有气泡产生,Y没有明显现象,X放入ZCln溶液,没有明显现象。判断这三种金属的活动性由强到弱的顺序是
A.X>Y>Z B.Z>X>Y C.X>Z>Y D.Y>X>Z
5.锰和镍(Ni)都是重要的金属,将镍丝插入MnSO4溶液中,无明显现象,插入CuSO4溶液中,镍丝表面有红色固体析出。则Mn、Ni、Cu三种金属的活动性由强到弱的顺序是( )
A.Mn、Ni、Cu B.Mn、Cu、Ni
C.Ni、Mn、Cu D.Cu、Mn 、Ni
6.在一密闭容器中加入a、b、c、d四种物质,测得反应前后各物质的质量如下表。
物质 a b c d
反应前质量/g 5.6 10 0 20
反应后质量/g 0 16.4 15.2 x
下列说法正确的是A.x等于36
B.b可能是单质
C.该反应一定为置换反应
D.a与b的相对分子质量之比为7:8
7.一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,下列说法不正确的是
A.t1时,产生氢气的质量锌比铁大
B.t1时,产生氢气的速率锌比铁大
C.t2时,参加反应锌的质量与铁相同
D.t2时,锌、铁消耗的盐酸质量相同
8.如图为某反应的微观示意图,下列关于该反应说法正确的是( )
A.此反应为置换反应 B.该反应涉及3种氧化物
C.生成物丙和丁的分子个数比为1:1 D.反应前后分子种类不变
9.下列有关模拟工业炼铁的叙述不正确的是
A.硬质玻璃管中红色固体变为银白色
B.用燃着的酒精灯可防止CO污染空气
C.赤铁矿的主要成分是Fe2O3
D.实验结束后先移去酒精喷灯,继续通CO直至硬质玻璃管冷却
10.向AgNO3、Cu(NO3)2和Mg(NO3)2的混合溶液中加入质量为a克的Al粉,充分反应后过滤得滤液和滤渣。下列说法不正确的是
A.若反应后滤液为无色,滤液中Mg(NO3)2的质量分数一定减小
B.若反应后滤液为蓝色,滤渣中一定有Ag,一定没有Al
C.若向滤渣中加盐酸无气泡,则滤渣质量一定大于3a克
D.若反应后滤液为无色,则滤液中一定有Mg(NO3)2、Al(NO3)3
二、简答题
11.2018年10月,江西省第十五届省运会火炬传递活动在景德镇举行,陶瓷火炬赢尽喝彩。
(1)火炬的主要材料为陶瓷,下列陶瓷制作工艺中发生化学变化的是_______。
A 混合 B 成型
C 晾干 D 烧结
(2)火炬的灭火方法为用灭火盖盖灭,它的灭火原理为__________________________。
(3)体育场的建设中采用了大量的金属材料,为防止钢铁制品锈蚀,采取的方法有________________(任写一种)。
(4)2018年世界环境日主题是“塑战速决”,塑料制品的使用方便了人类的生活,但大量废弃塑料带来的____________异常严重,作为一名中学生,要有意识的减少塑料制品的使用,保持赛场的清洁。
(5)为了保证运动员能够发挥出应有的水平,食堂阿姨们将榨好的蔬菜汁放到面粉中,做成口味独特、营养丰富的蔬菜馒头,这种馒头提供的营养素主要有______________(任写一种)。
12.归纳与比较,是学习化学的重要方法之一,对比CO和CO2 , 它们的组成元素 ________(填“相同”或“不同”,下同),但它们的化学性质 ________:工业上CO可用来炼铁,请写出反应的化学方程式 ________,废气不能随意排放,处理方法是 ________
13.有①Cu﹣Zn ②Cu﹣Ag 两种貌似黄金的合金,它们都有其特殊的用途,但一些骗子常用它们做成饰品冒充真黄金欺骗消费者.对此,化学科学有责任加以揭露.
(1)现有上述两种合金制成的假黄金饰品各一件,小明同学只用稀盐酸和必要的实验仪器就鉴别出其中一种饰品是假黄金,它是合金 (填写代号);若要证明另一种饰品也是假黄金,可选用一种盐溶液来验证,这种盐可以是 (写一种盐的名称或化学式);
(2)取与上述用稀盐酸鉴别出的同种合金10g,放入烧杯中,再向其中加入93.7g某稀盐酸恰好完全反应后,测得烧杯内剩余物质的质量共为103.5g.
①上述过程中变化的质量10g,+93.7g﹣103.5g=0.2g是 (填物质的名称或化学式)的质量;
②10g,该合金中铜的质量是多少?已知反应后的溶液中溶质全部溶解,求该溶液中溶质的质量分数是多少?
三、推断题
14.已知A、B为两种黑色粉末,D为红色单质。A、B、C、D、E五种物质之间的转化关系如下图所示。
请回答下列问题:
(1)E的化学式为_______;
(2)D的一种用途______;
(3)反应①的化学方程式为_______。
15.已知A、B、C、D、E分别是稀盐酸、氢氧化钠溶液、硫酸铜溶液、氧化铁和一氧化碳中的一种,E是实验室一种常见溶液,它们之间的关系如图所示,“─”两端的物质在一定条件下可以反应.请回答:
(1)C的一种用途是 ______ ;D、E反应的化学方程式为 ______ .
(2)上述各物质间的反应均可用“甲+乙→丙+丁”表示,其中不属于四种基本反应类型,但能用上式表示的一个化学方程式是 ______ .
(3)若B、C、D、E都不变,五种物质之间的关系也不变,A还可能是 ______ .
四、实验题
16.根据图回答问题:
(1)由实验1得到的结论是 ______________________________ 。为确保实验成功,操作时需注意的问题是 ________________________________________________ 。
(2)实验2的目的是 _________________________________ 。
(3)实验3中发生反应的化学方程式为 ____________________________ ,当观察到溶液由红色变为无色后,小明想知道反应后溶液中除NaCl外,是否还含有其它溶质(不考虑酚酞),于是他向反应后的溶液中加入一种试剂,从而得出了结论。小明加入的试剂可能是 _____________________ 。
17.金属冶炼历史悠久。
(1)火法炼铜—Cu2S在高温下与氧气反应的部分转化关系如下图:
①从环境保护的角度分析,火法炼铜的弊端______;
②《天工开物》中记载:“凡红铜(纯铜)升黄(黄铜)而后熔化造器”由此可知,黄铜的熔点比纯铜______(填“高”或“低”)。
(2)《浸铜要略序》中记载:“山麓有胆泉(硫酸铜),土人汲以浸铁,锻炼成铜”,反应的化学方程式为______。
(3)现行的铝冶炼方法是1886年美国的霍耳和法国的埃鲁发明的冰晶石—氧化铝熔盐电解法,其原理是氧化铝在通电条件下分解,反应的化学方程式为______。
18.金属材料广泛应用于生产生活中。
(1)生铁和______是两种常见的铁合金。用赤铁矿(主要成分是Fe2O3)冶炼铁的化学方程式为______。铁制品锈蚀,是铁与空气中的______发生了化学反应:防止铁锅锈蚀的一种方法是______。
(2)铝的抗腐蚀性很强,是因为铝在空气中能生成一层______,该反应的化学方程式为______。
五、计算题
19.锌与盐酸(HCl)反应生成氢气和氯化锌,实验室里用3.25g锌与足量的盐酸反应,可制得多少g氢气?
20.学校课外活动小组为了测定某钢铁厂生铁样品中铁的质量分数,在实验室称取生铁样品5.8g放入烧杯中(烧杯的质量为30g).然后再加入50g稀硫酸,使之充分反应后,称量,烧杯及烧杯中物质的总质量为85.6g(已知该反应中稀硫酸恰好完全反应,杂质不参与反应).请计算:
(1)产生氢气的质量是_____.
(2)该生铁样品中铁的质量分数?_____(精确到0.1%)
21.金属锰大量用于制造锰钢。地壳中含锰的矿石有软锰矿,软锰矿的主要成分是二氧化锰。金属锰可用软锰矿跟铝反应来制取,其反应为3MnO2+4Al2Al2O3+3Mn。
(1)用100t含MnO278.3%的软锰矿石,可冶炼出多少t锰(准确至0.1t,下同)。
(2)实际冶炼出的锰是含有5%杂质的粗锰,则实际得到多少t粗锰。
试卷第1页,共3页
试卷第2页,共2页
参考答案:
1.A
2.D
3.D
4.B
5.A
6.B
7.C
8.C
9.A
10.A
11. D 使可燃物与氧气隔绝 刷漆(合理即可) 白色污染 糖类(或维生素)
12. 相同; 不同; 3CO+Fe2O3 3Fe+3CO2; 回收利用或点燃
13.(1)①;硝酸银 (2)①氢气 ②3.6%
14.(1)CaCO3
(2)导线等
(3)
15. 除铁锈
C或H2
16. 二氧化碳不燃烧也不支持燃烧,密度比空气大 沿蜡烛对面一侧烧杯内壁缓缓倾倒二氧化碳 探究反应物的状态对反应速率的影响 紫色石蕊溶液(或锌等活泼金属或碳酸钠溶液等)
17.(1) 产生SO2造成大气污染(合理答案均可) 低
(2)
(3)
18.(1) 钢 水和氧气 洗完后保持铁锅干燥(合理即可)
(2) 致密氧化铝薄膜
19.解:设生成氢气质量为x
答:生成氢气质量为0.1g。
20. 0.2g 96.6%
21.(1)49.5t;(2)52.1t
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
