第12章盐基础练习---2021-2022学年九年级化学京改版(2013)下册(word版 含答案)
文档属性
| 名称 | 第12章盐基础练习---2021-2022学年九年级化学京改版(2013)下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 124.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-01 00:00:00 | ||
图片预览


文档简介
第12章《盐》基础练习 2021-2022学年九年级化学京改版(2013)下册
一、单选题
1.下列物质的名称、俗名与化学式完全相符的是( )
A.碳酸钠 小苏打 Na2CO3
B.碳酸氢钠 纯碱 NaHCO3
C.氢氧化钙 熟石灰 CaO
D.二氧化碳 干冰 CO2
2.金属钛(Ti)是重要的航空航天材料。金属钛可以由TiO2与Si在高温下制取,反应的化学方程式为TiO2+Si SiO2+Ti。该反应属于
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
3.将珍珠加入稀盐酸中,有气泡产生,生成的气体能使澄清石灰水变浑浊,则珍珠中含有下列离子中的( )
A.氯离子 B.硫酸根离子 C.碳酸根离子 D.氢氧根离子
4.磷元素对生命活动具有重要意义,其相关信息如图所示。下列有关磷元素的说法正确的是( )
A.属于金属元素
B.原子核外有16个电子
C.相对原子质量为30.97 g
D.是农作物必需的营养元素
5.下图是某反应前后的微观示意图,“”和“”表示两种不同元素的原子。下列有关说法正确的是
A.该反应没有单质生成
B.该反应属于复分解反应
C.该反应中,原子个数发生了改变
D.参加反应的两种分子(和)的个数比为1:1
6.某干燥剂含有CaO、NaOH和CaCl2中的两种物质,为探究其成分,设计了如图所示实验.
则下列说法正确的是( )
A.a、b溶液一定只含两种溶质
B.b溶液中一定有NaOH和Na2CO3
C.白色固体一定不是纯净物
D.干燥剂一定由NaOH和CaCl2组成
7.氯化铵(NH4Cl)是“侯氏制碱法”的一种副产品。已知氯化铵的水溶液显酸性,下列关于氯化铵的说法正确的是
A.氯化铵属于酸 B.氯化铵是一种复合肥
C.氯化铵与熟石灰混合使用可提高肥效 D.氯化铵溶液与硝酸银溶液混合会产生白色沉淀
8.下列除去杂质的方法不正确的是( )
A.FeSO4溶液(CuSO4):过量的铁粉过滤 B.H2(H2O):浓硫酸
C.CO2(CO):通过灼热的氧化铜粉末 D.CaO(CaCO3):稀盐酸
9.稀HCl和NaOH溶液混合后无明显现象,要证明两者已发生化学反应,如图操作及实验现象(或结果),不能证明反应发生的是
A.在混合液中加金属Zn,无气泡产生
B.在混合液中加无色酚酞,溶液呈无色的
C.在混合液中加AgNO3溶液,有白色沉淀
D.用pH试纸测混合液的pH,测得pH等于7
10.“河长制”有利于加强水资源保护,防治水体污染。研学小组对两个工厂排污口排放的污水进行检测,发现共含HNO3、K2SO4、MgCl2和NaOH四种物质,其中每个排污口排放两种不同物质。下列关于污水成分的分析合理的是( )
A.HNO3 和K2SO4一定来自同一排污口 B.HNO3 和MgCl2一定来自同 排污口
C.HNO3和NaOH一定来自同一排污口 D.将两处污水混合后,溶液一定呈中性
二、简答题
11.为了除去粗盐中CaCl2、MgCl2、Na2SO4等可溶性杂质,需进行如下操作:①溶解;②依次加过量的BaCl2、NaOH、Na2CO3溶液;③过滤;④加适量盐酸;⑤蒸发、结晶[提示:Mg(OH)2、BaSO4、BaCO3难溶于水;微溶物不形成沉淀;Na2CO3溶液星碱性]
(1)加入Na2CO3溶液的目的是什么?____
(2)最后制得氯化钠的质量大于粗盐中氯化钠的质量,写出一个可使氯化钠质量增加的化学方程式____。
(3)请设计实验方案证明操作③所得溶液中含有NaOH。(写出实验步骤和现象)____
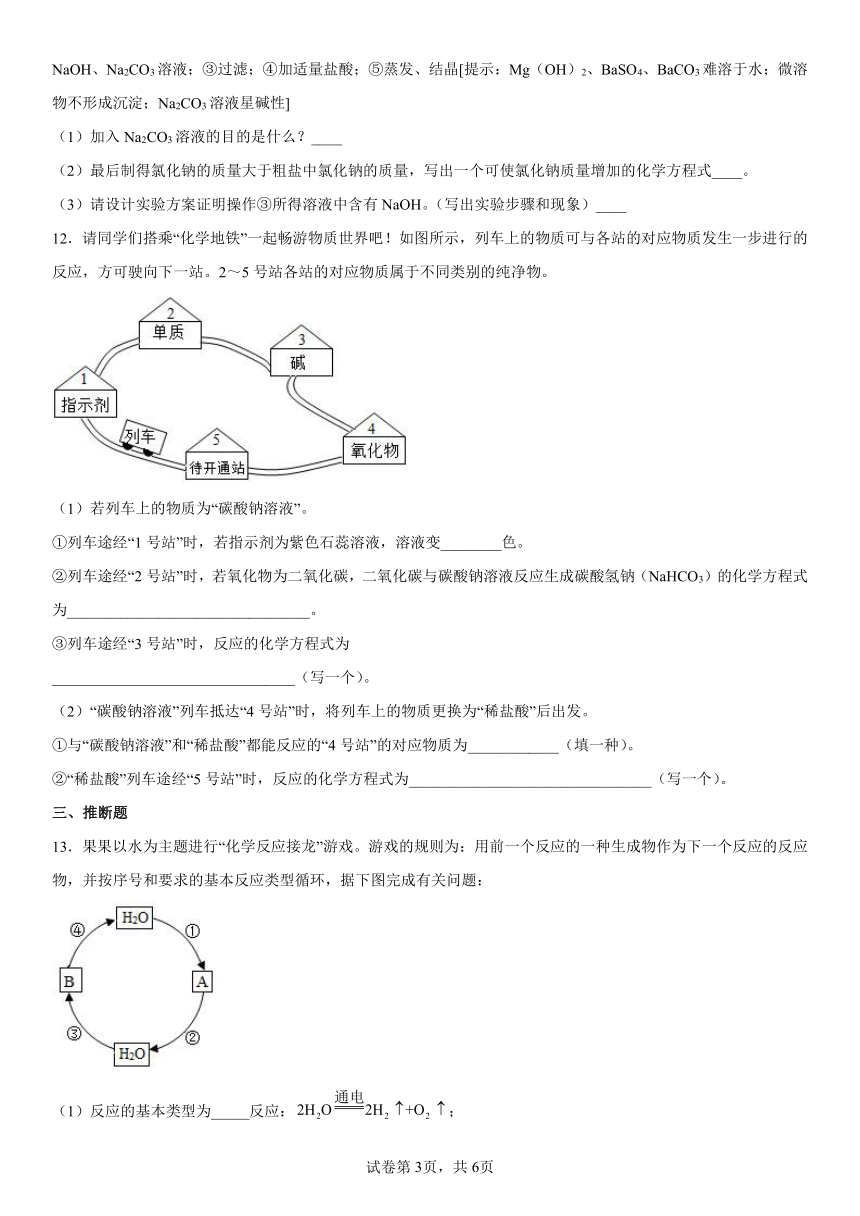
12.请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站。2~5号站各站的对应物质属于不同类别的纯净物。
(1)若列车上的物质为“碳酸钠溶液”。
①列车途经“1号站”时,若指示剂为紫色石蕊溶液,溶液变________色。
②列车途经“2号站”时,若氧化物为二氧化碳,二氧化碳与碳酸钠溶液反应生成碳酸氢钠(NaHCO3)的化学方程式为________________________________。
③列车途经“3号站”时,反应的化学方程式为
________________________________(写一个)。
(2)“碳酸钠溶液”列车抵达“4号站”时,将列车上的物质更换为“稀盐酸”后出发。
①与“碳酸钠溶液”和“稀盐酸”都能反应的“4号站”的对应物质为____________(填一种)。
②“稀盐酸”列车途经“5号站”时,反应的化学方程式为________________________________(写一个)。
三、推断题
13.果果以水为主题进行“化学反应接龙”游戏。游戏的规则为:用前一个反应的一种生成物作为下一个反应的反应物,并按序号和要求的基本反应类型循环,据下图完成有关问题:
(1)反应的基本类型为_____反应:;
(2)反应的基本类型为置换反应:_____;
(3)反应的基本类型为化合反应:________________________;
(4)反应的基本类型为复分解反应:__________________________。
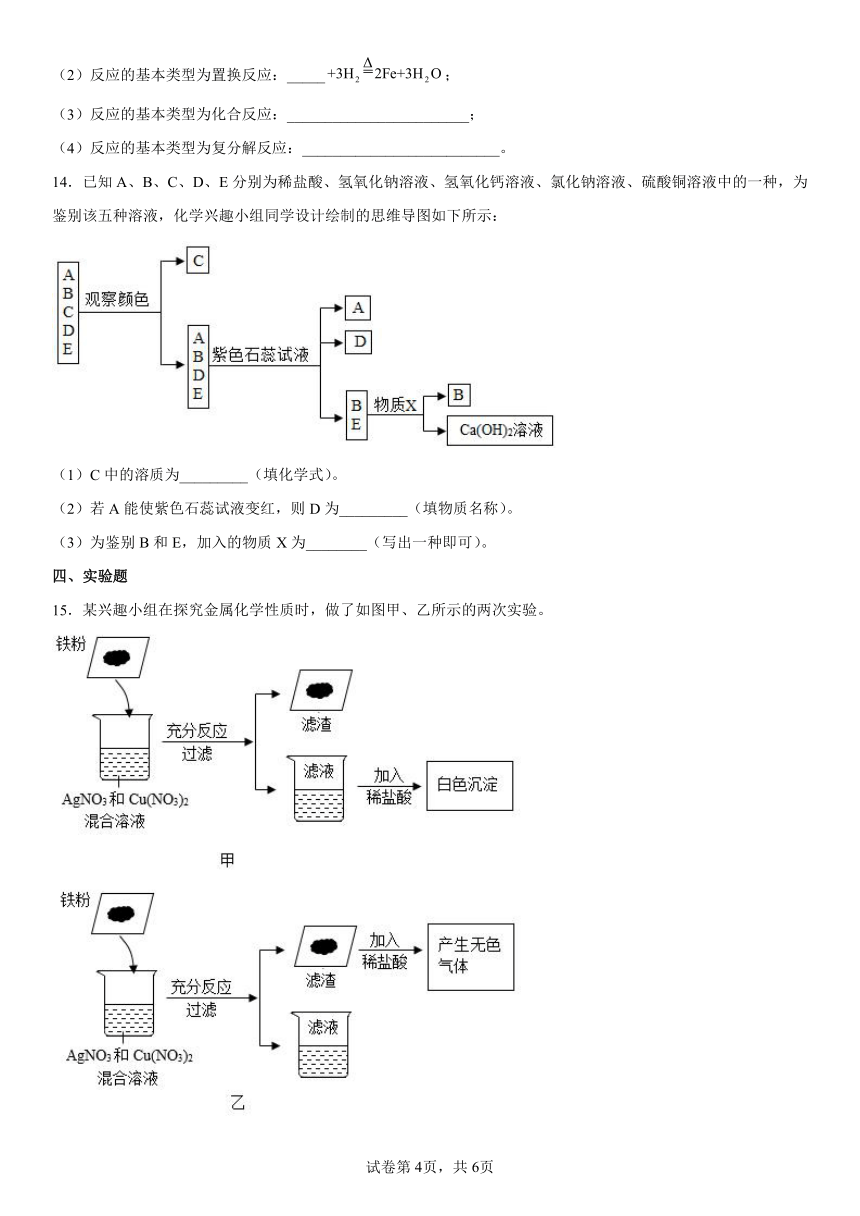
14.已知A、B、C、D、E分别为稀盐酸、氢氧化钠溶液、氢氧化钙溶液、氯化钠溶液、硫酸铜溶液中的一种,为鉴别该五种溶液,化学兴趣小组同学设计绘制的思维导图如下所示:
(1)C中的溶质为_________(填化学式)。
(2)若A能使紫色石蕊试液变红,则D为_________(填物质名称)。
(3)为鉴别B和E,加入的物质X为________(写出一种即可)。
四、实验题
15.某兴趣小组在探究金属化学性质时,做了如图甲、乙所示的两次实验。
(1)甲实验中滤渣的成分是______,产生白色沉淀的化学反应方程式为______。
(2)乙实验中滤液中含有的金属离子为______(填离子符号)。
16.请结合下图回答问题:
(1)仪器名称:①________,②______。
(2)用氯酸钾和二氧化锰制取氧气,可选用装置______(选填序号)和D组合,反应的化学方程式为________,二氧化锰的作用是_______。
(3)实验室可用装置B或C制H2,C装置相对于B的优点有__________。用E装置收集H2,气体应从________(选填“a”或“b”)端通入。
(4)有同学将实验室制得的CO2通入澄清石灰水,石灰水未变浑浊,于是作如右图探究:
①实验室制CO2反应的化学方程式_________。
②装置F、H中溶液变浑浊,G中溶液不变浑浊,则原石灰水未变浑浊的原因是________。
五、计算题
17.草木灰是农家肥料,其主要成分是碳酸钾。某化学兴趣小组进行如下实验,以下是他们的实验过程及数据(假设杂质不与稀盐酸反应,生成的气体全部逸出)。请你回答下列问题:
(1)碳酸钾中钾元素、碳元素、氧元素的质量比为______。
(2)反应生成的气体质量为________g。
(3)稀盐酸中溶质质量分数是______?
18.泡腾片配料表如下:
成分 柠檬酸 碳酸氢钠 维生素C 乳糖 色素香精
每片含量(4 g/片) 未知 未知 0.2 g 未知 极少量
泡腾片放入温开水中,浮于水面上,产生大量气泡,所得溶液喝起来酸甜可口。已知:柠檬酸的化学式为C6H8O7,相对分子质量为192;泡腾片溶于水时,碳酸氢钠刚好与柠檬酸完全反应,生成Na3C6H5O7。
(1)泡腾片在水中产生气体的化学式为_____。泡腾片中柠檬酸与碳酸氢钠的质量比为_____。
(2)称取5.00 g泡腾片放入200.00 g温开水中,待泡腾片完全溶解,不再产生气体后,测得溶液质量为203.68 g.通过计算确定泡腾片中柠檬酸的质量分数_____。
19.镁在国产大飞机C-919”的制造中大显身手,小亮在实验室模拟“海水制镁”的原理来富集镁,他将25g氯化钠和氯化镁的固体混合物全部溶解于盛有70g水的烧杯中,然后向其中加入63.6g氢氧化钠溶液至恰好完全反应(图像如下),过滤,称量滤液质量为147g,求:
(1)图像中m=_____g。
(2)滤液中溶质的质量分数是?
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.C
3.C
4.D
5.A
6.B
7.D
8.D
9.C
10.B
11. 加入过量碳酸钠的作用是除去氯化钙和氯化钡杂质 NaOH+HCl═NaCl+H2O,Na2CO3+2HCl=2NaCl+H2O+CO2↑ 取③所得溶液,加入足量的BaCl2溶液,静置,向上层清液中滴加无色酚酞溶液,溶液变红色,说明溶液中含有氢氧化钠
12. 蓝 Na2CO3+H2O+CO2===2NaHCO3 Na2CO3+Ca(OH)2===CaCO3↓+2NaOH AgNO3 Fe+2HCl===FeCl2+H2↑
13. 分解 Fe2O3 Ca(OH)2+2HCl=CaCl2+2H2O
14. CuSO4 氯化钠溶液 CO2或Na2CO3溶液(写物质的名称或化学式均可,答案合理即可)
15. 银 Fe2+
16. 铁架台 长颈漏斗 A 2KClO32KCl+3O2↑ 催化作用(催化、催化剂) 控制反应的发生和停止(或随开随用,随关随停) a CO2中含有HCl(或使用了浓盐酸)
17.(1)39:6:24;(2)8.8g;(3)14.6%
18.(1)CO2;16:21(2)38.4%
19.(1)11.6;(2)20%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列物质的名称、俗名与化学式完全相符的是( )
A.碳酸钠 小苏打 Na2CO3
B.碳酸氢钠 纯碱 NaHCO3
C.氢氧化钙 熟石灰 CaO
D.二氧化碳 干冰 CO2
2.金属钛(Ti)是重要的航空航天材料。金属钛可以由TiO2与Si在高温下制取,反应的化学方程式为TiO2+Si SiO2+Ti。该反应属于
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
3.将珍珠加入稀盐酸中,有气泡产生,生成的气体能使澄清石灰水变浑浊,则珍珠中含有下列离子中的( )
A.氯离子 B.硫酸根离子 C.碳酸根离子 D.氢氧根离子
4.磷元素对生命活动具有重要意义,其相关信息如图所示。下列有关磷元素的说法正确的是( )
A.属于金属元素
B.原子核外有16个电子
C.相对原子质量为30.97 g
D.是农作物必需的营养元素
5.下图是某反应前后的微观示意图,“”和“”表示两种不同元素的原子。下列有关说法正确的是
A.该反应没有单质生成
B.该反应属于复分解反应
C.该反应中,原子个数发生了改变
D.参加反应的两种分子(和)的个数比为1:1
6.某干燥剂含有CaO、NaOH和CaCl2中的两种物质,为探究其成分,设计了如图所示实验.
则下列说法正确的是( )
A.a、b溶液一定只含两种溶质
B.b溶液中一定有NaOH和Na2CO3
C.白色固体一定不是纯净物
D.干燥剂一定由NaOH和CaCl2组成
7.氯化铵(NH4Cl)是“侯氏制碱法”的一种副产品。已知氯化铵的水溶液显酸性,下列关于氯化铵的说法正确的是
A.氯化铵属于酸 B.氯化铵是一种复合肥
C.氯化铵与熟石灰混合使用可提高肥效 D.氯化铵溶液与硝酸银溶液混合会产生白色沉淀
8.下列除去杂质的方法不正确的是( )
A.FeSO4溶液(CuSO4):过量的铁粉过滤 B.H2(H2O):浓硫酸
C.CO2(CO):通过灼热的氧化铜粉末 D.CaO(CaCO3):稀盐酸
9.稀HCl和NaOH溶液混合后无明显现象,要证明两者已发生化学反应,如图操作及实验现象(或结果),不能证明反应发生的是
A.在混合液中加金属Zn,无气泡产生
B.在混合液中加无色酚酞,溶液呈无色的
C.在混合液中加AgNO3溶液,有白色沉淀
D.用pH试纸测混合液的pH,测得pH等于7
10.“河长制”有利于加强水资源保护,防治水体污染。研学小组对两个工厂排污口排放的污水进行检测,发现共含HNO3、K2SO4、MgCl2和NaOH四种物质,其中每个排污口排放两种不同物质。下列关于污水成分的分析合理的是( )
A.HNO3 和K2SO4一定来自同一排污口 B.HNO3 和MgCl2一定来自同 排污口
C.HNO3和NaOH一定来自同一排污口 D.将两处污水混合后,溶液一定呈中性
二、简答题
11.为了除去粗盐中CaCl2、MgCl2、Na2SO4等可溶性杂质,需进行如下操作:①溶解;②依次加过量的BaCl2、NaOH、Na2CO3溶液;③过滤;④加适量盐酸;⑤蒸发、结晶[提示:Mg(OH)2、BaSO4、BaCO3难溶于水;微溶物不形成沉淀;Na2CO3溶液星碱性]
(1)加入Na2CO3溶液的目的是什么?____
(2)最后制得氯化钠的质量大于粗盐中氯化钠的质量,写出一个可使氯化钠质量增加的化学方程式____。
(3)请设计实验方案证明操作③所得溶液中含有NaOH。(写出实验步骤和现象)____
12.请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站。2~5号站各站的对应物质属于不同类别的纯净物。
(1)若列车上的物质为“碳酸钠溶液”。
①列车途经“1号站”时,若指示剂为紫色石蕊溶液,溶液变________色。
②列车途经“2号站”时,若氧化物为二氧化碳,二氧化碳与碳酸钠溶液反应生成碳酸氢钠(NaHCO3)的化学方程式为________________________________。
③列车途经“3号站”时,反应的化学方程式为
________________________________(写一个)。
(2)“碳酸钠溶液”列车抵达“4号站”时,将列车上的物质更换为“稀盐酸”后出发。
①与“碳酸钠溶液”和“稀盐酸”都能反应的“4号站”的对应物质为____________(填一种)。
②“稀盐酸”列车途经“5号站”时,反应的化学方程式为________________________________(写一个)。
三、推断题
13.果果以水为主题进行“化学反应接龙”游戏。游戏的规则为:用前一个反应的一种生成物作为下一个反应的反应物,并按序号和要求的基本反应类型循环,据下图完成有关问题:
(1)反应的基本类型为_____反应:;
(2)反应的基本类型为置换反应:_____;
(3)反应的基本类型为化合反应:________________________;
(4)反应的基本类型为复分解反应:__________________________。
14.已知A、B、C、D、E分别为稀盐酸、氢氧化钠溶液、氢氧化钙溶液、氯化钠溶液、硫酸铜溶液中的一种,为鉴别该五种溶液,化学兴趣小组同学设计绘制的思维导图如下所示:
(1)C中的溶质为_________(填化学式)。
(2)若A能使紫色石蕊试液变红,则D为_________(填物质名称)。
(3)为鉴别B和E,加入的物质X为________(写出一种即可)。
四、实验题
15.某兴趣小组在探究金属化学性质时,做了如图甲、乙所示的两次实验。
(1)甲实验中滤渣的成分是______,产生白色沉淀的化学反应方程式为______。
(2)乙实验中滤液中含有的金属离子为______(填离子符号)。
16.请结合下图回答问题:
(1)仪器名称:①________,②______。
(2)用氯酸钾和二氧化锰制取氧气,可选用装置______(选填序号)和D组合,反应的化学方程式为________,二氧化锰的作用是_______。
(3)实验室可用装置B或C制H2,C装置相对于B的优点有__________。用E装置收集H2,气体应从________(选填“a”或“b”)端通入。
(4)有同学将实验室制得的CO2通入澄清石灰水,石灰水未变浑浊,于是作如右图探究:
①实验室制CO2反应的化学方程式_________。
②装置F、H中溶液变浑浊,G中溶液不变浑浊,则原石灰水未变浑浊的原因是________。
五、计算题
17.草木灰是农家肥料,其主要成分是碳酸钾。某化学兴趣小组进行如下实验,以下是他们的实验过程及数据(假设杂质不与稀盐酸反应,生成的气体全部逸出)。请你回答下列问题:
(1)碳酸钾中钾元素、碳元素、氧元素的质量比为______。
(2)反应生成的气体质量为________g。
(3)稀盐酸中溶质质量分数是______?
18.泡腾片配料表如下:
成分 柠檬酸 碳酸氢钠 维生素C 乳糖 色素香精
每片含量(4 g/片) 未知 未知 0.2 g 未知 极少量
泡腾片放入温开水中,浮于水面上,产生大量气泡,所得溶液喝起来酸甜可口。已知:柠檬酸的化学式为C6H8O7,相对分子质量为192;泡腾片溶于水时,碳酸氢钠刚好与柠檬酸完全反应,生成Na3C6H5O7。
(1)泡腾片在水中产生气体的化学式为_____。泡腾片中柠檬酸与碳酸氢钠的质量比为_____。
(2)称取5.00 g泡腾片放入200.00 g温开水中,待泡腾片完全溶解,不再产生气体后,测得溶液质量为203.68 g.通过计算确定泡腾片中柠檬酸的质量分数_____。
19.镁在国产大飞机C-919”的制造中大显身手,小亮在实验室模拟“海水制镁”的原理来富集镁,他将25g氯化钠和氯化镁的固体混合物全部溶解于盛有70g水的烧杯中,然后向其中加入63.6g氢氧化钠溶液至恰好完全反应(图像如下),过滤,称量滤液质量为147g,求:
(1)图像中m=_____g。
(2)滤液中溶质的质量分数是?
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.C
3.C
4.D
5.A
6.B
7.D
8.D
9.C
10.B
11. 加入过量碳酸钠的作用是除去氯化钙和氯化钡杂质 NaOH+HCl═NaCl+H2O,Na2CO3+2HCl=2NaCl+H2O+CO2↑ 取③所得溶液,加入足量的BaCl2溶液,静置,向上层清液中滴加无色酚酞溶液,溶液变红色,说明溶液中含有氢氧化钠
12. 蓝 Na2CO3+H2O+CO2===2NaHCO3 Na2CO3+Ca(OH)2===CaCO3↓+2NaOH AgNO3 Fe+2HCl===FeCl2+H2↑
13. 分解 Fe2O3 Ca(OH)2+2HCl=CaCl2+2H2O
14. CuSO4 氯化钠溶液 CO2或Na2CO3溶液(写物质的名称或化学式均可,答案合理即可)
15. 银 Fe2+
16. 铁架台 长颈漏斗 A 2KClO32KCl+3O2↑ 催化作用(催化、催化剂) 控制反应的发生和停止(或随开随用,随关随停) a CO2中含有HCl(或使用了浓盐酸)
17.(1)39:6:24;(2)8.8g;(3)14.6%
18.(1)CO2;16:21(2)38.4%
19.(1)11.6;(2)20%
答案第1页,共2页
答案第1页,共2页
