第11章酸与碱检测题-2021-2022学年九年级化学京改版(2013)下册(word 含答案)
文档属性
| 名称 | 第11章酸与碱检测题-2021-2022学年九年级化学京改版(2013)下册(word 含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 120.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-01 00:00:00 | ||
图片预览


文档简介
第11章《酸与碱》检测题
一、单选题
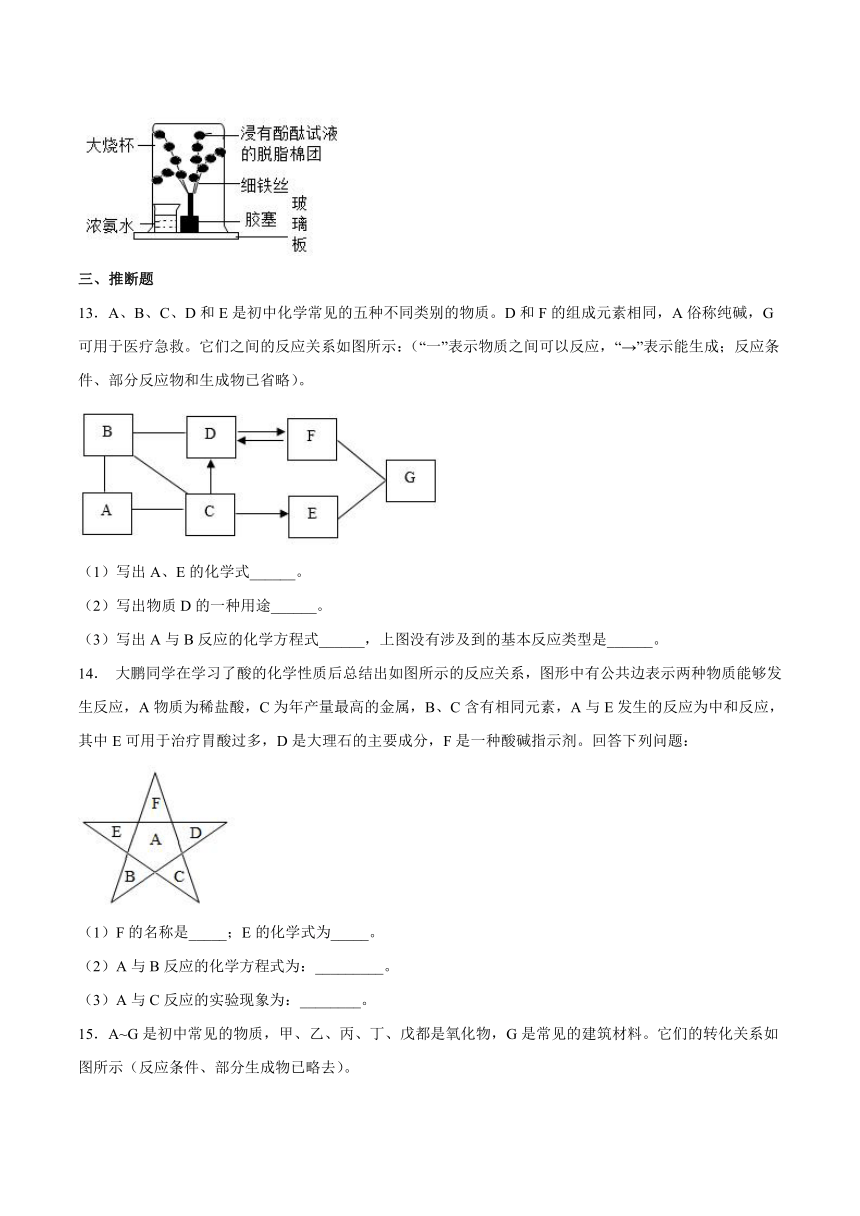
1.下列实验基本操作不正确的是
A. 读液体体积 B. 蒸发食盐水
C.测某溶液pH值 D.稀释浓硫酸
2.下列物质不能用于鉴别氢氧化钠溶液和稀盐酸的是( )
A.紫色石蕊溶液 B.氯化钠溶液 C.铁粉 D.pH试纸
3.下列四组溶液,只用紫色石蕊溶液就能鉴别的一组是
A.NaOH KOH HCl B.NaCl NaOH HCl
C.H2SO4 HCl NaOH D.NaCl Na2CO3 Na2SO4
4.加热蒸干氯化镁溶液可得到碱式氯化镁Mgx(OH)yClz,其不溶于水,能与酸反应,加热能分解。取一定质量的碱式氯化镁,加热分解生成16gMgO、7.3gHCl和3.6gH2O。下列说法不正确的是
A.碱式氯化镁的质量为26.9g B.MgO和HCl的分子个数比为2∶1
C.x∶y∶z=2∶1∶3 D.HCl气体溶于水可使紫色石蕊溶液变红
5.2021年“世界水日”的主题为“珍惜水、爱护水”。下列关于水的说法正确的是
A.过滤能将硬水转化为软水 B.用明矾对自来水进行杀菌消毒
C.用肥皂水区别硬水与软水 D.有水生成的反应一定是中和反应
6.下列溶液能使紫色石蕊溶液变成蓝色的是
A.澄清石灰水 B.NaCl溶液
C.稀硫酸 D.KNO3溶液
7.室温时,将氢氧化钠溶液与盐酸用滴加方式反应时,溶液的pH随滴入溶液体积变化如右下图所示。下列有关说法不正确的是
A.该图像表示的是将氢氧化钠溶液滴入盐酸中
B.氢氧化钠溶液和盐酸恰好完全反应时。溶液的pH等于7
C.当滴入溶液的体积为5mL时,所得溶液中的溶质只有NaCl
D.滴入溶液体积为15mL时,再加几滴紫色石蕊试液溶液呈蓝色
8.鉴别下列各组物质采用的方法或使用的试剂不正确的是
A.硬水和软水:肥皂水
B.氧气和二氧化碳:带火星的木条
C.氢氧化钠与硝酸铵:加水溶解测温度
D.蔗糖溶液与酒精溶液:测导电性
9.在Ca(OH)2的饱和溶液中加入下列物质,冷却至室温,溶液的pH没有改变的是
A.CO2 B.CaO C.Cu(NO3)2 D.HCl
10.下列溶液在空气中敞口放置后,溶液质量因发生化学反应而减小的是
A.石灰水 B.浓硫酸 C.浓盐酸 D.烧碱溶液
11.碱溶液中都含有OH—,因此不同的碱表现出一些共同的性质。下列关于Ba(OH)2性质的描述中不属于碱的共同性质的是
A.能使紫色石蕊溶液变蓝色
B.能与盐酸反应生成水
C.能与Na2SO4溶液反应生成BaSO4沉淀
D.能与CO2反应生成水
二、简答题
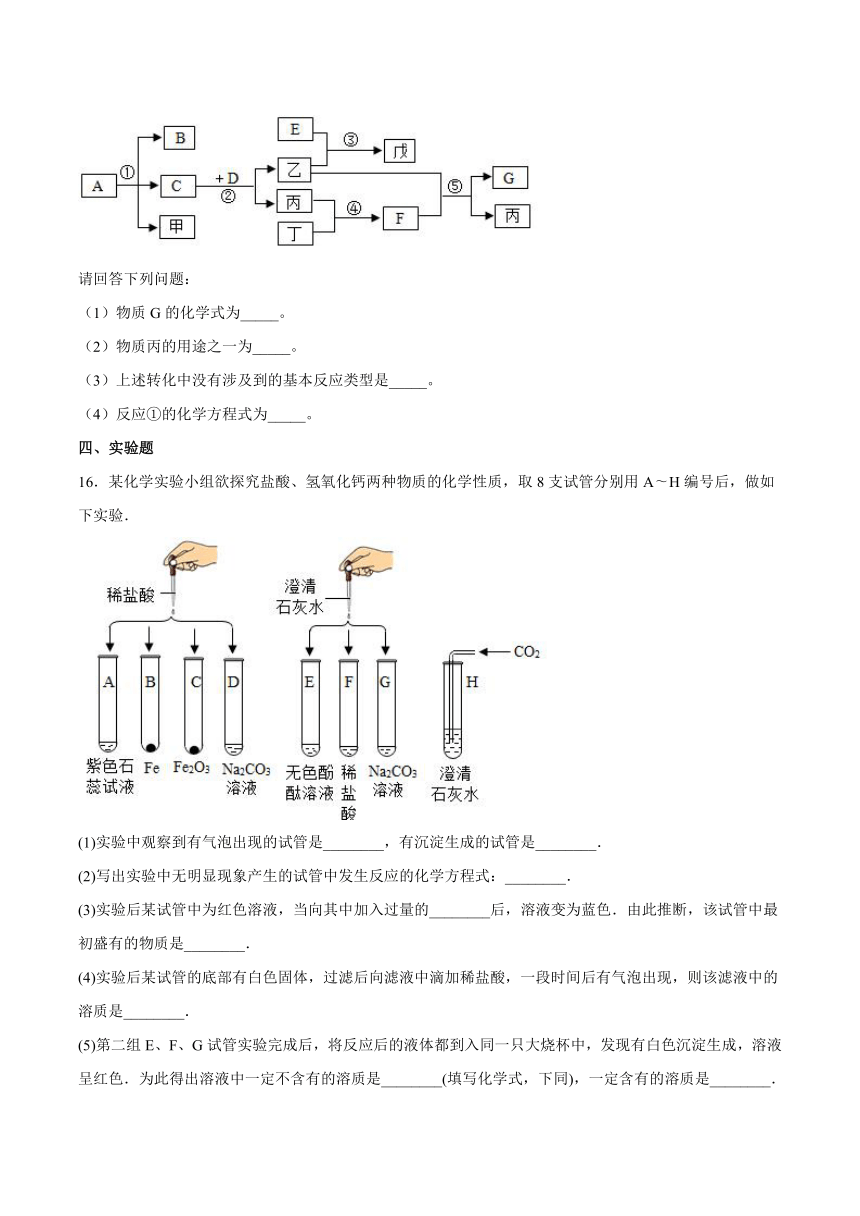
12.一位同学在新年晚会上给来宾表演了一个魔术节目,道具如图所示,通过该节目可观察到棉花团由白色变为红色,大烧杯中出现了一株美丽的“铁树”。你能用你学过的化学知识对此现象加以解释吗?_____。
三、推断题
13.A、B、C、D和E是初中化学常见的五种不同类别的物质。D和F的组成元素相同,A俗称纯碱,G可用于医疗急救。它们之间的反应关系如图所示:(“一”表示物质之间可以反应,“→”表示能生成;反应条件、部分反应物和生成物已省略)。
(1)写出A、E的化学式______。
(2)写出物质D的一种用途______。
(3)写出A与B反应的化学方程式______,上图没有涉及到的基本反应类型是______。
14. 大鹏同学在学习了酸的化学性质后总结出如图所示的反应关系,图形中有公共边表示两种物质能够发生反应,A物质为稀盐酸,C为年产量最高的金属,B、C含有相同元素,A与E发生的反应为中和反应,其中E可用于治疗胃酸过多,D是大理石的主要成分,F是一种酸碱指示剂。回答下列问题:
(1)F的名称是_____;E的化学式为_____。
(2)A与B反应的化学方程式为:_________。
(3)A与C反应的实验现象为:________。
15.A~G是初中常见的物质,甲、乙、丙、丁、戊都是氧化物,G是常见的建筑材料。它们的转化关系如图所示(反应条件、部分生成物已略去)。
请回答下列问题:
(1)物质G的化学式为_____。
(2)物质丙的用途之一为_____。
(3)上述转化中没有涉及到的基本反应类型是_____。
(4)反应①的化学方程式为_____。
四、实验题
16.某化学实验小组欲探究盐酸、氢氧化钙两种物质的化学性质,取8支试管分别用A H编号后,做如下实验.
(1)实验中观察到有气泡出现的试管是________,有沉淀生成的试管是________.
(2)写出实验中无明显现象产生的试管中发生反应的化学方程式:________.
(3)实验后某试管中为红色溶液,当向其中加入过量的________后,溶液变为蓝色.由此推断,该试管中最初盛有的物质是________.
(4)实验后某试管的底部有白色固体,过滤后向滤液中滴加稀盐酸,一段时间后有气泡出现,则该滤液中的溶质是________.
(5)第二组E、F、G试管实验完成后,将反应后的液体都到入同一只大烧杯中,发现有白色沉淀生成,溶液呈红色.为此得出溶液中一定不含有的溶质是________(填写化学式,下同),一定含有的溶质是________.
(6)通过上述实验,可归纳出盐酸的化学性质有________.
17.根据如图装置图回答问题。
(1)图中标有字母X的仪器的名称:______。
(2)实验室用高锰酸钾固体制取氧气时应选择______(填代号)作为发生装置。常温下,下列收集氧气的方法不可行的是______。(填字母序号)
a向上排空气法 b向下排空气法 c排水法
(3)实验室用过氧化氢制取氧气的化学方程式是______。欲收集干燥的氧气,应在发生装置和收集装置间连接装置G,并在其中装入的药品是______;收集时气体应从______(填“①”或“②”)端通入。
(4)实验室常用装置C代替装置B制取气体,装置C的优点是______。
五、计算题
18.某同学向质量分数为7.3%的稀盐酸溶液中加入碳酸钙样品(含有杂质,且杂质不与酸反应也不溶于水),记录反应过程中有关的实验数据,最后结果如图所示。
(1)甲图中a点的pH值为______;
(2)计算样品中碳酸钙的质量分数;
(3)丙图纵坐标上b、c两点的数值分别是______、______。
19.生活中有些胃药含有氢氧化铝|【Al(OH)3】。请回答下列问题:
(1)氢氧化铝在人的胃内起的作用是 。
(2)氢氧化铝中铝、氧、氢三种元素的质量比为 (写最简比);
(3)铝元素的质量分数为 。(结果精确至0.1%)
(4)在 g氢氧化铝中含有4.8g氧元素。
20.赤铁矿石的主要成分为氧化铁。将10g赤铁矿石样品(杂质既不溶于水,也不参加反应)放入烧杯中,再加入92g稀硫酸,恰好完全反应,过滤,得到滤液和2g滤渣。请计算:
(1)赤铁矿石样品中氧化铁的质量分数。
(2)反应后所得溶液中溶质质量分数。
参考答案:
1.D 2.B 3.B 4.C 5.C 6.A 7.C 8.D 9.B 10.A 11.C
12.氨分子是不断运动的,浓氨水中的氨分子不断向四周扩散,当和酚酞试液 相遇时形成氨水,氨水显碱性,能使酚酞试液变红色。因此大烧杯中出现了一株 美丽的“铁树”
13. Na2CO3、H2 人工降雨(用作气体肥料、用作制冷剂等合理答案都得分) (或等) 分解反应
14. 紫色石蕊溶液 Al(OH)3 Fe2O3+6HCl=2FeCl3+3H2O; 有气泡产生,溶液变为浅绿色
15. CaCO3 配制溶液、洗涤衣物、灌溉农田等 置换反应和复分解反应 2KMnO4K2MnO4 + MnO2 + O2↑
16. B D G H NaOH溶液 紫色石蕊溶液 NaOH和Na2CO3 HCl NaCl 和NaOH 与酸碱指示剂反应、与活泼金属反应、与某些金属氧化物反应、与碱反应、与某些盐反应
17. 锥形瓶 A b 浓硫酸 ① 可以控制反应的发生与停止
18.(1)7;(2)75%;(3)150g;158.4g
19.(1)中和胃酸
(2)9:16:1
(3)铝元素的质量分数为:
(4)含有4.8g氧元素的氢氧化铝的质量为:
20.(1)80%;
(2)解:设生成硫酸铁的质量为x
x=20g
滤液中溶质的质量分数为100%=20%。
答:反应后所得溶液中溶质质量分数20%。
一、单选题
1.下列实验基本操作不正确的是
A. 读液体体积 B. 蒸发食盐水
C.测某溶液pH值 D.稀释浓硫酸
2.下列物质不能用于鉴别氢氧化钠溶液和稀盐酸的是( )
A.紫色石蕊溶液 B.氯化钠溶液 C.铁粉 D.pH试纸
3.下列四组溶液,只用紫色石蕊溶液就能鉴别的一组是
A.NaOH KOH HCl B.NaCl NaOH HCl
C.H2SO4 HCl NaOH D.NaCl Na2CO3 Na2SO4
4.加热蒸干氯化镁溶液可得到碱式氯化镁Mgx(OH)yClz,其不溶于水,能与酸反应,加热能分解。取一定质量的碱式氯化镁,加热分解生成16gMgO、7.3gHCl和3.6gH2O。下列说法不正确的是
A.碱式氯化镁的质量为26.9g B.MgO和HCl的分子个数比为2∶1
C.x∶y∶z=2∶1∶3 D.HCl气体溶于水可使紫色石蕊溶液变红
5.2021年“世界水日”的主题为“珍惜水、爱护水”。下列关于水的说法正确的是
A.过滤能将硬水转化为软水 B.用明矾对自来水进行杀菌消毒
C.用肥皂水区别硬水与软水 D.有水生成的反应一定是中和反应
6.下列溶液能使紫色石蕊溶液变成蓝色的是
A.澄清石灰水 B.NaCl溶液
C.稀硫酸 D.KNO3溶液
7.室温时,将氢氧化钠溶液与盐酸用滴加方式反应时,溶液的pH随滴入溶液体积变化如右下图所示。下列有关说法不正确的是
A.该图像表示的是将氢氧化钠溶液滴入盐酸中
B.氢氧化钠溶液和盐酸恰好完全反应时。溶液的pH等于7
C.当滴入溶液的体积为5mL时,所得溶液中的溶质只有NaCl
D.滴入溶液体积为15mL时,再加几滴紫色石蕊试液溶液呈蓝色
8.鉴别下列各组物质采用的方法或使用的试剂不正确的是
A.硬水和软水:肥皂水
B.氧气和二氧化碳:带火星的木条
C.氢氧化钠与硝酸铵:加水溶解测温度
D.蔗糖溶液与酒精溶液:测导电性
9.在Ca(OH)2的饱和溶液中加入下列物质,冷却至室温,溶液的pH没有改变的是
A.CO2 B.CaO C.Cu(NO3)2 D.HCl
10.下列溶液在空气中敞口放置后,溶液质量因发生化学反应而减小的是
A.石灰水 B.浓硫酸 C.浓盐酸 D.烧碱溶液
11.碱溶液中都含有OH—,因此不同的碱表现出一些共同的性质。下列关于Ba(OH)2性质的描述中不属于碱的共同性质的是
A.能使紫色石蕊溶液变蓝色
B.能与盐酸反应生成水
C.能与Na2SO4溶液反应生成BaSO4沉淀
D.能与CO2反应生成水
二、简答题
12.一位同学在新年晚会上给来宾表演了一个魔术节目,道具如图所示,通过该节目可观察到棉花团由白色变为红色,大烧杯中出现了一株美丽的“铁树”。你能用你学过的化学知识对此现象加以解释吗?_____。
三、推断题
13.A、B、C、D和E是初中化学常见的五种不同类别的物质。D和F的组成元素相同,A俗称纯碱,G可用于医疗急救。它们之间的反应关系如图所示:(“一”表示物质之间可以反应,“→”表示能生成;反应条件、部分反应物和生成物已省略)。
(1)写出A、E的化学式______。
(2)写出物质D的一种用途______。
(3)写出A与B反应的化学方程式______,上图没有涉及到的基本反应类型是______。
14. 大鹏同学在学习了酸的化学性质后总结出如图所示的反应关系,图形中有公共边表示两种物质能够发生反应,A物质为稀盐酸,C为年产量最高的金属,B、C含有相同元素,A与E发生的反应为中和反应,其中E可用于治疗胃酸过多,D是大理石的主要成分,F是一种酸碱指示剂。回答下列问题:
(1)F的名称是_____;E的化学式为_____。
(2)A与B反应的化学方程式为:_________。
(3)A与C反应的实验现象为:________。
15.A~G是初中常见的物质,甲、乙、丙、丁、戊都是氧化物,G是常见的建筑材料。它们的转化关系如图所示(反应条件、部分生成物已略去)。
请回答下列问题:
(1)物质G的化学式为_____。
(2)物质丙的用途之一为_____。
(3)上述转化中没有涉及到的基本反应类型是_____。
(4)反应①的化学方程式为_____。
四、实验题
16.某化学实验小组欲探究盐酸、氢氧化钙两种物质的化学性质,取8支试管分别用A H编号后,做如下实验.
(1)实验中观察到有气泡出现的试管是________,有沉淀生成的试管是________.
(2)写出实验中无明显现象产生的试管中发生反应的化学方程式:________.
(3)实验后某试管中为红色溶液,当向其中加入过量的________后,溶液变为蓝色.由此推断,该试管中最初盛有的物质是________.
(4)实验后某试管的底部有白色固体,过滤后向滤液中滴加稀盐酸,一段时间后有气泡出现,则该滤液中的溶质是________.
(5)第二组E、F、G试管实验完成后,将反应后的液体都到入同一只大烧杯中,发现有白色沉淀生成,溶液呈红色.为此得出溶液中一定不含有的溶质是________(填写化学式,下同),一定含有的溶质是________.
(6)通过上述实验,可归纳出盐酸的化学性质有________.
17.根据如图装置图回答问题。
(1)图中标有字母X的仪器的名称:______。
(2)实验室用高锰酸钾固体制取氧气时应选择______(填代号)作为发生装置。常温下,下列收集氧气的方法不可行的是______。(填字母序号)
a向上排空气法 b向下排空气法 c排水法
(3)实验室用过氧化氢制取氧气的化学方程式是______。欲收集干燥的氧气,应在发生装置和收集装置间连接装置G,并在其中装入的药品是______;收集时气体应从______(填“①”或“②”)端通入。
(4)实验室常用装置C代替装置B制取气体,装置C的优点是______。
五、计算题
18.某同学向质量分数为7.3%的稀盐酸溶液中加入碳酸钙样品(含有杂质,且杂质不与酸反应也不溶于水),记录反应过程中有关的实验数据,最后结果如图所示。
(1)甲图中a点的pH值为______;
(2)计算样品中碳酸钙的质量分数;
(3)丙图纵坐标上b、c两点的数值分别是______、______。
19.生活中有些胃药含有氢氧化铝|【Al(OH)3】。请回答下列问题:
(1)氢氧化铝在人的胃内起的作用是 。
(2)氢氧化铝中铝、氧、氢三种元素的质量比为 (写最简比);
(3)铝元素的质量分数为 。(结果精确至0.1%)
(4)在 g氢氧化铝中含有4.8g氧元素。
20.赤铁矿石的主要成分为氧化铁。将10g赤铁矿石样品(杂质既不溶于水,也不参加反应)放入烧杯中,再加入92g稀硫酸,恰好完全反应,过滤,得到滤液和2g滤渣。请计算:
(1)赤铁矿石样品中氧化铁的质量分数。
(2)反应后所得溶液中溶质质量分数。
参考答案:
1.D 2.B 3.B 4.C 5.C 6.A 7.C 8.D 9.B 10.A 11.C
12.氨分子是不断运动的,浓氨水中的氨分子不断向四周扩散,当和酚酞试液 相遇时形成氨水,氨水显碱性,能使酚酞试液变红色。因此大烧杯中出现了一株 美丽的“铁树”
13. Na2CO3、H2 人工降雨(用作气体肥料、用作制冷剂等合理答案都得分) (或等) 分解反应
14. 紫色石蕊溶液 Al(OH)3 Fe2O3+6HCl=2FeCl3+3H2O; 有气泡产生,溶液变为浅绿色
15. CaCO3 配制溶液、洗涤衣物、灌溉农田等 置换反应和复分解反应 2KMnO4K2MnO4 + MnO2 + O2↑
16. B D G H NaOH溶液 紫色石蕊溶液 NaOH和Na2CO3 HCl NaCl 和NaOH 与酸碱指示剂反应、与活泼金属反应、与某些金属氧化物反应、与碱反应、与某些盐反应
17. 锥形瓶 A b 浓硫酸 ① 可以控制反应的发生与停止
18.(1)7;(2)75%;(3)150g;158.4g
19.(1)中和胃酸
(2)9:16:1
(3)铝元素的质量分数为:
(4)含有4.8g氧元素的氢氧化铝的质量为:
20.(1)80%;
(2)解:设生成硫酸铁的质量为x
x=20g
滤液中溶质的质量分数为100%=20%。
答:反应后所得溶液中溶质质量分数20%。
