第八单元 海水中的化学 测试题-2021-2022学年九年级化学鲁教版下册(word版 含答案)
文档属性
| 名称 | 第八单元 海水中的化学 测试题-2021-2022学年九年级化学鲁教版下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 204.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-01 00:00:00 | ||
图片预览

文档简介
第八单元《海水中的化学》测试题
一、单选题
1.下列有关盐的用途的说法错误的是
A.氯化钠是重要的调味品
B.可用亚硝酸钠代替食盐腌渍食品
C.小苏打可用于培制糕点
D.碳酸钾可用作化学肥料
2.以下是Na2CO3、NaHCO3的溶解度表。下列说法中错误的是( )
0℃ 10℃ 20℃ 30℃ 40℃ 50℃ 60℃
Na2CO3的溶解度(g/100g水) 7.1 12.5 21.5 39.7 49.0 48.5 46.0
NaHCO3的溶解度(g/100g水) 6.9 8.1 9.6 11.1 12.7 14.5 16.4
A.40℃的饱和Na2CO3溶液升温到60℃,会析出晶体
B.60℃的NaHCO3溶液蒸干并充分灼烧,可得到NaHCO3晶体
C.30℃的溶质质量分数为25%的Na2CO3溶液降温到20℃,有晶体析出
D.20℃的饱和Na2CO3溶液中通足量CO2,生成的NaHCO3会部分析出
3.粗盐含有少量的MgCl2,CaCl2,Na2SO4等杂质,为了将杂质除干净,先向粗盐溶液中分别加入过量的①NaOH②Na2CO3③BaCl2溶液,过滤,再加入④稀盐酸使溶液的pH=7将最后所得溶液进行蒸发可得到精盐,加入溶液的先后顺序错误的是( )
A.②③①④ B.③②①④ C.①③②④ D.③①②④
4.一澄清透明溶液,可能含有H+、Na+、Ba2+、Fe3+、Cl-、OH-、离子的一种或者几种,为确定溶液中可能存在的离子,进行下面实验:
①经测定,溶液的pH=1;
②取部分样品溶液滴加NaOH溶液,有沉淀生成,继续滴加NaOH溶液至不再产生沉淀为止,过滤;
③向实验②得到的溶液中滴加Na2CO3溶液,又观察到沉淀生成。
分析实验得到的以下结论中,正确的是
A.溶液中一定含有H+、Ba2+、Cl-,一定不含有Na+、Fe3+、OH-、
B.咨液中一定含有H+、Ba2+、Fe3+,一定不含有OH-,可能含有Na+、Cl-、
C.溶液中一定含有H+、Ba2+、Fe3+、Cl-,一定不含有、OH-,可能含有Na+
D.溶液中一定含有H+、Ba2+、Fe3+,一定不含有OH-、,可能含有CI-、Na+
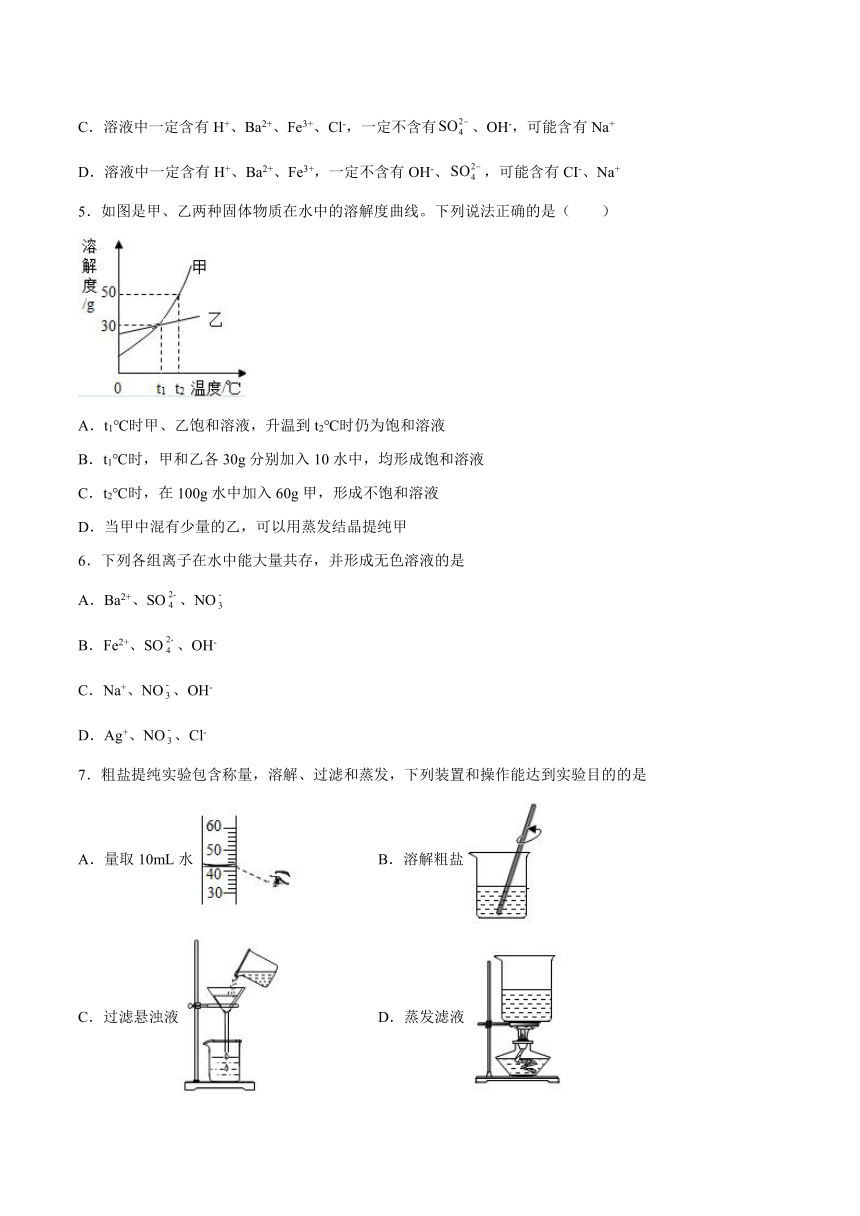
5.如图是甲、乙两种固体物质在水中的溶解度曲线。下列说法正确的是( )
A.t1℃时甲、乙饱和溶液,升温到t2℃时仍为饱和溶液
B.t1℃时,甲和乙各30g分别加入10水中,均形成饱和溶液
C.t2℃时,在100g水中加入60g甲,形成不饱和溶液
D.当甲中混有少量的乙,可以用蒸发结晶提纯甲
6.下列各组离子在水中能大量共存,并形成无色溶液的是
A.Ba2+、SO、NO
B.Fe2+、SO、OH-
C.Na+、NO、OH-
D.Ag+、NO、Cl-
7.粗盐提纯实验包含称量,溶解、过滤和蒸发,下列装置和操作能达到实验目的的是
A.量取10mL水 B.溶解粗盐
C.过滤悬浊液 D.蒸发滤液
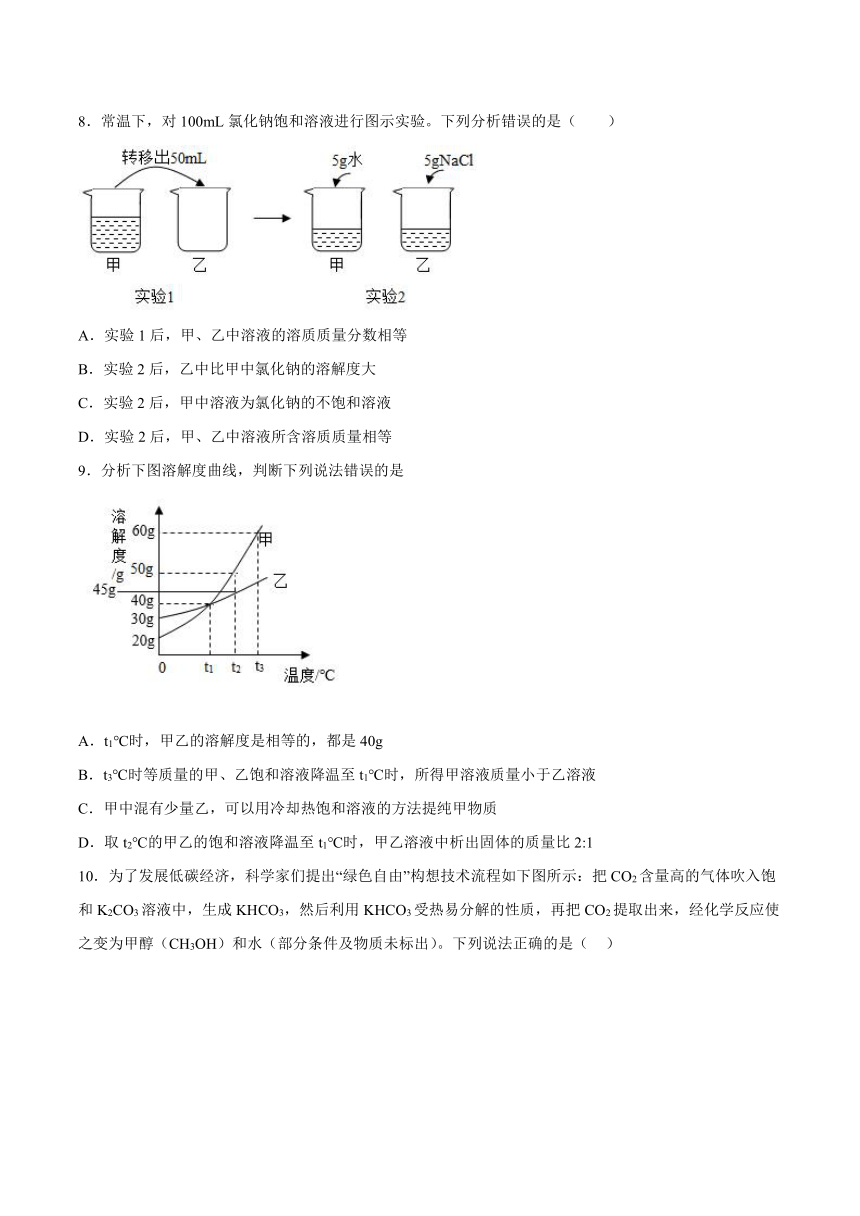
8.常温下,对100mL氯化钠饱和溶液进行图示实验。下列分析错误的是( )
A.实验1后,甲、乙中溶液的溶质质量分数相等
B.实验2后,乙中比甲中氯化钠的溶解度大
C.实验2后,甲中溶液为氯化钠的不饱和溶液
D.实验2后,甲、乙中溶液所含溶质质量相等
9.分析下图溶解度曲线,判断下列说法错误的是
A.t1℃时,甲乙的溶解度是相等的,都是40g
B.t3℃时等质量的甲、乙饱和溶液降温至t1℃时,所得甲溶液质量小于乙溶液
C.甲中混有少量乙,可以用冷却热饱和溶液的方法提纯甲物质
D.取t2℃的甲乙的饱和溶液降温至t1℃时,甲乙溶液中析出固体的质量比2:1
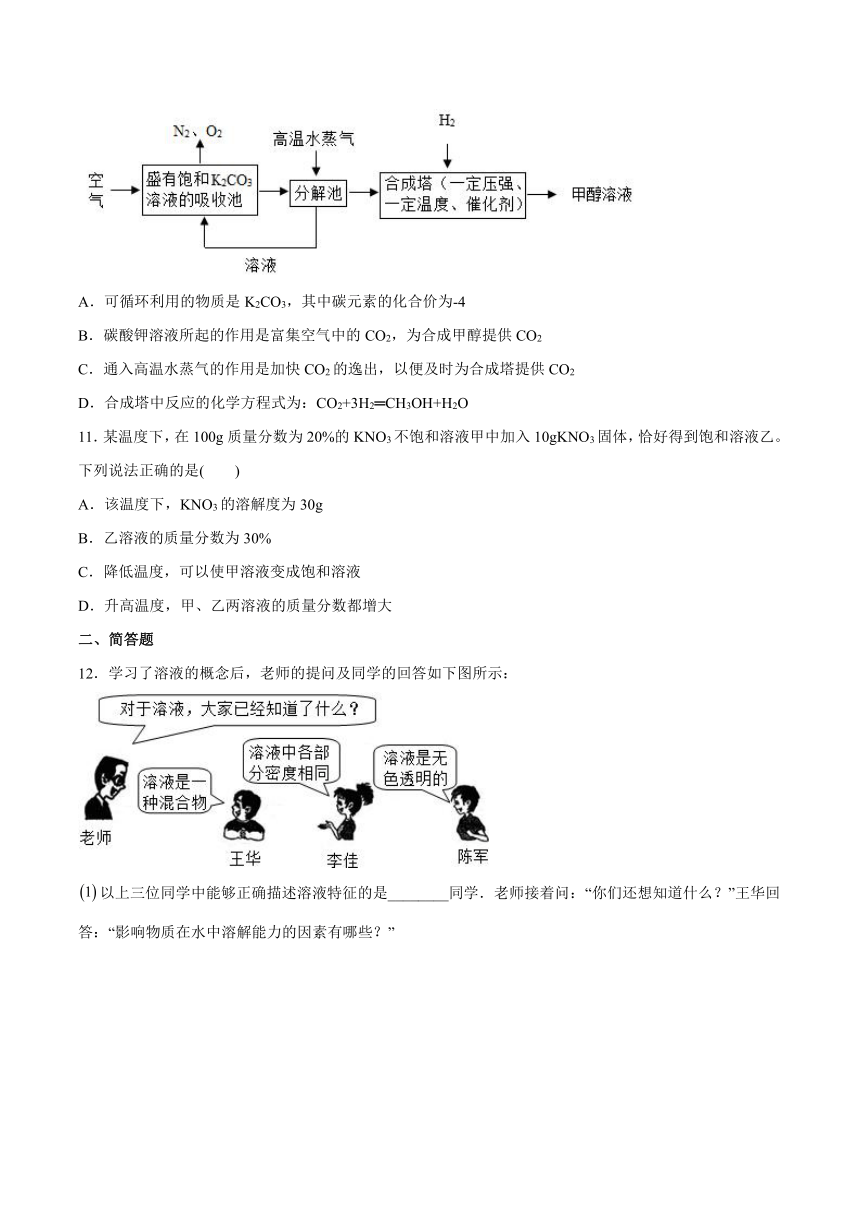
10.为了发展低碳经济,科学家们提出“绿色自由”构想技术流程如下图所示:把CO2含量高的气体吹入饱和K2CO3溶液中,生成KHCO3,然后利用KHCO3受热易分解的性质,再把CO2提取出来,经化学反应使之变为甲醇(CH3OH)和水(部分条件及物质未标出)。下列说法正确的是( )
A.可循环利用的物质是K2CO3,其中碳元素的化合价为-4
B.碳酸钾溶液所起的作用是富集空气中的CO2,为合成甲醇提供CO2
C.通入高温水蒸气的作用是加快CO2的逸出,以便及时为合成塔提供CO2
D.合成塔中反应的化学方程式为:CO2+3H2═CH3OH+H2O
11.某温度下,在100g质量分数为20%的KNO3不饱和溶液甲中加入10gKNO3固体,恰好得到饱和溶液乙。下列说法正确的是( )
A.该温度下,KNO3的溶解度为30g
B.乙溶液的质量分数为30%
C.降低温度,可以使甲溶液变成饱和溶液
D.升高温度,甲、乙两溶液的质量分数都增大
二、简答题
12.学习了溶液的概念后,老师的提问及同学的回答如下图所示:
以上三位同学中能够正确描述溶液特征的是________同学.老师接着问:“你们还想知道什么?”王华回答:“影响物质在水中溶解能力的因素有哪些?”
针对王华的问题,老师引导同学们进行了一系列探究,下表列出了从探究实验中获取的部分数据,请你根据这些下表中的数据,在右边的坐标图中绘制、两物质的溶解度曲线(图中注明、).________
温度
溶解度 物质
物质
该实验主要探究了温度对固体物质溶解度的影响,在一定温度范围内,物质的饱和溶液溶质质量分数大于物质的饱和溶液溶质质量分数,该温度范围是________.
将在゜时等量的、饱和溶液同时降温到゜,则析出晶体的质量________(填“大于”、“等于”或“小于”).
在゜时,向水中加入物质充分溶解后,形成的物质溶液质量是________.
三、推断题
13.有一包固体物质,可能含有硫酸钠、碳酸钠、氯化钙、氯化钾、氯化铁和氢氧化钠中的一种或几种。为探究这包固体物质组成,进行了以下实验。
(1)据①可知固体中一定不含有______。
(2)取白色沉淀B于烧杯中并逐滴加入稀硝酸,烧杯中沉淀质量随滴加稀硝酸质量的变化如图乙所示,由此确定原固体中一定含有______。
(3)取无色溶液C向其中通入二氧化碳气体,产生白色沉淀, 无色溶液C中一定含有的离子是______ (填离子符号)。
(4)为确定原固体中可能含有的物质是否存在的实验方案是______ (写明操作、现象和结论)。
14.酸、碱、盐在生产生活中具有广泛的用途。
(1)某公司生产的融雪剂可能含有NaCl、NaNO3、MgCl2、FeSO4、NaOH中的一种或几种物质。小明为探究其成分,设计并完成下列实验:
请根据以上设计过程,回答下列问题:
(1)该融雪剂中一定不含有___________(写化学式,下同);一定含有___________;可能含有___________。
(2)有A、B、C三种物质,已知A为钠盐,B为氯化物,C为碱,经下列实验操作,其结果分别是:
①A、B的溶液混合后无沉淀或气体产生
②B、C的溶液混合后出现蓝色沉淀
③A、C的溶液混合后出现白色沉淀,该沉淀不溶于稀HNO3
则A为___________,C为___________(填化学式)。
四、实验题
15.M是硝酸钾或氯化铵中的一种,硝酸钾和氯化铵的溶解度曲线如图1所示,某化学兴趣小组用物质M进行了如图2所示的实验。
(1)t1℃时,氯化铵的溶解度为_____g;
(2)烧杯①中溶质质量分数的计算式为_____;
(3)物质M是_____。
16.如图1是A、B、C三种物质的溶解度曲线图。请回答:
(1)t1℃时,A、B、C三种物质的饱和溶液中溶质质量分数最大的是______。
(2)t2℃时,将30gA物质放入50g水中,充分溶解后所得溶液的质量是______g。
(3)A物质中混有少量的B物质,若提纯A物质,可采用的结晶方法是____。
(4)t1℃时,取等质量的A、C饱和溶液分别置于甲、乙两支试管中,如图2所示,在大烧杯中加入一定质量的氢氧化钠固体溶解后,A、C溶液的溶质质量分数的大小关系是______。
五、计算题
17.家庭中常用洁厕剂的有效成分是盐酸。小明同学想测定某品牌洁厕剂中氯化氢的质量分数,他将足量的石灰石加入洁厕剂样品中(石灰石中的杂质既不与酸反应,也不溶于水),有关实验数据如下表:
反应前 反应后
实验数据 洁厕剂样 品的质量 加入石灰 石的质量 剩余物的总质量
36.5 g 25 g 57.1 g
请计算:
(1)反应后生成二氧化碳的质量为________。
(2)该洁厕剂中氯化氢的质量分数为________。
18.向160g硫酸铜溶液中,逐滴加入40g NaOH溶液,恰好完全反应,生成4.9g沉淀,回答下列问题:
(1)恰好完全反应后,溶液的质量为 g。
(2)将反应结束后的混合物过滤,滤液中溶质是 (填化学式)。
(3)求原硫酸铜溶液中溶质的质量分数(写出计算过程)。
19.把100克铁棒放入硫酸铜溶液里,过一会儿取出、洗净、干燥,铁棒的质量增加到103克。请计算:
(1)硫酸铜中铜元素、硫元素和氧元素的质量比为______。
(2)该反应生成铜的质量是多少?
参考答案:
1.B 2.B 3.A 4.C 5.B 6.C 7.B 8.B 9.D 10.B 11.C
12. 李佳、王华 小于
13. 氯化铁(或FeCl3) 碳酸钠和硫酸钠(或:Na2CO3和Na2SO4) 取适量无色溶液C于试管中,加入硝酸银溶液,再加入过量的稀硝酸,仍然有白色沉淀,证明有氯化钾。
14. FeSO4、NaOH MgCl2 NaCl、NaNO3 Na2SO4 Ba(OH)2
15. 40 KNO3
16. B 75 降温结晶 A>C
17.(1)4.4 g(2)20%
18.(1)195.1g
(2)Na2SO4
(3)5%
19.(1)2:1:2
(2)解:生成铜的质量为x。
答:生成铜的质量24g。
一、单选题
1.下列有关盐的用途的说法错误的是
A.氯化钠是重要的调味品
B.可用亚硝酸钠代替食盐腌渍食品
C.小苏打可用于培制糕点
D.碳酸钾可用作化学肥料
2.以下是Na2CO3、NaHCO3的溶解度表。下列说法中错误的是( )
0℃ 10℃ 20℃ 30℃ 40℃ 50℃ 60℃
Na2CO3的溶解度(g/100g水) 7.1 12.5 21.5 39.7 49.0 48.5 46.0
NaHCO3的溶解度(g/100g水) 6.9 8.1 9.6 11.1 12.7 14.5 16.4
A.40℃的饱和Na2CO3溶液升温到60℃,会析出晶体
B.60℃的NaHCO3溶液蒸干并充分灼烧,可得到NaHCO3晶体
C.30℃的溶质质量分数为25%的Na2CO3溶液降温到20℃,有晶体析出
D.20℃的饱和Na2CO3溶液中通足量CO2,生成的NaHCO3会部分析出
3.粗盐含有少量的MgCl2,CaCl2,Na2SO4等杂质,为了将杂质除干净,先向粗盐溶液中分别加入过量的①NaOH②Na2CO3③BaCl2溶液,过滤,再加入④稀盐酸使溶液的pH=7将最后所得溶液进行蒸发可得到精盐,加入溶液的先后顺序错误的是( )
A.②③①④ B.③②①④ C.①③②④ D.③①②④
4.一澄清透明溶液,可能含有H+、Na+、Ba2+、Fe3+、Cl-、OH-、离子的一种或者几种,为确定溶液中可能存在的离子,进行下面实验:
①经测定,溶液的pH=1;
②取部分样品溶液滴加NaOH溶液,有沉淀生成,继续滴加NaOH溶液至不再产生沉淀为止,过滤;
③向实验②得到的溶液中滴加Na2CO3溶液,又观察到沉淀生成。
分析实验得到的以下结论中,正确的是
A.溶液中一定含有H+、Ba2+、Cl-,一定不含有Na+、Fe3+、OH-、
B.咨液中一定含有H+、Ba2+、Fe3+,一定不含有OH-,可能含有Na+、Cl-、
C.溶液中一定含有H+、Ba2+、Fe3+、Cl-,一定不含有、OH-,可能含有Na+
D.溶液中一定含有H+、Ba2+、Fe3+,一定不含有OH-、,可能含有CI-、Na+
5.如图是甲、乙两种固体物质在水中的溶解度曲线。下列说法正确的是( )
A.t1℃时甲、乙饱和溶液,升温到t2℃时仍为饱和溶液
B.t1℃时,甲和乙各30g分别加入10水中,均形成饱和溶液
C.t2℃时,在100g水中加入60g甲,形成不饱和溶液
D.当甲中混有少量的乙,可以用蒸发结晶提纯甲
6.下列各组离子在水中能大量共存,并形成无色溶液的是
A.Ba2+、SO、NO
B.Fe2+、SO、OH-
C.Na+、NO、OH-
D.Ag+、NO、Cl-
7.粗盐提纯实验包含称量,溶解、过滤和蒸发,下列装置和操作能达到实验目的的是
A.量取10mL水 B.溶解粗盐
C.过滤悬浊液 D.蒸发滤液
8.常温下,对100mL氯化钠饱和溶液进行图示实验。下列分析错误的是( )
A.实验1后,甲、乙中溶液的溶质质量分数相等
B.实验2后,乙中比甲中氯化钠的溶解度大
C.实验2后,甲中溶液为氯化钠的不饱和溶液
D.实验2后,甲、乙中溶液所含溶质质量相等
9.分析下图溶解度曲线,判断下列说法错误的是
A.t1℃时,甲乙的溶解度是相等的,都是40g
B.t3℃时等质量的甲、乙饱和溶液降温至t1℃时,所得甲溶液质量小于乙溶液
C.甲中混有少量乙,可以用冷却热饱和溶液的方法提纯甲物质
D.取t2℃的甲乙的饱和溶液降温至t1℃时,甲乙溶液中析出固体的质量比2:1
10.为了发展低碳经济,科学家们提出“绿色自由”构想技术流程如下图所示:把CO2含量高的气体吹入饱和K2CO3溶液中,生成KHCO3,然后利用KHCO3受热易分解的性质,再把CO2提取出来,经化学反应使之变为甲醇(CH3OH)和水(部分条件及物质未标出)。下列说法正确的是( )
A.可循环利用的物质是K2CO3,其中碳元素的化合价为-4
B.碳酸钾溶液所起的作用是富集空气中的CO2,为合成甲醇提供CO2
C.通入高温水蒸气的作用是加快CO2的逸出,以便及时为合成塔提供CO2
D.合成塔中反应的化学方程式为:CO2+3H2═CH3OH+H2O
11.某温度下,在100g质量分数为20%的KNO3不饱和溶液甲中加入10gKNO3固体,恰好得到饱和溶液乙。下列说法正确的是( )
A.该温度下,KNO3的溶解度为30g
B.乙溶液的质量分数为30%
C.降低温度,可以使甲溶液变成饱和溶液
D.升高温度,甲、乙两溶液的质量分数都增大
二、简答题
12.学习了溶液的概念后,老师的提问及同学的回答如下图所示:
以上三位同学中能够正确描述溶液特征的是________同学.老师接着问:“你们还想知道什么?”王华回答:“影响物质在水中溶解能力的因素有哪些?”
针对王华的问题,老师引导同学们进行了一系列探究,下表列出了从探究实验中获取的部分数据,请你根据这些下表中的数据,在右边的坐标图中绘制、两物质的溶解度曲线(图中注明、).________
温度
溶解度 物质
物质
该实验主要探究了温度对固体物质溶解度的影响,在一定温度范围内,物质的饱和溶液溶质质量分数大于物质的饱和溶液溶质质量分数,该温度范围是________.
将在゜时等量的、饱和溶液同时降温到゜,则析出晶体的质量________(填“大于”、“等于”或“小于”).
在゜时,向水中加入物质充分溶解后,形成的物质溶液质量是________.
三、推断题
13.有一包固体物质,可能含有硫酸钠、碳酸钠、氯化钙、氯化钾、氯化铁和氢氧化钠中的一种或几种。为探究这包固体物质组成,进行了以下实验。
(1)据①可知固体中一定不含有______。
(2)取白色沉淀B于烧杯中并逐滴加入稀硝酸,烧杯中沉淀质量随滴加稀硝酸质量的变化如图乙所示,由此确定原固体中一定含有______。
(3)取无色溶液C向其中通入二氧化碳气体,产生白色沉淀, 无色溶液C中一定含有的离子是______ (填离子符号)。
(4)为确定原固体中可能含有的物质是否存在的实验方案是______ (写明操作、现象和结论)。
14.酸、碱、盐在生产生活中具有广泛的用途。
(1)某公司生产的融雪剂可能含有NaCl、NaNO3、MgCl2、FeSO4、NaOH中的一种或几种物质。小明为探究其成分,设计并完成下列实验:
请根据以上设计过程,回答下列问题:
(1)该融雪剂中一定不含有___________(写化学式,下同);一定含有___________;可能含有___________。
(2)有A、B、C三种物质,已知A为钠盐,B为氯化物,C为碱,经下列实验操作,其结果分别是:
①A、B的溶液混合后无沉淀或气体产生
②B、C的溶液混合后出现蓝色沉淀
③A、C的溶液混合后出现白色沉淀,该沉淀不溶于稀HNO3
则A为___________,C为___________(填化学式)。
四、实验题
15.M是硝酸钾或氯化铵中的一种,硝酸钾和氯化铵的溶解度曲线如图1所示,某化学兴趣小组用物质M进行了如图2所示的实验。
(1)t1℃时,氯化铵的溶解度为_____g;
(2)烧杯①中溶质质量分数的计算式为_____;
(3)物质M是_____。
16.如图1是A、B、C三种物质的溶解度曲线图。请回答:
(1)t1℃时,A、B、C三种物质的饱和溶液中溶质质量分数最大的是______。
(2)t2℃时,将30gA物质放入50g水中,充分溶解后所得溶液的质量是______g。
(3)A物质中混有少量的B物质,若提纯A物质,可采用的结晶方法是____。
(4)t1℃时,取等质量的A、C饱和溶液分别置于甲、乙两支试管中,如图2所示,在大烧杯中加入一定质量的氢氧化钠固体溶解后,A、C溶液的溶质质量分数的大小关系是______。
五、计算题
17.家庭中常用洁厕剂的有效成分是盐酸。小明同学想测定某品牌洁厕剂中氯化氢的质量分数,他将足量的石灰石加入洁厕剂样品中(石灰石中的杂质既不与酸反应,也不溶于水),有关实验数据如下表:
反应前 反应后
实验数据 洁厕剂样 品的质量 加入石灰 石的质量 剩余物的总质量
36.5 g 25 g 57.1 g
请计算:
(1)反应后生成二氧化碳的质量为________。
(2)该洁厕剂中氯化氢的质量分数为________。
18.向160g硫酸铜溶液中,逐滴加入40g NaOH溶液,恰好完全反应,生成4.9g沉淀,回答下列问题:
(1)恰好完全反应后,溶液的质量为 g。
(2)将反应结束后的混合物过滤,滤液中溶质是 (填化学式)。
(3)求原硫酸铜溶液中溶质的质量分数(写出计算过程)。
19.把100克铁棒放入硫酸铜溶液里,过一会儿取出、洗净、干燥,铁棒的质量增加到103克。请计算:
(1)硫酸铜中铜元素、硫元素和氧元素的质量比为______。
(2)该反应生成铜的质量是多少?
参考答案:
1.B 2.B 3.A 4.C 5.B 6.C 7.B 8.B 9.D 10.B 11.C
12. 李佳、王华 小于
13. 氯化铁(或FeCl3) 碳酸钠和硫酸钠(或:Na2CO3和Na2SO4) 取适量无色溶液C于试管中,加入硝酸银溶液,再加入过量的稀硝酸,仍然有白色沉淀,证明有氯化钾。
14. FeSO4、NaOH MgCl2 NaCl、NaNO3 Na2SO4 Ba(OH)2
15. 40 KNO3
16. B 75 降温结晶 A>C
17.(1)4.4 g(2)20%
18.(1)195.1g
(2)Na2SO4
(3)5%
19.(1)2:1:2
(2)解:生成铜的质量为x。
答:生成铜的质量24g。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
