专题8 金属和金属材料测试题—2021-2022学年九年级化学仁爱版下学期(word版有答案)
文档属性
| 名称 | 专题8 金属和金属材料测试题—2021-2022学年九年级化学仁爱版下学期(word版有答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 134.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 仁爱科普版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-03 00:00:00 | ||
图片预览


文档简介
专题8《金属和金属材料》检测题
一、单选题
1.把一枚无锈铁钉放在硫酸铜溶液中,一段时间后,可出现的是
A.溶液蓝色变浅直至无色 B.铁钉表面析出红色物质
C.产生大量气泡 D.溶液质量增加
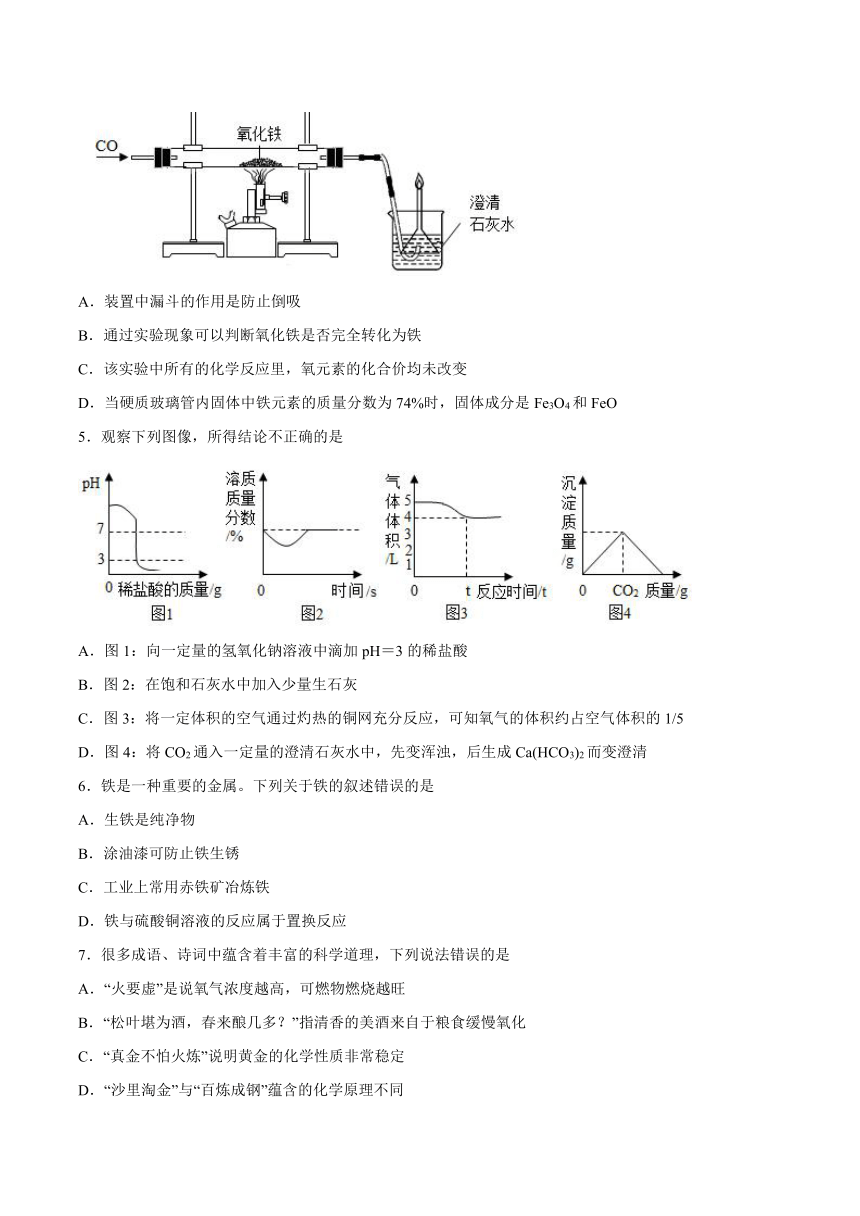
2.如图是某化学兴趣小组设计的观察铁制品锈蚀的实验装置。下列相关叙述中正确的是( )
①一段时间后,铁丝会由下向上出现锈蚀现象
②一段时间后,水面处铁丝锈蚀严重
③一段时间后,塑料瓶会变膨胀,因为铁生锈要放热
④一段时间后,塑料瓶会变瘪,因为铁生锈与空气有关
A.①② B.②④ C.②③ D.③④
3.通过对比实验可探究铁生锈的条件。下列实验设计与探究条件的对应关系正确的是
A.甲和乙:水
B.乙和丙:空气
C.甲和丙:空气
D.甲和丁:水
4.用一氧化碳还原氧化铁的实验中,Fe2O3转化为铁的具体过程是: 。已知铁的氧化物除Fe2O3外,其余均为黑色。下列说法正确的是
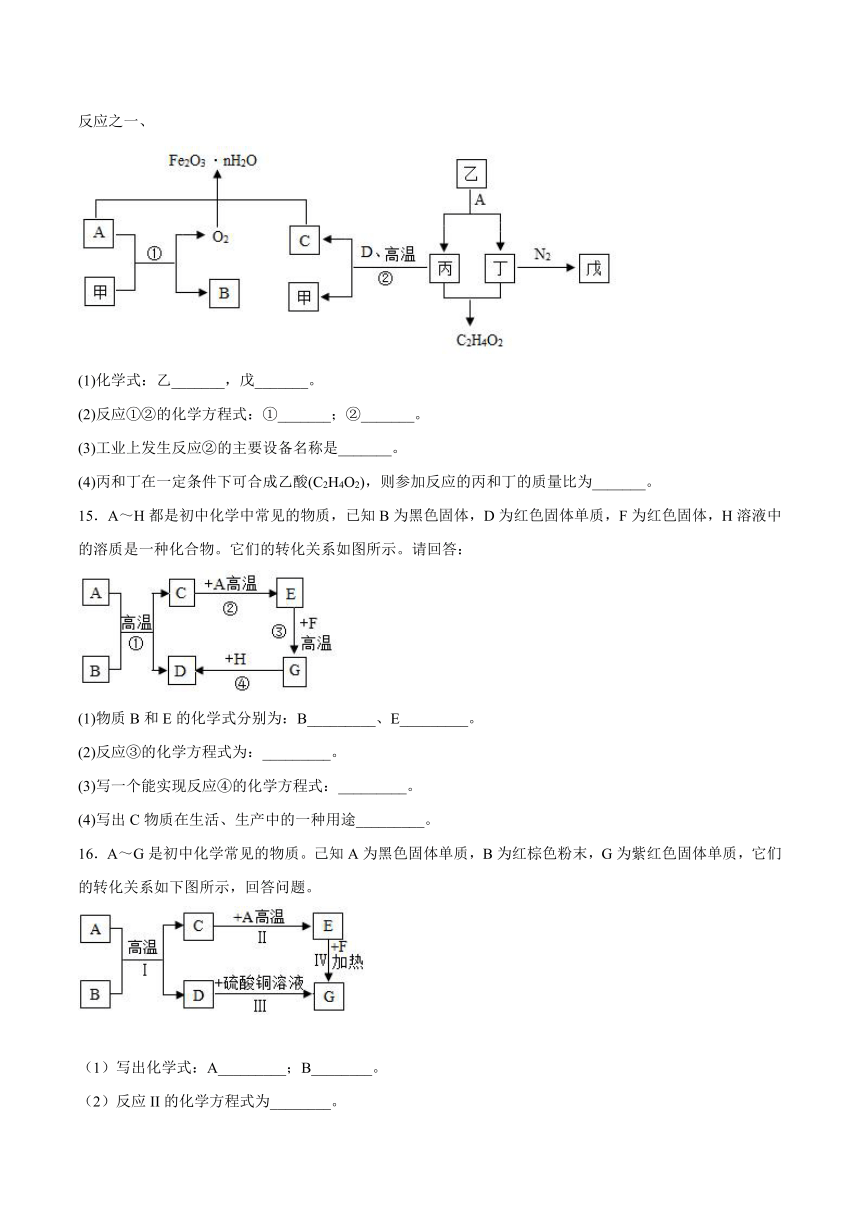
A.装置中漏斗的作用是防止倒吸
B.通过实验现象可以判断氧化铁是否完全转化为铁
C.该实验中所有的化学反应里,氧元素的化合价均未改变
D.当硬质玻璃管内固体中铁元素的质量分数为74%时,固体成分是Fe3O4和FeO
5.观察下列图像,所得结论不正确的是
A.图1:向一定量的氢氧化钠溶液中滴加pH=3的稀盐酸
B.图2:在饱和石灰水中加入少量生石灰
C.图3:将一定体积的空气通过灼热的铜网充分反应,可知氧气的体积约占空气体积的1/5
D.图4:将CO2通入一定量的澄清石灰水中,先变浑浊,后生成Ca(HCO3)2而变澄清
6.铁是一种重要的金属。下列关于铁的叙述错误的是
A.生铁是纯净物
B.涂油漆可防止铁生锈
C.工业上常用赤铁矿冶炼铁
D.铁与硫酸铜溶液的反应属于置换反应
7.很多成语、诗词中蕴含着丰富的科学道理,下列说法错误的是
A.“火要虚”是说氧气浓度越高,可燃物燃烧越旺
B.“松叶堪为酒,春来酿几多?”指清香的美酒来自于粮食缓慢氧化
C.“真金不怕火炼”说明黄金的化学性质非常稳定
D.“沙里淘金”与“百炼成钢”蕴含的化学原理不同
8.下列物质的转化中,不能由两种单质直接制得的是
A.H2→H2O B.Fe→FeCl2 C.P→P2O5 D.Al→Al2O3
9.下列措施中,不能防止金属制品锈蚀的是
A.在表面刷漆
B.改用不锈钢
C.在表面镀铬
D.用湿布擦拭
10.为了验证镁、铜、银三种金属的活动性顺序,某同学设计了如下实验,只需进行其中三个就能达到实验目的,你认为不必进行的是
A.将镁片放入稀盐酸中
B.将铜片放入稀盐酸中
C.将镁片放入硝酸银溶液中
D.将铜片放入硝酸银溶液中
11.将一定质量的铁粉加入到Mg(NO3)2、AgNO3的混合溶液中,充分反应后过滤,得到滤液和滤渣。向滤液中加入稀盐酸,无明显现象。下列叙述正确的是( )
A.滤液中一定含有Mg2+和Fe3+
B.滤液中含有Mg2+和Ag+
C.滤渣中一定含有Ag
D.滤渣中可能含有Mg
12.下列物质所对应的用途不正确的是( )
A.大理石﹣﹣用作建筑材料 B.钛合金﹣﹣制造人造骨
C.熟石灰﹣﹣改良酸性土壤 D.氢氧化钠﹣﹣治疗胃酸过多
二、简答题
13.请你判断,下列家庭小实验“能”或“不能”达到预期目的,并说明其理由。
(1)“品尝”:鉴别厨房中的白糖和食盐________________。
(2)“加食醋”:鉴别苏打和食盐___________________________。
(3)“观察”:鉴别黄铜和黄金___________________________。
三、推断题
14.如图为某些物质间的转化关系部分条件已略去。甲、乙、丙、丁、戊均为气体,乙是最简单的有机物,丙有毒,戊能使湿润的红色石蕊试纸变蓝,D是磁铁矿的主要成分。反应①是自然界普遍存在的重要反应之一、
(1)化学式:乙_______,戊_______。
(2)反应①②的化学方程式:①_______;②_______。
(3)工业上发生反应②的主要设备名称是_______。
(4)丙和丁在一定条件下可合成乙酸(C2H4O2),则参加反应的丙和丁的质量比为_______。
15.A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种化合物。它们的转化关系如图所示。请回答:
(1)物质B和E的化学式分别为:B_________、E_________。
(2)反应③的化学方程式为:_________。
(3)写一个能实现反应④的化学方程式:_________。
(4)写出C物质在生活、生产中的一种用途_________。
16.A~G是初中化学常见的物质。己知A为黑色固体单质,B为红棕色粉末,G为紫红色固体单质,它们的转化关系如下图所示,回答问题。
(1)写出化学式:A_________;B________。
(2)反应II的化学方程式为________。
(3)反应III的化学方程式为________。
四、实验题
17.某校实验室有一瓶久置的铁屑,其成分是铁、氧化铁和水。为测定其中各成分的质量分数,某兴趣小组按下图所示装置进行实验(装置气密性良好;固定装置已略去;氮气不与铁屑中的成分反应;碱石灰是氧化钙和氢氧化钠的混合物)。
部分实验步骤如下:
Ⅰ.称量硬质玻璃管的质量。将样品放入硬质玻璃管中,称量硬质玻璃管和样品的质量。
II.连接好装置。缓缓通入N2,点燃甲处的酒精喷灯,待硬质玻璃管中固体恒重,记录硬质玻璃管和剩余固体的质量。
Ⅲ.再次连接好装置,继续实验。通入CO,点燃丙处的酒精灯和甲处的酒精喷灯。待硬质玻璃管中固体恒重,熄灭酒精喷灯,继续通入CO直至硬质玻璃管冷却。再次记录硬质玻璃管和剩余固体的质量。
实验数据记录如下表:
硬质玻璃管 硬质玻璃管和样品 步骤II硬质玻璃 管和剩余固体 步骤步骤Ⅲ硬质玻璃 管和剩余固体
质量 m1 m2 m3 m4
请回答下列问题:
(1)步骤Ⅲ丙处酒精灯的作用是____________。
(2)步骤Ⅲ硬质玻璃管中反应的化学方程式为________。
(3)样品中氧化铁的质量分数为_____(用m1、m2、m3、m4的代数式表示)。若步骤Ⅲ中氧化铁没有完全反应,样品中水的质量分数测量结果将______(填“偏大”“偏小”或“不变”)。
(4)有关样品,下列说法正确的是_____(填字母标号)。
A样品中氢元素的质量为1/9(m2- m3) B样品中铁单质和氧化铁的质量总和为m3-m1
C样品中铁单质的质量为m4-m1 D样品中氧元素的质量为m3- m4
五、计算题
18.某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的组成,取黄铜样品50g放入锥形瓶中,向其中分5次共加入250克稀硫酸,测得数据记录如下表:
1 第1次 第2次 第3次 第4次 第5次
累计加入稀硫酸的质量/g 50 100 150 200 250
累计产生气体的质量/g 0.2 m 0.6 0.7 0.7
(1)表中m=______g;
(2)黄铜样品中铜的质量分数______;
(3)求所用稀硫酸中溶质的质量分数?(写出计算过程)
19.向盛有一定质量稀硫酸的烧杯中逐渐加入10g锌粒,产生气体质量与锌粒质量的关系如图所示,充分反应后,称得烧杯中剩余物质总质量为109.8g,请根据关系图分析并计算:
(1)稀硫酸反应完时,产生氢气的质量为_____g。
(2)该稀硫酸中溶质的质量分数_____(写出计算过程)。
参考答案:
1.B 2.B 3.D 4.D 5.A 6.A 7.A 8.B 9.D 10.C 11.C 12.D
13. 能,白糖有甜味,食盐有咸味 能,食醋中的醋酸与苏打中的碳酸钠能反应有气泡冒出,醋酸与食盐中的氯化钠不反应,没有气泡冒出; 不能,黄铜和黄金都呈黄色。
14. CH4 NH3 6CO2+6H2OC6H12O6+6O2 Fe3O4+4CO3Fe+4CO2 高炉 14:1
15. CuO、 CO 3CO+Fe2O32Fe+3CO2 Fe+CuCl2=FeCl2+Cu 灭火(或制汽水)
16. C Fe2O3
17. 把一氧化碳转化成二氧化碳,防止污染环境 ×100% 不变 AB
18.(1)0.4
(2)54.5%
(3)解:设50g稀硫酸中硫酸的质量为
=9.8g
所用稀硫酸中溶质的质量分数为×100%=19.6%
答:所用稀硫酸中溶质的质量分数为19.6%。
19.(1)由图可知,稀硫酸反应完时,产生氢气的质量为0.2g。
(2)设稀硫酸中溶质的质量为x,
,x=9.8g,
该稀硫酸中溶质的质量分数为。
答:该稀硫酸中溶质的质量分数是9.8%。
一、单选题
1.把一枚无锈铁钉放在硫酸铜溶液中,一段时间后,可出现的是
A.溶液蓝色变浅直至无色 B.铁钉表面析出红色物质
C.产生大量气泡 D.溶液质量增加
2.如图是某化学兴趣小组设计的观察铁制品锈蚀的实验装置。下列相关叙述中正确的是( )
①一段时间后,铁丝会由下向上出现锈蚀现象
②一段时间后,水面处铁丝锈蚀严重
③一段时间后,塑料瓶会变膨胀,因为铁生锈要放热
④一段时间后,塑料瓶会变瘪,因为铁生锈与空气有关
A.①② B.②④ C.②③ D.③④
3.通过对比实验可探究铁生锈的条件。下列实验设计与探究条件的对应关系正确的是
A.甲和乙:水
B.乙和丙:空气
C.甲和丙:空气
D.甲和丁:水
4.用一氧化碳还原氧化铁的实验中,Fe2O3转化为铁的具体过程是: 。已知铁的氧化物除Fe2O3外,其余均为黑色。下列说法正确的是
A.装置中漏斗的作用是防止倒吸
B.通过实验现象可以判断氧化铁是否完全转化为铁
C.该实验中所有的化学反应里,氧元素的化合价均未改变
D.当硬质玻璃管内固体中铁元素的质量分数为74%时,固体成分是Fe3O4和FeO
5.观察下列图像,所得结论不正确的是
A.图1:向一定量的氢氧化钠溶液中滴加pH=3的稀盐酸
B.图2:在饱和石灰水中加入少量生石灰
C.图3:将一定体积的空气通过灼热的铜网充分反应,可知氧气的体积约占空气体积的1/5
D.图4:将CO2通入一定量的澄清石灰水中,先变浑浊,后生成Ca(HCO3)2而变澄清
6.铁是一种重要的金属。下列关于铁的叙述错误的是
A.生铁是纯净物
B.涂油漆可防止铁生锈
C.工业上常用赤铁矿冶炼铁
D.铁与硫酸铜溶液的反应属于置换反应
7.很多成语、诗词中蕴含着丰富的科学道理,下列说法错误的是
A.“火要虚”是说氧气浓度越高,可燃物燃烧越旺
B.“松叶堪为酒,春来酿几多?”指清香的美酒来自于粮食缓慢氧化
C.“真金不怕火炼”说明黄金的化学性质非常稳定
D.“沙里淘金”与“百炼成钢”蕴含的化学原理不同
8.下列物质的转化中,不能由两种单质直接制得的是
A.H2→H2O B.Fe→FeCl2 C.P→P2O5 D.Al→Al2O3
9.下列措施中,不能防止金属制品锈蚀的是
A.在表面刷漆
B.改用不锈钢
C.在表面镀铬
D.用湿布擦拭
10.为了验证镁、铜、银三种金属的活动性顺序,某同学设计了如下实验,只需进行其中三个就能达到实验目的,你认为不必进行的是
A.将镁片放入稀盐酸中
B.将铜片放入稀盐酸中
C.将镁片放入硝酸银溶液中
D.将铜片放入硝酸银溶液中
11.将一定质量的铁粉加入到Mg(NO3)2、AgNO3的混合溶液中,充分反应后过滤,得到滤液和滤渣。向滤液中加入稀盐酸,无明显现象。下列叙述正确的是( )
A.滤液中一定含有Mg2+和Fe3+
B.滤液中含有Mg2+和Ag+
C.滤渣中一定含有Ag
D.滤渣中可能含有Mg
12.下列物质所对应的用途不正确的是( )
A.大理石﹣﹣用作建筑材料 B.钛合金﹣﹣制造人造骨
C.熟石灰﹣﹣改良酸性土壤 D.氢氧化钠﹣﹣治疗胃酸过多
二、简答题
13.请你判断,下列家庭小实验“能”或“不能”达到预期目的,并说明其理由。
(1)“品尝”:鉴别厨房中的白糖和食盐________________。
(2)“加食醋”:鉴别苏打和食盐___________________________。
(3)“观察”:鉴别黄铜和黄金___________________________。
三、推断题
14.如图为某些物质间的转化关系部分条件已略去。甲、乙、丙、丁、戊均为气体,乙是最简单的有机物,丙有毒,戊能使湿润的红色石蕊试纸变蓝,D是磁铁矿的主要成分。反应①是自然界普遍存在的重要反应之一、
(1)化学式:乙_______,戊_______。
(2)反应①②的化学方程式:①_______;②_______。
(3)工业上发生反应②的主要设备名称是_______。
(4)丙和丁在一定条件下可合成乙酸(C2H4O2),则参加反应的丙和丁的质量比为_______。
15.A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种化合物。它们的转化关系如图所示。请回答:
(1)物质B和E的化学式分别为:B_________、E_________。
(2)反应③的化学方程式为:_________。
(3)写一个能实现反应④的化学方程式:_________。
(4)写出C物质在生活、生产中的一种用途_________。
16.A~G是初中化学常见的物质。己知A为黑色固体单质,B为红棕色粉末,G为紫红色固体单质,它们的转化关系如下图所示,回答问题。
(1)写出化学式:A_________;B________。
(2)反应II的化学方程式为________。
(3)反应III的化学方程式为________。
四、实验题
17.某校实验室有一瓶久置的铁屑,其成分是铁、氧化铁和水。为测定其中各成分的质量分数,某兴趣小组按下图所示装置进行实验(装置气密性良好;固定装置已略去;氮气不与铁屑中的成分反应;碱石灰是氧化钙和氢氧化钠的混合物)。
部分实验步骤如下:
Ⅰ.称量硬质玻璃管的质量。将样品放入硬质玻璃管中,称量硬质玻璃管和样品的质量。
II.连接好装置。缓缓通入N2,点燃甲处的酒精喷灯,待硬质玻璃管中固体恒重,记录硬质玻璃管和剩余固体的质量。
Ⅲ.再次连接好装置,继续实验。通入CO,点燃丙处的酒精灯和甲处的酒精喷灯。待硬质玻璃管中固体恒重,熄灭酒精喷灯,继续通入CO直至硬质玻璃管冷却。再次记录硬质玻璃管和剩余固体的质量。
实验数据记录如下表:
硬质玻璃管 硬质玻璃管和样品 步骤II硬质玻璃 管和剩余固体 步骤步骤Ⅲ硬质玻璃 管和剩余固体
质量 m1 m2 m3 m4
请回答下列问题:
(1)步骤Ⅲ丙处酒精灯的作用是____________。
(2)步骤Ⅲ硬质玻璃管中反应的化学方程式为________。
(3)样品中氧化铁的质量分数为_____(用m1、m2、m3、m4的代数式表示)。若步骤Ⅲ中氧化铁没有完全反应,样品中水的质量分数测量结果将______(填“偏大”“偏小”或“不变”)。
(4)有关样品,下列说法正确的是_____(填字母标号)。
A样品中氢元素的质量为1/9(m2- m3) B样品中铁单质和氧化铁的质量总和为m3-m1
C样品中铁单质的质量为m4-m1 D样品中氧元素的质量为m3- m4
五、计算题
18.某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的组成,取黄铜样品50g放入锥形瓶中,向其中分5次共加入250克稀硫酸,测得数据记录如下表:
1 第1次 第2次 第3次 第4次 第5次
累计加入稀硫酸的质量/g 50 100 150 200 250
累计产生气体的质量/g 0.2 m 0.6 0.7 0.7
(1)表中m=______g;
(2)黄铜样品中铜的质量分数______;
(3)求所用稀硫酸中溶质的质量分数?(写出计算过程)
19.向盛有一定质量稀硫酸的烧杯中逐渐加入10g锌粒,产生气体质量与锌粒质量的关系如图所示,充分反应后,称得烧杯中剩余物质总质量为109.8g,请根据关系图分析并计算:
(1)稀硫酸反应完时,产生氢气的质量为_____g。
(2)该稀硫酸中溶质的质量分数_____(写出计算过程)。
参考答案:
1.B 2.B 3.D 4.D 5.A 6.A 7.A 8.B 9.D 10.C 11.C 12.D
13. 能,白糖有甜味,食盐有咸味 能,食醋中的醋酸与苏打中的碳酸钠能反应有气泡冒出,醋酸与食盐中的氯化钠不反应,没有气泡冒出; 不能,黄铜和黄金都呈黄色。
14. CH4 NH3 6CO2+6H2OC6H12O6+6O2 Fe3O4+4CO3Fe+4CO2 高炉 14:1
15. CuO、 CO 3CO+Fe2O32Fe+3CO2 Fe+CuCl2=FeCl2+Cu 灭火(或制汽水)
16. C Fe2O3
17. 把一氧化碳转化成二氧化碳,防止污染环境 ×100% 不变 AB
18.(1)0.4
(2)54.5%
(3)解:设50g稀硫酸中硫酸的质量为
=9.8g
所用稀硫酸中溶质的质量分数为×100%=19.6%
答:所用稀硫酸中溶质的质量分数为19.6%。
19.(1)由图可知,稀硫酸反应完时,产生氢气的质量为0.2g。
(2)设稀硫酸中溶质的质量为x,
,x=9.8g,
该稀硫酸中溶质的质量分数为。
答:该稀硫酸中溶质的质量分数是9.8%。
