2021-2022学年高一下学期化学人教版(2019)必修第二册第七章第二节 乙烯与有机高分子材料(第一课时)课件(39张ppt)
文档属性
| 名称 | 2021-2022学年高一下学期化学人教版(2019)必修第二册第七章第二节 乙烯与有机高分子材料(第一课时)课件(39张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 7.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-05 00:00:00 | ||
图片预览





文档简介
第五章
有机化合物
第二节
乙烯与有机高分子材料
课时一 乙烯及性质
讨论:
如果你是从事水果经商的老板,你如何催熟水果?如何延长水果的保质期?
这是谁的功劳?
乙 烯
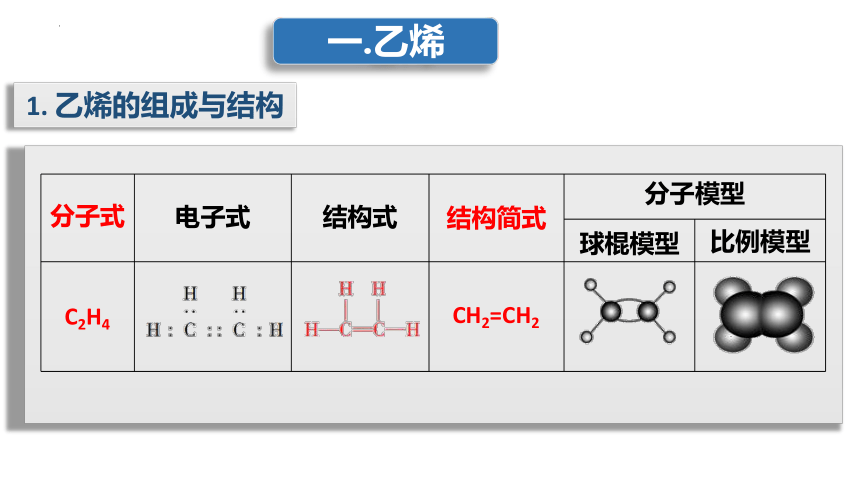
{5940675A-B579-460E-94D1-54222C63F5DA}分子式
电子式
结构式
结构简式
分子模型
球棍模型
比例模型
C2H4
CH2=CH2
一.乙烯
1. 乙烯的组成与结构
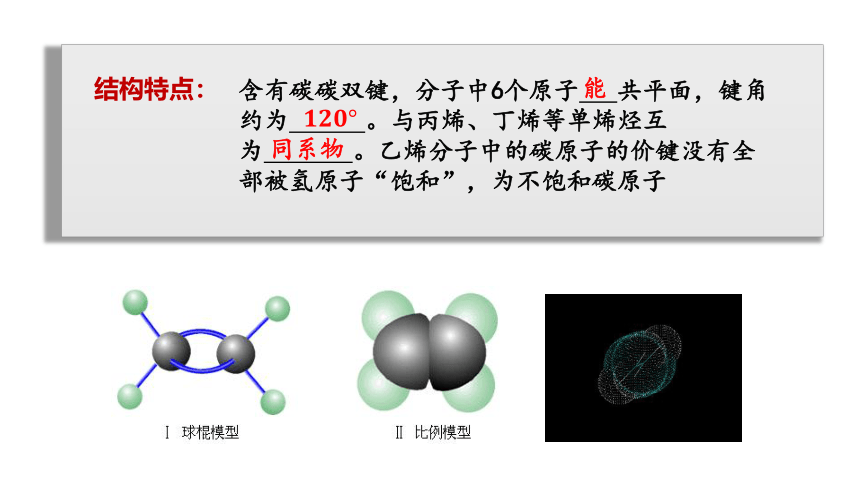
结构特点:
含有碳碳双键,分子中6个原子 共平面,键角约为 。与丙烯、丁烯等单烯烃互为 。乙烯分子中的碳原子的价键没有全部被氢原子“饱和”,为不饱和碳原子
能
同系物
????????????°
?
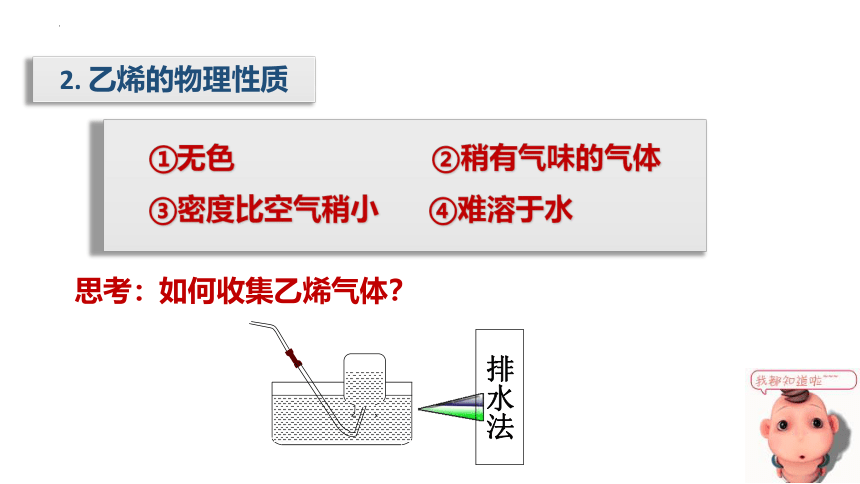
2. 乙烯的物理性质
①无色 ②稍有气味的气体
③密度比空气稍小 ④难溶于水
思考:
排水法
如何收集乙烯气体?
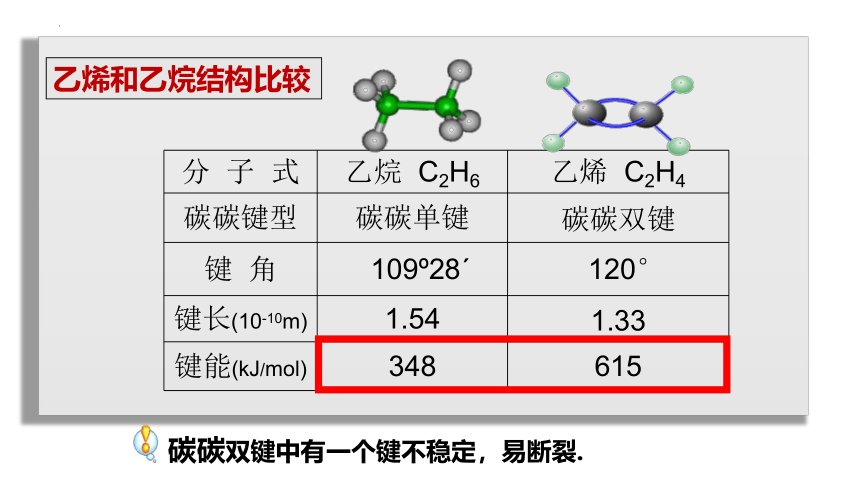
{5940675A-B579-460E-94D1-54222C63F5DA}分 子 式
乙烷 C2H6
乙烯 C2H4
碳碳键型
碳碳单键
碳碳双键
键 角
109?28ˊ
120°
键长(10-10m)
1.54
1.33
键能(kJ/mol)
348
615
碳碳双键中有一个键不稳定,易断裂.
乙烯和乙烷结构比较
①氧化反应(燃烧)
C2H4 + 3O2 ? 2CO2 + 2H2O
点燃
现象:火焰明亮,伴有黑烟。
3. 乙烯的化学性质
CH4
C2H4
产生黑烟是因为含碳量高,燃烧不充分;火焰明亮是碳微粒受灼热而发光。
1>氧化反应
C2H4 + 3O2 ? 2CO2 + 2H2O
点燃
现象:火焰明亮,伴有黑烟。
3. 乙烯的化学性质
CH4
C2H4
产生黑烟是因为含碳量高,燃烧不充分;火焰明亮是碳微粒受灼热而发光。
①燃烧
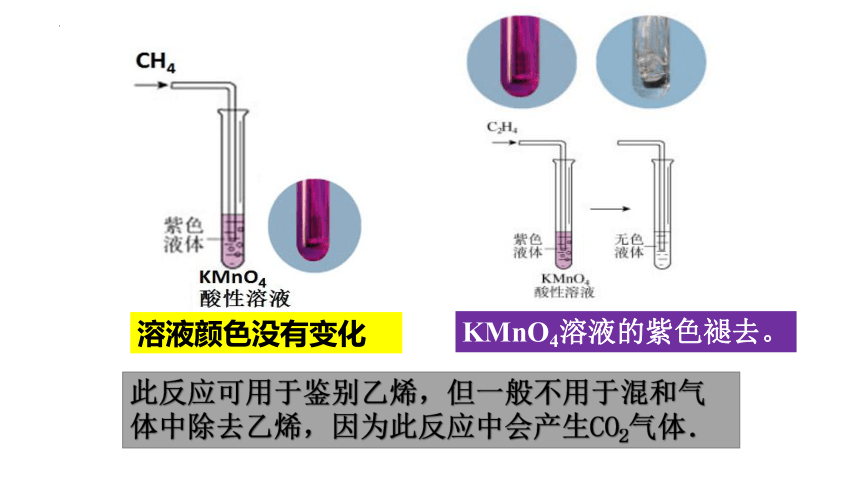
②被强氧化剂氧化(酸性KMnO4溶液)
CH2=CH2
CO2
KMnO4
溶液颜色没有变化
此反应可用于鉴别乙烯,但一般不用于混和气体中除去乙烯,因为此反应中会产生CO2气体.
KMnO4溶液的紫色褪去。
3. 乙烯的化学性质
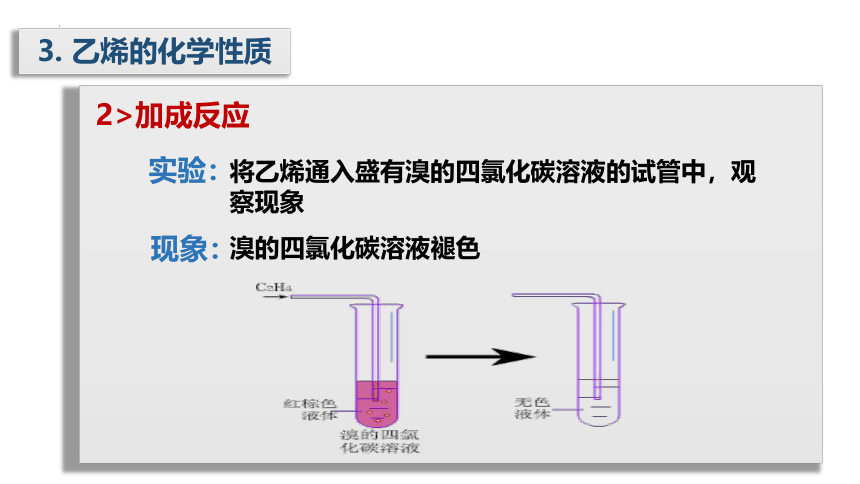
2>加成反应
实验:
将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象
现象:
溴的四氯化碳溶液褪色
3. 乙烯的化学性质
反应的化学方程式:
????????????=????????????+?????????????→????????????????????????????????????????
?
反应原理:
1,2-二溴乙烷
我是溴分子
我是乙烯分子
????????????=????????????+?????????????→????????????????????????????????????????
????????????=????????????+?????????催化剂????????????????????????
????????????=????????????+???????????? ?催化剂 ????????????????????????????????
?
加热、加压
有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应。
加成反应:
思考交流
(1)如想制备一氯乙烷,是采用乙烷与氯气的取代反应还是用乙烯与氯化氢的加成反应,为什么?
(2)乙烯能使溴的CCl4褪色,甲同学认为发生了取代反应,乙同学认为发生了加成反应,哪一位同学正确呢?试设计实验验证。
(1)乙烯与HCl的加成反应副反应更少,产物相对纯净。
(2)方法:向反应后溶液中加AgNO3溶液或石蕊
现象:若发生取代反应则生成HBr,则有淡黄色沉淀或加石蕊会变红;
若发生加成反应,则无此现象。
在适当的温度、压强和催化剂存在的条件下,乙烯分子能通过断键、成键生成相对分子质量很大的聚合物——聚乙烯。
????????2=????????2+????????2=????????2+????????2=????????2+???断键
??—?????????2—????????2—+—????????2—????????2—+—????????2—????????2—+?
?? 成键 ??—?????????2—????????2—????????2—????????2—????????2—????????2—??
?
单体
链节
3. 乙烯的化学性质
3>聚合反应
????????????????=????????????催化剂—?????????????????????????—
?
n
聚合度
乙烯发生聚合反应得到聚乙烯:
聚合反应:由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应。乙烯的聚合反应同样也是加成反应,这样的反应又被称为加成聚合反应,简称加聚反应。
聚乙烯、聚氯乙烯、聚四氟乙烯等高分子材料在现代生活中用途很广。
乙烯的自身聚合,是乙烯的最大用量。高密度聚乙烯和低密度聚乙烯总量占乙烯总产量的60%以上,使乙烯在塑料树脂生产中占有绝对优势。
PE管材
PVC型材
CH2=CH2
氧化
加成
聚合
使酸性至锰酸钾溶液褪色
2CO2+2H2O
H2
Ni
Br2(H2O/CCl4)
HCl
H2O
一定条件
CH3—CH3
CH2Br—CH2Br
CH3—CH2Cl
CH3—CH2OH
[ CH2—CH2]n
可用酸性高锰酸钾溶液区别甲烷和乙烯(烷烃和烯烃)
用溴水区别甲烷和乙烯
(烷烃和烯烃)或除去甲烷中的乙烯
总结乙烯的化学性质
O2
(1)植物生长调节剂, 催熟剂
(2)有机化工原料
4. 乙烯的用途
乙烯的产量作为衡量一个国家石油化工发展水平的标志
乙烯的用途:
塑料袋,薄膜
乳化剂,洗涤剂,防冻剂
乙烯的用途:
塑料,增塑剂
乙烯的用途:
无纺布,醋酸纤维,管材
乙烯的用途:
管材
泡沫
乙烯的用途:
杀虫剂
为了促进香蕉和青橘子成熟,可在密封袋子中放一些成熟的苹果.
植物在生命周期的许多阶段都会生成乙烯。
成熟的水果含有较多的乙烯。
乙烯可以作为水果的催熟剂。
有时为了延长果实和花朵的寿命,或是方便运输,人们常在袋子里放入浸过高锰酸钾溶液的硅土。
重要的化工原料
石油化学工业最重要的基础原料
实战演练1
方法一:将两种气体分别通入酸性KMnO4溶液中,能使KMnO4溶液褪色的是乙烯。
方法二:把两种气体分别点燃,淡蓝色火焰为甲烷;火焰明亮,伴有黑烟的是乙烯。
方法三:将两种气体分别通入溴的四氯化碳溶液中,能使溶液褪色的是乙烯。
根据乙烯的化学性质,鉴别甲烷与乙烯两种气体,你有几种方法?
在一定条件下,乙烷和乙烯都能制备氯乙烷CH3CH2Cl。
①乙烷制氯乙烷的化学方程式是
_______________________________________________
②乙烯制备氯乙烷的化学方程式是
________________________________________________
③比较两种方法,________方法制备氯乙烷更好,原因是
_____________________________________________
_____________________________________________
CH3CH3+ Cl2 CH3CH2Cl + HCl
光照
取代反应
加成反应
第2种
乙烷与Cl2发生取代反应,产物中有多种卤代烃;而乙烯与HCl发生加成反应,产物单一。
CH2=CH2 + HCl
CH3-CH2Cl
催化剂△
实战演练2
1、下列物质不可能是乙烯加成产物的是
( )
A.CH3CH3 ?? B.CH3CHCl2
? C.CH3CH2OH D.CH2BrCH2Br
B
练习:
2. 下列过程中发生的化学反应属于加成反应的是( )
B
A. 用光照射甲烷和氯气的混合气体
B. 将乙烯通入溴的四氯化碳溶液中
C. 甲烷在空气中不完全燃烧
D. 将乙烯通入酸性高锰酸钾溶液中
3. 柠檬烯具有良好的镇咳、祛痰、抑菌作用,其结构如图所示。下列关于柠檬烯的说法正确的是( )
B
A. 1mol柠檬烯只能与1molH2反应
B. 能发生取代反应和加成反应
C. 属于乙烯的同系物
D. 不能使酸性高锰酸钾溶液褪色
思考:1. 甲烷中的4个H与1个C的相对位置如何?分子的空间构型又是怎么样的?C—H键的夹角为多少?
4个H在正四面体的四个顶点,1个C在正四面体的中心,分子构型为正四面体,C—H键的夹角为109°28′。
甲烷中最多3个原子共平面。
拓展提升:原子共面问题
2. 乙烯中的4个H与2个C是否共面?共价键的夹角为多少?
共面,120°。
乙烯的结构是平面结构,2个C与4个H共平面。
乙烯中6个原子共平面。
谢谢欣赏
有机化合物
第二节
乙烯与有机高分子材料
课时一 乙烯及性质
讨论:
如果你是从事水果经商的老板,你如何催熟水果?如何延长水果的保质期?
这是谁的功劳?
乙 烯
{5940675A-B579-460E-94D1-54222C63F5DA}分子式
电子式
结构式
结构简式
分子模型
球棍模型
比例模型
C2H4
CH2=CH2
一.乙烯
1. 乙烯的组成与结构
结构特点:
含有碳碳双键,分子中6个原子 共平面,键角约为 。与丙烯、丁烯等单烯烃互为 。乙烯分子中的碳原子的价键没有全部被氢原子“饱和”,为不饱和碳原子
能
同系物
????????????°
?
2. 乙烯的物理性质
①无色 ②稍有气味的气体
③密度比空气稍小 ④难溶于水
思考:
排水法
如何收集乙烯气体?
{5940675A-B579-460E-94D1-54222C63F5DA}分 子 式
乙烷 C2H6
乙烯 C2H4
碳碳键型
碳碳单键
碳碳双键
键 角
109?28ˊ
120°
键长(10-10m)
1.54
1.33
键能(kJ/mol)
348
615
碳碳双键中有一个键不稳定,易断裂.
乙烯和乙烷结构比较
①氧化反应(燃烧)
C2H4 + 3O2 ? 2CO2 + 2H2O
点燃
现象:火焰明亮,伴有黑烟。
3. 乙烯的化学性质
CH4
C2H4
产生黑烟是因为含碳量高,燃烧不充分;火焰明亮是碳微粒受灼热而发光。
1>氧化反应
C2H4 + 3O2 ? 2CO2 + 2H2O
点燃
现象:火焰明亮,伴有黑烟。
3. 乙烯的化学性质
CH4
C2H4
产生黑烟是因为含碳量高,燃烧不充分;火焰明亮是碳微粒受灼热而发光。
①燃烧
②被强氧化剂氧化(酸性KMnO4溶液)
CH2=CH2
CO2
KMnO4
溶液颜色没有变化
此反应可用于鉴别乙烯,但一般不用于混和气体中除去乙烯,因为此反应中会产生CO2气体.
KMnO4溶液的紫色褪去。
3. 乙烯的化学性质
2>加成反应
实验:
将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象
现象:
溴的四氯化碳溶液褪色
3. 乙烯的化学性质
反应的化学方程式:
????????????=????????????+?????????????→????????????????????????????????????????
?
反应原理:
1,2-二溴乙烷
我是溴分子
我是乙烯分子
????????????=????????????+?????????????→????????????????????????????????????????
????????????=????????????+?????????催化剂????????????????????????
????????????=????????????+???????????? ?催化剂 ????????????????????????????????
?
加热、加压
有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应。
加成反应:
思考交流
(1)如想制备一氯乙烷,是采用乙烷与氯气的取代反应还是用乙烯与氯化氢的加成反应,为什么?
(2)乙烯能使溴的CCl4褪色,甲同学认为发生了取代反应,乙同学认为发生了加成反应,哪一位同学正确呢?试设计实验验证。
(1)乙烯与HCl的加成反应副反应更少,产物相对纯净。
(2)方法:向反应后溶液中加AgNO3溶液或石蕊
现象:若发生取代反应则生成HBr,则有淡黄色沉淀或加石蕊会变红;
若发生加成反应,则无此现象。
在适当的温度、压强和催化剂存在的条件下,乙烯分子能通过断键、成键生成相对分子质量很大的聚合物——聚乙烯。
????????2=????????2+????????2=????????2+????????2=????????2+???断键
??—?????????2—????????2—+—????????2—????????2—+—????????2—????????2—+?
?? 成键 ??—?????????2—????????2—????????2—????????2—????????2—????????2—??
?
单体
链节
3. 乙烯的化学性质
3>聚合反应
????????????????=????????????催化剂—?????????????????????????—
?
n
聚合度
乙烯发生聚合反应得到聚乙烯:
聚合反应:由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应。乙烯的聚合反应同样也是加成反应,这样的反应又被称为加成聚合反应,简称加聚反应。
聚乙烯、聚氯乙烯、聚四氟乙烯等高分子材料在现代生活中用途很广。
乙烯的自身聚合,是乙烯的最大用量。高密度聚乙烯和低密度聚乙烯总量占乙烯总产量的60%以上,使乙烯在塑料树脂生产中占有绝对优势。
PE管材
PVC型材
CH2=CH2
氧化
加成
聚合
使酸性至锰酸钾溶液褪色
2CO2+2H2O
H2
Ni
Br2(H2O/CCl4)
HCl
H2O
一定条件
CH3—CH3
CH2Br—CH2Br
CH3—CH2Cl
CH3—CH2OH
[ CH2—CH2]n
可用酸性高锰酸钾溶液区别甲烷和乙烯(烷烃和烯烃)
用溴水区别甲烷和乙烯
(烷烃和烯烃)或除去甲烷中的乙烯
总结乙烯的化学性质
O2
(1)植物生长调节剂, 催熟剂
(2)有机化工原料
4. 乙烯的用途
乙烯的产量作为衡量一个国家石油化工发展水平的标志
乙烯的用途:
塑料袋,薄膜
乳化剂,洗涤剂,防冻剂
乙烯的用途:
塑料,增塑剂
乙烯的用途:
无纺布,醋酸纤维,管材
乙烯的用途:
管材
泡沫
乙烯的用途:
杀虫剂
为了促进香蕉和青橘子成熟,可在密封袋子中放一些成熟的苹果.
植物在生命周期的许多阶段都会生成乙烯。
成熟的水果含有较多的乙烯。
乙烯可以作为水果的催熟剂。
有时为了延长果实和花朵的寿命,或是方便运输,人们常在袋子里放入浸过高锰酸钾溶液的硅土。
重要的化工原料
石油化学工业最重要的基础原料
实战演练1
方法一:将两种气体分别通入酸性KMnO4溶液中,能使KMnO4溶液褪色的是乙烯。
方法二:把两种气体分别点燃,淡蓝色火焰为甲烷;火焰明亮,伴有黑烟的是乙烯。
方法三:将两种气体分别通入溴的四氯化碳溶液中,能使溶液褪色的是乙烯。
根据乙烯的化学性质,鉴别甲烷与乙烯两种气体,你有几种方法?
在一定条件下,乙烷和乙烯都能制备氯乙烷CH3CH2Cl。
①乙烷制氯乙烷的化学方程式是
_______________________________________________
②乙烯制备氯乙烷的化学方程式是
________________________________________________
③比较两种方法,________方法制备氯乙烷更好,原因是
_____________________________________________
_____________________________________________
CH3CH3+ Cl2 CH3CH2Cl + HCl
光照
取代反应
加成反应
第2种
乙烷与Cl2发生取代反应,产物中有多种卤代烃;而乙烯与HCl发生加成反应,产物单一。
CH2=CH2 + HCl
CH3-CH2Cl
催化剂△
实战演练2
1、下列物质不可能是乙烯加成产物的是
( )
A.CH3CH3 ?? B.CH3CHCl2
? C.CH3CH2OH D.CH2BrCH2Br
B
练习:
2. 下列过程中发生的化学反应属于加成反应的是( )
B
A. 用光照射甲烷和氯气的混合气体
B. 将乙烯通入溴的四氯化碳溶液中
C. 甲烷在空气中不完全燃烧
D. 将乙烯通入酸性高锰酸钾溶液中
3. 柠檬烯具有良好的镇咳、祛痰、抑菌作用,其结构如图所示。下列关于柠檬烯的说法正确的是( )
B
A. 1mol柠檬烯只能与1molH2反应
B. 能发生取代反应和加成反应
C. 属于乙烯的同系物
D. 不能使酸性高锰酸钾溶液褪色
思考:1. 甲烷中的4个H与1个C的相对位置如何?分子的空间构型又是怎么样的?C—H键的夹角为多少?
4个H在正四面体的四个顶点,1个C在正四面体的中心,分子构型为正四面体,C—H键的夹角为109°28′。
甲烷中最多3个原子共平面。
拓展提升:原子共面问题
2. 乙烯中的4个H与2个C是否共面?共价键的夹角为多少?
共面,120°。
乙烯的结构是平面结构,2个C与4个H共平面。
乙烯中6个原子共平面。
谢谢欣赏
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
