第12章盐练习题-2021-2022学年九年级化学京改版(2013)下册(word版 含答案)
文档属性
| 名称 | 第12章盐练习题-2021-2022学年九年级化学京改版(2013)下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 108.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-05 00:00:00 | ||
图片预览


文档简介
第12章盐练习题—2021-2022学年九年级化学京改版(2013)下册
一、单选题
1.下列各组离子在溶液中能大量共存的是( )
A.NH、SO、NO
B.H+、Ba2+、OH-
C.Fe2+、Na+、OH-
D.Ca2+、Cl-、CO
2.俗称“纯碱”的物质是( )
A.H2SO4 B.HCl C.Na2CO3 D.Cu(OH)2
3.下列有关说法错误的是
A.化学是一门实用的、富有创造性的中心学科
B.硫酸铜和氢氧化钠反应生成蓝色沉淀,体现了硫酸铜的化学性质
C.研究开发新型可降解塑料属于化学研究范畴
D.门捷列夫等科学家创立的原子论和分子学说奠定了现代化学基础
4.同学们夏季郊游时,发现稻田里的水稻叶子发黄并倒下了一片,都认为应该向稻田中施用的复合肥是( )
A.NH4NO3 B.KNO3 C.K3PO4 D.KCl
5.硝石是主要含KNO3的天然矿物,历史上《本草经集注》中对硝石有记载:“强烧之,紫青烟起…云是真硝石也”。下列有关KNO3的叙述不正确的是( )
A.是一种化合物 B.可用作复合肥料
C.可能发生分解反应 D.其溶解度一定大于NaCl的溶解度
6.下列关于碳酸钙的说法错误的是
A.大理石的主要成分是碳酸钙
B.实验室常用碳酸钙与稀硫酸反应制取CO2
C.碳酸钙可用作补钙剂
D.石灰浆粉刷墙壁,“出汗”后变成碳酸钙
7.下列除去杂质的方法不正确的是( )
A.FeSO4溶液(CuSO4):过量的铁粉过滤 B.H2(H2O):浓硫酸
C.CO2(CO):通过灼热的氧化铜粉末 D.CaO(CaCO3):稀盐酸
8.我国制碱工业的先驱——侯德榜先生,1921年留美回国后,潜心研究制碱技术,发明了将制碱与制氨结合起来的联合制碱法(又称侯氏制碱法),为纯碱和氮肥工业技术的发展做出了杰出贡献。下列物质中能与纯碱发生反应的是
A.NaOH B.NaHCO3 C.H2SO4 D.K2SO4
9.关于碳酸钠的说法错误的是
A.易溶于水 B.可用于洗涤油污 C.受热易分解 D.可用于制造普通玻璃
10.某农技站货架上待售的化肥有NH4NO3、NH4H2PO4、CO(NH2)2,其中缺少的肥料品种是( )
A.氮肥 B.磷肥 C.钾肥 D.复合肥料
11.实验室中同学们进行了如图所示实验,成功探究出了久置氢氧化钠固体的变质情况。下列说法正确的是( )
A.甲溶液可以选择稀盐酸或CaC12溶液(查阅资料得知:CaC12溶液显中性)
B.若Ⅱ、Ⅲ均有明显现象,则说明样品部分变质
C.D物质可能是气体,也可能是沉淀
D.溶液B中的溶质一定只含有NaOH和甲
二、简答题
12.化学与生活、生产密切相关。请用学过的化学知识解决下列问题:
(1)家庭中使用松花蛋时,为消除皮蛋中碱性物质的涩味,可加入厨房中的_____调味品使味道更加。
(2)人体胃液中含有适量的盐酸,在医学中可用碳酸氢钠中和胃酸过多症,是因为_____(用化学方程时表示),同时,医生建议患有胃溃疡的患者不宜过多服用。
(3)锅炉水垢会降低燃料利用率,某锅炉水垢的主要成分有CaCO3、Mg(OH)2等,用“酸洗”法可除去水垢
①“酸洗”时,一般不选用稀硫酸的原因是_____。
②写出稀盐酸与CaCO3反应化学方程式_____。
(4)为除去SO2气体污染火力发电厂常用石灰浆喷雾处理,写出该反应的化学方程式_____。
13.长期盛放石灰水的试剂瓶内壁会形成一层不溶于水的白色物质,石灰水用完后,小明用稀盐酸除去了这层白色物质。请用化学原理解释这一现象,并写出除去白色物质的反应化学方程式。
14.下图中的几种物质是常见的盐,请回答下列问题。
(1)在碳酸钠溶液中滴入氯化钙溶液,现象是_______________。
(2)碳酸钙、碳酸钠均能与稀盐酸反应生成CO2,是因为碳酸钙、碳酸钠中均含有___________(写离子符号)。
(3)硫酸铜溶液与氢氧化钠溶液能发生反应,该反应的化学方程式为__________________;硫酸铜溶液与氯化钠溶液不能反应,其理由是__________________。
三、推断题
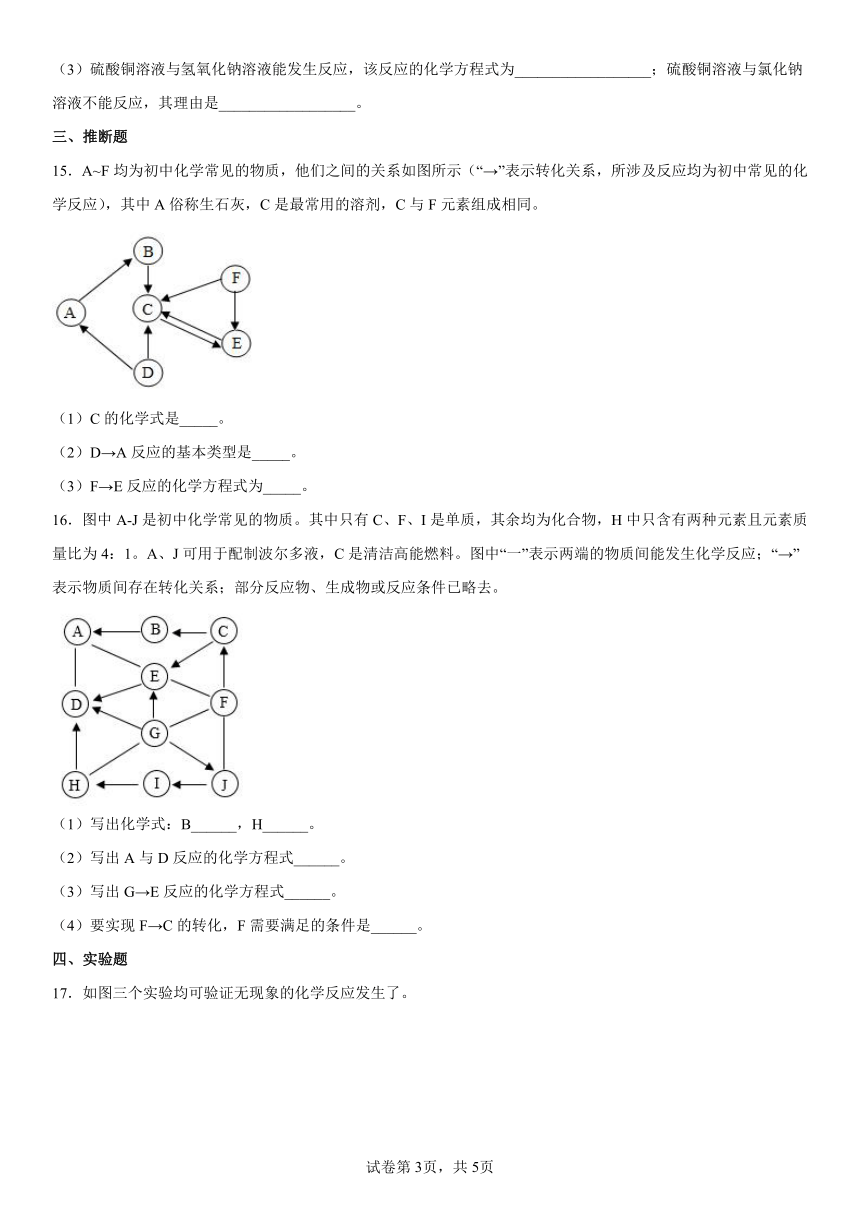
15.A~F均为初中化学常见的物质,他们之间的关系如图所示(“→”表示转化关系,所涉及反应均为初中常见的化学反应),其中A俗称生石灰,C是最常用的溶剂,C与F元素组成相同。
(1)C的化学式是_____。
(2)D→A反应的基本类型是_____。
(3)F→E反应的化学方程式为_____。
16.图中A-J是初中化学常见的物质。其中只有C、F、I是单质,其余均为化合物,H中只含有两种元素且元素质量比为4:1。A、J可用于配制波尔多液,C是清洁高能燃料。图中“一”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。
(1)写出化学式:B______,H______。
(2)写出A与D反应的化学方程式______。
(3)写出G→E反应的化学方程式______。
(4)要实现F→C的转化,F需要满足的条件是______。
四、实验题
17.如图三个实验均可验证无现象的化学反应发生了。
【实验一】当观察到______现象时,证明化学反应发生,化学方程式是______。
【实验二】加入 X 可验证稀硫酸与NaOH 能发生反应,符合此条件的X 是______。
A.FeCl3 B. C.Na2CO3 D.
【实验三】用气压传感器测得曲线1 和2,要证明CO2 与NaOH 一定发生了反应,左瓶中应加入______;曲线 1 变化平缓的原因是______。
【反思】上述实验的设计思想是通过证明______,来判断化学反应的发生。
18.如图是实验室常用来制取气体的实验装置,请根据要求回答下列问题:
(1)仪器a的名称是_______。
(2)实验室用氯酸钾和二氧化锰制氧气,选择的发生装置是_______,选择 E 装置收集氧气,因为氧气不与水反应,并且_______,应将收集满氧气的集气瓶_______(填“正”或“倒”)放在桌面上,实验结束后,先将导管撤离水槽,再_______。
(3)若选择B装置制取氢气,发生反应的化学方程式为_______。
(4)若选择B装置制取氧气,发生反应的化学方程式为_______。
(5)实验室制取二氧化碳的化学反应方程式是_______,属于_______反应(填基本反应类型),检验二氧化碳是否集满的方法是_______。
19.实验小组用下图装置进行实验。
已知:甲瓶中充满二氧化碳,乙中液体是水,实验前K关闭。
(1)将胶头滴管中的浓NaOH溶液挤入瓶中,振荡,该反应的化学方程式为___________。
(2)打开K,观察到乙中导管口有气泡冒出,原因是____________。
(3)将分液漏斗中的稀盐酸注入甲中,观察到乙中的现象是____________。
五、计算题
20.工业上,高温煅烧石灰石可制得生石灰(CaO)和二氧化碳。如果制取11.2t氧化钙,需要含碳酸钙80 %的石灰石质量是多少 同时可以得到二氧化碳的质量是多少
21.现有一瓶部分变质为碳酸钠的氢氧化钠固体。某同学想了解其变质情况,称取10.00g上述固体样品于烧杯中,加入足量水使之完全溶解,再向烧杯中缓缓加入过量的氢氧化钡溶液,充分反应后,过滤、洗涤、干燥,得到3.94g沉淀。求:
(1)样品中碳酸钠的质量分数为______。
(2)反应后所得溶液中氢氧化钠的质量。
22.某碳酸钠样品含有少量的硫酸钠,取一定质量的该样品,完全溶解在水中配制成100g溶液,将其全部加入到50g一定质量分数的硫酸溶液中,恰好完全反应,生成的气体全部逸出后,所得溶液质量是145.6g。将所得溶液蒸干,得到15.6g硫酸钠。试计算:
(1)加入的硫酸溶液的溶质质量分数;
(2)原碳酸钠样品中硫酸钠的质量分数(计算结果精确到0.1%)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.C
3.D
4.B
5.D
6.B
7.D
8.C
9.C
10.C
11.B
12. 食醋 NaHCO3+HCl═NaCl+H2O+CO2↑ 稀硫酸和碳酸钙反应生成的硫酸钙微溶于水,会阻止反应的进行 Ca(OH)2+SO2═CaSO3↓+H2O
13.石灰水中的氢氧化钙与空气中的CO2反应生成白色沉淀碳酸钙,碳酸钙与稀盐酸反应生成可溶于水的氯化钙。CaCO3+2HCl=CaCl2+H2O+CO2↑
14. 产生白色沉淀 CO32- CuSO4+2NaOH=Na2SO4+Cu(OH)2↓ 两种化合物互相交换成分,没有沉淀、没有气体、没有水生成,不符合复分解反应发生的条件。
15. H2O 分解反应
16. F需要在金属活动顺序表中位于氢之前,钾钙钠除外
17. 溶液由红色变为无色 A 20mL水 CO2 在水中的溶解度较小且与水反应的量小 反应物已转化为其他物质
18. 长颈漏斗 A 不易溶于水 正 熄灭酒精灯 Zn+H2SO4=ZnSO4+H2↑ 复分解 将燃着的木条放在集气瓶口,若木条熄灭,则说明二氧化碳已收集满
19. 2NaOH+CO2====Na2CO3+H2O 甲中二氧化碳被消耗,压强减小,乙中气体进入甲,压强减小,空气进入乙 长玻璃管内液面上升
20.25t;8.8 t
21.解:样品中碳酸钠的质量分数为x,生成氢氧化钠的质量为y
反应后所得溶液中氢氧化钠的质量10.00g-2.12g+1.6g=9.48g
答:(1)样品中碳酸钠的质量分数为21.2%。
(2)反应后所得溶液中氢氧化钠的质量9.48g。
22.(1);(2)11.7%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列各组离子在溶液中能大量共存的是( )
A.NH、SO、NO
B.H+、Ba2+、OH-
C.Fe2+、Na+、OH-
D.Ca2+、Cl-、CO
2.俗称“纯碱”的物质是( )
A.H2SO4 B.HCl C.Na2CO3 D.Cu(OH)2
3.下列有关说法错误的是
A.化学是一门实用的、富有创造性的中心学科
B.硫酸铜和氢氧化钠反应生成蓝色沉淀,体现了硫酸铜的化学性质
C.研究开发新型可降解塑料属于化学研究范畴
D.门捷列夫等科学家创立的原子论和分子学说奠定了现代化学基础
4.同学们夏季郊游时,发现稻田里的水稻叶子发黄并倒下了一片,都认为应该向稻田中施用的复合肥是( )
A.NH4NO3 B.KNO3 C.K3PO4 D.KCl
5.硝石是主要含KNO3的天然矿物,历史上《本草经集注》中对硝石有记载:“强烧之,紫青烟起…云是真硝石也”。下列有关KNO3的叙述不正确的是( )
A.是一种化合物 B.可用作复合肥料
C.可能发生分解反应 D.其溶解度一定大于NaCl的溶解度
6.下列关于碳酸钙的说法错误的是
A.大理石的主要成分是碳酸钙
B.实验室常用碳酸钙与稀硫酸反应制取CO2
C.碳酸钙可用作补钙剂
D.石灰浆粉刷墙壁,“出汗”后变成碳酸钙
7.下列除去杂质的方法不正确的是( )
A.FeSO4溶液(CuSO4):过量的铁粉过滤 B.H2(H2O):浓硫酸
C.CO2(CO):通过灼热的氧化铜粉末 D.CaO(CaCO3):稀盐酸
8.我国制碱工业的先驱——侯德榜先生,1921年留美回国后,潜心研究制碱技术,发明了将制碱与制氨结合起来的联合制碱法(又称侯氏制碱法),为纯碱和氮肥工业技术的发展做出了杰出贡献。下列物质中能与纯碱发生反应的是
A.NaOH B.NaHCO3 C.H2SO4 D.K2SO4
9.关于碳酸钠的说法错误的是
A.易溶于水 B.可用于洗涤油污 C.受热易分解 D.可用于制造普通玻璃
10.某农技站货架上待售的化肥有NH4NO3、NH4H2PO4、CO(NH2)2,其中缺少的肥料品种是( )
A.氮肥 B.磷肥 C.钾肥 D.复合肥料
11.实验室中同学们进行了如图所示实验,成功探究出了久置氢氧化钠固体的变质情况。下列说法正确的是( )
A.甲溶液可以选择稀盐酸或CaC12溶液(查阅资料得知:CaC12溶液显中性)
B.若Ⅱ、Ⅲ均有明显现象,则说明样品部分变质
C.D物质可能是气体,也可能是沉淀
D.溶液B中的溶质一定只含有NaOH和甲
二、简答题
12.化学与生活、生产密切相关。请用学过的化学知识解决下列问题:
(1)家庭中使用松花蛋时,为消除皮蛋中碱性物质的涩味,可加入厨房中的_____调味品使味道更加。
(2)人体胃液中含有适量的盐酸,在医学中可用碳酸氢钠中和胃酸过多症,是因为_____(用化学方程时表示),同时,医生建议患有胃溃疡的患者不宜过多服用。
(3)锅炉水垢会降低燃料利用率,某锅炉水垢的主要成分有CaCO3、Mg(OH)2等,用“酸洗”法可除去水垢
①“酸洗”时,一般不选用稀硫酸的原因是_____。
②写出稀盐酸与CaCO3反应化学方程式_____。
(4)为除去SO2气体污染火力发电厂常用石灰浆喷雾处理,写出该反应的化学方程式_____。
13.长期盛放石灰水的试剂瓶内壁会形成一层不溶于水的白色物质,石灰水用完后,小明用稀盐酸除去了这层白色物质。请用化学原理解释这一现象,并写出除去白色物质的反应化学方程式。
14.下图中的几种物质是常见的盐,请回答下列问题。
(1)在碳酸钠溶液中滴入氯化钙溶液,现象是_______________。
(2)碳酸钙、碳酸钠均能与稀盐酸反应生成CO2,是因为碳酸钙、碳酸钠中均含有___________(写离子符号)。
(3)硫酸铜溶液与氢氧化钠溶液能发生反应,该反应的化学方程式为__________________;硫酸铜溶液与氯化钠溶液不能反应,其理由是__________________。
三、推断题
15.A~F均为初中化学常见的物质,他们之间的关系如图所示(“→”表示转化关系,所涉及反应均为初中常见的化学反应),其中A俗称生石灰,C是最常用的溶剂,C与F元素组成相同。
(1)C的化学式是_____。
(2)D→A反应的基本类型是_____。
(3)F→E反应的化学方程式为_____。
16.图中A-J是初中化学常见的物质。其中只有C、F、I是单质,其余均为化合物,H中只含有两种元素且元素质量比为4:1。A、J可用于配制波尔多液,C是清洁高能燃料。图中“一”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。
(1)写出化学式:B______,H______。
(2)写出A与D反应的化学方程式______。
(3)写出G→E反应的化学方程式______。
(4)要实现F→C的转化,F需要满足的条件是______。
四、实验题
17.如图三个实验均可验证无现象的化学反应发生了。
【实验一】当观察到______现象时,证明化学反应发生,化学方程式是______。
【实验二】加入 X 可验证稀硫酸与NaOH 能发生反应,符合此条件的X 是______。
A.FeCl3 B. C.Na2CO3 D.
【实验三】用气压传感器测得曲线1 和2,要证明CO2 与NaOH 一定发生了反应,左瓶中应加入______;曲线 1 变化平缓的原因是______。
【反思】上述实验的设计思想是通过证明______,来判断化学反应的发生。
18.如图是实验室常用来制取气体的实验装置,请根据要求回答下列问题:
(1)仪器a的名称是_______。
(2)实验室用氯酸钾和二氧化锰制氧气,选择的发生装置是_______,选择 E 装置收集氧气,因为氧气不与水反应,并且_______,应将收集满氧气的集气瓶_______(填“正”或“倒”)放在桌面上,实验结束后,先将导管撤离水槽,再_______。
(3)若选择B装置制取氢气,发生反应的化学方程式为_______。
(4)若选择B装置制取氧气,发生反应的化学方程式为_______。
(5)实验室制取二氧化碳的化学反应方程式是_______,属于_______反应(填基本反应类型),检验二氧化碳是否集满的方法是_______。
19.实验小组用下图装置进行实验。
已知:甲瓶中充满二氧化碳,乙中液体是水,实验前K关闭。
(1)将胶头滴管中的浓NaOH溶液挤入瓶中,振荡,该反应的化学方程式为___________。
(2)打开K,观察到乙中导管口有气泡冒出,原因是____________。
(3)将分液漏斗中的稀盐酸注入甲中,观察到乙中的现象是____________。
五、计算题
20.工业上,高温煅烧石灰石可制得生石灰(CaO)和二氧化碳。如果制取11.2t氧化钙,需要含碳酸钙80 %的石灰石质量是多少 同时可以得到二氧化碳的质量是多少
21.现有一瓶部分变质为碳酸钠的氢氧化钠固体。某同学想了解其变质情况,称取10.00g上述固体样品于烧杯中,加入足量水使之完全溶解,再向烧杯中缓缓加入过量的氢氧化钡溶液,充分反应后,过滤、洗涤、干燥,得到3.94g沉淀。求:
(1)样品中碳酸钠的质量分数为______。
(2)反应后所得溶液中氢氧化钠的质量。
22.某碳酸钠样品含有少量的硫酸钠,取一定质量的该样品,完全溶解在水中配制成100g溶液,将其全部加入到50g一定质量分数的硫酸溶液中,恰好完全反应,生成的气体全部逸出后,所得溶液质量是145.6g。将所得溶液蒸干,得到15.6g硫酸钠。试计算:
(1)加入的硫酸溶液的溶质质量分数;
(2)原碳酸钠样品中硫酸钠的质量分数(计算结果精确到0.1%)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.C
3.D
4.B
5.D
6.B
7.D
8.C
9.C
10.C
11.B
12. 食醋 NaHCO3+HCl═NaCl+H2O+CO2↑ 稀硫酸和碳酸钙反应生成的硫酸钙微溶于水,会阻止反应的进行 Ca(OH)2+SO2═CaSO3↓+H2O
13.石灰水中的氢氧化钙与空气中的CO2反应生成白色沉淀碳酸钙,碳酸钙与稀盐酸反应生成可溶于水的氯化钙。CaCO3+2HCl=CaCl2+H2O+CO2↑
14. 产生白色沉淀 CO32- CuSO4+2NaOH=Na2SO4+Cu(OH)2↓ 两种化合物互相交换成分,没有沉淀、没有气体、没有水生成,不符合复分解反应发生的条件。
15. H2O 分解反应
16. F需要在金属活动顺序表中位于氢之前,钾钙钠除外
17. 溶液由红色变为无色 A 20mL水 CO2 在水中的溶解度较小且与水反应的量小 反应物已转化为其他物质
18. 长颈漏斗 A 不易溶于水 正 熄灭酒精灯 Zn+H2SO4=ZnSO4+H2↑ 复分解 将燃着的木条放在集气瓶口,若木条熄灭,则说明二氧化碳已收集满
19. 2NaOH+CO2====Na2CO3+H2O 甲中二氧化碳被消耗,压强减小,乙中气体进入甲,压强减小,空气进入乙 长玻璃管内液面上升
20.25t;8.8 t
21.解:样品中碳酸钠的质量分数为x,生成氢氧化钠的质量为y
反应后所得溶液中氢氧化钠的质量10.00g-2.12g+1.6g=9.48g
答:(1)样品中碳酸钠的质量分数为21.2%。
(2)反应后所得溶液中氢氧化钠的质量9.48g。
22.(1);(2)11.7%
答案第1页,共2页
答案第1页,共2页
