人教版化学九年级下册同步提优练习:第八单元 课题2 金属的化学性质(word版有答案)
文档属性
| 名称 | 人教版化学九年级下册同步提优练习:第八单元 课题2 金属的化学性质(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 286.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-05 00:00:00 | ||
图片预览



文档简介
课题2 金属的化学性质
第1课时 金属与氧气、盐酸、稀硫酸的反应
1.判断正误:(在括号内打“√”或“×”)
(1)“真金不怕火炼”说明黄金的硬度非常大 ( )
(2)铝的抗腐蚀性能比铁强,铝的金属活动性比铁弱 ( )
(3)铁丝在氧气中燃烧生成黑色的氧化铁 ( )
(4)利用稀盐酸可以区分黄铜和铜 ( )
2.判断下列化学方程式的正误(在括号内打“√”或“×”),并将错误的化学方程式更正,不能反应的写出错因。
(1)4Fe+3O22Fe2O3( )
(2)2Cu+O22CuO( )
(3)Cu+2HClCuCl2+H2↑( )
(4)2Fe+6HCl2FeCl3+3H2↑( )
(5)Al+H2SO4AlSO4+H2( )
[核心知识]
1.镁、铝等在常温下就能与氧气反应;铁、铜等在常温下几乎不与氧气反应,但在高温时能与氧气反应;金不与氧气反应。
2.镁、锌、铁能与盐酸、稀硫酸反应生成氢气,且镁反应最剧烈,锌次之,铁反应较为缓慢;铜不能与盐酸、稀硫酸反应。
[易错点拨]
1.铝的化学性质较活泼,由于其常温下能与氧气反应,表面生成一层致密的氧化铝薄膜,故其抗腐蚀性能很好。
2.铁与盐酸或稀硫酸等发生反应时,一般只能生成亚铁离子(铁元素由0价变为+2价),反应后的溶液颜色变成浅绿色。
1.黄铜是铜与锌的合金。下列关于黄铜的说法正确的是 ( )
A.比纯铜耐腐蚀
B.加热不与空气反应
C.硬度小于纯铜
D.可以完全溶解在稀盐酸中
2.“真金不怕火炼”主要是指金 ( )
A.熔点高 B.延展性好 C.有金属光泽 D.化学性质稳定
3.国产大飞机壳使用了先进的铝锂合金材料。已知金属锂(Li)的活动性比铝强。下列有关说法错误的是 ( )
A.铝锂合金硬度大、密度小
B.铝在空气中表面会形成致密的氧化膜
C.锂能与盐酸反应,放出热量,生成氢气
D.锂能与氧气反应,生成的Li2O中Li显+2价
4.不能由金属和酸直接反应得到的化合物是 ( )
A.ZnSO4 B.Al2(SO4)3 C.FeCl3 D.MgCl2
5.[2020·台州] 铁在海水中容易被锈蚀,通常在轮船的吃水线以下焊接比铁更活泼的金属块,用于保护铁质船壳。该金属块的材料可以是 ( )
A.金 B.银 C.铜 D.锌
6.[2020·百色] 探究铁、铜、镁的金属活动性时,下列现象、分析或结论正确的是 ( )
A.铜片表面有气泡产生
B.盛有镁片的试管外壁发烫
C.铁片与盐酸反应速率最快
D.它们的活动性:Cu>Fe>Mg
7.将一枚洁净的铁钉浸入稀硫酸中,下列叙述中正确的是 ( )
①铁钉表面产生气泡 ②液体由无色逐渐变为浅绿色 ③铁钉的质量减少 ④液体的质量减少
A.②③ B.①②④ C.①②③ D.①②③④
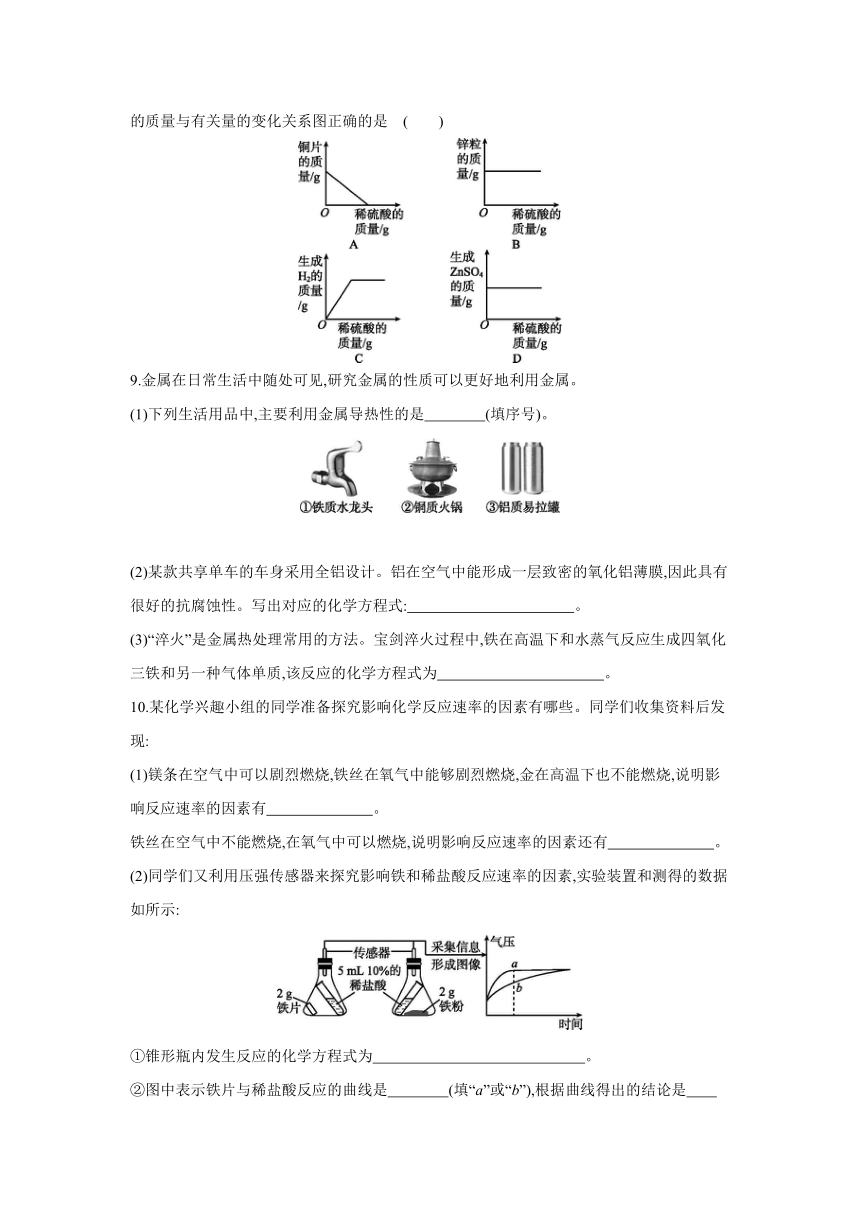
8.[2020·金华] 取一定质量的锌粒和铜片于同一敞口容器中,再逐渐加入稀硫酸。加入稀硫酸的质量与有关量的变化关系图正确的是 ( )
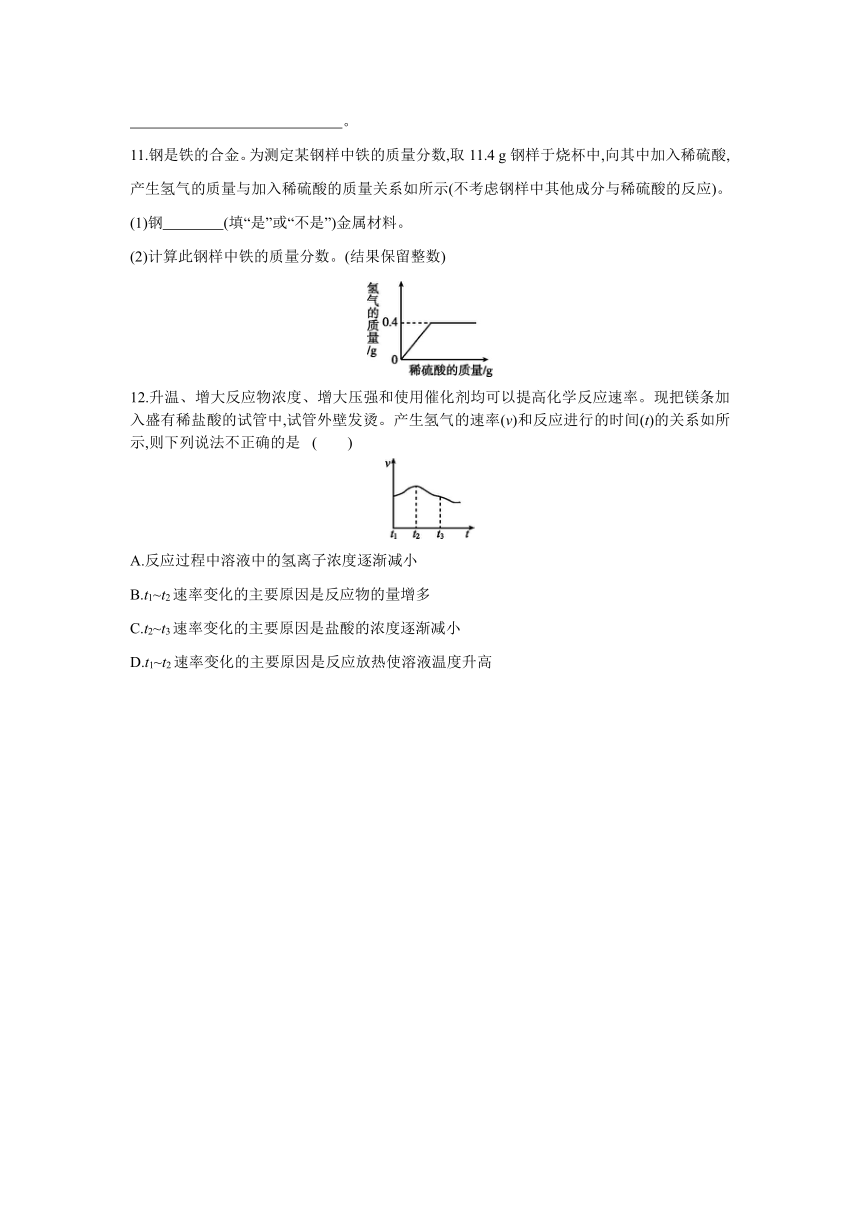
9.金属在日常生活中随处可见,研究金属的性质可以更好地利用金属。
(1)下列生活用品中,主要利用金属导热性的是 (填序号)。
(2)某款共享单车的车身采用全铝设计。铝在空气中能形成一层致密的氧化铝薄膜,因此具有很好的抗腐蚀性。写出对应的化学方程式: 。
(3)“淬火”是金属热处理常用的方法。宝剑淬火过程中,铁在高温下和水蒸气反应生成四氧化三铁和另一种气体单质,该反应的化学方程式为 。
10.某化学兴趣小组的同学准备探究影响化学反应速率的因素有哪些。同学们收集资料后发现:
(1)镁条在空气中可以剧烈燃烧,铁丝在氧气中能够剧烈燃烧,金在高温下也不能燃烧,说明影响反应速率的因素有 。
铁丝在空气中不能燃烧,在氧气中可以燃烧,说明影响反应速率的因素还有 。
(2)同学们又利用压强传感器来探究影响铁和稀盐酸反应速率的因素,实验装置和测得的数据如所示:
①锥形瓶内发生反应的化学方程式为 。
②图中表示铁片与稀盐酸反应的曲线是 (填“a”或“b”),根据曲线得出的结论是
。
11.钢是铁的合金。为测定某钢样中铁的质量分数,取11.4 g钢样于烧杯中,向其中加入稀硫酸,产生氢气的质量与加入稀硫酸的质量关系如所示(不考虑钢样中其他成分与稀硫酸的反应)。
(1)钢 (填“是”或“不是”)金属材料。
(2)计算此钢样中铁的质量分数。(结果保留整数)
12.升温、增大反应物浓度、增大压强和使用催化剂均可以提高化学反应速率。现把镁条加入盛有稀盐酸的试管中,试管外壁发烫。产生氢气的速率(v)和反应进行的时间(t)的关系如所示,则下列说法不正确的是 ( )
A.反应过程中溶液中的氢离子浓度逐渐减小
B.t1~t2速率变化的主要原因是反应物的量增多
C.t2~t3速率变化的主要原因是盐酸的浓度逐渐减小
D.t1~t2速率变化的主要原因是反应放热使溶液温度升高
课题2 金属的化学性质
第2课时 置换反应和金属活动性顺序
1.判断正误:(在括号内打“√”或“×”)
(1)有单质和化合物生成的反应一定是置换反应 ( )
(2)在金属活动性顺序中,铜是位于氢后面的金属,不能与硝酸银溶液反应 ( )
(3)比较铁和铜的活动性强弱可以用硫酸镁溶液 ( )
(4)Cu+AgNO3CuNO3+Ag ( )
(5)铁与硫酸铜溶液反应后,溶液质量增加 ( )
(6)SnO2+2CSn+2CO↑属于置换反应 ( )
2.下列反应属于置换反应的是 ( )
A.2Mg+O2 2MgO
B.3CO+Fe2O3 2Fe+3CO2
C.C+2CuO2Cu+CO2↑
D.2HgO 2Hg+O2 ↑
[核心知识]
1.在金属活动性顺序里:①金属的位置越靠前,它的活动性就越强;②位于氢前面的金属能置换出盐酸、稀硫酸中的氢;③位于前面的金属(K、Ca、Na除外)能把位于后面的金属从它们化合物的溶液中置换出来。
2. 置换反应的表达式:A+BCAC+B。
[易错点拨]
1. 有单质和化合物参加的反应不一定是置换反应,如:CH4+2O2CO2+2H2O;有单质和化合物生成的反应也不一定是置换反应,如:CuO+COCu+CO2。
2.金属(K、Ca、Na除外)与另一种金属化合物的溶液反应时,金属的位置与氢的位置无关。
1.根据金属活动性顺序判断,下列容器与所盛溶液不会发生化学反应的是 ( )
A.用铁质容器盛盐酸
B.用铜质容器盛盐酸
C.用铁质容器盛硝酸银溶液
D.用铜质容器盛硝酸银溶液
2.下列反应属于置换反应的是 ( )
A.Fe2O3+3CO2Fe+3CO2
B.CH4+2O2CO2+2H2O
C.2Na+2H2O2NaOH+H2↑
D.Na2CO3+CaCl2↓+2NaCl
3.以下实验能比较出铜和银的金属活动性强弱的是( )
A.测定两金属的密度
B.将铜片放入硝酸银溶液中
C.将两种金属片互相刻画
D.将铜片、银片分别放入稀硫酸中
4.[2021·青海] 现有X、Y、Z三种金属单质,如果把X和Y分别放入稀硫酸中,Y溶解并产生氢气,X不反应;又把X和Z分别放入硝酸银溶液中,过一会儿,在X表面有银析出,而Z没有变化。根据以上实验事实,判断X、Y、Z金属活动性由强到弱的顺序是 ( )
A.X、Y、Z B.Y、X、Z C.Z、Y、X D.X、Z、Y
5.已知化学反应:X+YSO4 Y+XSO4,根据此反应判断下列说法正确的是 ( )
A.X一定是金属铁
B.Y一定是金属铜
C.X的金属活动性比Y强
D.Y的金属活动性比X强
6.[2021·自贡] 为验证铁、铜、银的金属活动性顺序,某同学设计了如所示四组实验。下列说法错误的是 ( )
A.通过实验①②,能验证金属活动性:Fe>Cu
B.通过实验①②③,能验证金属活动性:Fe>Cu>Ag
C.实验④中X为Cu,Y为FeSO4溶液,能验证金属活动性:Fe>Cu
D.实验④中X为Cu,Y为AgNO3溶液,能验证金属活动性:Cu>Ag
7.某工厂排放只含有少量硫酸和硫酸铜的废液。某同学取适量废液,放入盛有一定量锌粉的烧杯中,搅拌,待充分反应后过滤,得少量滤渣和滤液。关于该实验,下列说法正确的是 ( )
A.反应后液体只含有硫酸锌
B.实验所得滤液是纯水,可直接排放
C.滤渣中一定含铜和锌
D.发生的反应都是置换反应
8.为验证铝的化学性质比铜活泼,在铝丝放入CuSO4溶液前要进行的一个操作是 ,原因是 ;将铝丝放入硫酸铜溶液中充分反应后,铝丝表面出现的变化是 ,溶液的变化是 。
9.用粗木棍在涂有蜡的锌板上写“明”“和”两个字,露出下面的锌板。向“明”字上滴加CuSO4溶液,向“和”字上滴加盐酸。
(1)“明”字上的现象是 。
(2)“和”字上产生气泡,用化学方程式解释: 。
10.下面是某小组探究金属化学性质的两组实验。
实验Ⅰ
实验Ⅱ
(1)实验Ⅰ中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不合理,理由是 。
(2)写出实验Ⅱ中C试管内反应的化学方程式: 。
(3)实验Ⅱ中要验证Cu、Fe、Ag的金属活动性顺序,至少要做的实验是 (填字母)。
11.[2020·江西改编] 小组同学收集了某种铝制易拉罐,剪成条状并打磨后进行0所示实验,发现纯铝片表面有划痕。
0
[发现问题] 根据所学知识,合金的硬度比组成它的纯金属硬度更 ,结合上述现象,可得出该易拉罐不是由纯铝制作的。那么易拉罐中除铝外,还含有什么金属呢
[查阅资料] ①铝制易拉罐中的主要成分是铝,可能还含有镁、铁。
②铝能与氢氧化钠溶液反应:2Al+2NaOH+2H2O2NaAlO2+3H2↑;镁和铁不能与氢氧化钠溶液反应。
[作出猜想] 组成该易拉罐的金属除铝外,可能还有镁、铁中的一种或两种。
[实验设计] 小明取打磨后的铝制易拉罐样品按如下方案进行实验:
实验步骤 实验现象 解释与结论
(1)取一定量样品于烧杯中,加入足量的 溶液,充分反应后过滤、洗涤、干燥 固体表面有大量气泡产生,过滤后得到黑色粉末 样品中含铝
(2)取少量上述黑色粉末于试管中,加入足量的稀盐酸 固体全部溶解,有气泡产生,溶液变成浅绿色 样品中含铁,发生反应的化学方程 式为
[实验结论] 小明得出该易拉罐由铝和铁组成。
[反思评价] 其他同学分析后认为小明的实验方案不严谨,理由是
。大家认为应该补充下列实验:取步骤(1)中少量黑色粉末于试管中,加入某种金属化合物溶液后,如果无现象产生,则小明的结论正确。你认为加入的金属化合物溶液中阳离子对应的金属理论上可以是 (填一种即可)。
[拓展应用] 1为国家颁布的“城市生活垃圾分类标志”,废弃易拉罐应放入标有
(填字母)图标的垃圾桶内。
1
答案
[核心·易错]
1.(1)× (2)× (3)× (4)√
2.(1)× 3Fe+2O2Fe3O4
(2)× 2Cu+O22CuO
(3)× 铜与盐酸不反应
(4)× Fe+2HClFeCl2+H2↑
(5)× 2Al +3H2SO4Al2(SO4)3+3H2↑
[应考能力提升练]
1.A 合金比组成它们的纯金属耐腐蚀性好;黄铜中的铜、锌在空气中加热均能与氧气发生反应;合金的硬度大于组成它们的纯金属的硬度,因此,黄铜的硬度大于纯铜的硬度;黄铜中的铜与稀盐酸不反应,锌与稀盐酸反应生成氯化锌和氢气,黄铜能部分溶解在稀盐酸中。
2.D “真金不怕火炼”是指金即使在高温条件下也不与氧气反应,说明金的化学性质稳定。
3.D 锂与氧气反应生成的Li2O中,O为-2价,Li为+1 价。
4.C
5.D 轮船的吃水线以下焊接比铁更活泼的金属块,用于保护铁质船壳,在所给出的金属中锌比铁活泼。
6.B 铜与盐酸不反应,不会产生气泡;镁与盐酸反应放出热量,故试管外壁发烫;镁比铁活泼,故镁与盐酸反应速率最快;由反应现象可知,它们的活动性:Mg>Fe>Cu。
7.C 铁和稀硫酸反应生成浅绿色的硫酸亚铁溶液和氢气,铁溶解到稀硫酸中,铁钉质量减少,液体的质量增加。
8.C 铜不与稀硫酸反应,铜片的质量在加入稀硫酸后不变;锌能与稀硫酸反应,随着稀硫酸的加入,锌粒质量逐渐减少直至为零;随着稀硫酸的加入,氢气和硫酸锌的质量由零逐渐增加,直至锌粒完全反应后不再增加。
9.(1)②
(2)4Al+3O22Al2O3
(3)3Fe+4H2O(气)Fe3O4+4H2
10.(1)反应物本身的性质 反应物的浓度
(2)①Fe+2HClFeCl2+H2↑
②b 其他条件相同时,反应物间的接触面积越大,反应速率越快
11.(1)是
(2)解:设11.4 g钢样中铁的质量为x。
Fe+H2SO4FeSO4+H2↑
56 2
x 0.4 g
= x=11.2 g
钢样中铁的质量分数为×100%=98%。
答:此钢样中铁的质量分数为98%。
[初高衔接拓展练]
12.B 反应过程中溶液中的氢离子浓度逐渐减小;随着反应进行,反应物的量减少;t2~t3速率变化的主要原因是盐酸的浓度逐渐减小;试管外壁发烫,说明反应放热,因此t1~t2速率变化的主要原因是反应放热使溶液温度升高。
答案
[核心·易错]
1.(1)× (2)× (3)× (4)× (5)× (6)√
2.C
[应考能力提升练]
1.B
2.C 置换反应是指一种单质和一种化合物反应,生成另一种单质和另一种化合物的反应。C选项的化学方程式中,Na和H2是单质,H2O和NaOH是化合物,符合置换反应的定义。
3.B 4.B
5.C 根据X+YSO4 Y+XSO4可判断X的金属活动性比Y强,但X不一定是金属铁,Y不一定是金属铜。
6.B ①中铁和稀硫酸反应生成氢气,说明铁排在氢前面,②中铜与稀硫酸不反应,说明铜排在氢后面,能验证金属活动性:Fe>Cu,③中铁和硝酸银反应生成银,说明铁比银活泼,但通过①②③不能比较铜和银的活动性强弱。
7.D 反应后的液体中一定含有硫酸锌,可能含有硫酸、硫酸铜;滤液直接排放会导致水体或土壤被污染;滤渣中一定有铜,可能含有锌,只有锌过量时,滤渣才含铜和锌;锌和硫酸反应生成硫酸锌和氢气,锌和硫酸铜反应生成铜和硫酸锌,都是一种单质和一种化合物反应生成另一种单质和另一种化合物,发生的反应都是置换反应。
8.用砂纸打磨 铝丝的表面有一层致密的氧化铝薄膜,要先除去 铝丝表面覆盖一层红色物质 溶液由蓝色变为无色
9.(1)“明”字位置逐渐出现红色固体,溶液由蓝色变为无色
(2)Zn+2HClZnCl2+H2↑
10.(1)所用酸的种类不同 (2)Cu+2AgNO32Ag+Cu(NO3)2 (3)CD
[初高衔接拓展练]
11.[发现问题] 大
[实验设计] (1)氢氧化钠
(2)Fe+2HClFeCl2+H2↑
[反思评价] 无法确定易拉罐中是否含有镁 铁(合理即可)
[拓展应用] B
第1课时 金属与氧气、盐酸、稀硫酸的反应
1.判断正误:(在括号内打“√”或“×”)
(1)“真金不怕火炼”说明黄金的硬度非常大 ( )
(2)铝的抗腐蚀性能比铁强,铝的金属活动性比铁弱 ( )
(3)铁丝在氧气中燃烧生成黑色的氧化铁 ( )
(4)利用稀盐酸可以区分黄铜和铜 ( )
2.判断下列化学方程式的正误(在括号内打“√”或“×”),并将错误的化学方程式更正,不能反应的写出错因。
(1)4Fe+3O22Fe2O3( )
(2)2Cu+O22CuO( )
(3)Cu+2HClCuCl2+H2↑( )
(4)2Fe+6HCl2FeCl3+3H2↑( )
(5)Al+H2SO4AlSO4+H2( )
[核心知识]
1.镁、铝等在常温下就能与氧气反应;铁、铜等在常温下几乎不与氧气反应,但在高温时能与氧气反应;金不与氧气反应。
2.镁、锌、铁能与盐酸、稀硫酸反应生成氢气,且镁反应最剧烈,锌次之,铁反应较为缓慢;铜不能与盐酸、稀硫酸反应。
[易错点拨]
1.铝的化学性质较活泼,由于其常温下能与氧气反应,表面生成一层致密的氧化铝薄膜,故其抗腐蚀性能很好。
2.铁与盐酸或稀硫酸等发生反应时,一般只能生成亚铁离子(铁元素由0价变为+2价),反应后的溶液颜色变成浅绿色。
1.黄铜是铜与锌的合金。下列关于黄铜的说法正确的是 ( )
A.比纯铜耐腐蚀
B.加热不与空气反应
C.硬度小于纯铜
D.可以完全溶解在稀盐酸中
2.“真金不怕火炼”主要是指金 ( )
A.熔点高 B.延展性好 C.有金属光泽 D.化学性质稳定
3.国产大飞机壳使用了先进的铝锂合金材料。已知金属锂(Li)的活动性比铝强。下列有关说法错误的是 ( )
A.铝锂合金硬度大、密度小
B.铝在空气中表面会形成致密的氧化膜
C.锂能与盐酸反应,放出热量,生成氢气
D.锂能与氧气反应,生成的Li2O中Li显+2价
4.不能由金属和酸直接反应得到的化合物是 ( )
A.ZnSO4 B.Al2(SO4)3 C.FeCl3 D.MgCl2
5.[2020·台州] 铁在海水中容易被锈蚀,通常在轮船的吃水线以下焊接比铁更活泼的金属块,用于保护铁质船壳。该金属块的材料可以是 ( )
A.金 B.银 C.铜 D.锌
6.[2020·百色] 探究铁、铜、镁的金属活动性时,下列现象、分析或结论正确的是 ( )
A.铜片表面有气泡产生
B.盛有镁片的试管外壁发烫
C.铁片与盐酸反应速率最快
D.它们的活动性:Cu>Fe>Mg
7.将一枚洁净的铁钉浸入稀硫酸中,下列叙述中正确的是 ( )
①铁钉表面产生气泡 ②液体由无色逐渐变为浅绿色 ③铁钉的质量减少 ④液体的质量减少
A.②③ B.①②④ C.①②③ D.①②③④
8.[2020·金华] 取一定质量的锌粒和铜片于同一敞口容器中,再逐渐加入稀硫酸。加入稀硫酸的质量与有关量的变化关系图正确的是 ( )
9.金属在日常生活中随处可见,研究金属的性质可以更好地利用金属。
(1)下列生活用品中,主要利用金属导热性的是 (填序号)。
(2)某款共享单车的车身采用全铝设计。铝在空气中能形成一层致密的氧化铝薄膜,因此具有很好的抗腐蚀性。写出对应的化学方程式: 。
(3)“淬火”是金属热处理常用的方法。宝剑淬火过程中,铁在高温下和水蒸气反应生成四氧化三铁和另一种气体单质,该反应的化学方程式为 。
10.某化学兴趣小组的同学准备探究影响化学反应速率的因素有哪些。同学们收集资料后发现:
(1)镁条在空气中可以剧烈燃烧,铁丝在氧气中能够剧烈燃烧,金在高温下也不能燃烧,说明影响反应速率的因素有 。
铁丝在空气中不能燃烧,在氧气中可以燃烧,说明影响反应速率的因素还有 。
(2)同学们又利用压强传感器来探究影响铁和稀盐酸反应速率的因素,实验装置和测得的数据如所示:
①锥形瓶内发生反应的化学方程式为 。
②图中表示铁片与稀盐酸反应的曲线是 (填“a”或“b”),根据曲线得出的结论是
。
11.钢是铁的合金。为测定某钢样中铁的质量分数,取11.4 g钢样于烧杯中,向其中加入稀硫酸,产生氢气的质量与加入稀硫酸的质量关系如所示(不考虑钢样中其他成分与稀硫酸的反应)。
(1)钢 (填“是”或“不是”)金属材料。
(2)计算此钢样中铁的质量分数。(结果保留整数)
12.升温、增大反应物浓度、增大压强和使用催化剂均可以提高化学反应速率。现把镁条加入盛有稀盐酸的试管中,试管外壁发烫。产生氢气的速率(v)和反应进行的时间(t)的关系如所示,则下列说法不正确的是 ( )
A.反应过程中溶液中的氢离子浓度逐渐减小
B.t1~t2速率变化的主要原因是反应物的量增多
C.t2~t3速率变化的主要原因是盐酸的浓度逐渐减小
D.t1~t2速率变化的主要原因是反应放热使溶液温度升高
课题2 金属的化学性质
第2课时 置换反应和金属活动性顺序
1.判断正误:(在括号内打“√”或“×”)
(1)有单质和化合物生成的反应一定是置换反应 ( )
(2)在金属活动性顺序中,铜是位于氢后面的金属,不能与硝酸银溶液反应 ( )
(3)比较铁和铜的活动性强弱可以用硫酸镁溶液 ( )
(4)Cu+AgNO3CuNO3+Ag ( )
(5)铁与硫酸铜溶液反应后,溶液质量增加 ( )
(6)SnO2+2CSn+2CO↑属于置换反应 ( )
2.下列反应属于置换反应的是 ( )
A.2Mg+O2 2MgO
B.3CO+Fe2O3 2Fe+3CO2
C.C+2CuO2Cu+CO2↑
D.2HgO 2Hg+O2 ↑
[核心知识]
1.在金属活动性顺序里:①金属的位置越靠前,它的活动性就越强;②位于氢前面的金属能置换出盐酸、稀硫酸中的氢;③位于前面的金属(K、Ca、Na除外)能把位于后面的金属从它们化合物的溶液中置换出来。
2. 置换反应的表达式:A+BCAC+B。
[易错点拨]
1. 有单质和化合物参加的反应不一定是置换反应,如:CH4+2O2CO2+2H2O;有单质和化合物生成的反应也不一定是置换反应,如:CuO+COCu+CO2。
2.金属(K、Ca、Na除外)与另一种金属化合物的溶液反应时,金属的位置与氢的位置无关。
1.根据金属活动性顺序判断,下列容器与所盛溶液不会发生化学反应的是 ( )
A.用铁质容器盛盐酸
B.用铜质容器盛盐酸
C.用铁质容器盛硝酸银溶液
D.用铜质容器盛硝酸银溶液
2.下列反应属于置换反应的是 ( )
A.Fe2O3+3CO2Fe+3CO2
B.CH4+2O2CO2+2H2O
C.2Na+2H2O2NaOH+H2↑
D.Na2CO3+CaCl2↓+2NaCl
3.以下实验能比较出铜和银的金属活动性强弱的是( )
A.测定两金属的密度
B.将铜片放入硝酸银溶液中
C.将两种金属片互相刻画
D.将铜片、银片分别放入稀硫酸中
4.[2021·青海] 现有X、Y、Z三种金属单质,如果把X和Y分别放入稀硫酸中,Y溶解并产生氢气,X不反应;又把X和Z分别放入硝酸银溶液中,过一会儿,在X表面有银析出,而Z没有变化。根据以上实验事实,判断X、Y、Z金属活动性由强到弱的顺序是 ( )
A.X、Y、Z B.Y、X、Z C.Z、Y、X D.X、Z、Y
5.已知化学反应:X+YSO4 Y+XSO4,根据此反应判断下列说法正确的是 ( )
A.X一定是金属铁
B.Y一定是金属铜
C.X的金属活动性比Y强
D.Y的金属活动性比X强
6.[2021·自贡] 为验证铁、铜、银的金属活动性顺序,某同学设计了如所示四组实验。下列说法错误的是 ( )
A.通过实验①②,能验证金属活动性:Fe>Cu
B.通过实验①②③,能验证金属活动性:Fe>Cu>Ag
C.实验④中X为Cu,Y为FeSO4溶液,能验证金属活动性:Fe>Cu
D.实验④中X为Cu,Y为AgNO3溶液,能验证金属活动性:Cu>Ag
7.某工厂排放只含有少量硫酸和硫酸铜的废液。某同学取适量废液,放入盛有一定量锌粉的烧杯中,搅拌,待充分反应后过滤,得少量滤渣和滤液。关于该实验,下列说法正确的是 ( )
A.反应后液体只含有硫酸锌
B.实验所得滤液是纯水,可直接排放
C.滤渣中一定含铜和锌
D.发生的反应都是置换反应
8.为验证铝的化学性质比铜活泼,在铝丝放入CuSO4溶液前要进行的一个操作是 ,原因是 ;将铝丝放入硫酸铜溶液中充分反应后,铝丝表面出现的变化是 ,溶液的变化是 。
9.用粗木棍在涂有蜡的锌板上写“明”“和”两个字,露出下面的锌板。向“明”字上滴加CuSO4溶液,向“和”字上滴加盐酸。
(1)“明”字上的现象是 。
(2)“和”字上产生气泡,用化学方程式解释: 。
10.下面是某小组探究金属化学性质的两组实验。
实验Ⅰ
实验Ⅱ
(1)实验Ⅰ中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不合理,理由是 。
(2)写出实验Ⅱ中C试管内反应的化学方程式: 。
(3)实验Ⅱ中要验证Cu、Fe、Ag的金属活动性顺序,至少要做的实验是 (填字母)。
11.[2020·江西改编] 小组同学收集了某种铝制易拉罐,剪成条状并打磨后进行0所示实验,发现纯铝片表面有划痕。
0
[发现问题] 根据所学知识,合金的硬度比组成它的纯金属硬度更 ,结合上述现象,可得出该易拉罐不是由纯铝制作的。那么易拉罐中除铝外,还含有什么金属呢
[查阅资料] ①铝制易拉罐中的主要成分是铝,可能还含有镁、铁。
②铝能与氢氧化钠溶液反应:2Al+2NaOH+2H2O2NaAlO2+3H2↑;镁和铁不能与氢氧化钠溶液反应。
[作出猜想] 组成该易拉罐的金属除铝外,可能还有镁、铁中的一种或两种。
[实验设计] 小明取打磨后的铝制易拉罐样品按如下方案进行实验:
实验步骤 实验现象 解释与结论
(1)取一定量样品于烧杯中,加入足量的 溶液,充分反应后过滤、洗涤、干燥 固体表面有大量气泡产生,过滤后得到黑色粉末 样品中含铝
(2)取少量上述黑色粉末于试管中,加入足量的稀盐酸 固体全部溶解,有气泡产生,溶液变成浅绿色 样品中含铁,发生反应的化学方程 式为
[实验结论] 小明得出该易拉罐由铝和铁组成。
[反思评价] 其他同学分析后认为小明的实验方案不严谨,理由是
。大家认为应该补充下列实验:取步骤(1)中少量黑色粉末于试管中,加入某种金属化合物溶液后,如果无现象产生,则小明的结论正确。你认为加入的金属化合物溶液中阳离子对应的金属理论上可以是 (填一种即可)。
[拓展应用] 1为国家颁布的“城市生活垃圾分类标志”,废弃易拉罐应放入标有
(填字母)图标的垃圾桶内。
1
答案
[核心·易错]
1.(1)× (2)× (3)× (4)√
2.(1)× 3Fe+2O2Fe3O4
(2)× 2Cu+O22CuO
(3)× 铜与盐酸不反应
(4)× Fe+2HClFeCl2+H2↑
(5)× 2Al +3H2SO4Al2(SO4)3+3H2↑
[应考能力提升练]
1.A 合金比组成它们的纯金属耐腐蚀性好;黄铜中的铜、锌在空气中加热均能与氧气发生反应;合金的硬度大于组成它们的纯金属的硬度,因此,黄铜的硬度大于纯铜的硬度;黄铜中的铜与稀盐酸不反应,锌与稀盐酸反应生成氯化锌和氢气,黄铜能部分溶解在稀盐酸中。
2.D “真金不怕火炼”是指金即使在高温条件下也不与氧气反应,说明金的化学性质稳定。
3.D 锂与氧气反应生成的Li2O中,O为-2价,Li为+1 价。
4.C
5.D 轮船的吃水线以下焊接比铁更活泼的金属块,用于保护铁质船壳,在所给出的金属中锌比铁活泼。
6.B 铜与盐酸不反应,不会产生气泡;镁与盐酸反应放出热量,故试管外壁发烫;镁比铁活泼,故镁与盐酸反应速率最快;由反应现象可知,它们的活动性:Mg>Fe>Cu。
7.C 铁和稀硫酸反应生成浅绿色的硫酸亚铁溶液和氢气,铁溶解到稀硫酸中,铁钉质量减少,液体的质量增加。
8.C 铜不与稀硫酸反应,铜片的质量在加入稀硫酸后不变;锌能与稀硫酸反应,随着稀硫酸的加入,锌粒质量逐渐减少直至为零;随着稀硫酸的加入,氢气和硫酸锌的质量由零逐渐增加,直至锌粒完全反应后不再增加。
9.(1)②
(2)4Al+3O22Al2O3
(3)3Fe+4H2O(气)Fe3O4+4H2
10.(1)反应物本身的性质 反应物的浓度
(2)①Fe+2HClFeCl2+H2↑
②b 其他条件相同时,反应物间的接触面积越大,反应速率越快
11.(1)是
(2)解:设11.4 g钢样中铁的质量为x。
Fe+H2SO4FeSO4+H2↑
56 2
x 0.4 g
= x=11.2 g
钢样中铁的质量分数为×100%=98%。
答:此钢样中铁的质量分数为98%。
[初高衔接拓展练]
12.B 反应过程中溶液中的氢离子浓度逐渐减小;随着反应进行,反应物的量减少;t2~t3速率变化的主要原因是盐酸的浓度逐渐减小;试管外壁发烫,说明反应放热,因此t1~t2速率变化的主要原因是反应放热使溶液温度升高。
答案
[核心·易错]
1.(1)× (2)× (3)× (4)× (5)× (6)√
2.C
[应考能力提升练]
1.B
2.C 置换反应是指一种单质和一种化合物反应,生成另一种单质和另一种化合物的反应。C选项的化学方程式中,Na和H2是单质,H2O和NaOH是化合物,符合置换反应的定义。
3.B 4.B
5.C 根据X+YSO4 Y+XSO4可判断X的金属活动性比Y强,但X不一定是金属铁,Y不一定是金属铜。
6.B ①中铁和稀硫酸反应生成氢气,说明铁排在氢前面,②中铜与稀硫酸不反应,说明铜排在氢后面,能验证金属活动性:Fe>Cu,③中铁和硝酸银反应生成银,说明铁比银活泼,但通过①②③不能比较铜和银的活动性强弱。
7.D 反应后的液体中一定含有硫酸锌,可能含有硫酸、硫酸铜;滤液直接排放会导致水体或土壤被污染;滤渣中一定有铜,可能含有锌,只有锌过量时,滤渣才含铜和锌;锌和硫酸反应生成硫酸锌和氢气,锌和硫酸铜反应生成铜和硫酸锌,都是一种单质和一种化合物反应生成另一种单质和另一种化合物,发生的反应都是置换反应。
8.用砂纸打磨 铝丝的表面有一层致密的氧化铝薄膜,要先除去 铝丝表面覆盖一层红色物质 溶液由蓝色变为无色
9.(1)“明”字位置逐渐出现红色固体,溶液由蓝色变为无色
(2)Zn+2HClZnCl2+H2↑
10.(1)所用酸的种类不同 (2)Cu+2AgNO32Ag+Cu(NO3)2 (3)CD
[初高衔接拓展练]
11.[发现问题] 大
[实验设计] (1)氢氧化钠
(2)Fe+2HClFeCl2+H2↑
[反思评价] 无法确定易拉罐中是否含有镁 铁(合理即可)
[拓展应用] B
同课章节目录
