第6章常用的金属和盐-测试题—2021-2022学年九年级化学沪教版(上海)第二学期(word版有答案)
文档属性
| 名称 | 第6章常用的金属和盐-测试题—2021-2022学年九年级化学沪教版(上海)第二学期(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 156.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-06 00:00:00 | ||
图片预览


文档简介
第6章常用的金属和盐-测试题-2021-2022学年九年级化学沪教版(上海)第二学期
一、单选题
1.下列变化不属于氧化反应的是( )
A.动物的呼吸 B.盐酸除铁锈 C.铁制品生锈 D.天然气燃烧
2.下列关于金属利用的说法错误的是( )
A.用铝制高压电线 B.用钨制灯丝
C.用纯铁制机床底座 D.用铝粉制防锈漆
3.下列离子能在含有硫酸的溶液中大量共存的是( )
A.Mg2+、
B.Na+、
C.K+、OH-
D.Ba2+、C1-
4.下列有关化肥或农药的叙述错误的是( )
A.硫酸铵属于复合肥料,所含的营养元素是氮和硫
B.氯化铵和磷矿粉从外观即可区分
C.农药施用后,会通过农作物、农产品等发生转移
D.化肥和农药施用不当,会对环境造成污染
5.若利用碱的性质进行下列实验,不能达到相应目的的是
A.分别加入少量Mg(OH)2固体,根据是否溶解,可鉴别稀盐酸和Na2CO3溶液
B.分别加入适量水溶解,根据温度是否明显升高,可鉴别NaOH固体和NaCl固体
C.分别加入Ba(OH)2溶液,根据是否产生沉淀,可鉴别MgCl2溶液和Na2SO4溶液
D.分别加入熟石灰粉末研磨,根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体
6.下列物品主要是由合金制成的是( )
A.塑料水杯 B.青铜铸像 C.汽车轮胎 D.羊毛大衣
7.将一定质量的铁粉加入到Mg(NO3)2、AgNO3的混合溶液中,充分反应后过滤,得到滤液和滤渣。向滤液中加入稀盐酸,无明显现象。下列叙述正确的是( )
A.滤液中一定含有Mg2+和Fe3+
B.滤液中含有Mg2+和Ag+
C.滤渣中一定含有Ag
D.滤渣中可能含有Mg
8.根据金属活动性顺序判断,下列容器与所盛溶液不会发生化学反应的是
A.用铁制容器盛盐酸 B.用铜制容器盛盐酸
C.用铁制容器盛硝酸银溶液 D.用铜制容器盛硝酸银溶液
9.下列除去物质中所含少量杂质的方法错误的是
选项 物质 杂质 除杂质的方法
A 稀硫酸 铜 过滤
B CaSO4溶液 稀硫酸 过量CaCO3 粉末、过滤
C FeCl2溶液 CuCl2 过量铁粉、过滤
D 二氧化碳 一氧化碳 点燃
A.A B.B C.C D.D
10.某同学根据铜锈的成分Cu2(OH)2CO3作出猜想:引起金属铜锈蚀的因素除有氧气和水外,还应该有二氧化碳。为证明“必须有二氧化碳”,需要进行下列实验中的
A.甲和乙 B.甲和丁 C.乙和丁 D.丙和丁
11.某学习小组同学做完铁与稀硫酸反应实验后,将反应后的混合物M全部倒入盛有一小块铜锌合金的烧杯中,发现有大量气泡产生。待充分反应后过滤,得到滤液和滤渣。他们得出的现象或结论如下:①M中一定不含铁单质;②烧杯中溶液由浅绿色变成蓝色;③滤液中一定含有ZnSO4;④滤渣中可能含有三种金属单质;⑤滤液中可能含有两种金属离子。其中正确的个数有:
A.4个 B.3个 C.2个 D.1个
二、简答题
12.化学材料直接影响人们的生活,下图是医院常用的药瓶和注射器,请回答下列问题:
(1)图中所示材料中,含有的金属单质为__(填化学式,写出一种即可,下同),属于有机合成材料的是__。
(2)瓶口橡皮塞用铝箔包裹,而不用铁皮的原因是____。
(3)钢针常用不锈钢制造,原因是钢的硬度大且不易生锈,钢和生铁的区别是__不同。
(4)若玻璃瓶内是氯化钠溶液,该溶液可以补充人体所需的__元素(填“常量”或“微量”)。
(5)废旧铝箔、钢针不能随意丢弃,应回收利用,这样做的意义是__。
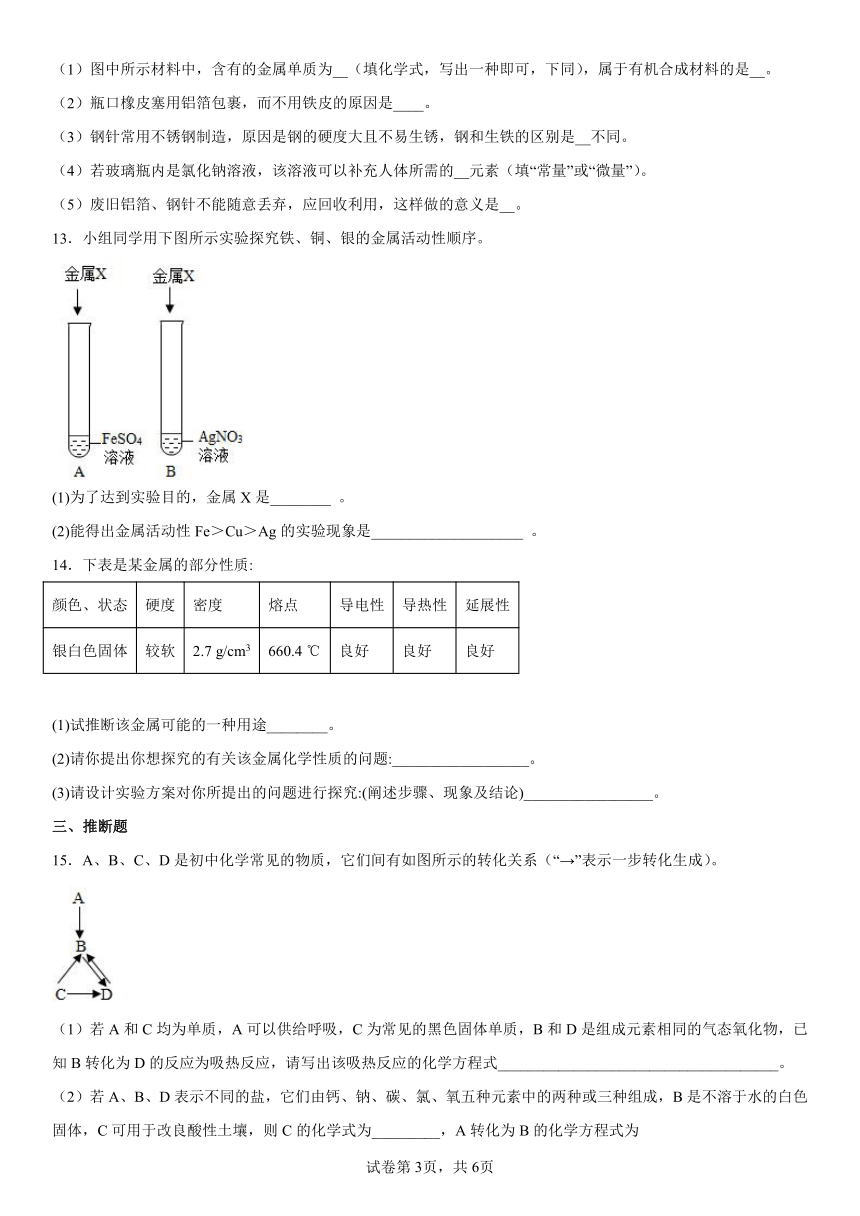
13.小组同学用下图所示实验探究铁、铜、银的金属活动性顺序。
(1)为了达到实验目的,金属X是________ 。
(2)能得出金属活动性Fe>Cu>Ag的实验现象是____________________ 。
14.下表是某金属的部分性质:
颜色、状态 硬度 密度 熔点 导电性 导热性 延展性
银白色固体 较软 2.7 g/cm3 660.4 ℃ 良好 良好 良好
(1)试推断该金属可能的一种用途________。
(2)请你提出你想探究的有关该金属化学性质的问题:__________________。
(3)请设计实验方案对你所提出的问题进行探究:(阐述步骤、现象及结论)_________________。
三、推断题
15.A、B、C、D是初中化学常见的物质,它们间有如图所示的转化关系(“→”表示一步转化生成)。
(1)若A和C均为单质,A可以供给呼吸,C为常见的黑色固体单质,B和D是组成元素相同的气态氧化物,已知B转化为D的反应为吸热反应,请写出该吸热反应的化学方程式_____________________________________。
(2)若A、B、D表示不同的盐,它们由钙、钠、碳、氯、氧五种元素中的两种或三种组成,B是不溶于水的白色固体,C可用于改良酸性土壤,则C的化学式为_________,A转化为B的化学方程式为_____________________________________________。
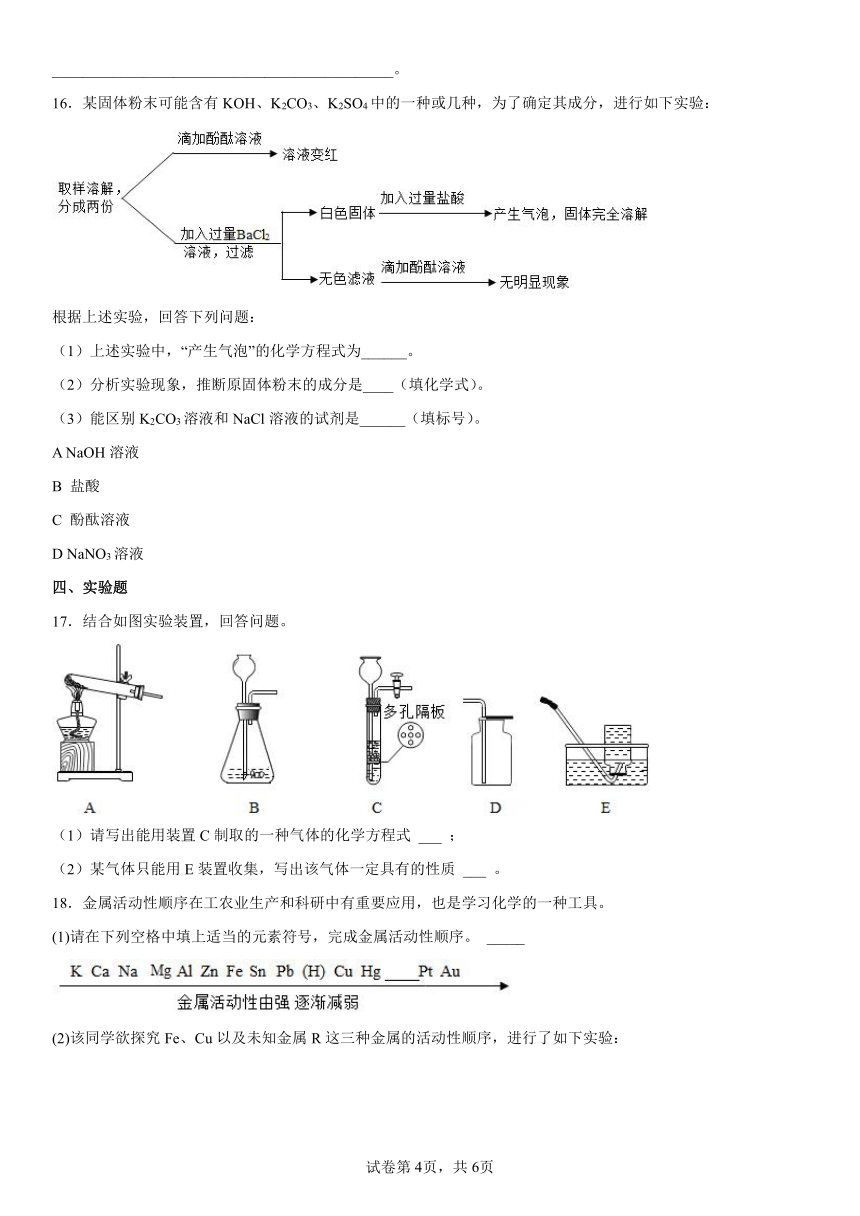
16.某固体粉末可能含有KOH、K2CO3、K2SO4中的一种或几种,为了确定其成分,进行如下实验:
根据上述实验,回答下列问题:
(1)上述实验中,“产生气泡”的化学方程式为______。
(2)分析实验现象,推断原固体粉末的成分是____(填化学式)。
(3)能区别K2CO3溶液和NaCl溶液的试剂是______(填标号)。
A NaOH溶液
B 盐酸
C 酚酞溶液
D NaNO3溶液
四、实验题
17.结合如图实验装置,回答问题。
(1)请写出能用装置C制取的一种气体的化学方程式 ___ ;
(2)某气体只能用E装置收集,写出该气体一定具有的性质 ___ 。
18.金属活动性顺序在工农业生产和科研中有重要应用,也是学习化学的一种工具。
(1)请在下列空格中填上适当的元素符号,完成金属活动性顺序。 _____
(2)该同学欲探究Fe、Cu以及未知金属R这三种金属的活动性顺序,进行了如下实验:
①A中只有铁片上产生气泡,则Cu、R排在H ___________ (填“前”“后”)。
②B中只有一片金属上覆盖了金属Cu,其化学反应方程式为 __________ ;联系(1)中的结论,得出三种金属的活动性由强到弱的顺序为 _______________ 。
(3)为了验证探究铁、铜、银的金属活动性强弱,设计了如下图所示的两个实验。
①实验1的目的是 ____________ ;其化学方程式是 __________ 。
②实验2中,为了达到实验目的,溶液甲可以是 __________ 或 ____________ (写两种物质)。
19.根据如图实验装置图,回答相关问题。
(1)甲是测定空气中氧气含量的两个实验,实验时发现实验B测量更准确,原因是___。
(2)乙中铁钉最易生锈的部位是___(填“a”或“b”)。
(3)丙中①④为用紫色石蕊溶液润湿的棉球,②③为浸过紫色石蕊溶液的干燥棉球,缓慢通入CO2后,最先变红的是___。(填编号,下同)不变红的是___。
(4)丁是探究Cu和Ag的金属活动性顺序,无色溶液可能是___(填编号)。
①稀H2SO4
②FeSO4溶液
③Cu(NO3)2溶液
④AgNO3溶液
写出相应反应的化学方程式___。
五、计算题
20.某工厂利用废铁屑与废硫酸反应制取硫酸亚铁。现有废硫酸20t,H2SO4的质量分数为9.8%,与足量的废铁屑反应,可生产FeSO4的质量是多少?(Fe+H2SO4=FeSO4+H2↑)
21.实验室里用8.0g粗锌与足量稀硫酸反应制得氢气0.2g,该反应的化学方程式为(粗锌所含的杂质不跟稀硫酸反应)。
(1)硫酸(H2SO4)中S、O元素质量比是 。
(2)列式计算粗锌中锌的质量分数。
22.钙是生物体骨骼的重要组成元素。鱼骨中含有碳酸钙,现设计图甲实验测定鱼骨中的碳酸钙含量,并将测得的数据绘制成图乙。
提示①食醋的主要成分是醋酸(HAc)。醋酸和碳酸钙反应的化学方程式为CaCO3+2Hac=CaAc2+H2O+CO2
②鱼骨中其它成分与食醋反应生成的气体可忽略不计
(1)该实验中浓硫酸的作用是___________。
(2)由图乙中的AB曲线,可知锥形瓶中反应速率的变化情况是___________(选填“变大”、“变小”或“不变)。
(3)根据图中的数据计算鱼骨中碳酸钙的质量分数___________。
(4)生活中,用喝醋的方法除去卡在咽上的鱼刺,这种做法是不科学的。请你结合实验结果加以说明___________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.C
3.A
4.A
5.C
6.B
7.C
8.B
9.D
10.B
11.A
12. Al 塑料 铝在空气中能与氧气反应生成一层致密的氧化物保护膜,阻止铝进一步被氧化,而铁皮易生锈; 含碳量; 常量; 可以减少环境污染,节约金属资源。
13. 铜 A中无明显现象,B中有固体析出(对析出固体的颜色不做要求),溶液逐渐变蓝
14. 作导线 该金属是否能与氧气反应 取一段该金属,打磨光亮,再用酒精灯灼烧,看有无变化;若金属表面有变化,说明该金属能与氧气反应,否则不能(其他合理答案也可)
15. C + CO2 2CO Ca(OH)2 CaCl2+Na2CO3=CaCO3↓+2NaCl
16. K2CO3 BC
17. CaCO3+2HCl=CaCl2+H2O+CO2↑ 一定具有不溶于水,不与水反应的性质
18. Ag “后” Fe+CuSO4=FeSO4+Cu Fe>Cu>R 验证铜、银的金属活动性强弱 Cu+2AgNO3=2Ag+Cu(NO3)2 稀盐酸 CuSO4溶液、FeSO4溶液(回答合理即可给分)
19. 装置始终密封,气密性更好 b ④ ②③ ④
20.设硫酸亚铁的质量为x,
所以生成硫酸亚铁的质量是3.04t。
21.(1)1:2
(2)81.25%
解:设参加反应的锌的质量为x,则有
粗锌中锌的质量分数为×100%=81.25%;
答:粗锌中锌的质量分数为81.25%。
22. 吸收二氧化碳携带的水蒸气,防止实验结果不准确 变小 生成二氧化碳的质量为:820g﹣819.89=0.11g
解:设鱼骨中碳酸钙的质量分数为x
x=1.25%
答:鱼骨中碳酸钙的质量分数为1.25% 要使鱼骨中的碳酸钙完全反应需要的时间太长
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列变化不属于氧化反应的是( )
A.动物的呼吸 B.盐酸除铁锈 C.铁制品生锈 D.天然气燃烧
2.下列关于金属利用的说法错误的是( )
A.用铝制高压电线 B.用钨制灯丝
C.用纯铁制机床底座 D.用铝粉制防锈漆
3.下列离子能在含有硫酸的溶液中大量共存的是( )
A.Mg2+、
B.Na+、
C.K+、OH-
D.Ba2+、C1-
4.下列有关化肥或农药的叙述错误的是( )
A.硫酸铵属于复合肥料,所含的营养元素是氮和硫
B.氯化铵和磷矿粉从外观即可区分
C.农药施用后,会通过农作物、农产品等发生转移
D.化肥和农药施用不当,会对环境造成污染
5.若利用碱的性质进行下列实验,不能达到相应目的的是
A.分别加入少量Mg(OH)2固体,根据是否溶解,可鉴别稀盐酸和Na2CO3溶液
B.分别加入适量水溶解,根据温度是否明显升高,可鉴别NaOH固体和NaCl固体
C.分别加入Ba(OH)2溶液,根据是否产生沉淀,可鉴别MgCl2溶液和Na2SO4溶液
D.分别加入熟石灰粉末研磨,根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体
6.下列物品主要是由合金制成的是( )
A.塑料水杯 B.青铜铸像 C.汽车轮胎 D.羊毛大衣
7.将一定质量的铁粉加入到Mg(NO3)2、AgNO3的混合溶液中,充分反应后过滤,得到滤液和滤渣。向滤液中加入稀盐酸,无明显现象。下列叙述正确的是( )
A.滤液中一定含有Mg2+和Fe3+
B.滤液中含有Mg2+和Ag+
C.滤渣中一定含有Ag
D.滤渣中可能含有Mg
8.根据金属活动性顺序判断,下列容器与所盛溶液不会发生化学反应的是
A.用铁制容器盛盐酸 B.用铜制容器盛盐酸
C.用铁制容器盛硝酸银溶液 D.用铜制容器盛硝酸银溶液
9.下列除去物质中所含少量杂质的方法错误的是
选项 物质 杂质 除杂质的方法
A 稀硫酸 铜 过滤
B CaSO4溶液 稀硫酸 过量CaCO3 粉末、过滤
C FeCl2溶液 CuCl2 过量铁粉、过滤
D 二氧化碳 一氧化碳 点燃
A.A B.B C.C D.D
10.某同学根据铜锈的成分Cu2(OH)2CO3作出猜想:引起金属铜锈蚀的因素除有氧气和水外,还应该有二氧化碳。为证明“必须有二氧化碳”,需要进行下列实验中的
A.甲和乙 B.甲和丁 C.乙和丁 D.丙和丁
11.某学习小组同学做完铁与稀硫酸反应实验后,将反应后的混合物M全部倒入盛有一小块铜锌合金的烧杯中,发现有大量气泡产生。待充分反应后过滤,得到滤液和滤渣。他们得出的现象或结论如下:①M中一定不含铁单质;②烧杯中溶液由浅绿色变成蓝色;③滤液中一定含有ZnSO4;④滤渣中可能含有三种金属单质;⑤滤液中可能含有两种金属离子。其中正确的个数有:
A.4个 B.3个 C.2个 D.1个
二、简答题
12.化学材料直接影响人们的生活,下图是医院常用的药瓶和注射器,请回答下列问题:
(1)图中所示材料中,含有的金属单质为__(填化学式,写出一种即可,下同),属于有机合成材料的是__。
(2)瓶口橡皮塞用铝箔包裹,而不用铁皮的原因是____。
(3)钢针常用不锈钢制造,原因是钢的硬度大且不易生锈,钢和生铁的区别是__不同。
(4)若玻璃瓶内是氯化钠溶液,该溶液可以补充人体所需的__元素(填“常量”或“微量”)。
(5)废旧铝箔、钢针不能随意丢弃,应回收利用,这样做的意义是__。
13.小组同学用下图所示实验探究铁、铜、银的金属活动性顺序。
(1)为了达到实验目的,金属X是________ 。
(2)能得出金属活动性Fe>Cu>Ag的实验现象是____________________ 。
14.下表是某金属的部分性质:
颜色、状态 硬度 密度 熔点 导电性 导热性 延展性
银白色固体 较软 2.7 g/cm3 660.4 ℃ 良好 良好 良好
(1)试推断该金属可能的一种用途________。
(2)请你提出你想探究的有关该金属化学性质的问题:__________________。
(3)请设计实验方案对你所提出的问题进行探究:(阐述步骤、现象及结论)_________________。
三、推断题
15.A、B、C、D是初中化学常见的物质,它们间有如图所示的转化关系(“→”表示一步转化生成)。
(1)若A和C均为单质,A可以供给呼吸,C为常见的黑色固体单质,B和D是组成元素相同的气态氧化物,已知B转化为D的反应为吸热反应,请写出该吸热反应的化学方程式_____________________________________。
(2)若A、B、D表示不同的盐,它们由钙、钠、碳、氯、氧五种元素中的两种或三种组成,B是不溶于水的白色固体,C可用于改良酸性土壤,则C的化学式为_________,A转化为B的化学方程式为_____________________________________________。
16.某固体粉末可能含有KOH、K2CO3、K2SO4中的一种或几种,为了确定其成分,进行如下实验:
根据上述实验,回答下列问题:
(1)上述实验中,“产生气泡”的化学方程式为______。
(2)分析实验现象,推断原固体粉末的成分是____(填化学式)。
(3)能区别K2CO3溶液和NaCl溶液的试剂是______(填标号)。
A NaOH溶液
B 盐酸
C 酚酞溶液
D NaNO3溶液
四、实验题
17.结合如图实验装置,回答问题。
(1)请写出能用装置C制取的一种气体的化学方程式 ___ ;
(2)某气体只能用E装置收集,写出该气体一定具有的性质 ___ 。
18.金属活动性顺序在工农业生产和科研中有重要应用,也是学习化学的一种工具。
(1)请在下列空格中填上适当的元素符号,完成金属活动性顺序。 _____
(2)该同学欲探究Fe、Cu以及未知金属R这三种金属的活动性顺序,进行了如下实验:
①A中只有铁片上产生气泡,则Cu、R排在H ___________ (填“前”“后”)。
②B中只有一片金属上覆盖了金属Cu,其化学反应方程式为 __________ ;联系(1)中的结论,得出三种金属的活动性由强到弱的顺序为 _______________ 。
(3)为了验证探究铁、铜、银的金属活动性强弱,设计了如下图所示的两个实验。
①实验1的目的是 ____________ ;其化学方程式是 __________ 。
②实验2中,为了达到实验目的,溶液甲可以是 __________ 或 ____________ (写两种物质)。
19.根据如图实验装置图,回答相关问题。
(1)甲是测定空气中氧气含量的两个实验,实验时发现实验B测量更准确,原因是___。
(2)乙中铁钉最易生锈的部位是___(填“a”或“b”)。
(3)丙中①④为用紫色石蕊溶液润湿的棉球,②③为浸过紫色石蕊溶液的干燥棉球,缓慢通入CO2后,最先变红的是___。(填编号,下同)不变红的是___。
(4)丁是探究Cu和Ag的金属活动性顺序,无色溶液可能是___(填编号)。
①稀H2SO4
②FeSO4溶液
③Cu(NO3)2溶液
④AgNO3溶液
写出相应反应的化学方程式___。
五、计算题
20.某工厂利用废铁屑与废硫酸反应制取硫酸亚铁。现有废硫酸20t,H2SO4的质量分数为9.8%,与足量的废铁屑反应,可生产FeSO4的质量是多少?(Fe+H2SO4=FeSO4+H2↑)
21.实验室里用8.0g粗锌与足量稀硫酸反应制得氢气0.2g,该反应的化学方程式为(粗锌所含的杂质不跟稀硫酸反应)。
(1)硫酸(H2SO4)中S、O元素质量比是 。
(2)列式计算粗锌中锌的质量分数。
22.钙是生物体骨骼的重要组成元素。鱼骨中含有碳酸钙,现设计图甲实验测定鱼骨中的碳酸钙含量,并将测得的数据绘制成图乙。
提示①食醋的主要成分是醋酸(HAc)。醋酸和碳酸钙反应的化学方程式为CaCO3+2Hac=CaAc2+H2O+CO2
②鱼骨中其它成分与食醋反应生成的气体可忽略不计
(1)该实验中浓硫酸的作用是___________。
(2)由图乙中的AB曲线,可知锥形瓶中反应速率的变化情况是___________(选填“变大”、“变小”或“不变)。
(3)根据图中的数据计算鱼骨中碳酸钙的质量分数___________。
(4)生活中,用喝醋的方法除去卡在咽上的鱼刺,这种做法是不科学的。请你结合实验结果加以说明___________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.C
3.A
4.A
5.C
6.B
7.C
8.B
9.D
10.B
11.A
12. Al 塑料 铝在空气中能与氧气反应生成一层致密的氧化物保护膜,阻止铝进一步被氧化,而铁皮易生锈; 含碳量; 常量; 可以减少环境污染,节约金属资源。
13. 铜 A中无明显现象,B中有固体析出(对析出固体的颜色不做要求),溶液逐渐变蓝
14. 作导线 该金属是否能与氧气反应 取一段该金属,打磨光亮,再用酒精灯灼烧,看有无变化;若金属表面有变化,说明该金属能与氧气反应,否则不能(其他合理答案也可)
15. C + CO2 2CO Ca(OH)2 CaCl2+Na2CO3=CaCO3↓+2NaCl
16. K2CO3 BC
17. CaCO3+2HCl=CaCl2+H2O+CO2↑ 一定具有不溶于水,不与水反应的性质
18. Ag “后” Fe+CuSO4=FeSO4+Cu Fe>Cu>R 验证铜、银的金属活动性强弱 Cu+2AgNO3=2Ag+Cu(NO3)2 稀盐酸 CuSO4溶液、FeSO4溶液(回答合理即可给分)
19. 装置始终密封,气密性更好 b ④ ②③ ④
20.设硫酸亚铁的质量为x,
所以生成硫酸亚铁的质量是3.04t。
21.(1)1:2
(2)81.25%
解:设参加反应的锌的质量为x,则有
粗锌中锌的质量分数为×100%=81.25%;
答:粗锌中锌的质量分数为81.25%。
22. 吸收二氧化碳携带的水蒸气,防止实验结果不准确 变小 生成二氧化碳的质量为:820g﹣819.89=0.11g
解:设鱼骨中碳酸钙的质量分数为x
x=1.25%
答:鱼骨中碳酸钙的质量分数为1.25% 要使鱼骨中的碳酸钙完全反应需要的时间太长
答案第1页,共2页
答案第1页,共2页
