第四单元 盐化肥同步练习—2021-2022学年九年级化学人教版(五四学制)全一册(word版有答案)
文档属性
| 名称 | 第四单元 盐化肥同步练习—2021-2022学年九年级化学人教版(五四学制)全一册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 95.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-06 00:00:00 | ||
图片预览



文档简介
第四单元《盐 化肥》同步练习—2021-2022学年九年级化学人教版(五四学制)全一册
一、单选题
1.下列各组离子在溶液中能大量共存的是( )
A.NH、SO、NO
B.H+、Ba2+、OH-
C.Fe2+、Na+、OH-
D.Ca2+、Cl-、CO
2.化肥对提高农作物的产量有重要作用。下列有关化肥的说法不正确的是
A.提倡农家肥与化肥综合使用
B.草木灰是一种农家肥,其主要成分中含有钾元素
C.磷肥的主要作用是促进植物茎、叶生长茂盛,叶色浓绿
D.常用作氮肥的化合物有尿素、碳酸氢铵等
3.若利用碱的性质进行下列实验,不能达到相应目的的是
A.分别加入少量Mg(OH)2固体,根据是否溶解,可鉴别稀盐酸和Na2CO3溶液
B.分别加入适量水溶解,根据温度是否明显升高,可鉴别NaOH固体和NaCl固体
C.分别加入Ba(OH)2溶液,根据是否产生沉淀,可鉴别MgCl2溶液和Na2SO4溶液
D.分别加入熟石灰粉末研磨,根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体
4.某pH=12的无色溶液中大量存在的离子有Na+、Ba2+、NO、X,则X可能是
A.Cu2+ B.Cl- C.H+ D.SO
5.下列有关水的说法正确的是
A.为了保护水资源,应禁止使用农药、化肥
B.水是由氢原子和氧原子构成的
C.净化水的方法有沉淀、过滤、吸附、蒸馏、加肥皂水等
D.电解水时,与电源正极相连的电极上产生的气体是氧气
6.下列溶液分别能跟硫酸铜、盐酸、碳酸钠溶液反应,并产生不同现象的是( )
A.Ca(OH)2 B.AgNO3 C.H2SO4 D.NaOH
7.下列物质的用途,利用了其物理性质的是
A.生石灰用作干燥剂 B.铁粉用作食品保鲜吸氧剂
C.氦气填充飞艇 D.小苏打用于治疗胃酸过多
8.河道两旁有甲、乙两厂,它们排放的工业废水中共含有H+、Na+、Ba2+、Cl-、SO、CO六种离子。两厂废水中各含三种离子,其中甲厂的废水明显呈酸性,甲厂废水中的离子是( )
A.H+、Na+、Ba2+
B.H+、Ba2+、Cl-
C.Na+、SO、CO
D.H+、SO、CO
9.下列实验目的与所用试剂相符的是
A.证明NaOH溶液中含有Na2CO3――酚酞试剂
B.证明NaOH溶液中含有Na2CO3――澄清石灰水
C.除去NaOH溶液中的Na2CO3杂质――稀盐酸
D.除去NaOH溶液中的Na2CO3杂质――CaCl2溶液
二、简答题
10.请用化学方程式表示下列反应的原理。
(1)铝比较活泼,但铝制品却有较好的抗腐蚀性能。
(2)干粉灭火器中的干粉(主要成分是NaHCO3)受热时分解生成碳酸钠、二氧化碳和水。
11.现有下列五种物质:稀盐酸、稀硫酸、石灰水、氢氧化钠溶液、碳酸钠溶液.请你从中任选取两种物质进行鉴别.
(1)你选择取的两种物质是:_____
(2)你鉴别它们的方法是:(只写出鉴别所用的试剂或方法即可)方法一:__方法二:__.
12.为除去粗盐中CaCl2、MgCl2、Na2SO4等可溶性杂质,需进行如下操作:①溶解;②依次加过量的BaCl2、NaOH、Na2CO3溶液;③过滤;④加适量盐酸;⑤蒸发、结晶。【提示:Mg(OH)2、BaSO4、BaCO3难溶于水;微溶物不形成沉淀;Na2CO3溶液呈碱性】
(1)操作①、③、⑤要用到同一种玻璃仪器,该仪器在操作⑤中的作用是什么?
(2)写出一个加入碳酸钠溶液时所发生反应的化学方程式。
(3)请设计实验方案证明操作③所得溶液中含有NaOH。(写出实验步骤和现象,结论)
三、推断题
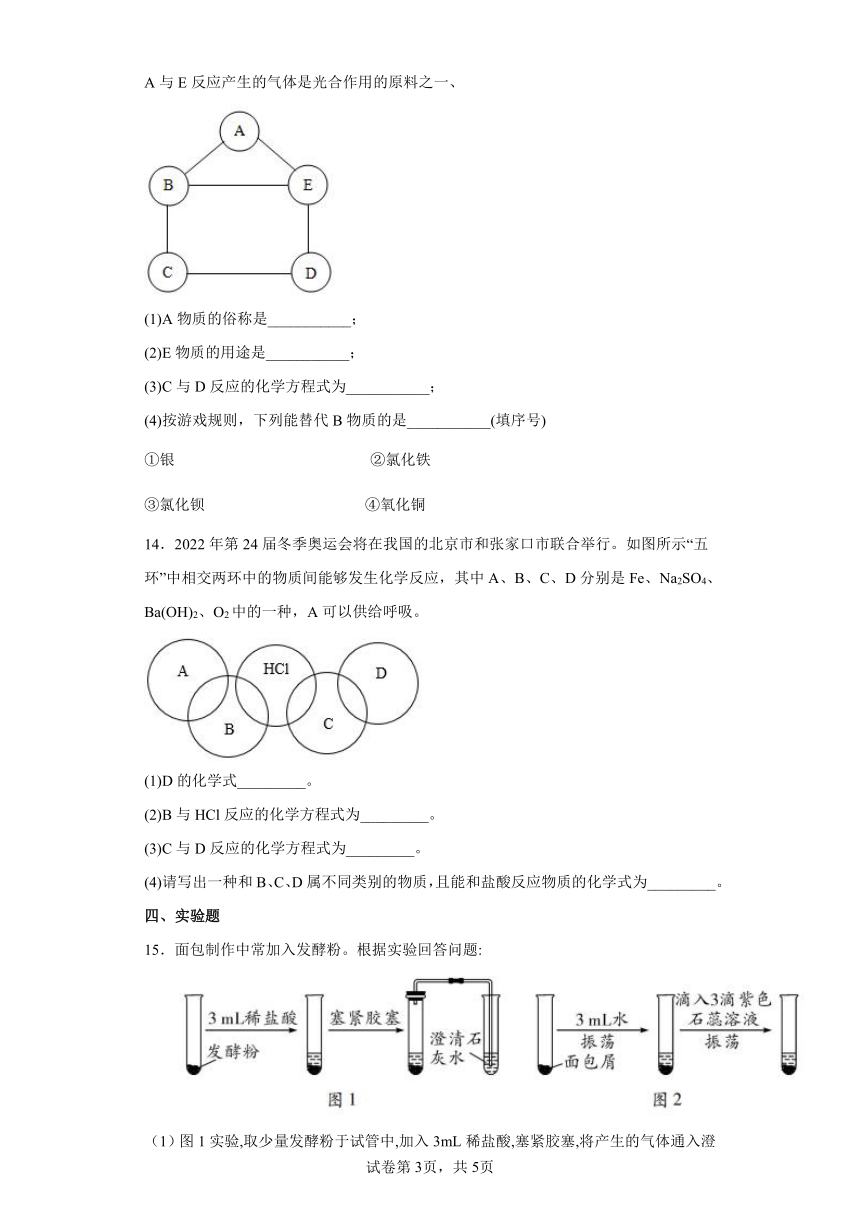
13.某化学兴趣小组用铁、硫酸、氢氧化钡、硫酸铜和碳酸钠五种物质玩化学拼图游戏(如图),游戏规则要求图中相邻物质之间能发生化学反应,其中C物质的溶液呈蓝色,A与E反应产生的气体是光合作用的原料之一、
(1)A物质的俗称是___________;
(2)E物质的用途是___________;
(3)C与D反应的化学方程式为___________;
(4)按游戏规则,下列能替代B物质的是___________(填序号)
①银 ②氯化铁
③氯化钡 ④氧化铜
14.2022年第24届冬季奥运会将在我国的北京市和张家口市联合举行。如图所示“五环”中相交两环中的物质间能够发生化学反应,其中A、B、C、D分别是Fe、Na2SO4、Ba(OH)2、O2中的一种,A可以供给呼吸。
(1)D的化学式_________。
(2)B与HCl反应的化学方程式为_________。
(3)C与D反应的化学方程式为_________。
(4)请写出一种和B、C、D属不同类别的物质,且能和盐酸反应物质的化学式为_________。
四、实验题
15.面包制作中常加入发酵粉。根据实验回答问题:
(1)图1实验,取少量发酵粉于试管中,加入3mL稀盐酸,塞紧胶塞,将产生的气体通入澄清石灰水中,澄清石灰水变浑浊。发酵粉的主要成分为__________,加入稀盐酸发生反应的化学方程式为__________________。
(2)有同学取适量面包屑于试管中充分加热,面包屑逐渐变黄再变黑,试管口有无色液体生成,由此认为制作面包的面粉中一定含有碳、氢、氧三种元素。你是否认同 ___________。(填“是”或“否”),理由是________________。
(3)面粉经发酵后会产生乳酸和醋酸,虽经过烘焙,但依然会有一些残留。图2中,将面包屑与少量水混合后滴入紫色石蕊溶液,溶液颜色变为_____________色。面包中含有较多的食品添加剂,用于改善其品质,“食品添加剂对人体都是有害的”,这种说法对吗 _____________。(填“不对”或“对”)。
16.进行如下实验,研究物质的性质。
(1)A中滴入稀盐酸后溶液由红色变为无色。此时A中一定含有的溶质是______。
(2)B中验证鸡蛋壳中含有碳酸盐,滴入稀盐酸后,应补充的操作是______。
(3)C中观察到______的实验现象,说明金属活动性顺序中锌位于铜前。
五、计算题
17.现有11 g含有少量氯化钠的某纯碱样品,为了测定该样品中的碳酸钠的质量分数,将该纯碱样品全部溶解在100 g水中,再加入氯化钙溶液141 g,恰好完全反应,经过滤后测得所得溶液质量为242 g,请计算:
(1)纯碱样品中碳酸钠的质量分数(计算结果保留到0.1%)。
(2)所得溶液中溶质的质量分数。
18.洁厕灵的有效成分为HCl,李强同学测定某品牌洁厕灵中HCl的质量分数。他将100.0g洁厕灵倒入锥形瓶中,逐次加入等质量相同质量分数的Na2CO3溶液,测出每次完全反应后溶液的总质量,实验数据记录如下表。
第一次 第二次 第三次 第四次 第五次
加入Na2CO3溶液的质量/g 20.0 20.0 20.0 20.0 20.0
反应后溶液的总质量/g 118.9 137.8 M 175.6 195.6
请根据实验数据分析解答下列问题:
(1)表格中M的数值为 。
(2)恰好完全反应时消耗Na2CO3的质量是多少
(3)该洁厕灵中HC1的质量分数是多少?
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.C
3.C
4.B
5.D
6.A
7.C
8.B
9.B
10.(1)
(2)
11. 稀盐酸、碳酸钠溶液 紫色石蕊溶液 锌粒或稀硫酸等
12.(1)防止液体局部过热,造成液体外溅
(2)Na2CO3+CaCl2═CaCO3↓+2NaCl
(3)取③所得溶液,加入足量氯化钡溶液,静置,向上层清液中滴加无色酚酞溶液,若溶液变红色,则证明所得溶液中含氢氧化钠
13.(1)纯碱或苏打
(2)金属除锈、做化工原料
(3)
(4)③
14. Na2SO4 Fe+2HCl=FeCl2+H2↑ Na2SO4+Ba(OH)2= BaSO4↓+2NaOH Fe2O3
15. 碳酸氢钠(或NaHCO3) 否 面包制作需加水,因此不能判断面粉中是否含有氢元素或氧元素(合理即可) 红 不对
16. NaCl(或NaCl和酚酞) 将产生的气体通入澄清石灰水 锌的表面出现红色固体,溶液由蓝色变为无色
17.(1)纯碱样品中碳酸钠的质量分数=
(2)反应后所得滤液中氯化钠的质量=11.7g +(11g – 10.6g)= 12.1g
所得滤液的溶质质量分数=
答:纯碱样品中碳酸钠的质量分数为96.4%,所得溶液中溶质质量分数为5%。
18.(1)156.7;(2)10.6g;(3)7.3%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列各组离子在溶液中能大量共存的是( )
A.NH、SO、NO
B.H+、Ba2+、OH-
C.Fe2+、Na+、OH-
D.Ca2+、Cl-、CO
2.化肥对提高农作物的产量有重要作用。下列有关化肥的说法不正确的是
A.提倡农家肥与化肥综合使用
B.草木灰是一种农家肥,其主要成分中含有钾元素
C.磷肥的主要作用是促进植物茎、叶生长茂盛,叶色浓绿
D.常用作氮肥的化合物有尿素、碳酸氢铵等
3.若利用碱的性质进行下列实验,不能达到相应目的的是
A.分别加入少量Mg(OH)2固体,根据是否溶解,可鉴别稀盐酸和Na2CO3溶液
B.分别加入适量水溶解,根据温度是否明显升高,可鉴别NaOH固体和NaCl固体
C.分别加入Ba(OH)2溶液,根据是否产生沉淀,可鉴别MgCl2溶液和Na2SO4溶液
D.分别加入熟石灰粉末研磨,根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体
4.某pH=12的无色溶液中大量存在的离子有Na+、Ba2+、NO、X,则X可能是
A.Cu2+ B.Cl- C.H+ D.SO
5.下列有关水的说法正确的是
A.为了保护水资源,应禁止使用农药、化肥
B.水是由氢原子和氧原子构成的
C.净化水的方法有沉淀、过滤、吸附、蒸馏、加肥皂水等
D.电解水时,与电源正极相连的电极上产生的气体是氧气
6.下列溶液分别能跟硫酸铜、盐酸、碳酸钠溶液反应,并产生不同现象的是( )
A.Ca(OH)2 B.AgNO3 C.H2SO4 D.NaOH
7.下列物质的用途,利用了其物理性质的是
A.生石灰用作干燥剂 B.铁粉用作食品保鲜吸氧剂
C.氦气填充飞艇 D.小苏打用于治疗胃酸过多
8.河道两旁有甲、乙两厂,它们排放的工业废水中共含有H+、Na+、Ba2+、Cl-、SO、CO六种离子。两厂废水中各含三种离子,其中甲厂的废水明显呈酸性,甲厂废水中的离子是( )
A.H+、Na+、Ba2+
B.H+、Ba2+、Cl-
C.Na+、SO、CO
D.H+、SO、CO
9.下列实验目的与所用试剂相符的是
A.证明NaOH溶液中含有Na2CO3――酚酞试剂
B.证明NaOH溶液中含有Na2CO3――澄清石灰水
C.除去NaOH溶液中的Na2CO3杂质――稀盐酸
D.除去NaOH溶液中的Na2CO3杂质――CaCl2溶液
二、简答题
10.请用化学方程式表示下列反应的原理。
(1)铝比较活泼,但铝制品却有较好的抗腐蚀性能。
(2)干粉灭火器中的干粉(主要成分是NaHCO3)受热时分解生成碳酸钠、二氧化碳和水。
11.现有下列五种物质:稀盐酸、稀硫酸、石灰水、氢氧化钠溶液、碳酸钠溶液.请你从中任选取两种物质进行鉴别.
(1)你选择取的两种物质是:_____
(2)你鉴别它们的方法是:(只写出鉴别所用的试剂或方法即可)方法一:__方法二:__.
12.为除去粗盐中CaCl2、MgCl2、Na2SO4等可溶性杂质,需进行如下操作:①溶解;②依次加过量的BaCl2、NaOH、Na2CO3溶液;③过滤;④加适量盐酸;⑤蒸发、结晶。【提示:Mg(OH)2、BaSO4、BaCO3难溶于水;微溶物不形成沉淀;Na2CO3溶液呈碱性】
(1)操作①、③、⑤要用到同一种玻璃仪器,该仪器在操作⑤中的作用是什么?
(2)写出一个加入碳酸钠溶液时所发生反应的化学方程式。
(3)请设计实验方案证明操作③所得溶液中含有NaOH。(写出实验步骤和现象,结论)
三、推断题
13.某化学兴趣小组用铁、硫酸、氢氧化钡、硫酸铜和碳酸钠五种物质玩化学拼图游戏(如图),游戏规则要求图中相邻物质之间能发生化学反应,其中C物质的溶液呈蓝色,A与E反应产生的气体是光合作用的原料之一、
(1)A物质的俗称是___________;
(2)E物质的用途是___________;
(3)C与D反应的化学方程式为___________;
(4)按游戏规则,下列能替代B物质的是___________(填序号)
①银 ②氯化铁
③氯化钡 ④氧化铜
14.2022年第24届冬季奥运会将在我国的北京市和张家口市联合举行。如图所示“五环”中相交两环中的物质间能够发生化学反应,其中A、B、C、D分别是Fe、Na2SO4、Ba(OH)2、O2中的一种,A可以供给呼吸。
(1)D的化学式_________。
(2)B与HCl反应的化学方程式为_________。
(3)C与D反应的化学方程式为_________。
(4)请写出一种和B、C、D属不同类别的物质,且能和盐酸反应物质的化学式为_________。
四、实验题
15.面包制作中常加入发酵粉。根据实验回答问题:
(1)图1实验,取少量发酵粉于试管中,加入3mL稀盐酸,塞紧胶塞,将产生的气体通入澄清石灰水中,澄清石灰水变浑浊。发酵粉的主要成分为__________,加入稀盐酸发生反应的化学方程式为__________________。
(2)有同学取适量面包屑于试管中充分加热,面包屑逐渐变黄再变黑,试管口有无色液体生成,由此认为制作面包的面粉中一定含有碳、氢、氧三种元素。你是否认同 ___________。(填“是”或“否”),理由是________________。
(3)面粉经发酵后会产生乳酸和醋酸,虽经过烘焙,但依然会有一些残留。图2中,将面包屑与少量水混合后滴入紫色石蕊溶液,溶液颜色变为_____________色。面包中含有较多的食品添加剂,用于改善其品质,“食品添加剂对人体都是有害的”,这种说法对吗 _____________。(填“不对”或“对”)。
16.进行如下实验,研究物质的性质。
(1)A中滴入稀盐酸后溶液由红色变为无色。此时A中一定含有的溶质是______。
(2)B中验证鸡蛋壳中含有碳酸盐,滴入稀盐酸后,应补充的操作是______。
(3)C中观察到______的实验现象,说明金属活动性顺序中锌位于铜前。
五、计算题
17.现有11 g含有少量氯化钠的某纯碱样品,为了测定该样品中的碳酸钠的质量分数,将该纯碱样品全部溶解在100 g水中,再加入氯化钙溶液141 g,恰好完全反应,经过滤后测得所得溶液质量为242 g,请计算:
(1)纯碱样品中碳酸钠的质量分数(计算结果保留到0.1%)。
(2)所得溶液中溶质的质量分数。
18.洁厕灵的有效成分为HCl,李强同学测定某品牌洁厕灵中HCl的质量分数。他将100.0g洁厕灵倒入锥形瓶中,逐次加入等质量相同质量分数的Na2CO3溶液,测出每次完全反应后溶液的总质量,实验数据记录如下表。
第一次 第二次 第三次 第四次 第五次
加入Na2CO3溶液的质量/g 20.0 20.0 20.0 20.0 20.0
反应后溶液的总质量/g 118.9 137.8 M 175.6 195.6
请根据实验数据分析解答下列问题:
(1)表格中M的数值为 。
(2)恰好完全反应时消耗Na2CO3的质量是多少
(3)该洁厕灵中HC1的质量分数是多少?
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.C
3.C
4.B
5.D
6.A
7.C
8.B
9.B
10.(1)
(2)
11. 稀盐酸、碳酸钠溶液 紫色石蕊溶液 锌粒或稀硫酸等
12.(1)防止液体局部过热,造成液体外溅
(2)Na2CO3+CaCl2═CaCO3↓+2NaCl
(3)取③所得溶液,加入足量氯化钡溶液,静置,向上层清液中滴加无色酚酞溶液,若溶液变红色,则证明所得溶液中含氢氧化钠
13.(1)纯碱或苏打
(2)金属除锈、做化工原料
(3)
(4)③
14. Na2SO4 Fe+2HCl=FeCl2+H2↑ Na2SO4+Ba(OH)2= BaSO4↓+2NaOH Fe2O3
15. 碳酸氢钠(或NaHCO3) 否 面包制作需加水,因此不能判断面粉中是否含有氢元素或氧元素(合理即可) 红 不对
16. NaCl(或NaCl和酚酞) 将产生的气体通入澄清石灰水 锌的表面出现红色固体,溶液由蓝色变为无色
17.(1)纯碱样品中碳酸钠的质量分数=
(2)反应后所得滤液中氯化钠的质量=11.7g +(11g – 10.6g)= 12.1g
所得滤液的溶质质量分数=
答:纯碱样品中碳酸钠的质量分数为96.4%,所得溶液中溶质质量分数为5%。
18.(1)156.7;(2)10.6g;(3)7.3%
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
