第6章常用的金属和盐-复习题-2021-2022学年九年级化学沪教版(上海)第二学期(word版有答案)
文档属性
| 名称 | 第6章常用的金属和盐-复习题-2021-2022学年九年级化学沪教版(上海)第二学期(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 93.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-06 00:00:00 | ||
图片预览



文档简介
第6章常用的金属和盐-复习题-2021-2022学年九年级化学沪教版(上海)第二学期
一、单选题
1.下列金属中,金属活动性最弱的是
A.金 B.银 C.铜 D.铁
2.北斗系统的全面建成彰显了中国航天的力量,在航天科技中会用到大量金属材料。下列有关金属材科的说法正确的是( )
A.合金中一定只含金属元素
B.纯铜比黄铜的硬度更大
C.生锈的钢铁制品没有回收价值
D.钛和钛合金被广泛用于火箭、导弹等
3.2018年3月9日,特朗普正式签署关税令“对进口钢铁和铝分别征收25%的关税”,这一做法严重违反国际贸易规则,严重损害我国利益。下列选项中不属于合金的是
A.钢 B.金刚石 C.焊锡 D.黄铜
4.明代宋应星著的《天工开物》中有关于“火法”冶炼金属锌的工艺记载:“炉甘石(注:主要成分是碳酸锌)十斤,装载入一泥罐內,然后逐层用煤炭饼(注:反应后生成一氧化碳)垫盛,其底铺薪,发火煅红,冷淀,毁罐取出,即倭铅也”。下列说法错误的是
A.煤炭中起作用的主要成分是C
B.冶炼Zn的化学方程式为:
C.该冶炼锌的反应属于置换反应
D.倭铅是指金属锌和铅的混合物
5.铁是一种重要的金属。下列关于铁的叙述错误的是
A.生铁是纯净物
B.涂油漆可防止铁生锈
C.工业上常用赤铁矿冶炼铁
D.铁与硫酸铜溶液的反应属于置换反应
6.下列各组物质在溶液中能大量共存且形成无色溶液的是
A.NaCl BaCl2Na2CO3 B.KNO3HCl CaCl2
C.H2SO4 FeCl3NaNO3 D.NaOH HNO3NH4NO3
7.已知在一定条件下发生反应:甲+乙→丙+丁,下列判断正确的是
A.甲、乙、丙、丁不可能含有同一种元素
B.丙为Cu(NO3)2,则甲可能为单质或氧化物或碱
C.参加反应的甲、乙质量比一定等于生成丙、丁质量比
D.若甲、乙为化合物,则该反应一定为复分解反应
8.西汉时期,人们就会用石灰水或草木灰水(主要成分是K2CO2)等碱性溶液为丝麻脱胶来造纸。下列物质属于碱的是
A.生石灰 B.水 C.熟石灰 D.草木灰
9.验证镁、铜的金属活动性顺序,下列试剂不能选用的是( )
A.MgSO4溶液 B.KCl溶液
C.稀盐酸 D.CuCl2溶液
10.关于"家庭小实验"的下列说法正确的是
A.用自制简易净水器制纯水
B.向洗净的碎鸡蛋壳中加入食醋可产生一氧化碳
C.用白糖、果汁、小苏打、柠檬酸、水自制汽水
D.把钢针烧红放入水中冷却后取出,钢针变得更容易弯曲
11.现有不纯的氧化铜样品16g,所含杂质有镁粉 铁粉 碳酸钙 向其中加入200g溶质质量分数为3.65%的稀盐酸有气泡产生,将气体通入到澄清石灰水变浑浊,充分反应后,过滤得到滤液和滤渣,观察滤液为蓝色 则下列判断不正确的是
A.滤液质量一定大于原稀盐酸的质量
B.滤渣最多有 3种,滤渣的质量一定小于16g
C.反应生成水的质量可能大于1.8g
D.滤液中一定有氯化铜 氯化亚铁 氯化镁 氯化钙
二、简答题
12.在宏观、微观、符号之间建立联系是化学学科的特点。图 1 为元素周期表中的一格, 图 2 是碳酸钠溶液与氢氧化钙溶液反应的微观示意图,
(1)在元素周期表中,钙元素的原子序数为 ____________ 。
(2)写出钙离子的结构示意图 ____________ 。
(3)人体如果缺钙会导致 ____________ 。
(4)图 2 所示反应的微观本质是 ____________ 。
13.你将选用哪种合金来制造下列物品?说明理由。
(1)外科手术刀
(2)防盗门
(3)门锁
(4)自行车支架
14.根据复分解反应发生的条件,并利用书后附录1所提供的信息,判断下列物质间能否发生复分解反应。如能发生反应,写出反应的化学方程式。
(1)碳酸钠溶液和氯化钙溶液
(2)氢氧化钾溶液和盐酸
(3)氢氧化钠溶液和氯化钾溶液
(4)碳酸钾溶液和盐酸
(5)硫酸铜溶液和氯化钡溶液
三、推断题
15.A~H内初中化学常见物质。己知A属于盐,常用作建筑材料, E是赤铁矿石的主要成分,F可用于中和酸性土壤, H 的溶液呈浅绿色。它们的转化关系如图所示(反应条件未完全棕标出)。
(1)写出A的化学式、F的名称: A_________,F________;
(2)写出反应②、④的化学方程式:反应②__________,反应④_________,其中反应④属于四种基本反应类型中的__________反应;
(3)比较D与G的活动性强弱关系: D______G(填“>”或“<”);
(4)C生成F的其化学方程式为_________。
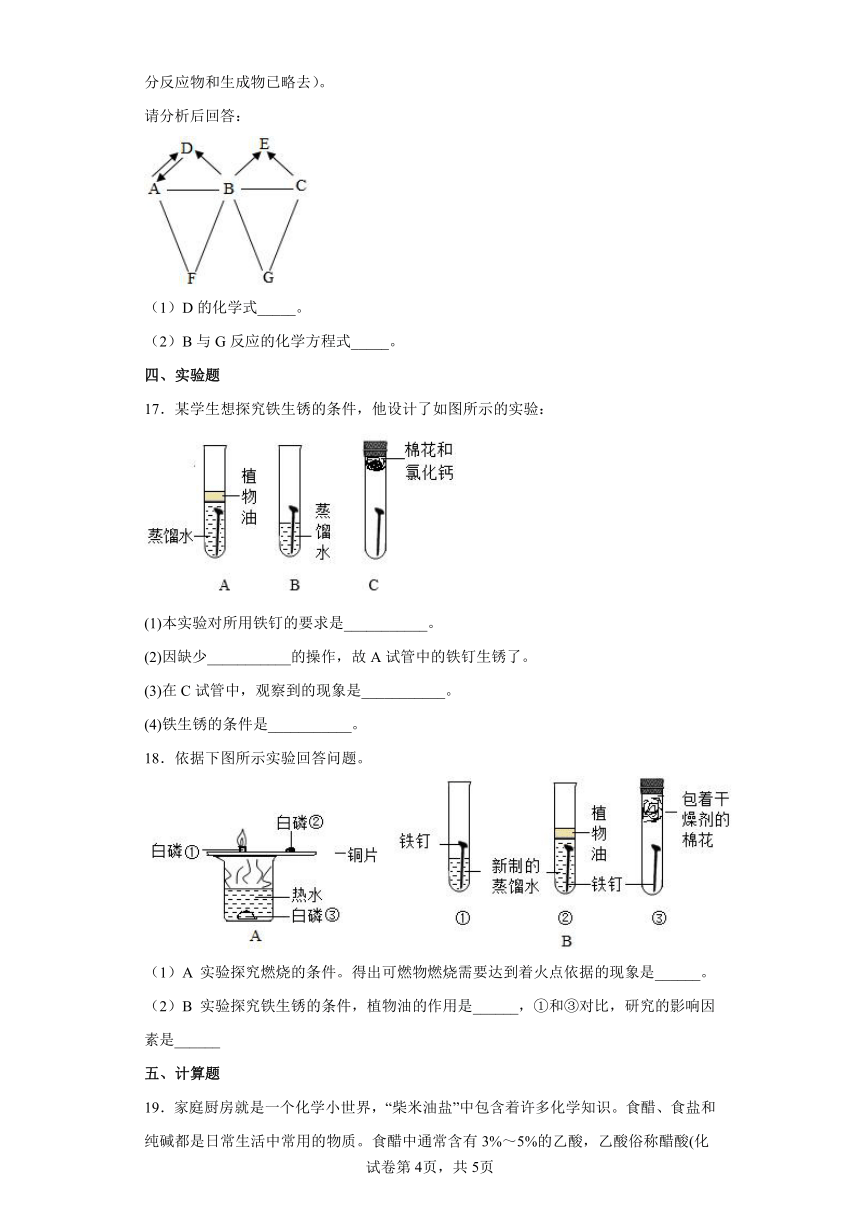
16.已知A~G为初中化学常见的七种物质。其中D的固体叫做“干冰”;B中只含两种元素,C与E不含相同元素。各种物质间的反应和转化关系如图所示(“﹣”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以转化为另一种物质,反应条件、部分反应物和生成物已略去)。
请分析后回答:
(1)D的化学式_____。
(2)B与G反应的化学方程式_____。
四、实验题
17.某学生想探究铁生锈的条件,他设计了如图所示的实验:
(1)本实验对所用铁钉的要求是___________。
(2)因缺少___________的操作,故A试管中的铁钉生锈了。
(3)在C试管中,观察到的现象是___________。
(4)铁生锈的条件是___________。
18.依据下图所示实验回答问题。
(1)A 实验探究燃烧的条件。得出可燃物燃烧需要达到着火点依据的现象是______。
(2)B 实验探究铁生锈的条件,植物油的作用是______,①和③对比,研究的影响因素是______
五、计算题
19.家庭厨房就是一个化学小世界,“柴米油盐”中包含着许多化学知识。食醋、食盐和纯碱都是日常生活中常用的物质。食醋中通常含有3%~5%的乙酸,乙酸俗称醋酸(化学式为CH3COOH),是一种无色液体。食盐和纯碱都是白色固体。
(1)醋酸和纯碱中属于无机物的是________(写化学式)。
(2)醋酸中,C、O两元素的质量之比为________(填最简整数比)。
20.某工厂利用废硫酸溶液与铁反应制取硫酸亚铁。49t废硫酸溶液中的硫酸 与5.6t铁恰好完全反应。求:
(1)废硫酸溶液中溶质的质量分数。
(2)理论上生产的硫酸亚铁的质量。
21.锌与硫酸(H2SO4)反应生成氢气和硫酸锌。实验室里用6.5 g锌与足量硫酸完全反应,请计算:
(1)参加反应硫酸的质量;
(2)可制得氢气的质量和标准状况下氢气的体积 (已知:标准状况下,氢气的密度为0.0899 g/L)(结果精确至0.1L)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.D
3.B
4.D
5.A
6.B
7.B
8.C
9.B
10.C
11.C
12. 20 骨质疏松(或佝偻病或发育不良,合理均可) Ca2+ 和CO32- 结合生成CaCO3沉淀
13.(1)外科手术刀用不锈钢,硬度大、耐腐蚀性好
(2)防盗门使用锰钢,硬度大、韧性好
(3)门锁使用黄铜,耐磨、耐腐蚀
(4)自行车支架使用锰钢,韧性好、硬度大
14.(1)
(2)
(3)不能发生反应
(4)
(5)
15.(1) 氢氧化钙
(2) 置换
(3)>
(4)
16. CO2 HCl+AgNO3=HNO3+AgCl↓
17.(1)洁净光亮
(2)蒸馏水煮沸
(3)铁钉没有生锈
(4)与氧气和水接触
18. 白磷①燃烧(先燃烧),白磷②不燃烧(后燃烧) 隔绝氧气 H2O
19.(1)Na2CO3;(2)3:4
20.解:设废硫酸溶液中溶质的质量分数为x;理论上生产的硫酸亚铁的质量为y
答:(1)废硫酸溶液中溶质的质量分数为20%。
(2)理论上生产的硫酸亚铁的质量15.2t。
21.(1)设参加反应的硫酸的质量x。
则参加反应硫酸的质量为9.8g。
(2)参加反应的硫酸的质量为9.8g、可制得氢气的质量和体积分别为0.2g、2.2L
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列金属中,金属活动性最弱的是
A.金 B.银 C.铜 D.铁
2.北斗系统的全面建成彰显了中国航天的力量,在航天科技中会用到大量金属材料。下列有关金属材科的说法正确的是( )
A.合金中一定只含金属元素
B.纯铜比黄铜的硬度更大
C.生锈的钢铁制品没有回收价值
D.钛和钛合金被广泛用于火箭、导弹等
3.2018年3月9日,特朗普正式签署关税令“对进口钢铁和铝分别征收25%的关税”,这一做法严重违反国际贸易规则,严重损害我国利益。下列选项中不属于合金的是
A.钢 B.金刚石 C.焊锡 D.黄铜
4.明代宋应星著的《天工开物》中有关于“火法”冶炼金属锌的工艺记载:“炉甘石(注:主要成分是碳酸锌)十斤,装载入一泥罐內,然后逐层用煤炭饼(注:反应后生成一氧化碳)垫盛,其底铺薪,发火煅红,冷淀,毁罐取出,即倭铅也”。下列说法错误的是
A.煤炭中起作用的主要成分是C
B.冶炼Zn的化学方程式为:
C.该冶炼锌的反应属于置换反应
D.倭铅是指金属锌和铅的混合物
5.铁是一种重要的金属。下列关于铁的叙述错误的是
A.生铁是纯净物
B.涂油漆可防止铁生锈
C.工业上常用赤铁矿冶炼铁
D.铁与硫酸铜溶液的反应属于置换反应
6.下列各组物质在溶液中能大量共存且形成无色溶液的是
A.NaCl BaCl2Na2CO3 B.KNO3HCl CaCl2
C.H2SO4 FeCl3NaNO3 D.NaOH HNO3NH4NO3
7.已知在一定条件下发生反应:甲+乙→丙+丁,下列判断正确的是
A.甲、乙、丙、丁不可能含有同一种元素
B.丙为Cu(NO3)2,则甲可能为单质或氧化物或碱
C.参加反应的甲、乙质量比一定等于生成丙、丁质量比
D.若甲、乙为化合物,则该反应一定为复分解反应
8.西汉时期,人们就会用石灰水或草木灰水(主要成分是K2CO2)等碱性溶液为丝麻脱胶来造纸。下列物质属于碱的是
A.生石灰 B.水 C.熟石灰 D.草木灰
9.验证镁、铜的金属活动性顺序,下列试剂不能选用的是( )
A.MgSO4溶液 B.KCl溶液
C.稀盐酸 D.CuCl2溶液
10.关于"家庭小实验"的下列说法正确的是
A.用自制简易净水器制纯水
B.向洗净的碎鸡蛋壳中加入食醋可产生一氧化碳
C.用白糖、果汁、小苏打、柠檬酸、水自制汽水
D.把钢针烧红放入水中冷却后取出,钢针变得更容易弯曲
11.现有不纯的氧化铜样品16g,所含杂质有镁粉 铁粉 碳酸钙 向其中加入200g溶质质量分数为3.65%的稀盐酸有气泡产生,将气体通入到澄清石灰水变浑浊,充分反应后,过滤得到滤液和滤渣,观察滤液为蓝色 则下列判断不正确的是
A.滤液质量一定大于原稀盐酸的质量
B.滤渣最多有 3种,滤渣的质量一定小于16g
C.反应生成水的质量可能大于1.8g
D.滤液中一定有氯化铜 氯化亚铁 氯化镁 氯化钙
二、简答题
12.在宏观、微观、符号之间建立联系是化学学科的特点。图 1 为元素周期表中的一格, 图 2 是碳酸钠溶液与氢氧化钙溶液反应的微观示意图,
(1)在元素周期表中,钙元素的原子序数为 ____________ 。
(2)写出钙离子的结构示意图 ____________ 。
(3)人体如果缺钙会导致 ____________ 。
(4)图 2 所示反应的微观本质是 ____________ 。
13.你将选用哪种合金来制造下列物品?说明理由。
(1)外科手术刀
(2)防盗门
(3)门锁
(4)自行车支架
14.根据复分解反应发生的条件,并利用书后附录1所提供的信息,判断下列物质间能否发生复分解反应。如能发生反应,写出反应的化学方程式。
(1)碳酸钠溶液和氯化钙溶液
(2)氢氧化钾溶液和盐酸
(3)氢氧化钠溶液和氯化钾溶液
(4)碳酸钾溶液和盐酸
(5)硫酸铜溶液和氯化钡溶液
三、推断题
15.A~H内初中化学常见物质。己知A属于盐,常用作建筑材料, E是赤铁矿石的主要成分,F可用于中和酸性土壤, H 的溶液呈浅绿色。它们的转化关系如图所示(反应条件未完全棕标出)。
(1)写出A的化学式、F的名称: A_________,F________;
(2)写出反应②、④的化学方程式:反应②__________,反应④_________,其中反应④属于四种基本反应类型中的__________反应;
(3)比较D与G的活动性强弱关系: D______G(填“>”或“<”);
(4)C生成F的其化学方程式为_________。
16.已知A~G为初中化学常见的七种物质。其中D的固体叫做“干冰”;B中只含两种元素,C与E不含相同元素。各种物质间的反应和转化关系如图所示(“﹣”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以转化为另一种物质,反应条件、部分反应物和生成物已略去)。
请分析后回答:
(1)D的化学式_____。
(2)B与G反应的化学方程式_____。
四、实验题
17.某学生想探究铁生锈的条件,他设计了如图所示的实验:
(1)本实验对所用铁钉的要求是___________。
(2)因缺少___________的操作,故A试管中的铁钉生锈了。
(3)在C试管中,观察到的现象是___________。
(4)铁生锈的条件是___________。
18.依据下图所示实验回答问题。
(1)A 实验探究燃烧的条件。得出可燃物燃烧需要达到着火点依据的现象是______。
(2)B 实验探究铁生锈的条件,植物油的作用是______,①和③对比,研究的影响因素是______
五、计算题
19.家庭厨房就是一个化学小世界,“柴米油盐”中包含着许多化学知识。食醋、食盐和纯碱都是日常生活中常用的物质。食醋中通常含有3%~5%的乙酸,乙酸俗称醋酸(化学式为CH3COOH),是一种无色液体。食盐和纯碱都是白色固体。
(1)醋酸和纯碱中属于无机物的是________(写化学式)。
(2)醋酸中,C、O两元素的质量之比为________(填最简整数比)。
20.某工厂利用废硫酸溶液与铁反应制取硫酸亚铁。49t废硫酸溶液中的硫酸 与5.6t铁恰好完全反应。求:
(1)废硫酸溶液中溶质的质量分数。
(2)理论上生产的硫酸亚铁的质量。
21.锌与硫酸(H2SO4)反应生成氢气和硫酸锌。实验室里用6.5 g锌与足量硫酸完全反应,请计算:
(1)参加反应硫酸的质量;
(2)可制得氢气的质量和标准状况下氢气的体积 (已知:标准状况下,氢气的密度为0.0899 g/L)(结果精确至0.1L)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.D
3.B
4.D
5.A
6.B
7.B
8.C
9.B
10.C
11.C
12. 20 骨质疏松(或佝偻病或发育不良,合理均可) Ca2+ 和CO32- 结合生成CaCO3沉淀
13.(1)外科手术刀用不锈钢,硬度大、耐腐蚀性好
(2)防盗门使用锰钢,硬度大、韧性好
(3)门锁使用黄铜,耐磨、耐腐蚀
(4)自行车支架使用锰钢,韧性好、硬度大
14.(1)
(2)
(3)不能发生反应
(4)
(5)
15.(1) 氢氧化钙
(2) 置换
(3)>
(4)
16. CO2 HCl+AgNO3=HNO3+AgCl↓
17.(1)洁净光亮
(2)蒸馏水煮沸
(3)铁钉没有生锈
(4)与氧气和水接触
18. 白磷①燃烧(先燃烧),白磷②不燃烧(后燃烧) 隔绝氧气 H2O
19.(1)Na2CO3;(2)3:4
20.解:设废硫酸溶液中溶质的质量分数为x;理论上生产的硫酸亚铁的质量为y
答:(1)废硫酸溶液中溶质的质量分数为20%。
(2)理论上生产的硫酸亚铁的质量15.2t。
21.(1)设参加反应的硫酸的质量x。
则参加反应硫酸的质量为9.8g。
(2)参加反应的硫酸的质量为9.8g、可制得氢气的质量和体积分别为0.2g、2.2L
答案第1页,共2页
答案第1页,共2页
