第八章常见的酸碱盐综合练习-2021-2022学年九年级化学科粤版(2012)下册(word版有答案)
文档属性
| 名称 | 第八章常见的酸碱盐综合练习-2021-2022学年九年级化学科粤版(2012)下册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 124.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-06 00:00:00 | ||
图片预览



文档简介
第八章常见的酸碱盐综合练习—2021—2022学年九年级化学科粤版(2012)下册
一、单选题
1.不同的物质溶于水后会形成酸碱性不同的溶液,下列溶液显酸性的是
A.食醋 B.氨水 C.NaCl溶液 D.Na2CO3溶液
2.每种植物都有适宜自己生长的酸碱性环境。下表为四种作物适宜生长的pH范围:
作物 水稻 茶树 玉米 马铃薯
pH 6.0~7.0 5.0~5.5 7.0~8.0 4.8~5.5
某土壤浸出液能使紫色石蕊溶液变蓝色,该土壤适宜种植的作物是( )
A.水稻 B.茶树 C.马铃薯 D.玉米
3.下列物质由离子构成的是( )
A.氦气 B.水 C.氯化钠 D.金刚石
4.下列溶液能使紫色石蕊溶液变成蓝色的是
A.澄清石灰水 B.NaCl溶液
C.稀硫酸 D.KNO3溶液
5.下列有关盐的用途的说法错误的是
A.氯化钠是重要的调味品
B.可用亚硝酸钠代替食盐腌渍食品
C.小苏打可用于培制糕点
D.碳酸钾可用作化学肥料
6.下列试剂瓶应有 标志的是
A.氯化钠 B.蒸馏水 C.浓硫酸 D.葡萄糖
7.分离、除杂和检验是化学实验的重要环节,下列说法不正确的是
A.分离CO2和CO,先用NaOH溶液吸收CO2,再向该溶液中加足量稀盐酸
B.只用一种试剂无法把稀盐酸、氯化钡溶液和硝酸钾三种溶液区别开
C.除去氯化钙溶液中混有的少量稀盐酸,可加入过量碳酸钙,充分反应后过滤
D.只用组内溶液相互混合方法,能将KOH、Na2SO4、CuSO4、MgCl2鉴别开
8.忘盖瓶塞的氢氧化钠溶液可能变质。下表中分析与设计错误的是
选项 问题 分析与设计
A 为何变质 2NaOH + CO2 = Na2CO3 + H2O
B 是否变质 取样,加入足量稀盐酸,观察是否产生气泡
C 是否全部变质 取样,加入足量氯化钙溶液,观察产生沉淀多少
D 如何除去杂质 取样,加入适量氢氧化钙溶液,过滤
A.A B.B C.C D.D
9.在一个密闭容器中加入四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
物质 甲 乙 丙 丁
反应前质量/g 3 5 20 7
反应后质量/g 10 5 8 待测
通过分析,判断下列说法正确的是( )A.测得反应后丁物质的质量为12g
B.乙物质一定是催化剂
C.该反应是化合反应
D.该反应是复分解反应
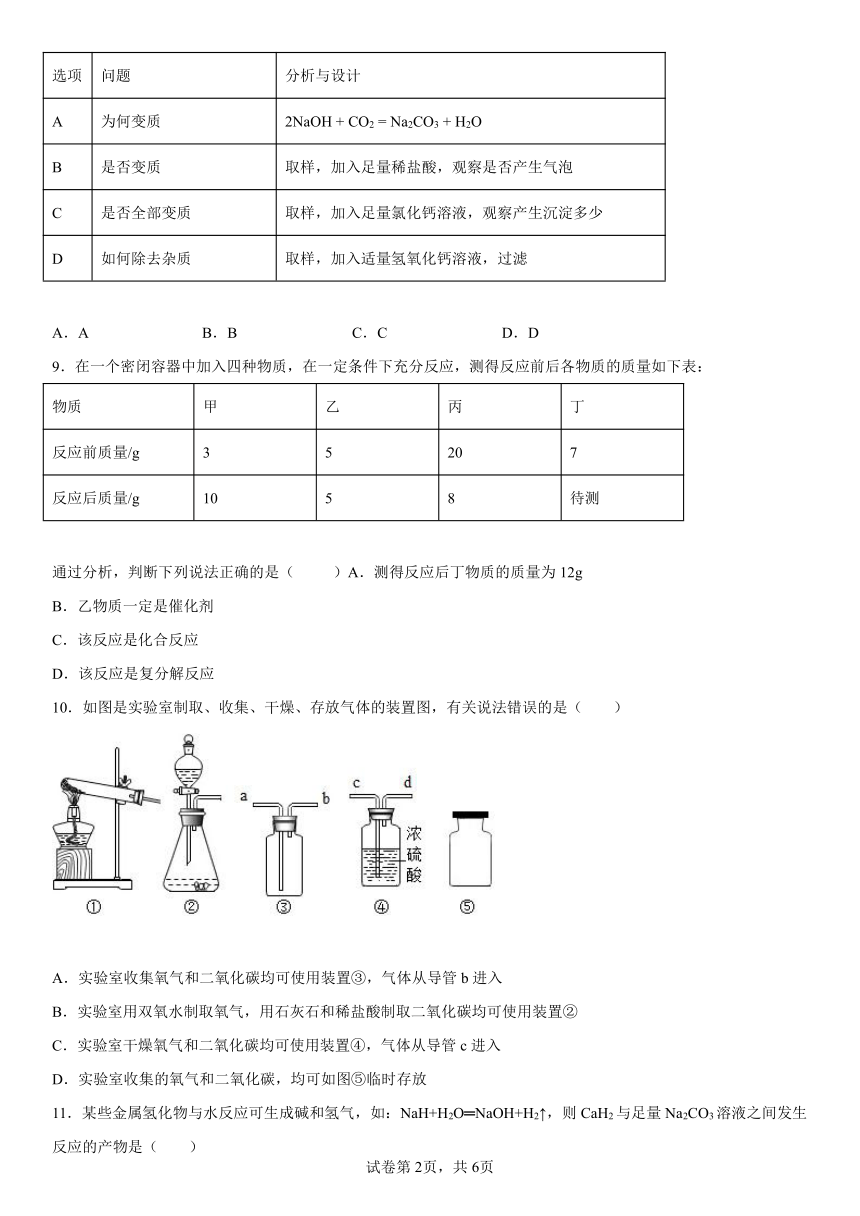
10.如图是实验室制取、收集、干燥、存放气体的装置图,有关说法错误的是( )
A.实验室收集氧气和二氧化碳均可使用装置③,气体从导管b进入
B.实验室用双氧水制取氧气,用石灰石和稀盐酸制取二氧化碳均可使用装置②
C.实验室干燥氧气和二氧化碳均可使用装置④,气体从导管c进入
D.实验室收集的氧气和二氧化碳,均可如图⑤临时存放
11.某些金属氢化物与水反应可生成碱和氢气,如:NaH+H2O═NaOH+H2↑,则CaH2与足量Na2CO3溶液之间发生反应的产物是( )
A.CaCO3、NaOH和H2 B.Ca(OH)2和H2
C.NaOH和Ca(OH)2 D.Ca(OH)2、CaCO3和H2
12.现有盐酸和氯化镁的混合溶液,向其中逐滴滴入氢氧化钠溶液,生成沉淀质量与滴入氢氧化钠溶液质量的变化关系如图所示。下列说法错误的是
A.滴加氢氧化钠液质量为a﹣cg时,溶液中发生的反应为:
B.滴加氢氧化钠溶液质量至ag时,溶液中溶质质量比原混合溶液中溶质质量大
C.滴加氢氧化钠溶液质量至bg时,溶液中含三种溶质
D.滴加氢氧化钠溶液质量至cg时,溶液呈中性
二、简答题
13.酸和碱之间反应的实质______。
14.海水是巨大的资源宝库。如图是某工厂对海水资源综合利用的示意图。
(1)分离粗盐和母液的操作名称为_____;母液中一定含有的金属元素为_____。
(2)步骤①的化学方程式是_____;步骤②的基本反应类型为_____。
(3)下表为氯化钠在不同温度时的溶解度。结合表中数据回答:
温度/'C 30 50 70 100
溶解度/g 36.3 37.0 37.8 39.8
时,氯化钠饱和溶液中溶质质量分数为_____(结果精确到1%);从海水中获取粗盐,宜选用_____(选填“蒸发结晶”或“降温结晶”)的方法。
15.(1)金属镁为______色,燃烧时的现象__________,该反应的文字表达式____________.若将镁条放入食醋中,可看到___________________.
(2)“铜绿”的颜色为______.用酒精灯加热“铜绿”时的现象是____________,由此可知“铜绿”加热后的生成物是___________,说明“铜绿”中含有的元素是_________,该反应的文字表达式_______;“铜绿”与盐酸作用时的现象_________.
三、推断题
16.A~F是初中化学常见的物质,它们之间的转化关系如图所示。其中A的过多排放会导致温室效应,B是相对分子质量为56的氧化物,C、F都属于盐且C常用于制造玻璃和肥皂。D常用于改良酸性土壤。物质E的化学式为 ______ ;反应①的化学方程式为 ______________ ;反应②为 ______ 反应(填基本反应类型)。
17.A~F是六种不同物质,A是单质,C和E都是酸,它们之间的反应关系如图所示(部分物质已略)分析辨识,解决问题:
(1)B和C反应的化学方程式是_____。基本反应类型是_____。
(2)D生成A的化学方程式是_____(写一个)。
(3)若F与其他物质类别不同,E和F反应的微观实质是_____。
四、实验题
18.如图为实验室常见气体的制备和进行性质实验的部分仪器,某校化学实验探究小组的同学欲用这组仪器完成各自的探究实验。根据探究过程回答下列问题:
(1)第一小组的同学用过氧化氢溶液和二氧化锰制备并收集干燥的氧气。
①制取氧气所发生反应的化学方程式为_____。
②要制备并收集一瓶干燥的氧气,所选仪器的连接顺序为_____(填装置字母序号)。
③向气体发生装置内加入药品前,应该进行的操作是_____。
(2)第二小组的同学探究碱溶液与二氧化碳的反应。如图甲、乙所示,分别向盛满二氧化碳的两个塑料瓶中,倒入等体积的氢氧化钠溶液和氢氧化钙溶液,盖紧瓶塞,充分振荡,发现两个塑料瓶变瘪的程度为甲>乙。
①同学们发现乙瓶内液体出现白色浑浊,请写出该反应的化学方程式_____。
②同学们看到甲瓶内的液体没有明显变化,小明同学想检验氢氧化钠溶液是否与二氧化碳发生了反应,他所想到的下列试剂中,不能得到结果的是_____。
A.稀盐酸
B.氯化钡溶液
C.石蕊试液
D.硝酸钙溶液
19.化学是一门以实验为基础的科学。根据下列图示回答问题。
(1)仪器①的名称是______;
(2)实验室用高锰酸钾制取氧气所选用的发生装置是______(填序号);
(3)用双氧水制取氧气用于探究石蜡燃烧的产物,应选择装置B与_____(填字母)组合。
20.常温下,一锥形瓶中盛有20g溶质质量分数为4%的氢氧化钠溶液,先向其中滴加2滴酚酞试液,再逐滴滴加溶质质量分数为6.3%的稀硝酸,用pH传感器测得溶液的pH与加入稀硝酸的关系曲线如图。请回答问题:
(1)本实验反应的化学方程式是____。
(2)pH=7时,锥形瓶中的溶液呈____色,此时溶液的溶质质量分数是____(结果精确到0.01%)。
(3)图中a点对应的溶液中溶质的化学式是____。
(4)若改用溶质质量分数为12.6%的稀硝酸进行本实验,pH传感器测得的曲线可能经过____(填“甲”“乙”或“丙”)点。
五、计算题
21.尿素〔CO(NH2)2〕是化肥中最主要的一种,其含氮量高,在土壤中不残留任何有害物质,长期施用没有不良影响。
(1)尿素属于化肥中的______肥(填“氮”“钾”或“复合”)。
(2)CO(NH2)2中共含有______(写数字)种元素;
(3)CO(NH2)2的相对分子质量是______
(4)CO(NH2)2中C、H、N、O元素的质量比为______。
22.某纯碱样品中混有少量NaCl,某兴趣小组同学称取6.25g的样品,滴入稀盐酸至恰好完全反应,实验数据记录如下。
反应前 反应后
实验 数据 (烧杯+样品+稀盐酸)的质量g 烧杯的质量g 烧杯+烧杯中溶液的质量g
205.2 103.0 203.0
(1)求反应生成的CO2质量 g。
(2)求反应后所得溶液的溶质质量分数。
23.某锥形瓶盛有盐酸和氯化铜的混合溶液100g,向其中逐滴加入溶质质量分数为10%的氢氧化钠溶液,锥形瓶内溶液质量与滴入的氢氧化钠溶液的质量的变化关系如图所示。请计算:
(l)反应至A点时加入氢氧化钠溶液的质量为__________;
(2)反应至B点时锥形瓶内所得溶液的溶质质量分数为_____(计算结果保留至0.1%)
24.某校化学课外活动小组的同学在实验室的一次探究性活动中,他们将50g氢氧化钠溶液与50g硫酸铜溶液混合恰好完全反应,得到9.8g沉淀。请你计算氢氧化钠溶液中溶质的质量分数。_______
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.D
3.C
4.A
5.B
6.C
7.B
8.C
9.A
10.A
11.A
12.C
13.氢离子和氢氧根离子结合生成水分子
14. 过滤 钠和镁 ↑↑ 复分解反应 27% 蒸发结晶
15. 银白色 发出耀眼的白光、放热、生成白色粉末 镁条逐渐减少,表面产生气泡 绿色 绿色固体变成黑色固体,试管壁有小水珠,生成了能使澄清石灰水变浑浊的气体 氧化铜、二氧化碳、水 碳元素、铜元素、氧元素、氢元素 “铜绿”逐渐减少,产生气泡,溶液变成蓝色
16. NaOH 2NaOH+CO2=Na2CO3+H2O 复分解
17. AgNO3+HCl=AgCl↓+HNO3 复分解反应 Fe2O3+3CO2Fe+3CO2 氢离子和氢氧根离子反应生成水
18. A、B、C 检查装置气密性 Ca(OH)2+CO2═CaCO3↓+H2O C
19.(1)集气瓶
(2)A
(3)EF FE
20. NaOH+HNO3=NaNO3+H2O 无 4.25% HNO3、NaNO3 甲
21.(1)尿素中含有氮元素,属于化肥中的氮肥。
(2)CO(NH2)2中共含有C、O、N、H,4种元素;
(3)CO(NH2)2的相对分子质量是12+16+(14+1×2)×2=60;
(4)CO(NH2)2中C、H、N、O元素的质量比为12:(1×4):(14×2):16=3:1:7:4。
22.(1)2.2
(2)设反应生成氯化钠的质量为x,碳酸钠的质量为y,
样品中得氯化钠质量为:6.25g-5.3g=0.95g,
所以反应后溶质质量分数为:。
23.(1)40g(2)10.4%
24.16%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.不同的物质溶于水后会形成酸碱性不同的溶液,下列溶液显酸性的是
A.食醋 B.氨水 C.NaCl溶液 D.Na2CO3溶液
2.每种植物都有适宜自己生长的酸碱性环境。下表为四种作物适宜生长的pH范围:
作物 水稻 茶树 玉米 马铃薯
pH 6.0~7.0 5.0~5.5 7.0~8.0 4.8~5.5
某土壤浸出液能使紫色石蕊溶液变蓝色,该土壤适宜种植的作物是( )
A.水稻 B.茶树 C.马铃薯 D.玉米
3.下列物质由离子构成的是( )
A.氦气 B.水 C.氯化钠 D.金刚石
4.下列溶液能使紫色石蕊溶液变成蓝色的是
A.澄清石灰水 B.NaCl溶液
C.稀硫酸 D.KNO3溶液
5.下列有关盐的用途的说法错误的是
A.氯化钠是重要的调味品
B.可用亚硝酸钠代替食盐腌渍食品
C.小苏打可用于培制糕点
D.碳酸钾可用作化学肥料
6.下列试剂瓶应有 标志的是
A.氯化钠 B.蒸馏水 C.浓硫酸 D.葡萄糖
7.分离、除杂和检验是化学实验的重要环节,下列说法不正确的是
A.分离CO2和CO,先用NaOH溶液吸收CO2,再向该溶液中加足量稀盐酸
B.只用一种试剂无法把稀盐酸、氯化钡溶液和硝酸钾三种溶液区别开
C.除去氯化钙溶液中混有的少量稀盐酸,可加入过量碳酸钙,充分反应后过滤
D.只用组内溶液相互混合方法,能将KOH、Na2SO4、CuSO4、MgCl2鉴别开
8.忘盖瓶塞的氢氧化钠溶液可能变质。下表中分析与设计错误的是
选项 问题 分析与设计
A 为何变质 2NaOH + CO2 = Na2CO3 + H2O
B 是否变质 取样,加入足量稀盐酸,观察是否产生气泡
C 是否全部变质 取样,加入足量氯化钙溶液,观察产生沉淀多少
D 如何除去杂质 取样,加入适量氢氧化钙溶液,过滤
A.A B.B C.C D.D
9.在一个密闭容器中加入四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
物质 甲 乙 丙 丁
反应前质量/g 3 5 20 7
反应后质量/g 10 5 8 待测
通过分析,判断下列说法正确的是( )A.测得反应后丁物质的质量为12g
B.乙物质一定是催化剂
C.该反应是化合反应
D.该反应是复分解反应
10.如图是实验室制取、收集、干燥、存放气体的装置图,有关说法错误的是( )
A.实验室收集氧气和二氧化碳均可使用装置③,气体从导管b进入
B.实验室用双氧水制取氧气,用石灰石和稀盐酸制取二氧化碳均可使用装置②
C.实验室干燥氧气和二氧化碳均可使用装置④,气体从导管c进入
D.实验室收集的氧气和二氧化碳,均可如图⑤临时存放
11.某些金属氢化物与水反应可生成碱和氢气,如:NaH+H2O═NaOH+H2↑,则CaH2与足量Na2CO3溶液之间发生反应的产物是( )
A.CaCO3、NaOH和H2 B.Ca(OH)2和H2
C.NaOH和Ca(OH)2 D.Ca(OH)2、CaCO3和H2
12.现有盐酸和氯化镁的混合溶液,向其中逐滴滴入氢氧化钠溶液,生成沉淀质量与滴入氢氧化钠溶液质量的变化关系如图所示。下列说法错误的是
A.滴加氢氧化钠液质量为a﹣cg时,溶液中发生的反应为:
B.滴加氢氧化钠溶液质量至ag时,溶液中溶质质量比原混合溶液中溶质质量大
C.滴加氢氧化钠溶液质量至bg时,溶液中含三种溶质
D.滴加氢氧化钠溶液质量至cg时,溶液呈中性
二、简答题
13.酸和碱之间反应的实质______。
14.海水是巨大的资源宝库。如图是某工厂对海水资源综合利用的示意图。
(1)分离粗盐和母液的操作名称为_____;母液中一定含有的金属元素为_____。
(2)步骤①的化学方程式是_____;步骤②的基本反应类型为_____。
(3)下表为氯化钠在不同温度时的溶解度。结合表中数据回答:
温度/'C 30 50 70 100
溶解度/g 36.3 37.0 37.8 39.8
时,氯化钠饱和溶液中溶质质量分数为_____(结果精确到1%);从海水中获取粗盐,宜选用_____(选填“蒸发结晶”或“降温结晶”)的方法。
15.(1)金属镁为______色,燃烧时的现象__________,该反应的文字表达式____________.若将镁条放入食醋中,可看到___________________.
(2)“铜绿”的颜色为______.用酒精灯加热“铜绿”时的现象是____________,由此可知“铜绿”加热后的生成物是___________,说明“铜绿”中含有的元素是_________,该反应的文字表达式_______;“铜绿”与盐酸作用时的现象_________.
三、推断题
16.A~F是初中化学常见的物质,它们之间的转化关系如图所示。其中A的过多排放会导致温室效应,B是相对分子质量为56的氧化物,C、F都属于盐且C常用于制造玻璃和肥皂。D常用于改良酸性土壤。物质E的化学式为 ______ ;反应①的化学方程式为 ______________ ;反应②为 ______ 反应(填基本反应类型)。
17.A~F是六种不同物质,A是单质,C和E都是酸,它们之间的反应关系如图所示(部分物质已略)分析辨识,解决问题:
(1)B和C反应的化学方程式是_____。基本反应类型是_____。
(2)D生成A的化学方程式是_____(写一个)。
(3)若F与其他物质类别不同,E和F反应的微观实质是_____。
四、实验题
18.如图为实验室常见气体的制备和进行性质实验的部分仪器,某校化学实验探究小组的同学欲用这组仪器完成各自的探究实验。根据探究过程回答下列问题:
(1)第一小组的同学用过氧化氢溶液和二氧化锰制备并收集干燥的氧气。
①制取氧气所发生反应的化学方程式为_____。
②要制备并收集一瓶干燥的氧气,所选仪器的连接顺序为_____(填装置字母序号)。
③向气体发生装置内加入药品前,应该进行的操作是_____。
(2)第二小组的同学探究碱溶液与二氧化碳的反应。如图甲、乙所示,分别向盛满二氧化碳的两个塑料瓶中,倒入等体积的氢氧化钠溶液和氢氧化钙溶液,盖紧瓶塞,充分振荡,发现两个塑料瓶变瘪的程度为甲>乙。
①同学们发现乙瓶内液体出现白色浑浊,请写出该反应的化学方程式_____。
②同学们看到甲瓶内的液体没有明显变化,小明同学想检验氢氧化钠溶液是否与二氧化碳发生了反应,他所想到的下列试剂中,不能得到结果的是_____。
A.稀盐酸
B.氯化钡溶液
C.石蕊试液
D.硝酸钙溶液
19.化学是一门以实验为基础的科学。根据下列图示回答问题。
(1)仪器①的名称是______;
(2)实验室用高锰酸钾制取氧气所选用的发生装置是______(填序号);
(3)用双氧水制取氧气用于探究石蜡燃烧的产物,应选择装置B与_____(填字母)组合。
20.常温下,一锥形瓶中盛有20g溶质质量分数为4%的氢氧化钠溶液,先向其中滴加2滴酚酞试液,再逐滴滴加溶质质量分数为6.3%的稀硝酸,用pH传感器测得溶液的pH与加入稀硝酸的关系曲线如图。请回答问题:
(1)本实验反应的化学方程式是____。
(2)pH=7时,锥形瓶中的溶液呈____色,此时溶液的溶质质量分数是____(结果精确到0.01%)。
(3)图中a点对应的溶液中溶质的化学式是____。
(4)若改用溶质质量分数为12.6%的稀硝酸进行本实验,pH传感器测得的曲线可能经过____(填“甲”“乙”或“丙”)点。
五、计算题
21.尿素〔CO(NH2)2〕是化肥中最主要的一种,其含氮量高,在土壤中不残留任何有害物质,长期施用没有不良影响。
(1)尿素属于化肥中的______肥(填“氮”“钾”或“复合”)。
(2)CO(NH2)2中共含有______(写数字)种元素;
(3)CO(NH2)2的相对分子质量是______
(4)CO(NH2)2中C、H、N、O元素的质量比为______。
22.某纯碱样品中混有少量NaCl,某兴趣小组同学称取6.25g的样品,滴入稀盐酸至恰好完全反应,实验数据记录如下。
反应前 反应后
实验 数据 (烧杯+样品+稀盐酸)的质量g 烧杯的质量g 烧杯+烧杯中溶液的质量g
205.2 103.0 203.0
(1)求反应生成的CO2质量 g。
(2)求反应后所得溶液的溶质质量分数。
23.某锥形瓶盛有盐酸和氯化铜的混合溶液100g,向其中逐滴加入溶质质量分数为10%的氢氧化钠溶液,锥形瓶内溶液质量与滴入的氢氧化钠溶液的质量的变化关系如图所示。请计算:
(l)反应至A点时加入氢氧化钠溶液的质量为__________;
(2)反应至B点时锥形瓶内所得溶液的溶质质量分数为_____(计算结果保留至0.1%)
24.某校化学课外活动小组的同学在实验室的一次探究性活动中,他们将50g氢氧化钠溶液与50g硫酸铜溶液混合恰好完全反应,得到9.8g沉淀。请你计算氢氧化钠溶液中溶质的质量分数。_______
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.D
3.C
4.A
5.B
6.C
7.B
8.C
9.A
10.A
11.A
12.C
13.氢离子和氢氧根离子结合生成水分子
14. 过滤 钠和镁 ↑↑ 复分解反应 27% 蒸发结晶
15. 银白色 发出耀眼的白光、放热、生成白色粉末 镁条逐渐减少,表面产生气泡 绿色 绿色固体变成黑色固体,试管壁有小水珠,生成了能使澄清石灰水变浑浊的气体 氧化铜、二氧化碳、水 碳元素、铜元素、氧元素、氢元素 “铜绿”逐渐减少,产生气泡,溶液变成蓝色
16. NaOH 2NaOH+CO2=Na2CO3+H2O 复分解
17. AgNO3+HCl=AgCl↓+HNO3 复分解反应 Fe2O3+3CO2Fe+3CO2 氢离子和氢氧根离子反应生成水
18. A、B、C 检查装置气密性 Ca(OH)2+CO2═CaCO3↓+H2O C
19.(1)集气瓶
(2)A
(3)EF FE
20. NaOH+HNO3=NaNO3+H2O 无 4.25% HNO3、NaNO3 甲
21.(1)尿素中含有氮元素,属于化肥中的氮肥。
(2)CO(NH2)2中共含有C、O、N、H,4种元素;
(3)CO(NH2)2的相对分子质量是12+16+(14+1×2)×2=60;
(4)CO(NH2)2中C、H、N、O元素的质量比为12:(1×4):(14×2):16=3:1:7:4。
22.(1)2.2
(2)设反应生成氯化钠的质量为x,碳酸钠的质量为y,
样品中得氯化钠质量为:6.25g-5.3g=0.95g,
所以反应后溶质质量分数为:。
23.(1)40g(2)10.4%
24.16%
答案第1页,共2页
答案第1页,共2页
