江苏省郑梁梅中学2012-2013学年高一上学期期末考试化学试题(带解析)
文档属性
| 名称 | 江苏省郑梁梅中学2012-2013学年高一上学期期末考试化学试题(带解析) |  | |
| 格式 | zip | ||
| 文件大小 | 72.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2013-01-31 17:11:39 | ||
图片预览


文档简介
郑梁梅中学2012-2013学年高一上学期期末考试化学试题
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上
第I卷(选择题)
一、选择题
1.电解下列熔融物,析出同质量的金属时,消耗电量最少的是()
A.NaOH
B.KCl
C.CaCl2
D.Al2O3
2.要配制浓度约为2mol/L NaOH溶液100mL,下列操作正确的是
A.称取8gNaOH固体,放入100mL量筒中,边搅拌边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100mL
B.称取8gNaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀
C.称取8gNaOH固体,放入100mL烧杯中,将烧杯中加满蒸馏水,同时不断搅拌至固体溶解
D.用100mL量筒量取40ml 5mol/L NaOH溶液,倒入250mL烧杯中,再用同一量筒取60mL蒸馏水,不断搅拌下,慢慢倒入烧杯中
3.在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
物质
X
Y
Z
Q
反应前质量/g
2
2
48
5
反应后质量/g
待测
24
0
14
试判断该密闭容器中发生反应属于:
A、化合反应??? B、置换反应???? C、分解反应???? D、复分解反应
4.下列物质中只含有离子键的是( )
A.H2O B.NaCl
C.NH4Cl D.CCl4
5.已知Na2S2O3+H2SO4═Na2SO4+SO2+SO2+H2O下列各组实验中溶液最先变浑浊的是
组号
参加反应的物质
反应温度(℃)
V(mL)
C(mol/L)
V(mL)
C(mol/L)
V(mL)
A
10
5
0.1
5
0.1
5
B
10
5
0.1
5
0.1
10
C
30
5
0.2
5
0.2
5
D
30
5
0.2
5
0.2
10
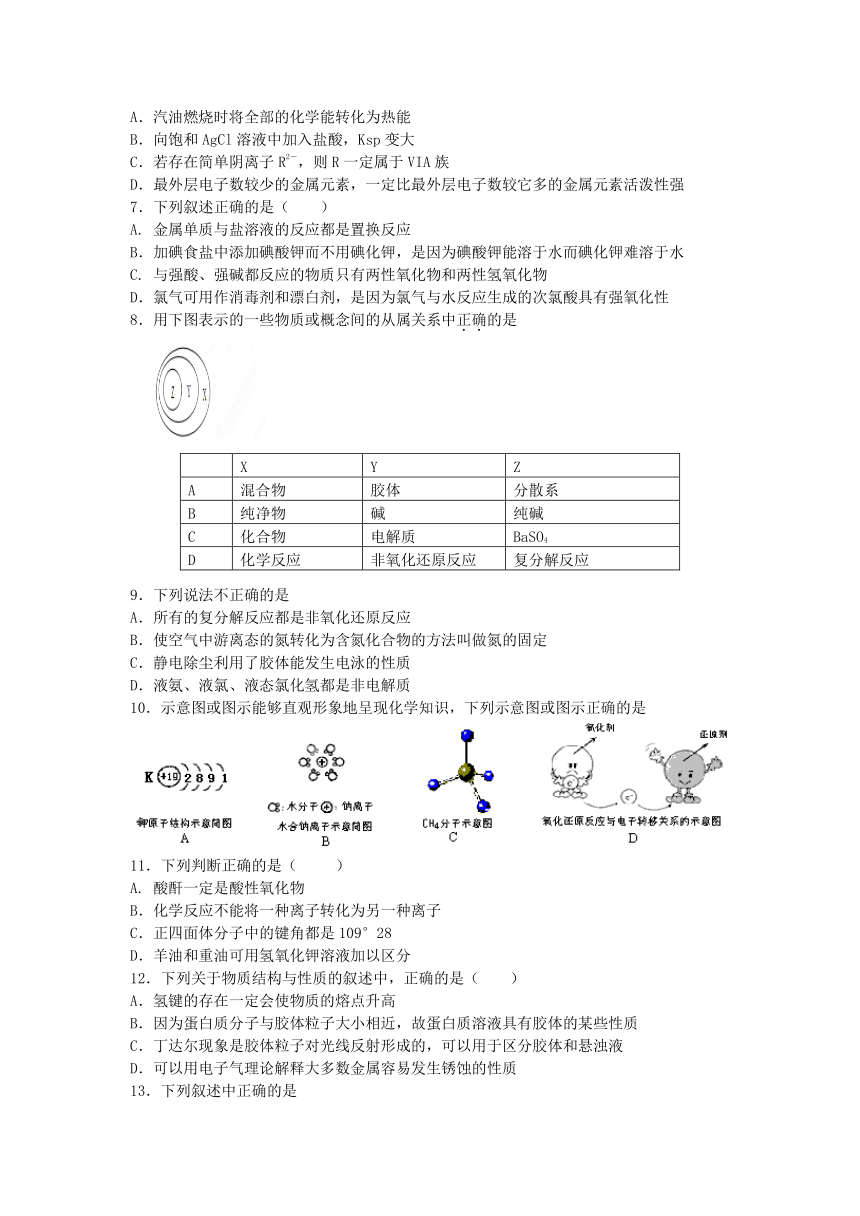
6.下列说法中正确的是
A.汽油燃烧时将全部的化学能转化为热能
B.向饱和AgCl溶液中加入盐酸,Ksp变大
C.若存在简单阴离子R2-,则R一定属于VIA族
D.最外层电子数较少的金属元素,一定比最外层电子数较它多的金属元素活泼性强
7.下列叙述正确的是( )
A. 金属单质与盐溶液的反应都是置换反应
B.加碘食盐中添加碘酸钾而不用碘化钾,是因为碘酸钾能溶于水而碘化钾难溶于水
C. 与强酸、强碱都反应的物质只有两性氧化物和两性氢氧化物
D.氯气可用作消毒剂和漂白剂,是因为氯气与水反应生成的次氯酸具有强氧化性
8.用下图表示的一些物质或概念间的从属关系中正确的是
X
Y
Z
A
混合物
胶体
分散系
B
纯净物
碱
纯碱
C
化合物
电解质
BaSO4
D
化学反应
非氧化还原反应
复分解反应
9.下列说法不正确的是
A.所有的复分解反应都是非氧化还原反应
B.使空气中游离态的氮转化为含氮化合物的方法叫做氮的固定
C.静电除尘利用了胶体能发生电泳的性质
D.液氨、液氯、液态氯化氢都是非电解质
10.示意图或图示能够直观形象地呈现化学知识,下列示意图或图示正确的是
11.下列判断正确的是( )
A. 酸酐一定是酸性氧化物
B.化学反应不能将一种离子转化为另一种离子
C.正四面体分子中的键角都是109°28
D.羊油和重油可用氢氧化钾溶液加以区分
12.下列关于物质结构与性质的叙述中,正确的是( )
A.氢键的存在一定会使物质的熔点升高
B.因为蛋白质分子与胶体粒子大小相近,故蛋白质溶液具有胶体的某些性质
C.丁达尔现象是胶体粒子对光线反射形成的,可以用于区分胶体和悬浊液
D.可以用电子气理论解释大多数金属容易发生锈蚀的性质
13.下列叙述中正确的是
A.锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后,再将不溶物用稀盐酸溶解去除
B.向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进了Fe3+水解
C.向纯水中加入盐酸或降温都能使水的离子积减小,电离平衡逆向移动
D.反应2A(g) + B(g) = 3C (s) + D(g)在一定条件下能自发进行,说明该反应的ΔH>0
14.下列说法正确的是( )
A、酸性氧化物就是非金属氧化物
B、纯净物与混合物的区别是看是否只含有一种元素
C、强弱电解质的区别是溶液的导电能力的大小
D、氧化还原反应的判断依据是反应过程中元素的化合价是否发生变化
15.化学中图象可以直观地描述化学反应的进程或结果,下列图像描述正确的是( )
A.图5表示化学反应H2(g)+Cl2(g)=2HCl(g)的能量变化,则该反应的反应热△H =183kJ·mol-1
B.图6表示室温时用0.1mol·L-1盐酸滴定20mL0.1mol·L-1NaOH溶液,溶液pH随加入酸体积变化
C.图7表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液
D.图8表示10mL0.1mol/LNa2CO3和NaHCO3两种溶液中,分别滴加0.1mol/LHCl,产生CO2的体积随盐酸体积的变化,则b表示Na2CO3溶液
第II卷(非选择题)
二、填空题
16.(14分)随着石油资源的日趋紧张,天然气资源的开发利用受到越来越多的关注。以天然气(主要成分CH4)为原料经合成气(主要成分CO、H2)制化学品,是目前天然气转化利用的主要技术路线。而采用渣油、煤、焦炭为原料制合成气,常因含羰基铁[Fe(CO)5]等而导致以合成气为原料合成甲醇和合成氨等生产过程中的催化剂产生中毒。
请问答下列问题:
(1)Fe(CO)5中铁的化合价为0,写出铁原子的基态电子排布式
(2)原子数目和电子总数(或价电子总数)相同的微粒互为等电子体,等电子体具有相似的结构特征。与CO分子互为等电子体的分子和离子分别为 和 (填化学式),CO分子的结构式可表示成 。
(3)Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂。据此可判断Fe(CO)5晶体为 晶体。
(4)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有 ,CH3OH的熔、沸点比CH4的熔、沸点比高,其主要原因是 。
17.(12分)高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ΔH = a kJ (mol-1
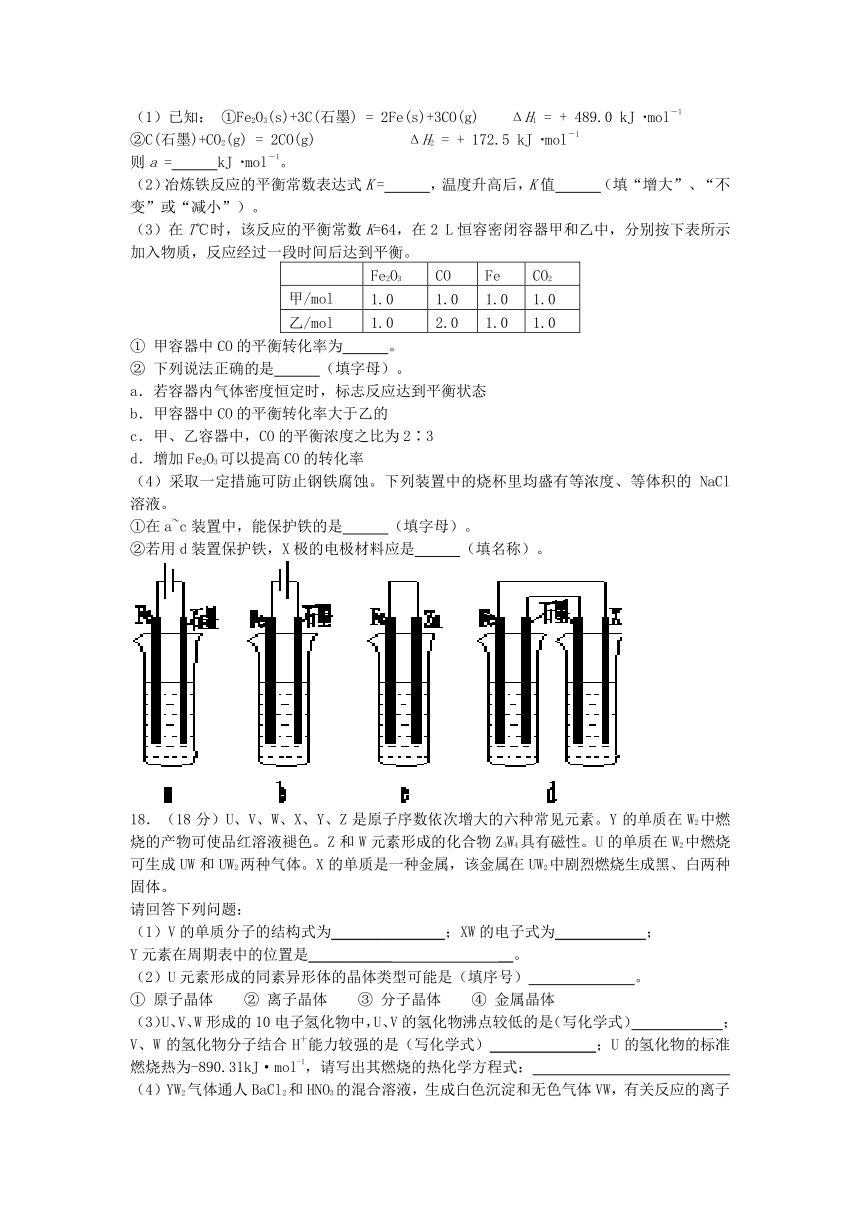
(1)已知: ①Fe2O3(s)+3C(石墨) = 2Fe(s)+3CO(g) ΔH1 = + 489.0 kJ (mol-1
②C(石墨)+CO2(g) = 2CO(g) ΔH2 = + 172.5 kJ (mol-1
则a = kJ (mol-1。
(2)冶炼铁反应的平衡常数表达式K = ,温度升高后,K值 (填“增大”、“不
变”或“减小”)。
(3)在T℃时,该反应的平衡常数K=64,在2 L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
Fe2O3
CO
Fe
CO2
甲/mol
1.0
1.0
1.0
1.0
乙/mol
1.0
2.0
1.0
1.0
① 甲容器中CO的平衡转化率为 。
② 下列说法正确的是 (填字母)。
a.若容器内气体密度恒定时,标志反应达到平衡状态
b.甲容器中CO的平衡转化率大于乙的
c.甲、乙容器中,CO的平衡浓度之比为2∶3
d.增加Fe2O3可以提高CO的转化率
(4)采取一定措施可防止钢铁腐蚀。下列装置中的烧杯里均盛有等浓度、等体积的NaCl溶液。
①在a~c装置中,能保护铁的是 (填字母)。
②若用d装置保护铁,X极的电极材料应是 (填名称)。
18.(18分)U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
(1)V的单质分子的结构式为_______________;XW的电子式为____________;
Y元素在周期表中的位置是___________ __。
(2)U元素形成的同素异形体的晶体类型可能是(填序号) 。
① 原子晶体 ② 离子晶体 ③ 分子晶体 ④ 金属晶体
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)____________;V、W的氢化物分子结合H+能力较强的是(写化学式)______________;U的氢化物的标准燃烧热为-890.31kJ·mol-1,请写出其燃烧的热化学方程式:
(4)YW2气体通人BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为__________________________________________,由此可知VW和YW2还原性较强的是(写化学式)______________________________。
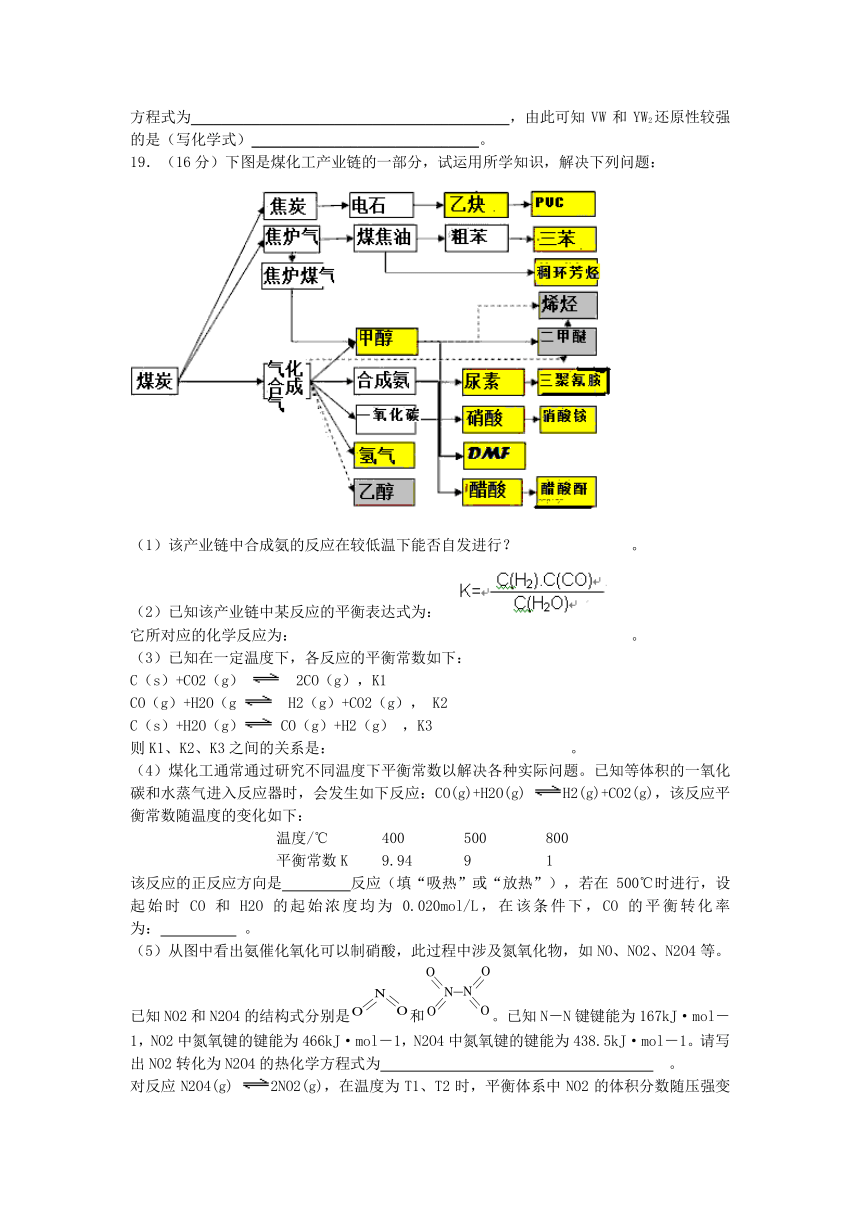
19.(16分)下图是煤化工产业链的一部分,试运用所学知识,解决下列问题:
(1)该产业链中合成氨的反应在较低温下能否自发进行? 。
(2)已知该产业链中某反应的平衡表达式为:
它所对应的化学反应为: 。
(3)已知在一定温度下,各反应的平衡常数如下:
C(s)+CO2(g) 2CO(g),K1
CO(g)+H2O(g H2(g)+CO2(g), K2
C(s)+H2O(g) CO(g)+H2(g) ,K3
则K1、K2、K3之间的关系是: 。
(4)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g) H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
温度/℃
400
500
800
平衡常数K
9.94
9
1
该反应的正反应方向是 反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,CO的平衡转化率为: 。
(5)从图中看出氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO2、N2O4等。已知NO2和N2O4的结构式分别是和。已知N-N键键能为167kJ·mol-1,NO2中氮氧键的键能为466kJ·mol-1,N2O4中氮氧键的键能为438.5kJ·mol-1。请写出NO2转化为N2O4的热化学方程式为 。
对反应N2O4(g) 2NO2(g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。
下列说法正确的是 。
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法
(6)以上述产业链中甲醇为燃料制成燃料电池,请写出在氢氧化钾介质中该电池的负极反应式 。
20.(14分) 研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)利用反应6NO2+8NH3 7N2+12H2O可处理NO2。当转移3.6mol电子时,生成的N2在标准状况下是 L。
(2)已知:反应1:2SO2(g)+O2(g) 2SO3(g) ΔH = —196.6 kJ·mol-1
反应2:NO2(g)+SO2(g) SO3(g)+NO(g) ΔH = —41.8kJ·mol-1
则反3:2NO(g)+O2(g) 2NO2(g)的 ΔH = _________ kJ·mol-1
(3) 一定条件下,将2molNO与2molO2置于恒容密闭容器中发生上述反应3,下列各项能说明反应达到平衡状态的是 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.NO和O2的物质的量之比保持不变 d.每消耗1 molO2同时生成2 molNO2
(4)CO可用于合成甲醇,一定温度下,向体积为2L的密闭容器中加入CO和H2,发生反应CO(g)+2H2(g) CH3OH(g),达平衡后测得各组分浓度如下:
物质
CO
H2
CH3OH
浓度(mol?L—1)
0.9
1.0
0.6
①混合气体的平均相对分子质量__________________________。
②列式并计算平衡常数K=__________________________。
③若将容器体积压缩为1L,不经计算,预测新平衡中c(H2)的取值范围是__________。
④若保持体积不变,再充入0.6molCO和0.4molCH3OH,此时v正___v逆(填“>”、“<”或“=”)。
三、计算题
21.某金属M的氢氧化物的结晶水合物M(OH)2·xH2O与Na2CO3的混合物共36.8g,加入足量的水后,生成白色沉淀(沉淀中不含结晶水),将沉淀过滤、洗涤、烘干,称得其质量为9.85g,将得到的沉淀高温灼烧后,质量变为7.65g,滤液与酸作用不产生气体,若用足量的铵盐与滤液共热,则产生4.48L气体(标准状况)。
(1)滤液中n(OH-)=____________mol
(2)M的相对原子质量_____________________
(3)M的氢氧化物的结晶水合物的化学式为____________________
(4)将M的此氢氧化物与NH4Cl置右图所示装置(玻璃片中与烧杯底部之间有一薄层水)中混合反应后,用手拿起烧杯时,玻璃片将___________________,与该反应对应的能量变化关系图是_________
参考答案
1.B
【解析】“析出同质量的金属,消耗电量最少”即可转化为选“通过相同电量,析出金属最多”者。由
Na++e-Na K++e-K
23 g 39 g
Ca2++2e-Ca Al3++3e-Al
40 g 27 g
知,都通过1 mol e-,四者分别析出金属23 g、39 g、20 g、9 g。
2.D
【解析】容量瓶是精密的玻璃仪器,不能用于溶于固体;排除选项AB;配成100ml溶液,并非加入100ml水,选项C排除。
点评:考查一定物质的量浓度溶液配置!
3.C
【解析】Z 减小了48g,Y增加了22g,Q增加了9g,根据质量守恒定律,反应物和生成物的质量相等,所以X也要增加17g,X也是生成物,此反应是一种生成三种,是分解反应
4.B
【解析】
5.C
【解析】影响反应速率的因素中,影响由大到小为催化剂、温度、浓度和压强;故排除AB。浓度为混合后的浓度,C中总体积下,浓度大。故C速率最大。
6.C
【解析】汽油燃烧伴随发光,不可能全部转化为热能,A是错误的。溶度积常数只与温度和难溶电解质的性质有关系,B不正确。D不一定,例如钙的活泼性强于锂的。所以正确的答案是C。
7.D
【解析】
正确答案:D
A. 不正确,金属单质与盐溶液的反应有的不是置换反应,Fe+2FeCl3=3FeCl2
B.不正确,加碘食盐中添加碘酸钾而不用碘化钾,是因为碘化钾易被空气氧化。
C. 不正确,与强酸、强碱都反应的物质也可以是盐,如NH4HCO3
8.CD
【解析】略
9.D
【解析】
试题分析:液氯是单质,不属于非电解质。答案选D。
考点:基本概念基本理论
点评:电解质和非电解质都是在化合物的范围内讨论,单质和混合物既不属于电解质也不属于非电解质。
10.C
【解析】K原子M层电子数是8个,选项A不正确;水合钠离子的结构示意图是,所以选项B不正确;氧化还原反应反应中,还原剂失去电子被氧化剂得到,选项D不正确,所以正确的答案选C。
11.D
【解析】A不正确,例如乙酸的酸酐是(CH3CO)2O不属于酸性氧化物。B不正确,例如MnO4-能把Fe2+转化为Fe3+。C不正确,例如白磷分子中键角是60°。羊油是是油脂,属于酯类,能发生皂化反应,但重油是烃类,和氢氧化钾不反应,D正确,答案选D。
12.B
【解析】
试题分析:氢键分为2种,一种是分子间氢键,一种是分子内氢键,通常前者使物质的熔点升高,而后者使物质的熔点降低,A错。丁达尔现象是胶体粒子对光线的散射形成的,可以用于区分胶体和溶液,C错。金属发生锈蚀属于化学变化,而电子气理论主要解释金属的一些物理性质,如导电性、延展性等,D错。
考点:物质结构与性质及氢键、电子气理论
点评:直接考查概念的应用,属于较简单题。
13.AB
【解析】水的离子积常数只与温度有关系,所以C不正确。根据△G=△H-T·△S可知,由于反应是熵值减小的反应,所以反应应该是放热反应,D不正确。AB都是正确的,答案选AB。
14.D
【解析】
试题分析:酸性氧化物是能与碱反应生成盐和水的氧化物,酸性氧化物不一定是非金属氧化物,如Mn2O7是酸性氧化物,A错误;纯净物只含一种物质,混合物不止一种物质,B错误;强弱电解质的区别是看电解质能否完全电离,C错误。
考点:化学基本概念。
点评:电解质溶液导电能力与电解质强弱无关。溶液导电能力与离子浓度与离子电荷有关。
15.C
【解析】
试题分析:A不正确,该反应中,反应物的总能量高于生成物的总能量,是放热反应;B不正确,因为临近终点时pH应该发生突变;醋酸是弱酸,在pH相等的条件下,醋酸的浓度大于盐酸的,反应速率快,C正确;碳酸钠和盐酸反应是分步进行的,所以b表示的是碳酸氢钠,D不正确,答案选C。
考点:考查反应热的判断、图像识别、反应速率的大小比较等。
点评:该题容易错选B。由于图像符合pH的变化趋势,所以很容易给人以错觉,而错选主要是由于忽略了临近终点时pH的变化导致的,所以掌握知识和应用知识是两个不同的方面。
16.(14分)(1)1s2 2s2 2p6 3s 23p6 3d6 4s2(2分)(2) N2(2分)、CN-(2分),C≡O(2分)
(3) 分子晶体(2分)(4) CH4和CH3OH(2分) ,CH3OH形成分子间氢键(2分)
【解析】(1)根据构造原理可知,铁原子的基态电子排布式为1s2 2s2 2p6 3s 23p6 3d6 4s2。
(2)应用价电子数和原子数分别都相等的是等电子体,所以与CO分子互为等电子体的分子和离子分别为N2和CN-;由于氮气是直线型结构,所以CO分子的结构式可表示成C≡O。
(3)Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂。据此可判断Fe(CO)5晶体应该是分子晶体。
(4)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子是CH4、CH3OH,CO是直线型结构,采用sp杂化。由于CH3OH形成分子间氢键,所以CH3OH的熔、沸点比CH4的熔、沸点比高。
17.(12分)
(1)(2分)-28.5
(2)(1分)———— (1分)减小
(3)①(2分)60 % ②(2分)ac(漏选得1分,错选不得分)
(4)①(2分)bc(漏选得1分,错选不得分)
②(2分)锌
【解析】
18.(1)N≡N; ; 第三周期ⅥA族。(2) ①③
(3)CH4; NH3, CH4(g) +2O2(g)=CO2(g)+2H2O(l) △H=-890.31KJ·mol-1。
(4)3SO2+3Ba2+ +2H2O +2NO3- =3BaSO4↓+2NO↑ + 4H+, SO2。
【解析】Y的单质在W2中燃烧的产物可使品红溶液褪色,所以Y是S,W是O元素;Z和W元素形成的化合物Z3W4具有磁性,因此Z是Fe。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体,因此U是碳,X是镁。营业务U、V、W、X、Y、Z是原子序数依次增大的六种常见元素,所以V是氮元素。
(1)氮气中含有氮氮三键,所以气结构式是N≡N;XW是氧化镁,氧化镁是含有离子键的离子化合物,电子式为。S元素的原子序数是16,位于第三周期ⅥA族。由于氨水是弱碱,所以氨气极易结合氢离子生成NH4+。
(2)在碳元素形成的单质中金刚石是原子晶体,而C60是分子晶体,不存在离子晶体和金属晶体,答案选①③。
(3)U、V、W形成的10电子氢化物是甲烷、氨气和水。由于水分子间存在氢键,所以水的沸点最高,较低是甲烷和氨气。燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,所以热化学方程式是CH4(g) +2O2(g)=CO2(g)+2H2O(l) △H=-890.31KJ·mol-1。
(4)由于硝酸具有氧化性,能把SO2氧化生成硫酸,而还原产物是NO,反应的离子方程式是3SO2+3Ba2+ +2H2O +2NO3- =3BaSO4↓+2NO↑ + 4H+。在氧化还原反应中还原剂的还原性强于还原产物的,所以还原性较强的是SO2。
19.(16分)
(1)可以
(2)C(s)+H2O(g) CO(g)+H2(g)
(3)K3=K1×K2
(4)放热,75%
(5)2NO2(g) N2O4(g) ΔH=-57 kJ·mol-1 , D
(6)CH3OH+8OH——6e—==CO32—+6H2O
【解析】略
20.(14分)(1) 23.52(2分) (2)-113(2分) (3)abc(2分)
(4)①18.56(2分) ②0.6/(0.9×1.02)=2/3 L2? moL—2 (或0.67 L2? moL—2) (2分)
③1 mol?L—1【解析】(1)根据反应式可知,NO2是氧化剂,氮元素的化合价从+4价降低到0价,得到4个电子,则生成7mol氮气,转移24mol电子。因此当转移3.6mol电子时,生成的N2是7×3.6mol÷24=1.05mol,则在标准状况下的体积是1.05mol×22.4L/mol=23.52L。
(2)考查盖斯定律的应用。根据盖斯定律可知,①-②×2即得到反应2NO(g)+O2(g)2NO2(g),所以该反应热△H=—196.6 kJ·mol-1+41.8kJ·mol-1×2=-113kJ/mol。
(3)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。颜色深浅和浓度有关系,所以b正确。反应是体积减小的,所以压强也是减小的,则a可以说明;NO和O2的物质的量之比保持不变,即说明物质的含量不再发生变化,c正确;d中反应速率的方向是相同的,速率之比是相应的化学计量数之比,因此d中的关系始终是成立,不正确,答案选abc。
(4)①平衡时CO、氢气和甲醇的物质的量分别是1.8mol、2.0mol和1.2mol,所以混合气体的平均相对分子质量是。
②平衡常数K=
③正反应是体积减小的,所以增大压强,平衡向正反应方向进行,则根据勒夏特列原理可知,平衡时氢气的浓度一定是1 mol?L—1④若保持体积不变,再充入0.6molCO和0.4molCH3OH,,则此时,所以是平衡状态,则正反应速率等于逆反应速率。
21.(1)0.2,(2)137 (3) Ba(OH)2·8H2O (4) 随烧杯一起被拿起来,A
【解析】:由生成的氨气可求得n(OH-)=0.2mol/L,因OH-在前一阶段没有参与反应,故知M(OH)2·xH2O为0.1mol/L,由滤液与酸作用不产生气体知M(OH)2·xH2O与Na2CO3时,后者全部反应完了。又沉淀是碳酸盐,由MCO3MO+CO2↑可求得M的相对原子质量为137,故M是钡元素。由生成的9.85gBaCO3可求得n(Na2CO3)=0.05mL,再结合混合物总质量可求出x=8。Ba(OH)2·8H2O与NH4Cl反应时会吸收大量的热而导致水结冰,将烧杯与玻璃片沾结在一起,该反应是吸热反应,生成物能量高于反应物。
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上
第I卷(选择题)
一、选择题
1.电解下列熔融物,析出同质量的金属时,消耗电量最少的是()
A.NaOH
B.KCl
C.CaCl2
D.Al2O3
2.要配制浓度约为2mol/L NaOH溶液100mL,下列操作正确的是
A.称取8gNaOH固体,放入100mL量筒中,边搅拌边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100mL
B.称取8gNaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀
C.称取8gNaOH固体,放入100mL烧杯中,将烧杯中加满蒸馏水,同时不断搅拌至固体溶解
D.用100mL量筒量取40ml 5mol/L NaOH溶液,倒入250mL烧杯中,再用同一量筒取60mL蒸馏水,不断搅拌下,慢慢倒入烧杯中
3.在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
物质
X
Y
Z
Q
反应前质量/g
2
2
48
5
反应后质量/g
待测
24
0
14
试判断该密闭容器中发生反应属于:
A、化合反应??? B、置换反应???? C、分解反应???? D、复分解反应
4.下列物质中只含有离子键的是( )
A.H2O B.NaCl
C.NH4Cl D.CCl4
5.已知Na2S2O3+H2SO4═Na2SO4+SO2+SO2+H2O下列各组实验中溶液最先变浑浊的是
组号
参加反应的物质
反应温度(℃)
V(mL)
C(mol/L)
V(mL)
C(mol/L)
V(mL)
A
10
5
0.1
5
0.1
5
B
10
5
0.1
5
0.1
10
C
30
5
0.2
5
0.2
5
D
30
5
0.2
5
0.2
10
6.下列说法中正确的是
A.汽油燃烧时将全部的化学能转化为热能
B.向饱和AgCl溶液中加入盐酸,Ksp变大
C.若存在简单阴离子R2-,则R一定属于VIA族
D.最外层电子数较少的金属元素,一定比最外层电子数较它多的金属元素活泼性强
7.下列叙述正确的是( )
A. 金属单质与盐溶液的反应都是置换反应
B.加碘食盐中添加碘酸钾而不用碘化钾,是因为碘酸钾能溶于水而碘化钾难溶于水
C. 与强酸、强碱都反应的物质只有两性氧化物和两性氢氧化物
D.氯气可用作消毒剂和漂白剂,是因为氯气与水反应生成的次氯酸具有强氧化性
8.用下图表示的一些物质或概念间的从属关系中正确的是
X
Y
Z
A
混合物
胶体
分散系
B
纯净物
碱
纯碱
C
化合物
电解质
BaSO4
D
化学反应
非氧化还原反应
复分解反应
9.下列说法不正确的是
A.所有的复分解反应都是非氧化还原反应
B.使空气中游离态的氮转化为含氮化合物的方法叫做氮的固定
C.静电除尘利用了胶体能发生电泳的性质
D.液氨、液氯、液态氯化氢都是非电解质
10.示意图或图示能够直观形象地呈现化学知识,下列示意图或图示正确的是
11.下列判断正确的是( )
A. 酸酐一定是酸性氧化物
B.化学反应不能将一种离子转化为另一种离子
C.正四面体分子中的键角都是109°28
D.羊油和重油可用氢氧化钾溶液加以区分
12.下列关于物质结构与性质的叙述中,正确的是( )
A.氢键的存在一定会使物质的熔点升高
B.因为蛋白质分子与胶体粒子大小相近,故蛋白质溶液具有胶体的某些性质
C.丁达尔现象是胶体粒子对光线反射形成的,可以用于区分胶体和悬浊液
D.可以用电子气理论解释大多数金属容易发生锈蚀的性质
13.下列叙述中正确的是
A.锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后,再将不溶物用稀盐酸溶解去除
B.向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进了Fe3+水解
C.向纯水中加入盐酸或降温都能使水的离子积减小,电离平衡逆向移动
D.反应2A(g) + B(g) = 3C (s) + D(g)在一定条件下能自发进行,说明该反应的ΔH>0
14.下列说法正确的是( )
A、酸性氧化物就是非金属氧化物
B、纯净物与混合物的区别是看是否只含有一种元素
C、强弱电解质的区别是溶液的导电能力的大小
D、氧化还原反应的判断依据是反应过程中元素的化合价是否发生变化
15.化学中图象可以直观地描述化学反应的进程或结果,下列图像描述正确的是( )
A.图5表示化学反应H2(g)+Cl2(g)=2HCl(g)的能量变化,则该反应的反应热△H =183kJ·mol-1
B.图6表示室温时用0.1mol·L-1盐酸滴定20mL0.1mol·L-1NaOH溶液,溶液pH随加入酸体积变化
C.图7表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液
D.图8表示10mL0.1mol/LNa2CO3和NaHCO3两种溶液中,分别滴加0.1mol/LHCl,产生CO2的体积随盐酸体积的变化,则b表示Na2CO3溶液
第II卷(非选择题)
二、填空题
16.(14分)随着石油资源的日趋紧张,天然气资源的开发利用受到越来越多的关注。以天然气(主要成分CH4)为原料经合成气(主要成分CO、H2)制化学品,是目前天然气转化利用的主要技术路线。而采用渣油、煤、焦炭为原料制合成气,常因含羰基铁[Fe(CO)5]等而导致以合成气为原料合成甲醇和合成氨等生产过程中的催化剂产生中毒。
请问答下列问题:
(1)Fe(CO)5中铁的化合价为0,写出铁原子的基态电子排布式
(2)原子数目和电子总数(或价电子总数)相同的微粒互为等电子体,等电子体具有相似的结构特征。与CO分子互为等电子体的分子和离子分别为 和 (填化学式),CO分子的结构式可表示成 。
(3)Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂。据此可判断Fe(CO)5晶体为 晶体。
(4)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有 ,CH3OH的熔、沸点比CH4的熔、沸点比高,其主要原因是 。
17.(12分)高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ΔH = a kJ (mol-1
(1)已知: ①Fe2O3(s)+3C(石墨) = 2Fe(s)+3CO(g) ΔH1 = + 489.0 kJ (mol-1
②C(石墨)+CO2(g) = 2CO(g) ΔH2 = + 172.5 kJ (mol-1
则a = kJ (mol-1。
(2)冶炼铁反应的平衡常数表达式K = ,温度升高后,K值 (填“增大”、“不
变”或“减小”)。
(3)在T℃时,该反应的平衡常数K=64,在2 L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
Fe2O3
CO
Fe
CO2
甲/mol
1.0
1.0
1.0
1.0
乙/mol
1.0
2.0
1.0
1.0
① 甲容器中CO的平衡转化率为 。
② 下列说法正确的是 (填字母)。
a.若容器内气体密度恒定时,标志反应达到平衡状态
b.甲容器中CO的平衡转化率大于乙的
c.甲、乙容器中,CO的平衡浓度之比为2∶3
d.增加Fe2O3可以提高CO的转化率
(4)采取一定措施可防止钢铁腐蚀。下列装置中的烧杯里均盛有等浓度、等体积的NaCl溶液。
①在a~c装置中,能保护铁的是 (填字母)。
②若用d装置保护铁,X极的电极材料应是 (填名称)。
18.(18分)U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
(1)V的单质分子的结构式为_______________;XW的电子式为____________;
Y元素在周期表中的位置是___________ __。
(2)U元素形成的同素异形体的晶体类型可能是(填序号) 。
① 原子晶体 ② 离子晶体 ③ 分子晶体 ④ 金属晶体
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)____________;V、W的氢化物分子结合H+能力较强的是(写化学式)______________;U的氢化物的标准燃烧热为-890.31kJ·mol-1,请写出其燃烧的热化学方程式:
(4)YW2气体通人BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为__________________________________________,由此可知VW和YW2还原性较强的是(写化学式)______________________________。
19.(16分)下图是煤化工产业链的一部分,试运用所学知识,解决下列问题:
(1)该产业链中合成氨的反应在较低温下能否自发进行? 。
(2)已知该产业链中某反应的平衡表达式为:
它所对应的化学反应为: 。
(3)已知在一定温度下,各反应的平衡常数如下:
C(s)+CO2(g) 2CO(g),K1
CO(g)+H2O(g H2(g)+CO2(g), K2
C(s)+H2O(g) CO(g)+H2(g) ,K3
则K1、K2、K3之间的关系是: 。
(4)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g) H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
温度/℃
400
500
800
平衡常数K
9.94
9
1
该反应的正反应方向是 反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,CO的平衡转化率为: 。
(5)从图中看出氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO2、N2O4等。已知NO2和N2O4的结构式分别是和。已知N-N键键能为167kJ·mol-1,NO2中氮氧键的键能为466kJ·mol-1,N2O4中氮氧键的键能为438.5kJ·mol-1。请写出NO2转化为N2O4的热化学方程式为 。
对反应N2O4(g) 2NO2(g),在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。
下列说法正确的是 。
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法
(6)以上述产业链中甲醇为燃料制成燃料电池,请写出在氢氧化钾介质中该电池的负极反应式 。
20.(14分) 研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)利用反应6NO2+8NH3 7N2+12H2O可处理NO2。当转移3.6mol电子时,生成的N2在标准状况下是 L。
(2)已知:反应1:2SO2(g)+O2(g) 2SO3(g) ΔH = —196.6 kJ·mol-1
反应2:NO2(g)+SO2(g) SO3(g)+NO(g) ΔH = —41.8kJ·mol-1
则反3:2NO(g)+O2(g) 2NO2(g)的 ΔH = _________ kJ·mol-1
(3) 一定条件下,将2molNO与2molO2置于恒容密闭容器中发生上述反应3,下列各项能说明反应达到平衡状态的是 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.NO和O2的物质的量之比保持不变 d.每消耗1 molO2同时生成2 molNO2
(4)CO可用于合成甲醇,一定温度下,向体积为2L的密闭容器中加入CO和H2,发生反应CO(g)+2H2(g) CH3OH(g),达平衡后测得各组分浓度如下:
物质
CO
H2
CH3OH
浓度(mol?L—1)
0.9
1.0
0.6
①混合气体的平均相对分子质量__________________________。
②列式并计算平衡常数K=__________________________。
③若将容器体积压缩为1L,不经计算,预测新平衡中c(H2)的取值范围是__________。
④若保持体积不变,再充入0.6molCO和0.4molCH3OH,此时v正___v逆(填“>”、“<”或“=”)。
三、计算题
21.某金属M的氢氧化物的结晶水合物M(OH)2·xH2O与Na2CO3的混合物共36.8g,加入足量的水后,生成白色沉淀(沉淀中不含结晶水),将沉淀过滤、洗涤、烘干,称得其质量为9.85g,将得到的沉淀高温灼烧后,质量变为7.65g,滤液与酸作用不产生气体,若用足量的铵盐与滤液共热,则产生4.48L气体(标准状况)。
(1)滤液中n(OH-)=____________mol
(2)M的相对原子质量_____________________
(3)M的氢氧化物的结晶水合物的化学式为____________________
(4)将M的此氢氧化物与NH4Cl置右图所示装置(玻璃片中与烧杯底部之间有一薄层水)中混合反应后,用手拿起烧杯时,玻璃片将___________________,与该反应对应的能量变化关系图是_________
参考答案
1.B
【解析】“析出同质量的金属,消耗电量最少”即可转化为选“通过相同电量,析出金属最多”者。由
Na++e-Na K++e-K
23 g 39 g
Ca2++2e-Ca Al3++3e-Al
40 g 27 g
知,都通过1 mol e-,四者分别析出金属23 g、39 g、20 g、9 g。
2.D
【解析】容量瓶是精密的玻璃仪器,不能用于溶于固体;排除选项AB;配成100ml溶液,并非加入100ml水,选项C排除。
点评:考查一定物质的量浓度溶液配置!
3.C
【解析】Z 减小了48g,Y增加了22g,Q增加了9g,根据质量守恒定律,反应物和生成物的质量相等,所以X也要增加17g,X也是生成物,此反应是一种生成三种,是分解反应
4.B
【解析】
5.C
【解析】影响反应速率的因素中,影响由大到小为催化剂、温度、浓度和压强;故排除AB。浓度为混合后的浓度,C中总体积下,浓度大。故C速率最大。
6.C
【解析】汽油燃烧伴随发光,不可能全部转化为热能,A是错误的。溶度积常数只与温度和难溶电解质的性质有关系,B不正确。D不一定,例如钙的活泼性强于锂的。所以正确的答案是C。
7.D
【解析】
正确答案:D
A. 不正确,金属单质与盐溶液的反应有的不是置换反应,Fe+2FeCl3=3FeCl2
B.不正确,加碘食盐中添加碘酸钾而不用碘化钾,是因为碘化钾易被空气氧化。
C. 不正确,与强酸、强碱都反应的物质也可以是盐,如NH4HCO3
8.CD
【解析】略
9.D
【解析】
试题分析:液氯是单质,不属于非电解质。答案选D。
考点:基本概念基本理论
点评:电解质和非电解质都是在化合物的范围内讨论,单质和混合物既不属于电解质也不属于非电解质。
10.C
【解析】K原子M层电子数是8个,选项A不正确;水合钠离子的结构示意图是,所以选项B不正确;氧化还原反应反应中,还原剂失去电子被氧化剂得到,选项D不正确,所以正确的答案选C。
11.D
【解析】A不正确,例如乙酸的酸酐是(CH3CO)2O不属于酸性氧化物。B不正确,例如MnO4-能把Fe2+转化为Fe3+。C不正确,例如白磷分子中键角是60°。羊油是是油脂,属于酯类,能发生皂化反应,但重油是烃类,和氢氧化钾不反应,D正确,答案选D。
12.B
【解析】
试题分析:氢键分为2种,一种是分子间氢键,一种是分子内氢键,通常前者使物质的熔点升高,而后者使物质的熔点降低,A错。丁达尔现象是胶体粒子对光线的散射形成的,可以用于区分胶体和溶液,C错。金属发生锈蚀属于化学变化,而电子气理论主要解释金属的一些物理性质,如导电性、延展性等,D错。
考点:物质结构与性质及氢键、电子气理论
点评:直接考查概念的应用,属于较简单题。
13.AB
【解析】水的离子积常数只与温度有关系,所以C不正确。根据△G=△H-T·△S可知,由于反应是熵值减小的反应,所以反应应该是放热反应,D不正确。AB都是正确的,答案选AB。
14.D
【解析】
试题分析:酸性氧化物是能与碱反应生成盐和水的氧化物,酸性氧化物不一定是非金属氧化物,如Mn2O7是酸性氧化物,A错误;纯净物只含一种物质,混合物不止一种物质,B错误;强弱电解质的区别是看电解质能否完全电离,C错误。
考点:化学基本概念。
点评:电解质溶液导电能力与电解质强弱无关。溶液导电能力与离子浓度与离子电荷有关。
15.C
【解析】
试题分析:A不正确,该反应中,反应物的总能量高于生成物的总能量,是放热反应;B不正确,因为临近终点时pH应该发生突变;醋酸是弱酸,在pH相等的条件下,醋酸的浓度大于盐酸的,反应速率快,C正确;碳酸钠和盐酸反应是分步进行的,所以b表示的是碳酸氢钠,D不正确,答案选C。
考点:考查反应热的判断、图像识别、反应速率的大小比较等。
点评:该题容易错选B。由于图像符合pH的变化趋势,所以很容易给人以错觉,而错选主要是由于忽略了临近终点时pH的变化导致的,所以掌握知识和应用知识是两个不同的方面。
16.(14分)(1)1s2 2s2 2p6 3s 23p6 3d6 4s2(2分)(2) N2(2分)、CN-(2分),C≡O(2分)
(3) 分子晶体(2分)(4) CH4和CH3OH(2分) ,CH3OH形成分子间氢键(2分)
【解析】(1)根据构造原理可知,铁原子的基态电子排布式为1s2 2s2 2p6 3s 23p6 3d6 4s2。
(2)应用价电子数和原子数分别都相等的是等电子体,所以与CO分子互为等电子体的分子和离子分别为N2和CN-;由于氮气是直线型结构,所以CO分子的结构式可表示成C≡O。
(3)Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂。据此可判断Fe(CO)5晶体应该是分子晶体。
(4)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子是CH4、CH3OH,CO是直线型结构,采用sp杂化。由于CH3OH形成分子间氢键,所以CH3OH的熔、沸点比CH4的熔、沸点比高。
17.(12分)
(1)(2分)-28.5
(2)(1分)———— (1分)减小
(3)①(2分)60 % ②(2分)ac(漏选得1分,错选不得分)
(4)①(2分)bc(漏选得1分,错选不得分)
②(2分)锌
【解析】
18.(1)N≡N; ; 第三周期ⅥA族。(2) ①③
(3)CH4; NH3, CH4(g) +2O2(g)=CO2(g)+2H2O(l) △H=-890.31KJ·mol-1。
(4)3SO2+3Ba2+ +2H2O +2NO3- =3BaSO4↓+2NO↑ + 4H+, SO2。
【解析】Y的单质在W2中燃烧的产物可使品红溶液褪色,所以Y是S,W是O元素;Z和W元素形成的化合物Z3W4具有磁性,因此Z是Fe。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体,因此U是碳,X是镁。营业务U、V、W、X、Y、Z是原子序数依次增大的六种常见元素,所以V是氮元素。
(1)氮气中含有氮氮三键,所以气结构式是N≡N;XW是氧化镁,氧化镁是含有离子键的离子化合物,电子式为。S元素的原子序数是16,位于第三周期ⅥA族。由于氨水是弱碱,所以氨气极易结合氢离子生成NH4+。
(2)在碳元素形成的单质中金刚石是原子晶体,而C60是分子晶体,不存在离子晶体和金属晶体,答案选①③。
(3)U、V、W形成的10电子氢化物是甲烷、氨气和水。由于水分子间存在氢键,所以水的沸点最高,较低是甲烷和氨气。燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,所以热化学方程式是CH4(g) +2O2(g)=CO2(g)+2H2O(l) △H=-890.31KJ·mol-1。
(4)由于硝酸具有氧化性,能把SO2氧化生成硫酸,而还原产物是NO,反应的离子方程式是3SO2+3Ba2+ +2H2O +2NO3- =3BaSO4↓+2NO↑ + 4H+。在氧化还原反应中还原剂的还原性强于还原产物的,所以还原性较强的是SO2。
19.(16分)
(1)可以
(2)C(s)+H2O(g) CO(g)+H2(g)
(3)K3=K1×K2
(4)放热,75%
(5)2NO2(g) N2O4(g) ΔH=-57 kJ·mol-1 , D
(6)CH3OH+8OH——6e—==CO32—+6H2O
【解析】略
20.(14分)(1) 23.52(2分) (2)-113(2分) (3)abc(2分)
(4)①18.56(2分) ②0.6/(0.9×1.02)=2/3 L2? moL—2 (或0.67 L2? moL—2) (2分)
③1 mol?L—1
(2)考查盖斯定律的应用。根据盖斯定律可知,①-②×2即得到反应2NO(g)+O2(g)2NO2(g),所以该反应热△H=—196.6 kJ·mol-1+41.8kJ·mol-1×2=-113kJ/mol。
(3)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。颜色深浅和浓度有关系,所以b正确。反应是体积减小的,所以压强也是减小的,则a可以说明;NO和O2的物质的量之比保持不变,即说明物质的含量不再发生变化,c正确;d中反应速率的方向是相同的,速率之比是相应的化学计量数之比,因此d中的关系始终是成立,不正确,答案选abc。
(4)①平衡时CO、氢气和甲醇的物质的量分别是1.8mol、2.0mol和1.2mol,所以混合气体的平均相对分子质量是。
②平衡常数K=
③正反应是体积减小的,所以增大压强,平衡向正反应方向进行,则根据勒夏特列原理可知,平衡时氢气的浓度一定是1 mol?L—1
21.(1)0.2,(2)137 (3) Ba(OH)2·8H2O (4) 随烧杯一起被拿起来,A
【解析】:由生成的氨气可求得n(OH-)=0.2mol/L,因OH-在前一阶段没有参与反应,故知M(OH)2·xH2O为0.1mol/L,由滤液与酸作用不产生气体知M(OH)2·xH2O与Na2CO3时,后者全部反应完了。又沉淀是碳酸盐,由MCO3MO+CO2↑可求得M的相对原子质量为137,故M是钡元素。由生成的9.85gBaCO3可求得n(Na2CO3)=0.05mL,再结合混合物总质量可求出x=8。Ba(OH)2·8H2O与NH4Cl反应时会吸收大量的热而导致水结冰,将烧杯与玻璃片沾结在一起,该反应是吸热反应,生成物能量高于反应物。
同课章节目录
