第十单元 课题1 常见的酸和碱第1课时 酸碱盐的概念课件(共14张PPT)
文档属性
| 名称 | 第十单元 课题1 常见的酸和碱第1课时 酸碱盐的概念课件(共14张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 884.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-08 00:00:00 | ||
图片预览



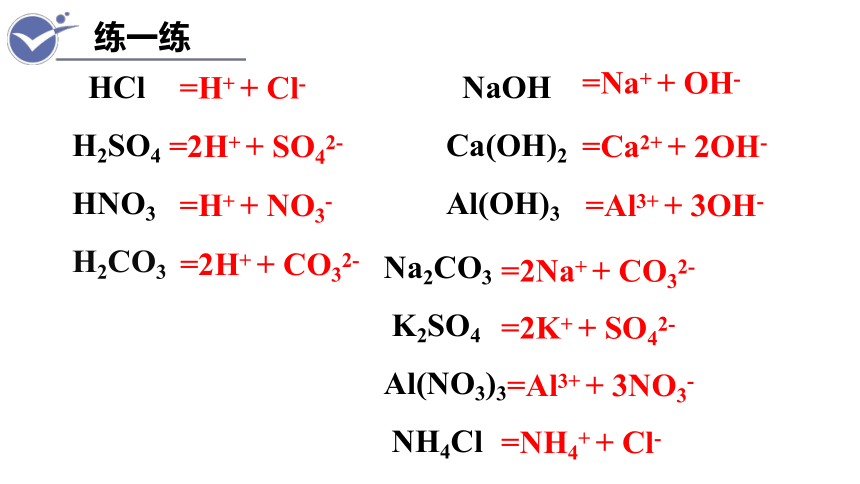
文档简介
(共14张PPT)
课题1 常见的酸和碱
第1课时 酸碱盐的概念
第十单元 酸和碱
学习目标
1、知道酸、碱、盐的溶液能导电的原因。
2、掌握电离方程式的书写。
3、根据酸、碱、盐电离生成离子的特点,了解酸、
碱、盐的概念和组成特点,能准确区分酸、碱、盐。
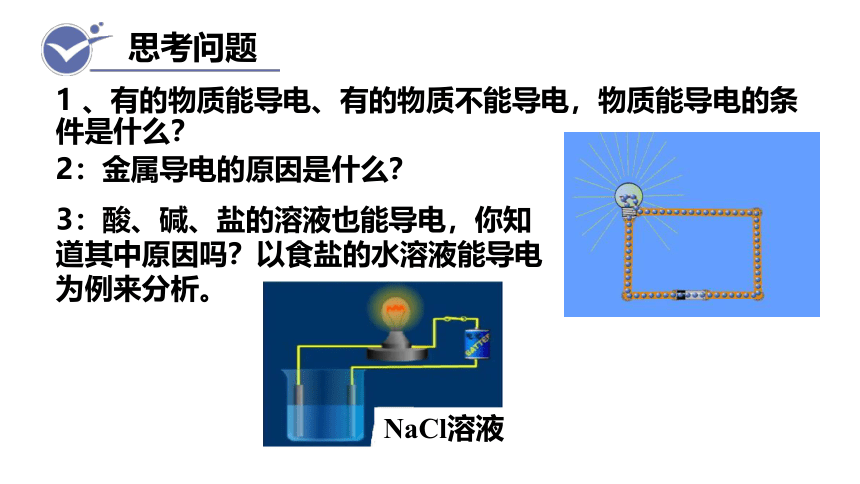
1 、有的物质能导电、有的物质不能导电,物质能导电的条件是什么?
2:金属导电的原因是什么?
思考问题
3:酸、碱、盐的溶液也能导电,你知道其中原因吗?以食盐的水溶液能导电为例来分析。
NaCl溶液
一:酸、碱、盐溶液导电的原因:
在水分子的作用下酸碱盐能电离成自由移动的离子。
二:电离—物质溶入水时,离解成自由移动的离子的过程。
三:电离方程式的书写
1、拆:将化学式拆成阴阳离子
2、写:在右边写出离子符号
3、查:﹙遵守质量守恒和电荷守恒﹚
电离方程式书写
NaCl
=Na+ + Cl-
练一练
=H+ + Cl-
=2H+ + SO42-
=H+ + NO3-
=Na+ + OH-
=Ca2+ + 2OH-
=Al3+ + 3OH-
HCl
H2SO4
HNO3
H2CO3
NaOH Ca(OH)2 Al(OH)3
Na2CO3
K2SO4
Al(NO3)3
NH4Cl
=2Na+ + CO32-
=2K+ + SO42-
=Al3+ + 3NO3-
=NH4+ + Cl-
=2H+ + CO32-
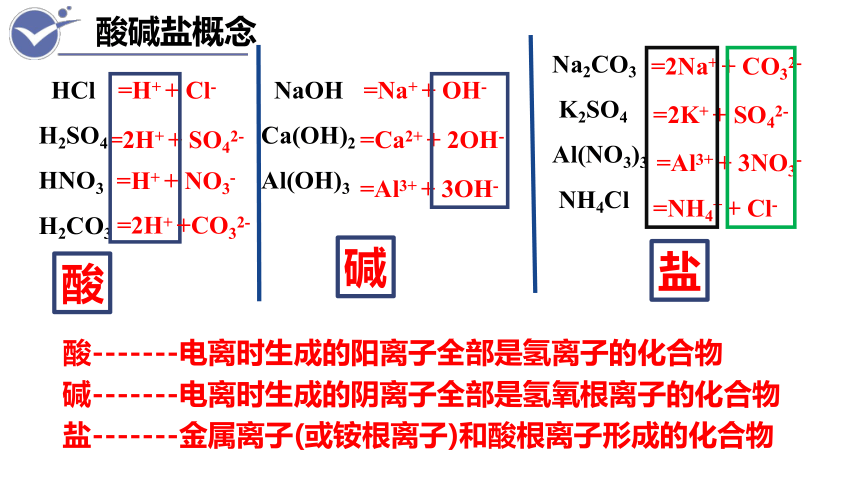
酸-------电离时生成的阳离子全部是氢离子的化合物
碱-------电离时生成的阴离子全部是氢氧根离子的化合物
盐-------金属离子(或铵根离子)和酸根离子形成的化合物
酸碱盐概念
=H+ + Cl-
=2H+ + SO42-
=H+ + NO3-
HCl
H2SO4
HNO3
H2CO3
=Na+ + OH-
=Ca2+ + 2OH-
=Al3+ + 3OH-
NaOH Ca(OH)2 Al(OH)3
Na2CO3
K2SO4
Al(NO3)3
NH4Cl
=2Na+ + CO32-
=2K+ + SO42-
=Al3+ + 3NO3-
=NH4+ + Cl-
酸
=2H+ +CO32-
碱
盐
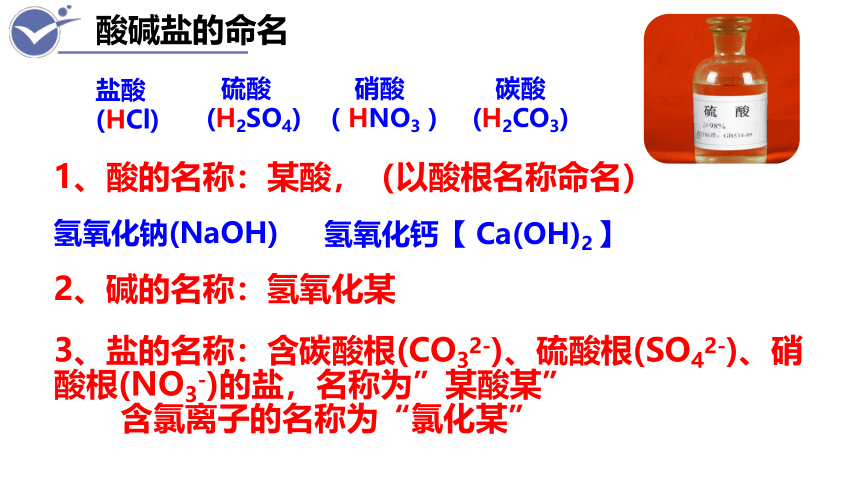
酸碱盐的命名
盐酸
(HCl)
硫酸
(H2SO4)
碳酸
(H2CO3)
硝酸
( HNO3 )
1、酸的名称:某酸,(以酸根名称命名)
氢氧化钠(NaOH)
氢氧化钙【 Ca(OH)2 】
2、碱的名称:氢氧化某
3、盐的名称:含碳酸根(CO32-)、硫酸根(SO42-)、硝酸根(NO3-)的盐,名称为”某酸某”
含氯离子的名称为“氯化某”
Na2CO3 、k2CO3、 MgCO3 、 FeCO3 、 CaCO3
Na2SO4 、K2SO4 、MgSO4 、 FeSO4 、 CaSO4
NaCl 、 KCl 、 MgCl2、 FeCl2、 CaCl2
NaNO3 、 KNO3 、 Mg(NO3)2、Fe (NO3)2 、Ca (NO3)2
碳酸盐
硫酸盐
盐酸盐
硝酸盐
钠盐
钾盐
镁盐
亚铁盐
钙盐
(NH4) 2CO3
(NH4) 2SO4
NH4 Cl
NH4 NO3
铵盐
从盐的组成上,我们怎样对盐进行分类?
盐
阳离子
阴离子
碳酸盐
钠盐
铵盐
镁盐
钾盐
硝酸盐
硫酸盐
盐酸盐
Na2CO3、Na2SO4 、NaCl、NaNO3
k2CO3、K2SO4、 KCl、 KNO3
(NH4) 2CO3 、 (NH4) 2SO4 、NH4 Cl 、NH4 NO3
MgCO3、MgSO4 、MgCl2、Mg(NO3)2
Na2CO3 、CaCO3
Na2SO4 、K2SO4
NaCl 、CaCl2
NaNO3 、 KNO3
化
合
物
单
质
碱
酸
金属
单质
非金
属单质
盐
物质
混
合
物
纯
净
物
如盐酸(HCl)、硫酸( H2SO4 )、碳酸(H2CO3)、硝酸(HNO3)
如氢氧化钠(NaOH)、氢氧化钙(Ca(OH)2)
如氯化钠(NaCl)、硫酸铜(CuSO4)
如MgO 、Fe3O4 、Al2O3 、SO2、 CO2 、P2O5、 H2O、 H2O2
如Mg、 Fe、 Cu 、Al、Hg、K、Mn
如S、 C、 P 、O2、 O3、H2、 N2
氧化物
物质分类
请你根据所学知识将下列物质分分类:
HCl
CaCO3
Na2CO3
Mg(OH)2
NaOH
CuSO4
Ba(OH)2
CaO
SO2
Fe
S
CuSO4
酸:
碱:
HCl
H2SO4
NaOH
Mg(OH)2
Ba(OH)2
CaCO3
Na2CO3
NH4Cl
单质:
盐:
S
Fe
氧化物:
CaO
SO2
练一练
NH4Cl
酸-------电离时生成的阳离子全部是氢离子的化合物
碱-------电离时生成的阴离子全部是氢氧根离子的化合物
盐-------金属离子(或铵根离子)和酸根离子形成的化合物
课堂小结
1、某化合物溶液中通过实验证明只有Na+ 和SO42- ,则该化合物是( )
A.Na2CO3 B.NaCl C.Na2SO4 D.NaHSO4
2.下列电离方程式正确的是( )
A. FeSO4=Fe3+ +SO42- B. Ca(OH)2=Ca2+ +(OH)2-
C. AlCl3=Al3+ +3Cl- D. H2SO4=H+ +SO42-
3.下列不属于盐的是( )
A.Cu2(OH)2CO3 B.CH3COOH
C.NaHSO4 D.Na2CO3
当堂练习
C
C
B
4.含有下列离子的溶液中,溶质全部为酸的是( )
A.H+ Na+ SO42- B.H+ Cl- NO3-
C.OH- K+ Ba2+ D.Ag+ K+ NO3-
5、下列物质按酸、碱、盐顺序排列的是( )
A.Mg(OH)2 CuSO4 H2CO3
B.HNO3 KOH NaCl
C.CaCO3 NaOH H3PO4
D.H2SO4 KNO3 NaOH
当堂练习
B
B
课题1 常见的酸和碱
第1课时 酸碱盐的概念
第十单元 酸和碱
学习目标
1、知道酸、碱、盐的溶液能导电的原因。
2、掌握电离方程式的书写。
3、根据酸、碱、盐电离生成离子的特点,了解酸、
碱、盐的概念和组成特点,能准确区分酸、碱、盐。
1 、有的物质能导电、有的物质不能导电,物质能导电的条件是什么?
2:金属导电的原因是什么?
思考问题
3:酸、碱、盐的溶液也能导电,你知道其中原因吗?以食盐的水溶液能导电为例来分析。
NaCl溶液
一:酸、碱、盐溶液导电的原因:
在水分子的作用下酸碱盐能电离成自由移动的离子。
二:电离—物质溶入水时,离解成自由移动的离子的过程。
三:电离方程式的书写
1、拆:将化学式拆成阴阳离子
2、写:在右边写出离子符号
3、查:﹙遵守质量守恒和电荷守恒﹚
电离方程式书写
NaCl
=Na+ + Cl-
练一练
=H+ + Cl-
=2H+ + SO42-
=H+ + NO3-
=Na+ + OH-
=Ca2+ + 2OH-
=Al3+ + 3OH-
HCl
H2SO4
HNO3
H2CO3
NaOH Ca(OH)2 Al(OH)3
Na2CO3
K2SO4
Al(NO3)3
NH4Cl
=2Na+ + CO32-
=2K+ + SO42-
=Al3+ + 3NO3-
=NH4+ + Cl-
=2H+ + CO32-
酸-------电离时生成的阳离子全部是氢离子的化合物
碱-------电离时生成的阴离子全部是氢氧根离子的化合物
盐-------金属离子(或铵根离子)和酸根离子形成的化合物
酸碱盐概念
=H+ + Cl-
=2H+ + SO42-
=H+ + NO3-
HCl
H2SO4
HNO3
H2CO3
=Na+ + OH-
=Ca2+ + 2OH-
=Al3+ + 3OH-
NaOH Ca(OH)2 Al(OH)3
Na2CO3
K2SO4
Al(NO3)3
NH4Cl
=2Na+ + CO32-
=2K+ + SO42-
=Al3+ + 3NO3-
=NH4+ + Cl-
酸
=2H+ +CO32-
碱
盐
酸碱盐的命名
盐酸
(HCl)
硫酸
(H2SO4)
碳酸
(H2CO3)
硝酸
( HNO3 )
1、酸的名称:某酸,(以酸根名称命名)
氢氧化钠(NaOH)
氢氧化钙【 Ca(OH)2 】
2、碱的名称:氢氧化某
3、盐的名称:含碳酸根(CO32-)、硫酸根(SO42-)、硝酸根(NO3-)的盐,名称为”某酸某”
含氯离子的名称为“氯化某”
Na2CO3 、k2CO3、 MgCO3 、 FeCO3 、 CaCO3
Na2SO4 、K2SO4 、MgSO4 、 FeSO4 、 CaSO4
NaCl 、 KCl 、 MgCl2、 FeCl2、 CaCl2
NaNO3 、 KNO3 、 Mg(NO3)2、Fe (NO3)2 、Ca (NO3)2
碳酸盐
硫酸盐
盐酸盐
硝酸盐
钠盐
钾盐
镁盐
亚铁盐
钙盐
(NH4) 2CO3
(NH4) 2SO4
NH4 Cl
NH4 NO3
铵盐
从盐的组成上,我们怎样对盐进行分类?
盐
阳离子
阴离子
碳酸盐
钠盐
铵盐
镁盐
钾盐
硝酸盐
硫酸盐
盐酸盐
Na2CO3、Na2SO4 、NaCl、NaNO3
k2CO3、K2SO4、 KCl、 KNO3
(NH4) 2CO3 、 (NH4) 2SO4 、NH4 Cl 、NH4 NO3
MgCO3、MgSO4 、MgCl2、Mg(NO3)2
Na2CO3 、CaCO3
Na2SO4 、K2SO4
NaCl 、CaCl2
NaNO3 、 KNO3
化
合
物
单
质
碱
酸
金属
单质
非金
属单质
盐
物质
混
合
物
纯
净
物
如盐酸(HCl)、硫酸( H2SO4 )、碳酸(H2CO3)、硝酸(HNO3)
如氢氧化钠(NaOH)、氢氧化钙(Ca(OH)2)
如氯化钠(NaCl)、硫酸铜(CuSO4)
如MgO 、Fe3O4 、Al2O3 、SO2、 CO2 、P2O5、 H2O、 H2O2
如Mg、 Fe、 Cu 、Al、Hg、K、Mn
如S、 C、 P 、O2、 O3、H2、 N2
氧化物
物质分类
请你根据所学知识将下列物质分分类:
HCl
CaCO3
Na2CO3
Mg(OH)2
NaOH
CuSO4
Ba(OH)2
CaO
SO2
Fe
S
CuSO4
酸:
碱:
HCl
H2SO4
NaOH
Mg(OH)2
Ba(OH)2
CaCO3
Na2CO3
NH4Cl
单质:
盐:
S
Fe
氧化物:
CaO
SO2
练一练
NH4Cl
酸-------电离时生成的阳离子全部是氢离子的化合物
碱-------电离时生成的阴离子全部是氢氧根离子的化合物
盐-------金属离子(或铵根离子)和酸根离子形成的化合物
课堂小结
1、某化合物溶液中通过实验证明只有Na+ 和SO42- ,则该化合物是( )
A.Na2CO3 B.NaCl C.Na2SO4 D.NaHSO4
2.下列电离方程式正确的是( )
A. FeSO4=Fe3+ +SO42- B. Ca(OH)2=Ca2+ +(OH)2-
C. AlCl3=Al3+ +3Cl- D. H2SO4=H+ +SO42-
3.下列不属于盐的是( )
A.Cu2(OH)2CO3 B.CH3COOH
C.NaHSO4 D.Na2CO3
当堂练习
C
C
B
4.含有下列离子的溶液中,溶质全部为酸的是( )
A.H+ Na+ SO42- B.H+ Cl- NO3-
C.OH- K+ Ba2+ D.Ag+ K+ NO3-
5、下列物质按酸、碱、盐顺序排列的是( )
A.Mg(OH)2 CuSO4 H2CO3
B.HNO3 KOH NaCl
C.CaCO3 NaOH H3PO4
D.H2SO4 KNO3 NaOH
当堂练习
B
B
同课章节目录
