8.2.1 常见的酸(2)——酸的化学性质-2021-2022学年科粤版九年级化学科粤版下册(共20张PPT)
文档属性
| 名称 | 8.2.1 常见的酸(2)——酸的化学性质-2021-2022学年科粤版九年级化学科粤版下册(共20张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 635.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-08 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
8.2.1 常见的酸(2)——酸的化学性质
学习目标
1.通过复习回顾和实验探究,总结稀酸的化学性质。
Ca(OH)2 HNO3 NaCl Ba(OH)2 KOH HCl NH4F
NH4Cl H2 H2CO3 MgO N2 CuO H2SO4 NH4NO3 KCl H3PO4 MgF2 O2
酸:解离出阳离子全是H+的化合物
HCl==H+ +Cl-
HNO3==H+ +NO3-
H2SO4 ==2H++SO42-
H2CO3 2H++CO32-
酸的共性——H+
酸的特性——酸根离子
氢离子 酸根离子
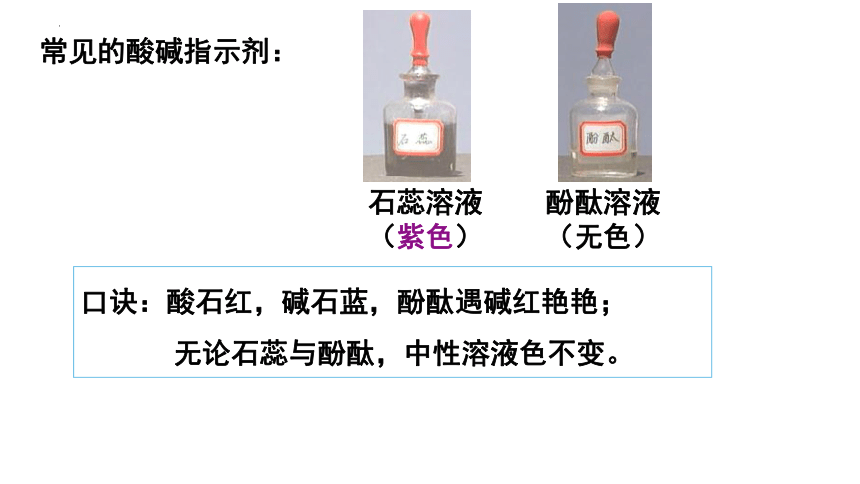
常见的酸碱指示剂:
石蕊溶液
(紫色)
酚酞溶液
(无色)
口诀:酸石红,碱石蓝,酚酞遇碱红艳艳;
无论石蕊与酚酞,中性溶液色不变。
加紫色石蕊溶液 加无色酚酞溶液
稀盐酸(HCl)
稀硫酸(H2SO4)
归纳:
1.酸能使紫色石蕊溶液变红,不能使酚酞溶液变色。
紫色石蕊变红色
紫色石蕊变红色
无色酚酞不变色
无色酚酞不变色
与稀盐酸反应 与稀硫酸反应
镁
锌
铁
Mg+2HCl=MgCl2+H2↑
Zn+2HCl=ZnCl2+H2↑
Fe+2HCl=FeCl2+H2↑
Mg+H2SO4=MgSO4+H2↑
Zn+H2SO4=ZnSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
2.酸能跟排在H前面的金属反应,生成盐和氢气(硝酸除外)
归纳:
金属活动性顺序:K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
酸+较活泼金属 盐+氢气
问题:家里的醋能装在铁制容器里?为什么
现 象 化学方程式
铁锈+稀盐酸
铁锈逐渐消失,溶液变成黄色
Fe2O3+6HCl=2FeCl3+3H2O
3.酸能与金属氧化物反应生成盐和水
归纳:
铁锈+稀硫酸
铁锈逐渐消失,溶液变成黄色
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
CuO+2HCl=
CuO+H2SO4=
CuCl2+H2O
CuSO4+H2O
酸+金属氧化物 盐+水
生锈的铁器在用稀盐酸或稀硫酸除锈时,能否长时间浸泡?为什么?
Fe+2HCl=FeCl2+H2↑
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
Fe2O3+6HCl=2FeCl3+3H2O
Fe+H2SO4=FeSO4+H2↑
若用稀盐酸浸泡:
若用稀硫酸浸泡:
酸是除锈专家 !
生锈的铜器呢?
问题:请写出实验室制CO2的化学方程式。
CaCO3 + 2HCl == CaCl2+ CO2↑+ H2O
Na2CO3 + 2HCl == 2NaCl+ CO2↑+ H2O
4.酸能与某些盐反应新酸和新盐
归纳:
酸+盐 新酸+新盐
Na2CO3 + H2SO4== Na2SO4 + CO2↑+ H2O
①盐酸特性:
AgNO3 + HCl ==AgCl ↓+ HNO3
Cl-的检验方法:
防止其他离子的干扰
a.取少量待测液于试管中,加硝酸银溶液
b.如果产生白色沉淀,再滴入稀硝酸,如果白色沉淀不溶解
c.则证明含有Cl-
加HNO3的目的:
盐酸制硝酸
AgCl:白色沉淀,不溶于水,也不溶于酸
白色沉淀
AgNO3 + NaCl ==AgCl ↓+ NaNO3
②硫酸特性:
BaCl2 + H2SO4 ==BaSO4↓+ 2HCl
SO42-的检验方法:
防止CO32-的干扰
a.取少量待测液于试管中,滴加几滴硝酸钡溶液,
b.如果产生白色沉淀,再滴入稀硝酸,如果白色沉淀不溶解
c.则一定含有硫酸根
加HNO3的目的:
硫酸制盐酸
白色沉淀
BaSO4:白色沉淀,不溶于水,也不溶于酸
Ba(NO3)2 + K2SO4 ==BaSO4↓+ 2KNO3
1.酸能使紫色石蕊溶液变红色,酸不能使无色酚酞溶液变色。
3.酸能与金属氧化物反应生成盐和水。
2.酸能与活泼金属反应生成盐和氢气。
酸能解离出 H+
决定
小结:
4.酸能与盐反应新酸和新盐。
酸+较活泼金属 盐+氢气
酸+金属氧化物 盐+水
酸+盐 新酸+新盐
考点三:常见酸的用途
【典型例题3】下列关于物质的用途的叙述不正确的是( )
A.盐酸可用来除铁锈
B.稀硫酸在实验室里常用作干燥剂
C.硫酸可用于精炼石油和金属除锈
D.盐酸是重要化工产品
B
【迁移训练3】下列有关酸的说法错误的是( )
A.人体胃液中含有盐酸,可帮助消化
B.硫酸可用于生产化肥、农药、火药等
C.浓硫酸可以干燥所有气体
D.稀盐酸和稀硫酸都可以用于除铁锈
C
【典型例题1】在①氧化铁②金属锌③氢氧化铜④氯化钡溶液四种物质中,跟稀硫酸、稀盐酸都能发生反应且反应中表现了“酸的通性”的组合是( )
A.①②③④ B.①②③ C.①③④ D.②③④
B
选项 X的物质类别 观点描述
A 金属 若X为Cu,则反应能够发生
B 金属氧化物 若X为MgO,则Y为H2O
C 碱 若X为NaOH,则盐为Na2SO4
D 盐 若X为BaCl2,则生成白色沉淀
【迁移训练2】小明同学归纳总结了初中所学稀硫酸的化学性质,并用“H2SO4+X―→盐+Y”这种表达式进行整理。小明的下列观点错误的是( )
A
THANKS
Ca(OH)2 HNO3 NaCl Ba(OH)2
KOH HCl NH4F NH4Cl
H2 H2CO3 MgO N2
CuO H2SO4 NH4NO3 KCl
H3PO4 MgF2 O2
Ca(OH)2 HNO3 NaCl Ba(OH)2 KOH HCl
NH4F NH4Cl H2 H2CO3 MgO N2
CuO H2SO4 NH4Cl KCl H3PO4 MgF2 O2
NH4Br NH4NO3 NaOH H2O CaCl2 AlCl3 F2
KCl MgCl2 Fe3O4 P2O5 Mg(OH)2 (NH4)2CO3
(NH4)2SO4 Al(OH)3 FeCl2 FeCl3 HCl H2S Cl2
CO2 CO SiO2 KMnO4 K2MnO4 Na2S CaF2
8.2.1 常见的酸(2)——酸的化学性质
学习目标
1.通过复习回顾和实验探究,总结稀酸的化学性质。
Ca(OH)2 HNO3 NaCl Ba(OH)2 KOH HCl NH4F
NH4Cl H2 H2CO3 MgO N2 CuO H2SO4 NH4NO3 KCl H3PO4 MgF2 O2
酸:解离出阳离子全是H+的化合物
HCl==H+ +Cl-
HNO3==H+ +NO3-
H2SO4 ==2H++SO42-
H2CO3 2H++CO32-
酸的共性——H+
酸的特性——酸根离子
氢离子 酸根离子
常见的酸碱指示剂:
石蕊溶液
(紫色)
酚酞溶液
(无色)
口诀:酸石红,碱石蓝,酚酞遇碱红艳艳;
无论石蕊与酚酞,中性溶液色不变。
加紫色石蕊溶液 加无色酚酞溶液
稀盐酸(HCl)
稀硫酸(H2SO4)
归纳:
1.酸能使紫色石蕊溶液变红,不能使酚酞溶液变色。
紫色石蕊变红色
紫色石蕊变红色
无色酚酞不变色
无色酚酞不变色
与稀盐酸反应 与稀硫酸反应
镁
锌
铁
Mg+2HCl=MgCl2+H2↑
Zn+2HCl=ZnCl2+H2↑
Fe+2HCl=FeCl2+H2↑
Mg+H2SO4=MgSO4+H2↑
Zn+H2SO4=ZnSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
2.酸能跟排在H前面的金属反应,生成盐和氢气(硝酸除外)
归纳:
金属活动性顺序:K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
酸+较活泼金属 盐+氢气
问题:家里的醋能装在铁制容器里?为什么
现 象 化学方程式
铁锈+稀盐酸
铁锈逐渐消失,溶液变成黄色
Fe2O3+6HCl=2FeCl3+3H2O
3.酸能与金属氧化物反应生成盐和水
归纳:
铁锈+稀硫酸
铁锈逐渐消失,溶液变成黄色
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
CuO+2HCl=
CuO+H2SO4=
CuCl2+H2O
CuSO4+H2O
酸+金属氧化物 盐+水
生锈的铁器在用稀盐酸或稀硫酸除锈时,能否长时间浸泡?为什么?
Fe+2HCl=FeCl2+H2↑
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
Fe2O3+6HCl=2FeCl3+3H2O
Fe+H2SO4=FeSO4+H2↑
若用稀盐酸浸泡:
若用稀硫酸浸泡:
酸是除锈专家 !
生锈的铜器呢?
问题:请写出实验室制CO2的化学方程式。
CaCO3 + 2HCl == CaCl2+ CO2↑+ H2O
Na2CO3 + 2HCl == 2NaCl+ CO2↑+ H2O
4.酸能与某些盐反应新酸和新盐
归纳:
酸+盐 新酸+新盐
Na2CO3 + H2SO4== Na2SO4 + CO2↑+ H2O
①盐酸特性:
AgNO3 + HCl ==AgCl ↓+ HNO3
Cl-的检验方法:
防止其他离子的干扰
a.取少量待测液于试管中,加硝酸银溶液
b.如果产生白色沉淀,再滴入稀硝酸,如果白色沉淀不溶解
c.则证明含有Cl-
加HNO3的目的:
盐酸制硝酸
AgCl:白色沉淀,不溶于水,也不溶于酸
白色沉淀
AgNO3 + NaCl ==AgCl ↓+ NaNO3
②硫酸特性:
BaCl2 + H2SO4 ==BaSO4↓+ 2HCl
SO42-的检验方法:
防止CO32-的干扰
a.取少量待测液于试管中,滴加几滴硝酸钡溶液,
b.如果产生白色沉淀,再滴入稀硝酸,如果白色沉淀不溶解
c.则一定含有硫酸根
加HNO3的目的:
硫酸制盐酸
白色沉淀
BaSO4:白色沉淀,不溶于水,也不溶于酸
Ba(NO3)2 + K2SO4 ==BaSO4↓+ 2KNO3
1.酸能使紫色石蕊溶液变红色,酸不能使无色酚酞溶液变色。
3.酸能与金属氧化物反应生成盐和水。
2.酸能与活泼金属反应生成盐和氢气。
酸能解离出 H+
决定
小结:
4.酸能与盐反应新酸和新盐。
酸+较活泼金属 盐+氢气
酸+金属氧化物 盐+水
酸+盐 新酸+新盐
考点三:常见酸的用途
【典型例题3】下列关于物质的用途的叙述不正确的是( )
A.盐酸可用来除铁锈
B.稀硫酸在实验室里常用作干燥剂
C.硫酸可用于精炼石油和金属除锈
D.盐酸是重要化工产品
B
【迁移训练3】下列有关酸的说法错误的是( )
A.人体胃液中含有盐酸,可帮助消化
B.硫酸可用于生产化肥、农药、火药等
C.浓硫酸可以干燥所有气体
D.稀盐酸和稀硫酸都可以用于除铁锈
C
【典型例题1】在①氧化铁②金属锌③氢氧化铜④氯化钡溶液四种物质中,跟稀硫酸、稀盐酸都能发生反应且反应中表现了“酸的通性”的组合是( )
A.①②③④ B.①②③ C.①③④ D.②③④
B
选项 X的物质类别 观点描述
A 金属 若X为Cu,则反应能够发生
B 金属氧化物 若X为MgO,则Y为H2O
C 碱 若X为NaOH,则盐为Na2SO4
D 盐 若X为BaCl2,则生成白色沉淀
【迁移训练2】小明同学归纳总结了初中所学稀硫酸的化学性质,并用“H2SO4+X―→盐+Y”这种表达式进行整理。小明的下列观点错误的是( )
A
THANKS
Ca(OH)2 HNO3 NaCl Ba(OH)2
KOH HCl NH4F NH4Cl
H2 H2CO3 MgO N2
CuO H2SO4 NH4NO3 KCl
H3PO4 MgF2 O2
Ca(OH)2 HNO3 NaCl Ba(OH)2 KOH HCl
NH4F NH4Cl H2 H2CO3 MgO N2
CuO H2SO4 NH4Cl KCl H3PO4 MgF2 O2
NH4Br NH4NO3 NaOH H2O CaCl2 AlCl3 F2
KCl MgCl2 Fe3O4 P2O5 Mg(OH)2 (NH4)2CO3
(NH4)2SO4 Al(OH)3 FeCl2 FeCl3 HCl H2S Cl2
CO2 CO SiO2 KMnO4 K2MnO4 Na2S CaF2
