9.3溶液的浓度课后提升练习--2021-2022学年九年级化学人教版下册(word版 含答案)
文档属性
| 名称 | 9.3溶液的浓度课后提升练习--2021-2022学年九年级化学人教版下册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 104.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-09 00:00:00 | ||
图片预览

文档简介
课题3 溶液的浓度
一、单选题
1.实验室配制质量分数为6%的NaCl溶液,除托盘天平、烧杯、玻璃棒、量筒、药匙外,还需要的仪器是( )
A.胶头滴管 B.铁架台 C.酒精灯 D.蒸发皿
2.实验室配制50g溶质质量分数为15%的氯化钠溶液。下列说法中错误的是( )
A.实验的步骤为计算、称量、量取、溶解、装瓶
B.若称量时托盘天平指针偏左,移动游码至天平平衡
C.把配制好的氯化钠溶液倒入干燥的试剂瓶中,并贴上标签
D.量取水时,若仰视读数,则配制的溶液中溶质的质量分数小于15%
3.从冰箱中取出一杯底部有少量蔗糖固体的糖水甲,待其恢复至室温,发现底部固体完全溶解,得到液体乙。甲和乙的比较中说法正确的是( )
A.乙溶液一定能再溶解蔗糖 B.乙中蔗糖的溶解度较大
C.乙中溶质的质量分数较小 D.甲中溶质的质量较大
4.如图,海水淡化可采用膜分离技术,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是( )
A.溶质质量增加 B.溶剂质量减小
C.溶液质量不变 D.溶质质量分数减小
5.实验室配制150 g质量分数为16%的氯化钠溶液时,下列操作会导致质量分数偏大的是( )
①称量时将氯化钠固体放在托盘天平右盘上称量;②用量筒量取水时俯视读数;
③将量筒中的水倒入烧杯中时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。
A.③④ B.②③ C.①④ D.①③④
6.欲配制 100g 质量分数为 10%的氢氧化钠溶液。下列说法中不正确的是( )
A.要用托盘天平称取 10.0g 氢氧化钠固体
B.实验中用到的玻璃仪器只有烧杯和量筒
C.量取水的体积时,仰视读数会导致溶质的质量分数偏低
D.将配好的溶液装入试剂瓶中,塞好瓶塞并贴上标签
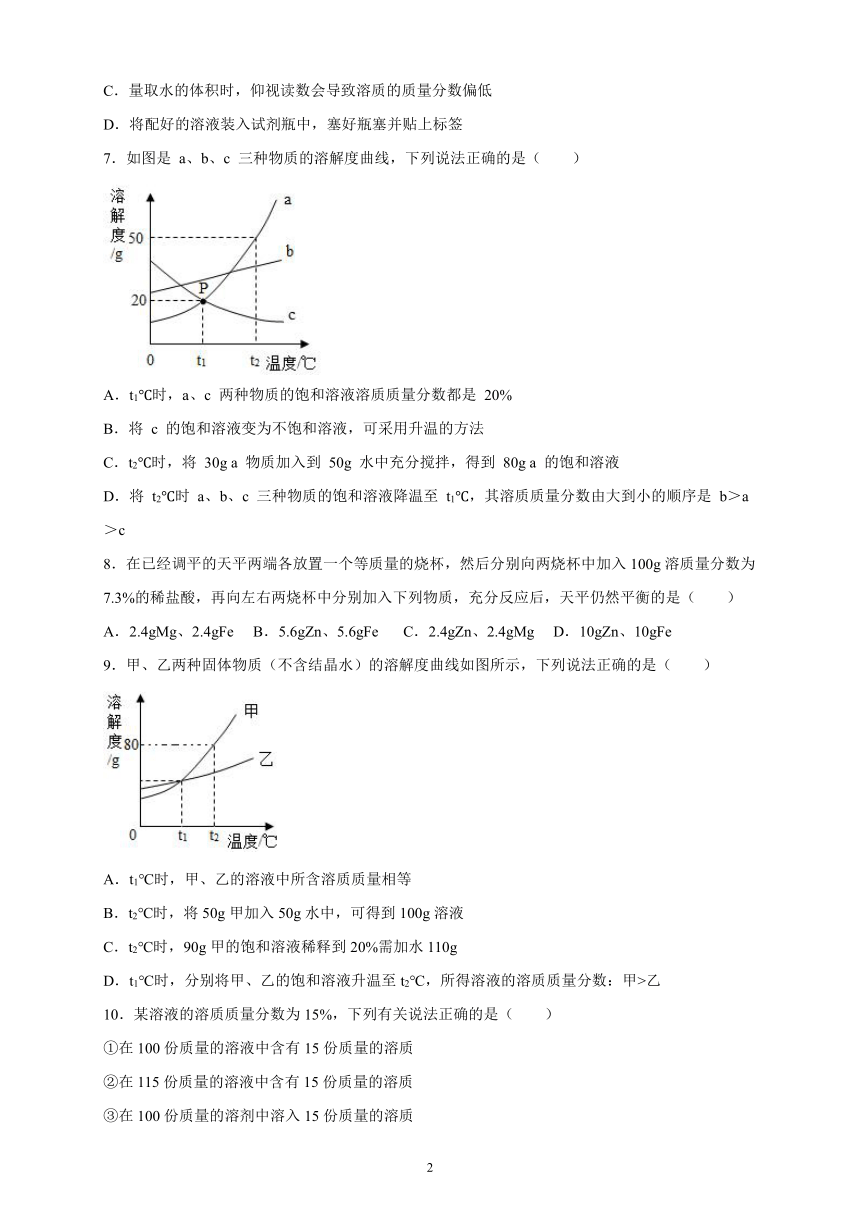
7.如图是 a、b、c 三种物质的溶解度曲线,下列说法正确的是( )
A.t1℃时,a、c 两种物质的饱和溶液溶质质量分数都是 20%
B.将 c 的饱和溶液变为不饱和溶液,可采用升温的方法
C.t2℃时,将 30g a 物质加入到 50g 水中充分搅拌,得到 80g a 的饱和溶液
D.将 t2℃时 a、b、c 三种物质的饱和溶液降温至 t1℃,其溶质质量分数由大到小的顺序是 b>a>c
8.在已经调平的天平两端各放置一个等质量的烧杯,然后分别向两烧杯中加入100g溶质量分数为7.3%的稀盐酸,再向左右两烧杯中分别加入下列物质,充分反应后,天平仍然平衡的是( )
A.2.4gMg、2.4gFe B.5.6gZn、5.6gFe C.2.4gZn、2.4gMg D.10gZn、10gFe
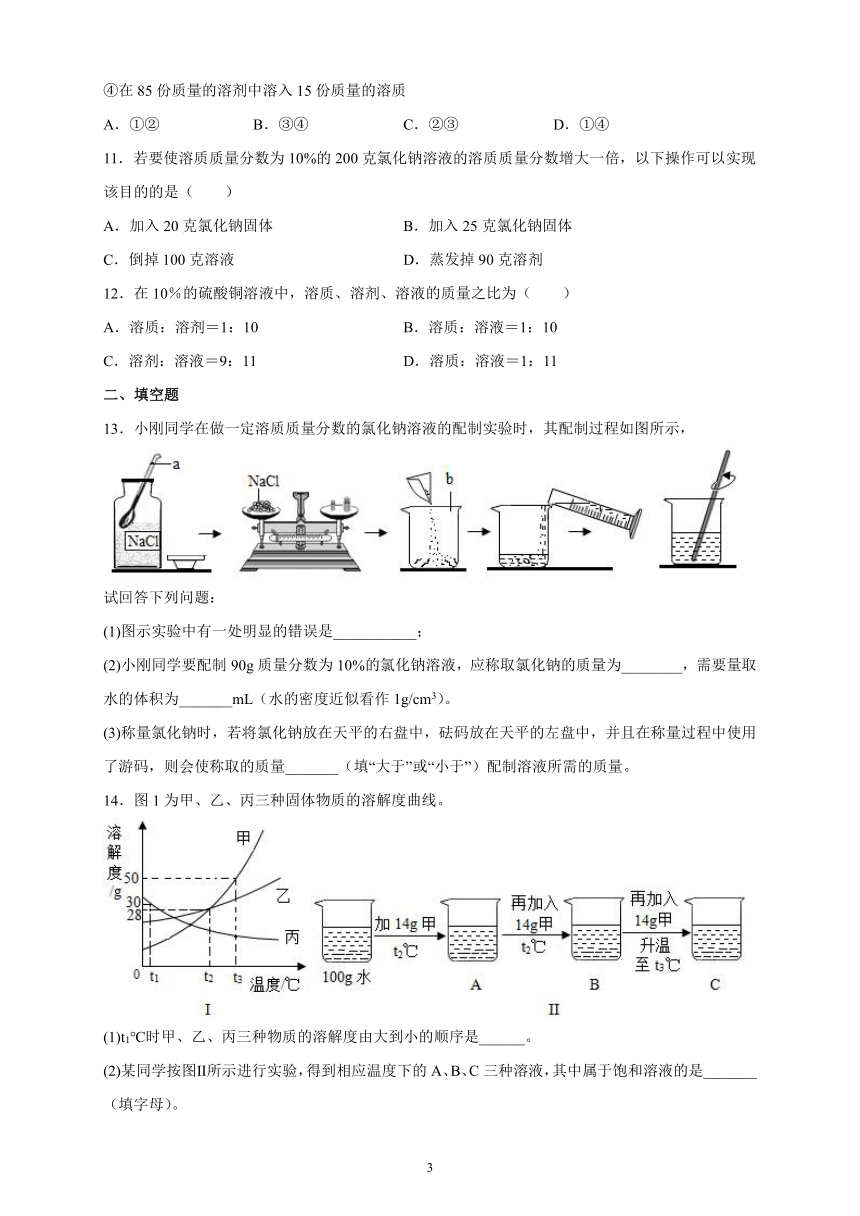
9.甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )
A.t1℃时,甲、乙的溶液中所含溶质质量相等
B.t2℃时,将50g甲加入50g水中,可得到100g溶液
C.t2℃时,90g甲的饱和溶液稀释到20%需加水110g
D.t1℃时,分别将甲、乙的饱和溶液升温至t2℃,所得溶液的溶质质量分数:甲>乙
10.某溶液的溶质质量分数为15%,下列有关说法正确的是( )
①在100份质量的溶液中含有15份质量的溶质
②在115份质量的溶液中含有15份质量的溶质
③在100份质量的溶剂中溶入15份质量的溶质
④在85份质量的溶剂中溶入15份质量的溶质
A.①② B.③④ C.②③ D.①④
11.若要使溶质质量分数为10%的200克氯化钠溶液的溶质质量分数增大一倍,以下操作可以实现该目的的是( )
A.加入20克氯化钠固体 B.加入25克氯化钠固体
C.倒掉100克溶液 D.蒸发掉90克溶剂
12.在10%的硫酸铜溶液中,溶质、溶剂、溶液的质量之比为( )
A.溶质:溶剂=1:10 B.溶质:溶液=1:10
C.溶剂:溶液=9:11 D.溶质:溶液=1:11
二、填空题
13.小刚同学在做一定溶质质量分数的氯化钠溶液的配制实验时,其配制过程如图所示,
试回答下列问题:
(1)图示实验中有一处明显的错误是___________;
(2)小刚同学要配制90g质量分数为10%的氯化钠溶液,应称取氯化钠的质量为________,需要量取水的体积为_______mL(水的密度近似看作1g/cm3)。
(3)称量氯化钠时,若将氯化钠放在天平的右盘中,砝码放在天平的左盘中,并且在称量过程中使用了游码,则会使称取的质量_______(填“大于”或“小于”)配制溶液所需的质量。
14.图1为甲、乙、丙三种固体物质的溶解度曲线。
(1)t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是______。
(2)某同学按图Ⅱ所示进行实验,得到相应温度下的A、B、C三种溶液,其中属于饱和溶液的是_______(填字母)。
(3)t3℃时向盛有40g甲物质的烧杯中加入50g水充分溶解后,所得溶液溶质的质量分数为______(结果精确到0.1%)。
(4)现将t2℃时甲、乙、丙三物质的饱和溶液降温到t1℃,所得溶液溶质质量分数大小关系为________。
(5)保持t2℃不变,要使接近饱和的甲溶液变为饱和溶液,你采取的方法是________。
(6)若甲物质中混有少量乙物质,最好采用________的方法提纯甲。
(7)将t3℃时甲的饱和溶液60g稀释成质量分数为10.0%的甲溶液,需加水________g。
三、实验题
15.某同学配制50g溶质质量分数为8%的氯化钠溶液,整个操作过程如下图所示,回答下列问题:
(1)配制溶液的正确操作顺序为______(填序号,下同)
(2)量水时选用量筒的量程最合适的是______(填序号)。
A.10mL B.20mL C.50mL D.100mL
(3)经检测,该同学配制的溶液溶质质量分数偏大,可能的原因是______(填序号)。
A.氯化钠固体不纯 B.用生锈砝码称量
C.量水时俯视读数 D.装瓶时溅出少量溶液
(4)取10g配制好的质量分数为8%的氯化钠溶液,稀释成质量分数为4%的氯化钠溶,需加水______g。
四、判断题
16.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液。( )
17.某实验小组用质量分数为6%的氯化钠溶液(密度约为1.04g/cm3)和水(密度约为1g/cm3)配制50g质量分数为3%的氯化钠溶液,计算需要6%的氯化钠溶液的质量是25g(约24.0mL),水的质量是25g( )
18.实验室需要配制10%的氯化钠溶液,氯化钠固体可以直接放在托盘上称量( )
19.实验室用溶质质量分数为6%的NaCl溶液配制溶质质量分数为2%的NaCl溶液,已配好的溶液转移到试剂瓶时有滴洒,溶质质量分数仍为2%( )
20.用氯化钠固体与蒸馏水配制一定溶质质量分数的氯化钠溶液时,将配制好的溶液倒入试剂瓶时有少量溶液溅出,对溶质的质量分数没有影响( )
试卷第1页,共3页
参考答案:
1.A
2.B
3.B
4.B
5.B
6.B
7.B
8.D
9.C
10.D
11.B
12.B
13.(1)试剂瓶塞正放在桌面上
(2) 9
81
(3)小于
14.(1)丙>乙>甲(或丙、乙、甲)
(2)B
(3)33.3%
(4)乙>丙>甲
(5)加溶质甲或恒温蒸发水分
(6)降温结晶(或冷却结晶)
(7)140
15.(1)②①⑤③④
(2)C
(3)BC
(4)10g
16.错误
17.正确
18.错误
19.正确
20.正确
答案第1页,共2页
一、单选题
1.实验室配制质量分数为6%的NaCl溶液,除托盘天平、烧杯、玻璃棒、量筒、药匙外,还需要的仪器是( )
A.胶头滴管 B.铁架台 C.酒精灯 D.蒸发皿
2.实验室配制50g溶质质量分数为15%的氯化钠溶液。下列说法中错误的是( )
A.实验的步骤为计算、称量、量取、溶解、装瓶
B.若称量时托盘天平指针偏左,移动游码至天平平衡
C.把配制好的氯化钠溶液倒入干燥的试剂瓶中,并贴上标签
D.量取水时,若仰视读数,则配制的溶液中溶质的质量分数小于15%
3.从冰箱中取出一杯底部有少量蔗糖固体的糖水甲,待其恢复至室温,发现底部固体完全溶解,得到液体乙。甲和乙的比较中说法正确的是( )
A.乙溶液一定能再溶解蔗糖 B.乙中蔗糖的溶解度较大
C.乙中溶质的质量分数较小 D.甲中溶质的质量较大
4.如图,海水淡化可采用膜分离技术,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是( )
A.溶质质量增加 B.溶剂质量减小
C.溶液质量不变 D.溶质质量分数减小
5.实验室配制150 g质量分数为16%的氯化钠溶液时,下列操作会导致质量分数偏大的是( )
①称量时将氯化钠固体放在托盘天平右盘上称量;②用量筒量取水时俯视读数;
③将量筒中的水倒入烧杯中时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。
A.③④ B.②③ C.①④ D.①③④
6.欲配制 100g 质量分数为 10%的氢氧化钠溶液。下列说法中不正确的是( )
A.要用托盘天平称取 10.0g 氢氧化钠固体
B.实验中用到的玻璃仪器只有烧杯和量筒
C.量取水的体积时,仰视读数会导致溶质的质量分数偏低
D.将配好的溶液装入试剂瓶中,塞好瓶塞并贴上标签
7.如图是 a、b、c 三种物质的溶解度曲线,下列说法正确的是( )
A.t1℃时,a、c 两种物质的饱和溶液溶质质量分数都是 20%
B.将 c 的饱和溶液变为不饱和溶液,可采用升温的方法
C.t2℃时,将 30g a 物质加入到 50g 水中充分搅拌,得到 80g a 的饱和溶液
D.将 t2℃时 a、b、c 三种物质的饱和溶液降温至 t1℃,其溶质质量分数由大到小的顺序是 b>a>c
8.在已经调平的天平两端各放置一个等质量的烧杯,然后分别向两烧杯中加入100g溶质量分数为7.3%的稀盐酸,再向左右两烧杯中分别加入下列物质,充分反应后,天平仍然平衡的是( )
A.2.4gMg、2.4gFe B.5.6gZn、5.6gFe C.2.4gZn、2.4gMg D.10gZn、10gFe
9.甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )
A.t1℃时,甲、乙的溶液中所含溶质质量相等
B.t2℃时,将50g甲加入50g水中,可得到100g溶液
C.t2℃时,90g甲的饱和溶液稀释到20%需加水110g
D.t1℃时,分别将甲、乙的饱和溶液升温至t2℃,所得溶液的溶质质量分数:甲>乙
10.某溶液的溶质质量分数为15%,下列有关说法正确的是( )
①在100份质量的溶液中含有15份质量的溶质
②在115份质量的溶液中含有15份质量的溶质
③在100份质量的溶剂中溶入15份质量的溶质
④在85份质量的溶剂中溶入15份质量的溶质
A.①② B.③④ C.②③ D.①④
11.若要使溶质质量分数为10%的200克氯化钠溶液的溶质质量分数增大一倍,以下操作可以实现该目的的是( )
A.加入20克氯化钠固体 B.加入25克氯化钠固体
C.倒掉100克溶液 D.蒸发掉90克溶剂
12.在10%的硫酸铜溶液中,溶质、溶剂、溶液的质量之比为( )
A.溶质:溶剂=1:10 B.溶质:溶液=1:10
C.溶剂:溶液=9:11 D.溶质:溶液=1:11
二、填空题
13.小刚同学在做一定溶质质量分数的氯化钠溶液的配制实验时,其配制过程如图所示,
试回答下列问题:
(1)图示实验中有一处明显的错误是___________;
(2)小刚同学要配制90g质量分数为10%的氯化钠溶液,应称取氯化钠的质量为________,需要量取水的体积为_______mL(水的密度近似看作1g/cm3)。
(3)称量氯化钠时,若将氯化钠放在天平的右盘中,砝码放在天平的左盘中,并且在称量过程中使用了游码,则会使称取的质量_______(填“大于”或“小于”)配制溶液所需的质量。
14.图1为甲、乙、丙三种固体物质的溶解度曲线。
(1)t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是______。
(2)某同学按图Ⅱ所示进行实验,得到相应温度下的A、B、C三种溶液,其中属于饱和溶液的是_______(填字母)。
(3)t3℃时向盛有40g甲物质的烧杯中加入50g水充分溶解后,所得溶液溶质的质量分数为______(结果精确到0.1%)。
(4)现将t2℃时甲、乙、丙三物质的饱和溶液降温到t1℃,所得溶液溶质质量分数大小关系为________。
(5)保持t2℃不变,要使接近饱和的甲溶液变为饱和溶液,你采取的方法是________。
(6)若甲物质中混有少量乙物质,最好采用________的方法提纯甲。
(7)将t3℃时甲的饱和溶液60g稀释成质量分数为10.0%的甲溶液,需加水________g。
三、实验题
15.某同学配制50g溶质质量分数为8%的氯化钠溶液,整个操作过程如下图所示,回答下列问题:
(1)配制溶液的正确操作顺序为______(填序号,下同)
(2)量水时选用量筒的量程最合适的是______(填序号)。
A.10mL B.20mL C.50mL D.100mL
(3)经检测,该同学配制的溶液溶质质量分数偏大,可能的原因是______(填序号)。
A.氯化钠固体不纯 B.用生锈砝码称量
C.量水时俯视读数 D.装瓶时溅出少量溶液
(4)取10g配制好的质量分数为8%的氯化钠溶液,稀释成质量分数为4%的氯化钠溶,需加水______g。
四、判断题
16.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液。( )
17.某实验小组用质量分数为6%的氯化钠溶液(密度约为1.04g/cm3)和水(密度约为1g/cm3)配制50g质量分数为3%的氯化钠溶液,计算需要6%的氯化钠溶液的质量是25g(约24.0mL),水的质量是25g( )
18.实验室需要配制10%的氯化钠溶液,氯化钠固体可以直接放在托盘上称量( )
19.实验室用溶质质量分数为6%的NaCl溶液配制溶质质量分数为2%的NaCl溶液,已配好的溶液转移到试剂瓶时有滴洒,溶质质量分数仍为2%( )
20.用氯化钠固体与蒸馏水配制一定溶质质量分数的氯化钠溶液时,将配制好的溶液倒入试剂瓶时有少量溶液溅出,对溶质的质量分数没有影响( )
试卷第1页,共3页
参考答案:
1.A
2.B
3.B
4.B
5.B
6.B
7.B
8.D
9.C
10.D
11.B
12.B
13.(1)试剂瓶塞正放在桌面上
(2) 9
81
(3)小于
14.(1)丙>乙>甲(或丙、乙、甲)
(2)B
(3)33.3%
(4)乙>丙>甲
(5)加溶质甲或恒温蒸发水分
(6)降温结晶(或冷却结晶)
(7)140
15.(1)②①⑤③④
(2)C
(3)BC
(4)10g
16.错误
17.正确
18.错误
19.正确
20.正确
答案第1页,共2页
同课章节目录
