《质量守恒定律》说课
图片预览







文档简介
课件22张PPT。质量守恒定律 质量守恒定律是初中化学的一个重要化学规律,是分析物质在化学反应中的质量关系的理论依据,它的应用贯穿于整个中学化学。本节教材在初中化学里有着承上启下的作用。本节课的教学将引领学生对化学反应的认识开始了从“质”到“量”的过渡,也为之后化学方程式的书写和计算的教学构建了理论铺垫,所以本课内容不仅是本单元的一个重点,也是整个中学化学的教学重点之一。一、说教材1.教材分析(1)知识与技能: 使学生理解质量守恒定律以及守恒的原因,学会运用质量守恒定律解释和解决一些化学现象和问题。(2)过程与方法: 通过实验及分析,培养学生利用实验发现问题、探究问题的能力和逻辑推理能力。(3)情感、态度、价值观:通过探究学习,培养学生善于合作、勇于探索、严谨求实的科学态度。2.教学目标教学重点:理解质量守恒定律的涵义 及应用教学难点:引导学生通过实验探究得出结论 , 使学生理解质量守恒的原因,从而达到从定量角度理解化学反应。3.重点、难点 中国教育家陶行知说过:“ 好的先生不是教书,不是教学生,而是教学生学。”在学习本节课内容之前, 学生的化学知识和对于化学探究学习方法的了解都属于启蒙阶段, 若探究过程不符合学生现有的认知水平和心理特点, 过于放开或加大难度,不仅不能收到理想的探究效果, 而且会挫伤学生参与探究性学习的积极性。因此本节课我采用的是教师引导下的学生自主探究法和讨论法。二、说教法1.学情分析
(1)学生的知识状况:已掌握了元素符号、化学式及一些简单的化学反应。
(2)学生的能力状况:初步掌握了简单的化学实验基本操作技能。
(3)学生的心理状况:学生刚开始化学学习,情绪和心理都处于比较兴奋、好奇状态。2.学法指导
(1)实验探究法:学会在科学探究中如何发现问题、分析问题、解决问题、获得知识、培养能力。
(2)合作学习法:通过合作探究,培养学生合作互助的团体意识。三、说学法创设情境
引发问题实验探究
研发问题动画模拟
突破难点联系实际
学以致用课堂小结
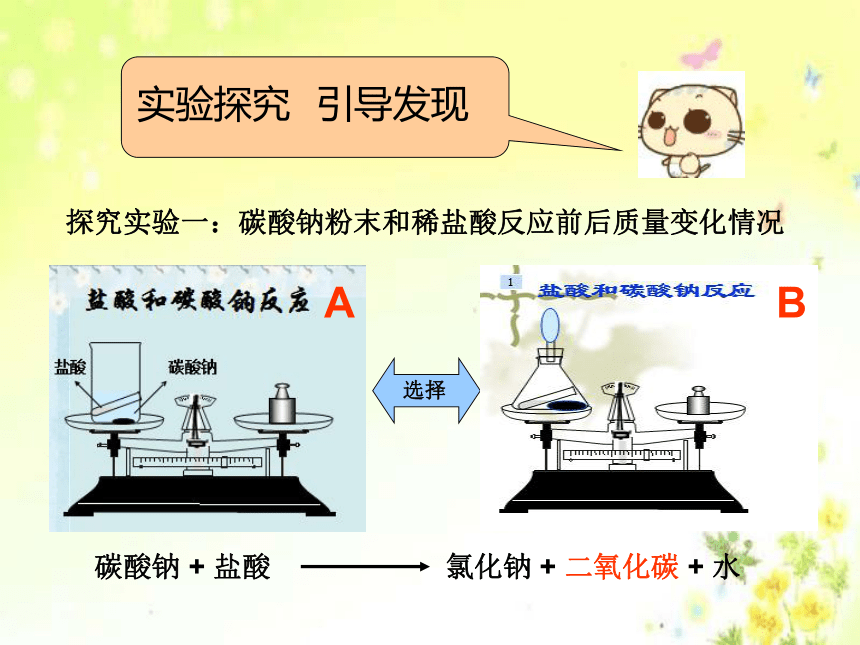
巩固知识四、说教学过程创设情境 引发问题 在化学反应前后各物质的质量总和是否发生改变?如果改变,可能会有怎样的变化呢?实验探究 引导发现探究实验一:碳酸钠粉末和稀盐酸反应前后质量变化情况碳酸钠 + 盐酸 氯化钠 + 二氧化碳 + 水AB
第一种方案有缺陷,因为没有考虑反应生成了气体,逸散到了空气中,所以得出生成物质量变小的结论是不准确的;
第二种方案在密闭条件下进行,整个操作过程中容器内外没有物质的交换,实验过程严密科学,结论令人信服。设计意图:通过引发学生的思维冲突,激起学生强烈的探究欲望,既可强化其设计兴趣,又调动了学生主动思维。经讨论得出:探究实验二:红磷在空气中燃烧前后质量变化情况 (1)反应前称量锥形瓶及瓶内的总质量
(2)点燃红磷,观察实验现象
(3)反应后称量锥形瓶及瓶内的总质量现象:剧烈燃烧,放热,产生大量白烟 ( 气球先膨胀后缩小)
红磷+氧气 → 五氧化二磷总质量总质量=点燃P + O2P2O5点 燃探究实验三:铁钉和硫酸铜溶液反应前后质量变化情况1.反应前称量铁钉、烧杯和硫酸铜的总质量
2.放入铁钉后再称量
3.观察天平是否平衡铁+硫酸铜→铜+硫酸亚铁探究实验二、三共同的结果是------反应前后的质量不变。这是为什么呢? 质量守恒定律 参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。这个规律叫做质量守恒定律。适用范围:化学变化。联系实际 学以致用
②高锰酸钾在空气中加热后,固体质量减少了,有人说这个事实不符合质量守恒定律,你说对吗?为什么?
③已知12 g木炭与32 g氧气恰好完全反应,则生成二氧化碳的质量是_______g;若12g碳在38 g的氧气中充分燃烧,生成二氧化碳______g,剩余______:______g,为什么?①10 g白糖放入200 g水中,形成质量等于210 g的糖 水,这是否符合质量守恒定律?为什么?化学反应反应物和生成物的质量总和参加 资料链接:质量守恒定律的发现波义耳的实验(1673年)拉瓦锡的实验(1777年)失败成功敞口密闭动画模拟 突破难点 为什么物质在发生化学变化前后,质量总和相等呢?分 子原 子新分子新物质原子种类
原子数目
原子质量不变原子数目原子质量原子种类元素种类物质的种类分子的种类可能
改变分子数目化学反应前后课堂小结.
巩固练习:教材98页习题3、4 一、内容:
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。课题一 质量守恒定律 板书设计原子种类
原子数目
原子质量不变二、实质:谢谢指导
(1)学生的知识状况:已掌握了元素符号、化学式及一些简单的化学反应。
(2)学生的能力状况:初步掌握了简单的化学实验基本操作技能。
(3)学生的心理状况:学生刚开始化学学习,情绪和心理都处于比较兴奋、好奇状态。2.学法指导
(1)实验探究法:学会在科学探究中如何发现问题、分析问题、解决问题、获得知识、培养能力。
(2)合作学习法:通过合作探究,培养学生合作互助的团体意识。三、说学法创设情境
引发问题实验探究
研发问题动画模拟
突破难点联系实际
学以致用课堂小结
巩固知识四、说教学过程创设情境 引发问题 在化学反应前后各物质的质量总和是否发生改变?如果改变,可能会有怎样的变化呢?实验探究 引导发现探究实验一:碳酸钠粉末和稀盐酸反应前后质量变化情况碳酸钠 + 盐酸 氯化钠 + 二氧化碳 + 水AB
第一种方案有缺陷,因为没有考虑反应生成了气体,逸散到了空气中,所以得出生成物质量变小的结论是不准确的;
第二种方案在密闭条件下进行,整个操作过程中容器内外没有物质的交换,实验过程严密科学,结论令人信服。设计意图:通过引发学生的思维冲突,激起学生强烈的探究欲望,既可强化其设计兴趣,又调动了学生主动思维。经讨论得出:探究实验二:红磷在空气中燃烧前后质量变化情况 (1)反应前称量锥形瓶及瓶内的总质量
(2)点燃红磷,观察实验现象
(3)反应后称量锥形瓶及瓶内的总质量现象:剧烈燃烧,放热,产生大量白烟 ( 气球先膨胀后缩小)
红磷+氧气 → 五氧化二磷总质量总质量=点燃P + O2P2O5点 燃探究实验三:铁钉和硫酸铜溶液反应前后质量变化情况1.反应前称量铁钉、烧杯和硫酸铜的总质量
2.放入铁钉后再称量
3.观察天平是否平衡铁+硫酸铜→铜+硫酸亚铁探究实验二、三共同的结果是------反应前后的质量不变。这是为什么呢? 质量守恒定律 参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。这个规律叫做质量守恒定律。适用范围:化学变化。联系实际 学以致用
②高锰酸钾在空气中加热后,固体质量减少了,有人说这个事实不符合质量守恒定律,你说对吗?为什么?
③已知12 g木炭与32 g氧气恰好完全反应,则生成二氧化碳的质量是_______g;若12g碳在38 g的氧气中充分燃烧,生成二氧化碳______g,剩余______:______g,为什么?①10 g白糖放入200 g水中,形成质量等于210 g的糖 水,这是否符合质量守恒定律?为什么?化学反应反应物和生成物的质量总和参加 资料链接:质量守恒定律的发现波义耳的实验(1673年)拉瓦锡的实验(1777年)失败成功敞口密闭动画模拟 突破难点 为什么物质在发生化学变化前后,质量总和相等呢?分 子原 子新分子新物质原子种类
原子数目
原子质量不变原子数目原子质量原子种类元素种类物质的种类分子的种类可能
改变分子数目化学反应前后课堂小结.
巩固练习:教材98页习题3、4 一、内容:
参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。课题一 质量守恒定律 板书设计原子种类
原子数目
原子质量不变二、实质:谢谢指导
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
