第十一单元 盐 化肥A卷-2021-2022学年九年级化学人教版下册(word版有答案)
文档属性
| 名称 | 第十一单元 盐 化肥A卷-2021-2022学年九年级化学人教版下册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 177.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-12 00:00:00 | ||
图片预览


文档简介
第十一单元 盐 化肥
A卷
(满分100分,考试时间45分钟)
可能用到的相对原子质量:H——1 O——16 Mg——24 Al——27 S——32 K——39
一、选择题(每小题2分,共30分,每小题只有一个选项符合题意)
1.下列物质中,属于盐的是( )
A.MnO2 B.HNO3 C.Mg(OH)2 D.K2SO4
2.下列关于常见盐的用途,错误的是( )
A.氯化钠用来消除积雪 B.纯碱用作干燥剂
C.碳酸钙用作补钙剂 D.碳酸氢钠用作糕点膨松剂
3.下列有关物质的俗称(或主要成分)、化学式完全对应的一组是( )
A.大理石一CaCO3 B.食盐一NaNO2
C.苏打一NaHCO3 D.纯碱一NaHCO3
4.同学们春季外出郊游时,发现麦田里的麦苗叶子发黄,你认为应该向麦田中施用的化肥是( )
A.K2CO3 B.NH4NO3 C.KCl D.Ca3(PO4)2
5.分类法是初中化学学习的一种重要方法。下列各组物质分类正确的是( )
A.氧化物:H2O2、ZnSO4、CO
B.碱:Cu(OH)2、Ba(OH)2、C2H5OH
C.酸:H2CO3、H2SO4、CH3COOH
D.盐:NH3·H2O、Ca3(PO4)2、AlCl3
6.下列属于复分解反应的是( )
A.2H2O2H2↑+O2↑ B.CO+CuOCu+CO2
C.Cu +2AgNO3===Cu(NO3)2+2Ag D.BaCl2+CuSO4===BaSO4↓+CuCl2
7.下列有关化肥或农药的叙述错误的是( )
A.硫酸铵属于氮肥,长期施用会使土壤酸化、板结
B.硝酸钾属于复合肥
C.农药有毒,应禁止施用
D.农药施用后,会通过农作物、农产品等发生转移
8.下列物质中能与ZnCl2溶液发生复分解反应的是( )
A.Al B.Mg(OH)2 C.稀盐酸 D.AgNO3溶液
9.尿素、磷矿粉、氯化铵三种化肥,按下列方法能将它们区别开来的是( )
A.看颜色,与碱混合 B.比较溶解性,闻气味
C.看状态,比较溶解性 D.闻气味,与碱混合
10.下列各项中物质不能实现如图所示的转化关系的是( )
A.盐一Na2SO4 B.碱一Cu(OH)2
C.金属氧化物一CuO D.酸一H2SO4
11.学会推理和归纳是学习化学的重要思维方法。下列推理或归纳正确的是( )
A.向氯化铵溶液中滴加紫色石蕊溶液,溶液变成红色,说明氯化铵属于酸
B.碳酸钾、碳酸钙都能与盐酸反应生成CO2,那么碳酸钡也可与盐酸反应生成CO2
C.NaCl、Na2SO4、KNO3的水溶液都呈中性,所以盐的水溶液都呈中性
D.复分解反应中有沉淀、气体或水生成,则有上述物质生成的反应就是复分解反应
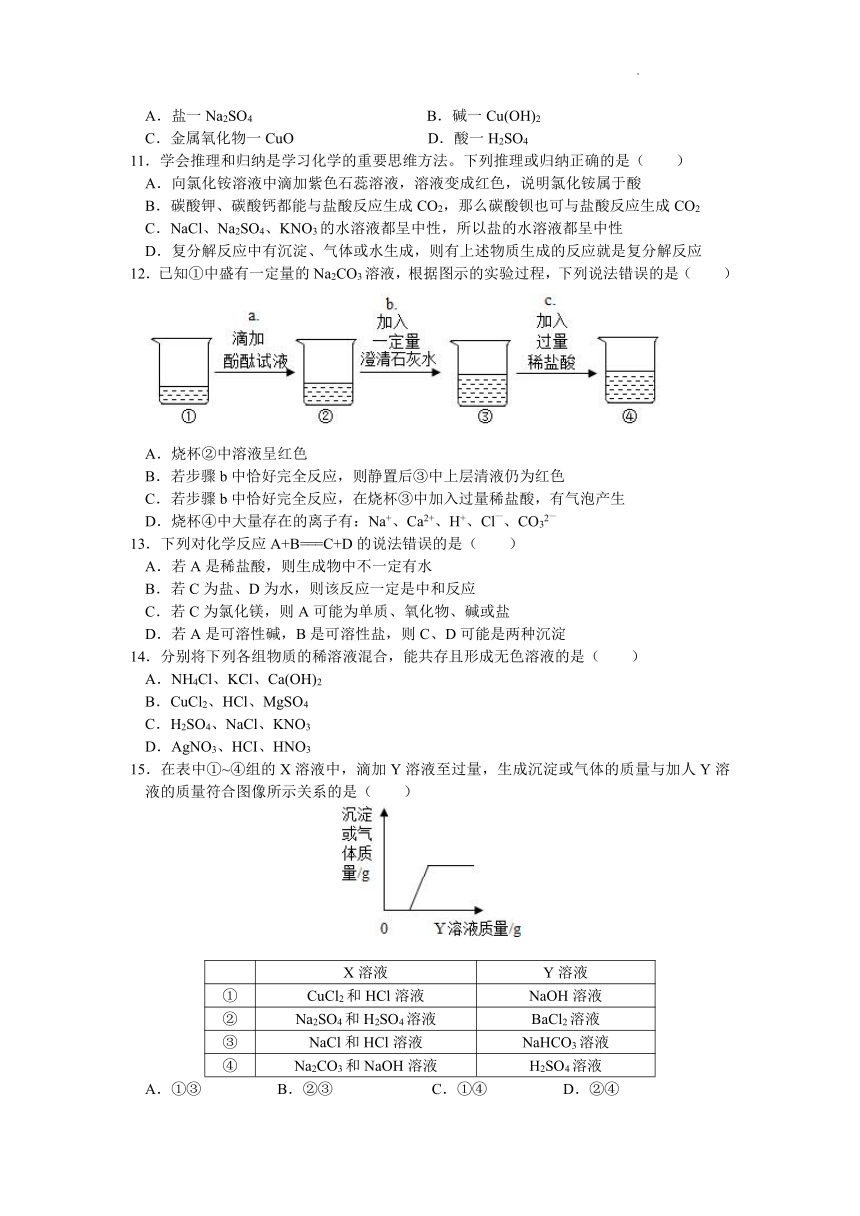
12.已知①中盛有一定量的Na2CO3溶液,根据图示的实验过程,下列说法错误的是( )
A.烧杯②中溶液呈红色
B.若步骤b中恰好完全反应,则静置后③中上层清液仍为红色
C.若步骤b中恰好完全反应,在烧杯③中加入过量稀盐酸,有气泡产生
D.烧杯④中大量存在的离子有:Na+、Ca2+、H+、Cl—、CO32—
13.下列对化学反应A+B===C+D的说法错误的是( )
A.若A是稀盐酸,则生成物中不一定有水
B.若C为盐、D为水,则该反应一定是中和反应
C.若C为氯化镁,则A可能为单质、氧化物、碱或盐
D.若A是可溶性碱,B是可溶性盐,则C、D可能是两种沉淀
14.分别将下列各组物质的稀溶液混合,能共存且形成无色溶液的是( )
A.NH4Cl、KCl、Ca(OH)2
B.CuCl2、HCl、MgSO4
C.H2SO4、NaCl、KNO3
D.AgNO3、HCI、HNO3
15.在表中①~④组的X溶液中,滴加Y溶液至过量,生成沉淀或气体的质量与加人Y溶液的质量符合图像所示关系的是( )
X溶液 Y溶液
① CuCl2和HCl溶液 NaOH溶液
② Na2SO4和H2SO4溶液 BaCl2溶液
③ NaCl和HCl溶液 NaHCO3溶液
④ Na2CO3和NaOH溶液 H2SO4溶液
A.①③ B.②③ C.①④ D.②④
二、填空及简答题(每空2分,共38分)
16.(6分)下图是某化肥标签上的部分内容:
⑴一袋该化肥中至少含氮元素 kg。
⑵根据标签上的“注意事项”推测,碳酸氢铵可能具有的性质是 (答一点即可)。
⑶铵态氮肥不能与碱性物质混合施用的原因是 。
17.(8分)厨房里有两瓶白色固体,分别是食盐和纯碱。
⑴可用来腌制肉类和蔬菜,使食物不易腐败的是 (填化学式)。
⑵为鉴别这两种物质,小华同学取少量固体,进行如下实验。
方案一:分别滴加少量食醋,有气泡产生的是 (填化学式)。
方案二:加水溶解,滴加氯化钙溶液,有 产生的是纯碱,写出发生反应的
化学方程式 。
18.(8分)某化学研究小组为了验证复分解反应发生的条件,选用了下列部分药品进行实验。
①氢氧化钠溶液 ②硫酸铜溶液 ③稀盐酸 ④硝酸钾溶液
⑴为了验证有水生成的复分解反应能发生,某同学选择了①和③。你认为除上述药品外,还需要的一种试剂是 。
⑵选择 (填序号)两种物质进行实验,验证有沉淀生成的复分解反应能发生,其反应的化学方程式为 。
⑶下列反应中,验证有气体生成的复分解反应能发生的是 (填序号)。
A.锌与稀硫酸反应 B.天然气燃烧
C.碳酸钠与稀盐酸反应 D.过氧化氢分解
19.(8分)组成相似的盐具有一些相似的化学性质。
⑴①向Cu(NO3)2溶液中加人Ca(OH)2溶液,充分振荡。发生反应的化学方程式为
。
②向CuSO4溶液中加入过量的铁粉,充分反应前后溶液中存在的主要离子如图,写
出代表的离子: (填离子符号)。
⑵在溶液中能与CuSO4反应而不与Cu(NO3)2反应的物质有 (举一例,填化学式)。
⑶向硫酸铜溶液中加人某纯净物的溶液,能同时将铜离子和硫酸根离子转变成沉淀,该纯净物的化学式为 。
20.(8分)已知A、B、C、D、E是初中化学常见的物质。A是胃酸的主要成分,D是一种钠盐,广泛用于玻璃、造纸、纺织和洗涤剂的生产,C、E为氧化物,C是参与光合作用的气体。它们之间的关系如图所示(“一”表示两种物质能发生化学反应,“→”表示两种物质间的转化关系,部分反应物、生成物及反应条件已略去)。
请回答:
⑴A的化学式为 ;C的化学式为 。
⑵A与D反应的化学方程式为 。
⑶B→D反应的化学方程式为 。
三、实验与探究题(每空2分,共26分)
21.(12分)某化学兴趣小组的同学进行5g粗盐(含难溶性杂质约20%)的提纯实验,并计算产率。如图是他们实验的部分操作示意图(在实验条件下NaCl的溶解度为36g,水的密度为1g/mL)。请回答下列问题。
⑴写出仪器a的名称 。
⑵图中所示操作中错误的有 处,操作③中玻璃棒的作用是 。
⑶上述粗盐提纯实验的步骤为 (填序号)、称量精盐并计算产率。
⑷操作③中,当观察到 时,停止加热。
⑸某同学所得产率与其他同学比较明显偏低,下列情况不会导致产率明显偏低的是
(填序号)。
A.溶解时将5g粗盐一次全部倒入10g水中,立即过滤
B.操作②中,用10mL的水溶解
C.提纯后的精盐尚未完全干燥就称其质量
D.蒸发时,有一些液体、固体溅出
22.(14分)糕点膨松剂的主要成分之一是碳酸氢钠,某化学兴趣小组对碳酸氢钠的化学性质进行了探究。
实验一:探究碳酸氢钠溶液的酸碱性,用pH试纸测得碳酸氢钠溶液的pH约为10,由此可知碳酸氢钠溶液呈 性。
实验二:探究碳酸氢钠溶液能否与酸反应,取少量固体放入试管中,滴加足量的稀盐酸,现象为 。
结论:碳酸氢钠能与酸反应。
实验三:探究碳酸氢钠的热稳定性,取一定量的碳酸氢钠放在铜片上加热,如图所示。
⑴加热一段时间后,观察到烧杯内壁有水珠。
⑵充分加热后,将烧杯迅速倒转过来,加入适量的澄清石灰水,振荡,观察到石灰水变浑
浊。写出石灰水变浑浊的化学方程式 。
⑶通过进一步实验探究来确定充分加热后的固体产物的成分。
【提出假设】①可能是Na2CO3;②可能是NaOH。
【设计实验】
方案一:取少量充分加热后的固体于试管中,加入适量水充分溶解,再向试管中加人适量的氢氧化钙溶液,观察到有白色沉淀产生,则假设①成立,请写出发生反应的化学方程式
。
方案二:请选用与方案一中不同类别的试剂再设计一个方案。
实验操作 实验现象 结论
假设①成立, 假设②不成立
【实验结论】请写出NaHCO3受热分解的化学方程式 。
四、计算题(共6分)
23.(6分)为测定某纯碱样品(主要成分是碳酸钠,含氯化钠杂质)中碳酸钠的含量,进
行如下实验:取72g纯碱样品平均分为6份,分别加入相同质量分数的氯化钙溶液。获得如表实验数据:
实验序号 1 2 3 4 5 6
样品的质量/g 12 12 12 12 12 12
加入氯化钙溶液质量/g 20 40 60 80 100 120
产生沉淀的质量/g 2.0 4.0 6.0 8.0 10.0 10.0
⑴12g样品完全反应时产生的沉淀的质量是 g。
⑵纯碱样品中Na2CO3的质量分数是多少?(写出计算过程,结果保留小数点后一位)
参考答案
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
D B A B C D C D A A B D B C C
⑴8.5 ⑵受热易分解(或易潮解等,合理即可)
⑶两种物质发生化学反应降低肥效
⑴NaCl
⑵Na2CO3 沉淀(或白色沉淀) CaCl2+Na2CO3===CaCO3↓+2NaCl
18.⑴酚酞溶液(或石蕊溶液等)
⑵① ② 2NaOH+CuSO4===Cu(OH)2↓+Na2SO4
⑶C
⑴①Cu(NO3)2+Ca(OH)2===Cu(OH)2↓+Ca(NO3)2
② Fe2+
⑵BaCl2(合理即可)
⑶Ba(OH)2
⑴HCl CO2
⑵2HCl+Na2CO3===2NaCl+H2O+CO2↑
⑶CO2+2NaOH===Na2CO+H2O
⑴蒸发皿
⑵1 搅拌,使液体受热均匀,防止液滴飞溅
⑶①④②⑤③
⑷蒸发皿中有较多固体析出
⑸C
实验一:碱 实验二:固体溶解,产生气泡
实验三:⑵Ca(OH)2+CO2===CaCO3↓+H2O
⑶【设计实验】方案一:Na2CO3+Ca(OH)2===CaCO3↓+2NaOH
方案二:取少量充分加热后的固体于试管中,再向试管中加入适量的稀盐酸
产生气泡
【实验结论】2NaHCO3Na2CO3+H2O+CO2↑
23.⑴10.0 (2分)
⑵解:设每份样品中碳酸钠的质量为x。
CaCl2+Na2CO3===CaCO3↓+2NaCl
106 100
X 10.0g
x=10.6g (2分)
样品中碳酸钠的质量分数为:×100%≈88.3% (2分)
答:纯碱样品中Na2CO3的质量分数约为88.3%。
A卷
(满分100分,考试时间45分钟)
可能用到的相对原子质量:H——1 O——16 Mg——24 Al——27 S——32 K——39
一、选择题(每小题2分,共30分,每小题只有一个选项符合题意)
1.下列物质中,属于盐的是( )
A.MnO2 B.HNO3 C.Mg(OH)2 D.K2SO4
2.下列关于常见盐的用途,错误的是( )
A.氯化钠用来消除积雪 B.纯碱用作干燥剂
C.碳酸钙用作补钙剂 D.碳酸氢钠用作糕点膨松剂
3.下列有关物质的俗称(或主要成分)、化学式完全对应的一组是( )
A.大理石一CaCO3 B.食盐一NaNO2
C.苏打一NaHCO3 D.纯碱一NaHCO3
4.同学们春季外出郊游时,发现麦田里的麦苗叶子发黄,你认为应该向麦田中施用的化肥是( )
A.K2CO3 B.NH4NO3 C.KCl D.Ca3(PO4)2
5.分类法是初中化学学习的一种重要方法。下列各组物质分类正确的是( )
A.氧化物:H2O2、ZnSO4、CO
B.碱:Cu(OH)2、Ba(OH)2、C2H5OH
C.酸:H2CO3、H2SO4、CH3COOH
D.盐:NH3·H2O、Ca3(PO4)2、AlCl3
6.下列属于复分解反应的是( )
A.2H2O2H2↑+O2↑ B.CO+CuOCu+CO2
C.Cu +2AgNO3===Cu(NO3)2+2Ag D.BaCl2+CuSO4===BaSO4↓+CuCl2
7.下列有关化肥或农药的叙述错误的是( )
A.硫酸铵属于氮肥,长期施用会使土壤酸化、板结
B.硝酸钾属于复合肥
C.农药有毒,应禁止施用
D.农药施用后,会通过农作物、农产品等发生转移
8.下列物质中能与ZnCl2溶液发生复分解反应的是( )
A.Al B.Mg(OH)2 C.稀盐酸 D.AgNO3溶液
9.尿素、磷矿粉、氯化铵三种化肥,按下列方法能将它们区别开来的是( )
A.看颜色,与碱混合 B.比较溶解性,闻气味
C.看状态,比较溶解性 D.闻气味,与碱混合
10.下列各项中物质不能实现如图所示的转化关系的是( )
A.盐一Na2SO4 B.碱一Cu(OH)2
C.金属氧化物一CuO D.酸一H2SO4
11.学会推理和归纳是学习化学的重要思维方法。下列推理或归纳正确的是( )
A.向氯化铵溶液中滴加紫色石蕊溶液,溶液变成红色,说明氯化铵属于酸
B.碳酸钾、碳酸钙都能与盐酸反应生成CO2,那么碳酸钡也可与盐酸反应生成CO2
C.NaCl、Na2SO4、KNO3的水溶液都呈中性,所以盐的水溶液都呈中性
D.复分解反应中有沉淀、气体或水生成,则有上述物质生成的反应就是复分解反应
12.已知①中盛有一定量的Na2CO3溶液,根据图示的实验过程,下列说法错误的是( )
A.烧杯②中溶液呈红色
B.若步骤b中恰好完全反应,则静置后③中上层清液仍为红色
C.若步骤b中恰好完全反应,在烧杯③中加入过量稀盐酸,有气泡产生
D.烧杯④中大量存在的离子有:Na+、Ca2+、H+、Cl—、CO32—
13.下列对化学反应A+B===C+D的说法错误的是( )
A.若A是稀盐酸,则生成物中不一定有水
B.若C为盐、D为水,则该反应一定是中和反应
C.若C为氯化镁,则A可能为单质、氧化物、碱或盐
D.若A是可溶性碱,B是可溶性盐,则C、D可能是两种沉淀
14.分别将下列各组物质的稀溶液混合,能共存且形成无色溶液的是( )
A.NH4Cl、KCl、Ca(OH)2
B.CuCl2、HCl、MgSO4
C.H2SO4、NaCl、KNO3
D.AgNO3、HCI、HNO3
15.在表中①~④组的X溶液中,滴加Y溶液至过量,生成沉淀或气体的质量与加人Y溶液的质量符合图像所示关系的是( )
X溶液 Y溶液
① CuCl2和HCl溶液 NaOH溶液
② Na2SO4和H2SO4溶液 BaCl2溶液
③ NaCl和HCl溶液 NaHCO3溶液
④ Na2CO3和NaOH溶液 H2SO4溶液
A.①③ B.②③ C.①④ D.②④
二、填空及简答题(每空2分,共38分)
16.(6分)下图是某化肥标签上的部分内容:
⑴一袋该化肥中至少含氮元素 kg。
⑵根据标签上的“注意事项”推测,碳酸氢铵可能具有的性质是 (答一点即可)。
⑶铵态氮肥不能与碱性物质混合施用的原因是 。
17.(8分)厨房里有两瓶白色固体,分别是食盐和纯碱。
⑴可用来腌制肉类和蔬菜,使食物不易腐败的是 (填化学式)。
⑵为鉴别这两种物质,小华同学取少量固体,进行如下实验。
方案一:分别滴加少量食醋,有气泡产生的是 (填化学式)。
方案二:加水溶解,滴加氯化钙溶液,有 产生的是纯碱,写出发生反应的
化学方程式 。
18.(8分)某化学研究小组为了验证复分解反应发生的条件,选用了下列部分药品进行实验。
①氢氧化钠溶液 ②硫酸铜溶液 ③稀盐酸 ④硝酸钾溶液
⑴为了验证有水生成的复分解反应能发生,某同学选择了①和③。你认为除上述药品外,还需要的一种试剂是 。
⑵选择 (填序号)两种物质进行实验,验证有沉淀生成的复分解反应能发生,其反应的化学方程式为 。
⑶下列反应中,验证有气体生成的复分解反应能发生的是 (填序号)。
A.锌与稀硫酸反应 B.天然气燃烧
C.碳酸钠与稀盐酸反应 D.过氧化氢分解
19.(8分)组成相似的盐具有一些相似的化学性质。
⑴①向Cu(NO3)2溶液中加人Ca(OH)2溶液,充分振荡。发生反应的化学方程式为
。
②向CuSO4溶液中加入过量的铁粉,充分反应前后溶液中存在的主要离子如图,写
出代表的离子: (填离子符号)。
⑵在溶液中能与CuSO4反应而不与Cu(NO3)2反应的物质有 (举一例,填化学式)。
⑶向硫酸铜溶液中加人某纯净物的溶液,能同时将铜离子和硫酸根离子转变成沉淀,该纯净物的化学式为 。
20.(8分)已知A、B、C、D、E是初中化学常见的物质。A是胃酸的主要成分,D是一种钠盐,广泛用于玻璃、造纸、纺织和洗涤剂的生产,C、E为氧化物,C是参与光合作用的气体。它们之间的关系如图所示(“一”表示两种物质能发生化学反应,“→”表示两种物质间的转化关系,部分反应物、生成物及反应条件已略去)。
请回答:
⑴A的化学式为 ;C的化学式为 。
⑵A与D反应的化学方程式为 。
⑶B→D反应的化学方程式为 。
三、实验与探究题(每空2分,共26分)
21.(12分)某化学兴趣小组的同学进行5g粗盐(含难溶性杂质约20%)的提纯实验,并计算产率。如图是他们实验的部分操作示意图(在实验条件下NaCl的溶解度为36g,水的密度为1g/mL)。请回答下列问题。
⑴写出仪器a的名称 。
⑵图中所示操作中错误的有 处,操作③中玻璃棒的作用是 。
⑶上述粗盐提纯实验的步骤为 (填序号)、称量精盐并计算产率。
⑷操作③中,当观察到 时,停止加热。
⑸某同学所得产率与其他同学比较明显偏低,下列情况不会导致产率明显偏低的是
(填序号)。
A.溶解时将5g粗盐一次全部倒入10g水中,立即过滤
B.操作②中,用10mL的水溶解
C.提纯后的精盐尚未完全干燥就称其质量
D.蒸发时,有一些液体、固体溅出
22.(14分)糕点膨松剂的主要成分之一是碳酸氢钠,某化学兴趣小组对碳酸氢钠的化学性质进行了探究。
实验一:探究碳酸氢钠溶液的酸碱性,用pH试纸测得碳酸氢钠溶液的pH约为10,由此可知碳酸氢钠溶液呈 性。
实验二:探究碳酸氢钠溶液能否与酸反应,取少量固体放入试管中,滴加足量的稀盐酸,现象为 。
结论:碳酸氢钠能与酸反应。
实验三:探究碳酸氢钠的热稳定性,取一定量的碳酸氢钠放在铜片上加热,如图所示。
⑴加热一段时间后,观察到烧杯内壁有水珠。
⑵充分加热后,将烧杯迅速倒转过来,加入适量的澄清石灰水,振荡,观察到石灰水变浑
浊。写出石灰水变浑浊的化学方程式 。
⑶通过进一步实验探究来确定充分加热后的固体产物的成分。
【提出假设】①可能是Na2CO3;②可能是NaOH。
【设计实验】
方案一:取少量充分加热后的固体于试管中,加入适量水充分溶解,再向试管中加人适量的氢氧化钙溶液,观察到有白色沉淀产生,则假设①成立,请写出发生反应的化学方程式
。
方案二:请选用与方案一中不同类别的试剂再设计一个方案。
实验操作 实验现象 结论
假设①成立, 假设②不成立
【实验结论】请写出NaHCO3受热分解的化学方程式 。
四、计算题(共6分)
23.(6分)为测定某纯碱样品(主要成分是碳酸钠,含氯化钠杂质)中碳酸钠的含量,进
行如下实验:取72g纯碱样品平均分为6份,分别加入相同质量分数的氯化钙溶液。获得如表实验数据:
实验序号 1 2 3 4 5 6
样品的质量/g 12 12 12 12 12 12
加入氯化钙溶液质量/g 20 40 60 80 100 120
产生沉淀的质量/g 2.0 4.0 6.0 8.0 10.0 10.0
⑴12g样品完全反应时产生的沉淀的质量是 g。
⑵纯碱样品中Na2CO3的质量分数是多少?(写出计算过程,结果保留小数点后一位)
参考答案
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
D B A B C D C D A A B D B C C
⑴8.5 ⑵受热易分解(或易潮解等,合理即可)
⑶两种物质发生化学反应降低肥效
⑴NaCl
⑵Na2CO3 沉淀(或白色沉淀) CaCl2+Na2CO3===CaCO3↓+2NaCl
18.⑴酚酞溶液(或石蕊溶液等)
⑵① ② 2NaOH+CuSO4===Cu(OH)2↓+Na2SO4
⑶C
⑴①Cu(NO3)2+Ca(OH)2===Cu(OH)2↓+Ca(NO3)2
② Fe2+
⑵BaCl2(合理即可)
⑶Ba(OH)2
⑴HCl CO2
⑵2HCl+Na2CO3===2NaCl+H2O+CO2↑
⑶CO2+2NaOH===Na2CO+H2O
⑴蒸发皿
⑵1 搅拌,使液体受热均匀,防止液滴飞溅
⑶①④②⑤③
⑷蒸发皿中有较多固体析出
⑸C
实验一:碱 实验二:固体溶解,产生气泡
实验三:⑵Ca(OH)2+CO2===CaCO3↓+H2O
⑶【设计实验】方案一:Na2CO3+Ca(OH)2===CaCO3↓+2NaOH
方案二:取少量充分加热后的固体于试管中,再向试管中加入适量的稀盐酸
产生气泡
【实验结论】2NaHCO3Na2CO3+H2O+CO2↑
23.⑴10.0 (2分)
⑵解:设每份样品中碳酸钠的质量为x。
CaCl2+Na2CO3===CaCO3↓+2NaCl
106 100
X 10.0g
x=10.6g (2分)
样品中碳酸钠的质量分数为:×100%≈88.3% (2分)
答:纯碱样品中Na2CO3的质量分数约为88.3%。
同课章节目录
