2021-2022学年下学期高一化学人教版(2019)必修第二册第七章第一节 第2课时 烷烃的性质课件(23张ppt))
文档属性
| 名称 | 2021-2022学年下学期高一化学人教版(2019)必修第二册第七章第一节 第2课时 烷烃的性质课件(23张ppt)) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-13 00:00:00 | ||
图片预览








文档简介
(共23张PPT)
第七章 有机化合物
第一节 认识有机化合物
第2课时 烷烃的性质
奶牛
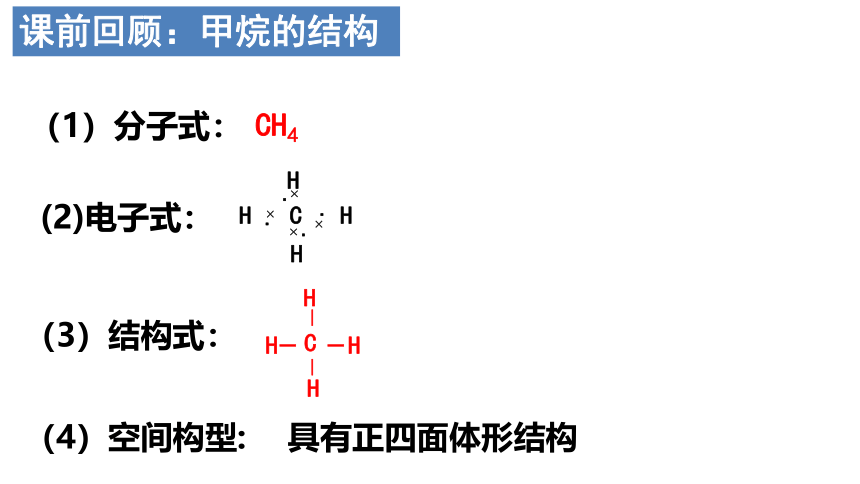
课前回顾:甲烷的结构
(1)分子式:
(2)电子式:
(3)结构式:
(4)空间构型:
H C H
H
H
×
.
×
.
×
.
×
.
│
━ C ━
│
H
H
H
H
具有正四面体形结构
CH4
甲烷的性质
任务1:阅读课本p64-65,总结出甲烷的化学性质
1.稳定性
2.可燃性
3.取代反应(特征反应)
4.分解反应
不与强酸、强碱、酸性KMnO4溶液反应
一般的,大部分有机物均可燃(即与氧气反应)
与纯净卤素气态单质光照下发生反应
学以致用
下列新闻说明了甲烷的什么性质?你能写出化学方程式吗?通过该条新闻你对甲烷的使用有何启示?
2.可燃性
点燃甲烷和空气的混合气体会有什么后果呢?
爆炸
启示:甲烷点燃一定要验纯
3.取代反应(特征反应)
取2支硬质大试管,通过排饱和食盐水的方法先后各收集半试管甲烷和半试管氯气,分别用铁架台固定好,如图所示。其中1支试管用预先准备好的黑色纸套套上,另一支试管放在光亮处。片刻后,比较2支试管中的物质,二者是否出现了区别?
【实验7-1】
1.你从实验中得到哪些信息?
2.从所得的实验信息中你能得到哪些启示?
甲烷与氯气的取代反应
室温时,混合气体无光照时,不发生反应;光照时混合气体的黄绿色变浅,试管壁上出现油滴,试管中有少量白雾,试管内的液面上升。
1 说明试管内的混合气体在光照的条件下发生了化学反应。
2 试管壁上出现液滴,说明反应中生成了新的油状物质,且不溶于水。
3 试管内液面上升,说明随着反应的进行,试管内的气压在减小,即气体总体积在减小。
分析上述实验中所观察到的现象,从中可以得到那些结论?
现象
讨论
结论
现象与结论
观看下列甲烷取代反应的动画,并将每一步的化学方程式书写出来
有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应,叫取代反应.
甲烷的取代反应的历程
标准状态下:气体
标准状态下:液体
标准状态下:液体
标准状态下:液体
注意:
①甲烷与氯气反应可能有五种产物,其中有两种气体产物。
③多数有机物都难溶于水,易溶于有机溶剂。
②有机反应很复杂,产物较多。故有机反应一般用“ ” 而不用“ ” 表示。
(哪个产物的产量最多?)
光照下甲烷与氯气发生取代反应
CH4 + Cl2 CH3Cl +HCl
光照
CH3Cl + Cl2 CH2Cl2 + HCl
CH2Cl2 + Cl2 CHCl3 + HCl
CHCl3 + Cl2 CCl4 + HCl
光照
光照
光照
4.分解反应
在加热至1500℃的条件下,甲烷分解生成炭黑和氢气。
反应方程式:CH4 C + 2H2
高温
得到的氢气是合成氨及合成汽油等工业的原料;炭黑是橡胶工业的原料。
光
C、CH4+2O2 CO2+2H2O
D、CHCl3+HF CHFCl2+HCl
B、Zn+H2SO4 ZnSO4+H2
1、下列反应不属于取代反应的是( )
A、CH4+Br2 CH3Br+HBr
点燃
BC
练一练
2、在光照下,将等物质的量的CH4和Cl2充分 反应,得到的产物物质的量最多的是( )
A、CH3Cl B、CH2Cl2 C、CCl4 D、HCl
D
观察烷烃结构简式和物理性质,有哪些规律?
逐 渐 升 高
气 液 固
逐 渐 增 大
烷烃的性质
1.物理性质
烷烃都不溶于水,可溶于有机溶剂(汽油,苯等)的无色物质,随着碳原子增多,其熔点、沸点和密度而增大,都小于水的密度,室温时C1-C4气态,C5-C17液态,C18以上固态。
甲烷属于烷烃,前面我们已经学习了甲烷的性质,你能类比甲烷的性质写出烷烃的化学性质吗?
烷烃的性质
2.化学性质
1.稳定性
2.可燃性
3.取代反应
4.分解反应
不与强酸、强碱、酸性KMnO4溶液反应
一般的,大部分有机物均可燃(即与氧气反应)
与纯卤素气态单质光照下发生反应
以丙烷为例,写出可燃性和取代反应对应化学方程式
2.可燃性
链状烷烃燃烧通式:
3.取代反应
思考:1.上述反应产物一氯代物中哪两种是同种物质,哪两种又互为同分异构体
2.通过上述烷烃与氯气反应生成一氯代物你有什么启示?
同一个碳原子上的氢是等效氢
同一个碳原子上的甲基上的氢是等效氢
处于分子中对称位置的碳上的氢原子是等效氢
判断“等效氢”的三条原则是:
补充:烃的一氯取代产物同分异构体数目的判断---等效氢法
-C-
H
H
H
H
-C-
CH3
CH3
CH3
CH3
C
-C-
H
H
H
H
H
H
下面烷烃一氯代物有___________种同分异构体.
CH3—CH—CH—CH—CH3
l l l
CH3 CH3 CH3
4
CH3CH2CH2CH2CH3
CH3
CH3 – C – CH2- CH3
CH3
下面烷烃一氯代物有多少种?
练一练
(2)在通常条件下,烷烃和硫酸、氢氧化钠不反应,和酸性KMnO4溶液也不反应( )
(3)在做甲烷、乙烷燃烧试验前,气体一定要验纯( )
(1)常温常压下,CH4、C2H6和C3H8为气体,C4H10、C6H14呈液态( )
×
√
√
提示:常温常压下,分子中碳原子数n≤4的烷烃为气态,故C4H10为气态。
提示:等体积的CH4和C4H10,C4H10用的氧气更多,如不减小进气量(或增大进风量),则C4H10燃烧不充分,会产生CO等有毒气体。
(4)使用天然气(主要成分为CH4)的燃气灶,改用液化石油气(主要成分为C4H10),应减小进气量或增大进风量( )
√
练习
小结:烷烃的性质归纳
链状烷烃通式:CnH2n+2 (n为整数)
烷烃的性质(与甲烷类似)
1物理性质:熔点低,难溶于水,易溶于有机溶剂,熔沸点随C原子数增多而升高
2化学性质:
a.稳定性,不与强酸、强碱、高锰酸钾溶液反应
b.可燃性
c.取代反应
d.分解反应
第七章 有机化合物
第一节 认识有机化合物
第2课时 烷烃的性质
奶牛
课前回顾:甲烷的结构
(1)分子式:
(2)电子式:
(3)结构式:
(4)空间构型:
H C H
H
H
×
.
×
.
×
.
×
.
│
━ C ━
│
H
H
H
H
具有正四面体形结构
CH4
甲烷的性质
任务1:阅读课本p64-65,总结出甲烷的化学性质
1.稳定性
2.可燃性
3.取代反应(特征反应)
4.分解反应
不与强酸、强碱、酸性KMnO4溶液反应
一般的,大部分有机物均可燃(即与氧气反应)
与纯净卤素气态单质光照下发生反应
学以致用
下列新闻说明了甲烷的什么性质?你能写出化学方程式吗?通过该条新闻你对甲烷的使用有何启示?
2.可燃性
点燃甲烷和空气的混合气体会有什么后果呢?
爆炸
启示:甲烷点燃一定要验纯
3.取代反应(特征反应)
取2支硬质大试管,通过排饱和食盐水的方法先后各收集半试管甲烷和半试管氯气,分别用铁架台固定好,如图所示。其中1支试管用预先准备好的黑色纸套套上,另一支试管放在光亮处。片刻后,比较2支试管中的物质,二者是否出现了区别?
【实验7-1】
1.你从实验中得到哪些信息?
2.从所得的实验信息中你能得到哪些启示?
甲烷与氯气的取代反应
室温时,混合气体无光照时,不发生反应;光照时混合气体的黄绿色变浅,试管壁上出现油滴,试管中有少量白雾,试管内的液面上升。
1 说明试管内的混合气体在光照的条件下发生了化学反应。
2 试管壁上出现液滴,说明反应中生成了新的油状物质,且不溶于水。
3 试管内液面上升,说明随着反应的进行,试管内的气压在减小,即气体总体积在减小。
分析上述实验中所观察到的现象,从中可以得到那些结论?
现象
讨论
结论
现象与结论
观看下列甲烷取代反应的动画,并将每一步的化学方程式书写出来
有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应,叫取代反应.
甲烷的取代反应的历程
标准状态下:气体
标准状态下:液体
标准状态下:液体
标准状态下:液体
注意:
①甲烷与氯气反应可能有五种产物,其中有两种气体产物。
③多数有机物都难溶于水,易溶于有机溶剂。
②有机反应很复杂,产物较多。故有机反应一般用“ ” 而不用“ ” 表示。
(哪个产物的产量最多?)
光照下甲烷与氯气发生取代反应
CH4 + Cl2 CH3Cl +HCl
光照
CH3Cl + Cl2 CH2Cl2 + HCl
CH2Cl2 + Cl2 CHCl3 + HCl
CHCl3 + Cl2 CCl4 + HCl
光照
光照
光照
4.分解反应
在加热至1500℃的条件下,甲烷分解生成炭黑和氢气。
反应方程式:CH4 C + 2H2
高温
得到的氢气是合成氨及合成汽油等工业的原料;炭黑是橡胶工业的原料。
光
C、CH4+2O2 CO2+2H2O
D、CHCl3+HF CHFCl2+HCl
B、Zn+H2SO4 ZnSO4+H2
1、下列反应不属于取代反应的是( )
A、CH4+Br2 CH3Br+HBr
点燃
BC
练一练
2、在光照下,将等物质的量的CH4和Cl2充分 反应,得到的产物物质的量最多的是( )
A、CH3Cl B、CH2Cl2 C、CCl4 D、HCl
D
观察烷烃结构简式和物理性质,有哪些规律?
逐 渐 升 高
气 液 固
逐 渐 增 大
烷烃的性质
1.物理性质
烷烃都不溶于水,可溶于有机溶剂(汽油,苯等)的无色物质,随着碳原子增多,其熔点、沸点和密度而增大,都小于水的密度,室温时C1-C4气态,C5-C17液态,C18以上固态。
甲烷属于烷烃,前面我们已经学习了甲烷的性质,你能类比甲烷的性质写出烷烃的化学性质吗?
烷烃的性质
2.化学性质
1.稳定性
2.可燃性
3.取代反应
4.分解反应
不与强酸、强碱、酸性KMnO4溶液反应
一般的,大部分有机物均可燃(即与氧气反应)
与纯卤素气态单质光照下发生反应
以丙烷为例,写出可燃性和取代反应对应化学方程式
2.可燃性
链状烷烃燃烧通式:
3.取代反应
思考:1.上述反应产物一氯代物中哪两种是同种物质,哪两种又互为同分异构体
2.通过上述烷烃与氯气反应生成一氯代物你有什么启示?
同一个碳原子上的氢是等效氢
同一个碳原子上的甲基上的氢是等效氢
处于分子中对称位置的碳上的氢原子是等效氢
判断“等效氢”的三条原则是:
补充:烃的一氯取代产物同分异构体数目的判断---等效氢法
-C-
H
H
H
H
-C-
CH3
CH3
CH3
CH3
C
-C-
H
H
H
H
H
H
下面烷烃一氯代物有___________种同分异构体.
CH3—CH—CH—CH—CH3
l l l
CH3 CH3 CH3
4
CH3CH2CH2CH2CH3
CH3
CH3 – C – CH2- CH3
CH3
下面烷烃一氯代物有多少种?
练一练
(2)在通常条件下,烷烃和硫酸、氢氧化钠不反应,和酸性KMnO4溶液也不反应( )
(3)在做甲烷、乙烷燃烧试验前,气体一定要验纯( )
(1)常温常压下,CH4、C2H6和C3H8为气体,C4H10、C6H14呈液态( )
×
√
√
提示:常温常压下,分子中碳原子数n≤4的烷烃为气态,故C4H10为气态。
提示:等体积的CH4和C4H10,C4H10用的氧气更多,如不减小进气量(或增大进风量),则C4H10燃烧不充分,会产生CO等有毒气体。
(4)使用天然气(主要成分为CH4)的燃气灶,改用液化石油气(主要成分为C4H10),应减小进气量或增大进风量( )
√
练习
小结:烷烃的性质归纳
链状烷烃通式:CnH2n+2 (n为整数)
烷烃的性质(与甲烷类似)
1物理性质:熔点低,难溶于水,易溶于有机溶剂,熔沸点随C原子数增多而升高
2化学性质:
a.稳定性,不与强酸、强碱、高锰酸钾溶液反应
b.可燃性
c.取代反应
d.分解反应
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
