鲁教版九年级化学下册 第九单元 第一节 常见的金属材料 课件(共33张PPT)
文档属性
| 名称 | 鲁教版九年级化学下册 第九单元 第一节 常见的金属材料 课件(共33张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 5.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-13 00:00:00 | ||
图片预览








文档简介
(共33张PPT)
第九单元 金属
第一节 常见的金属材料
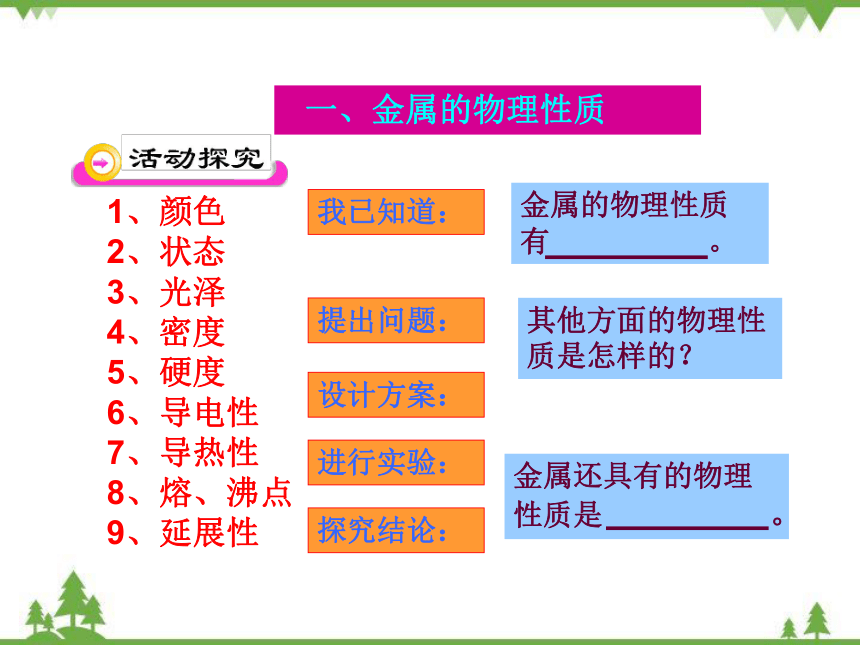
1、颜色
2、状态
3、光泽
4、密度
5、硬度
6、导电性
7、导热性
8、熔、沸点
9、延展性
一、金属的物理性质
提出问题:
设计方案:
进行实验:
探究结论:
其他方面的物理性质是怎样的?
金属还具有的物理性质是 。
我已知道:
金属的物理性质有 。
大多数为银白色
常温下一般为固体
金属光泽
一般较大
一般较大
金属共有的物理性质:
优良
优良
一般较高
延展性好
1.颜色
2.状态
3.光泽
4.密度
5.硬度
6.导电性
7.导热性
8.熔、沸点
9.延展性
金属
性质 金
(Au) 银
(Ag) 铜
(Cu) 铁
(Fe) 铝
(Al) 铬
(Cr)
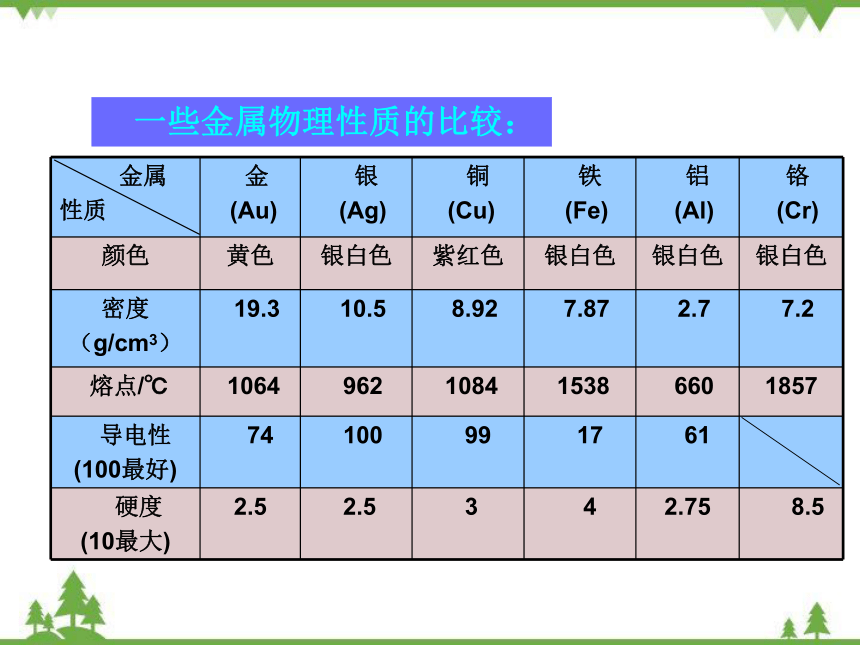
颜色 黄色 银白色 紫红色 银白色 银白色 银白色
密度
(g/cm3) 19.3 10.5 8.92 7.87 2.7 7.2
熔点/℃ 1064 962 1084 1538 660 1857
导电性
(100最好) 74 100 99 17 61
硬度
(10最大) 2.5 2.5 3 4 2.75 8.5
一些金属物理性质的比较:
这些金属各有什么用途
分别利用了它们的什么物理性质?
敢于提问
对于合金你想知道什么?
小资料
一种铝合金的成分配比为:
0.1%~5%的镁、0.1%~3%的锆、
0.1%~15%的铈,75 % ~ 99.7 %的铝。
生产工艺: 1.配制原料;2.真空熔炼;3.锻压;4.热轧;5.粗拉;6.热处理;7.煮洗;8.精拉;9.成品。
性质:有导电性、导热性、延展性等金属性质 。
从资料中你能获得有关合金的哪些信息?
合金 主要成分
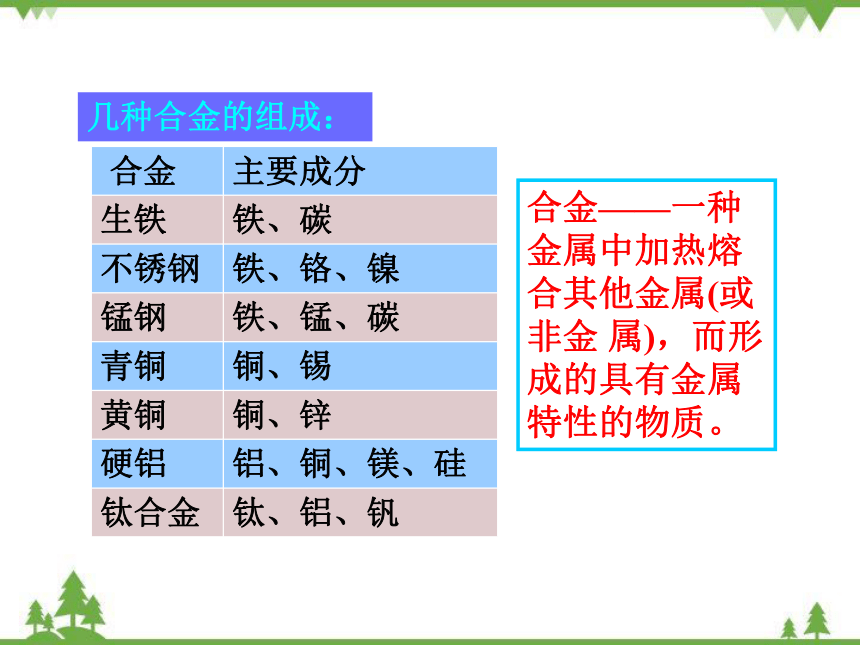
生铁 铁、碳
不锈钢 铁、铬、镍
锰钢 铁、锰、碳
青铜 铜、锡
黄铜 铜、锌
硬铝 铝、铜、镁、硅
钛合金 钛、铝、钒
几种合金的组成:
合金——一种金属中加热熔合其他金属(或非金 属),而形成的具有金属特性的物质。
金属与合金在硬度、熔点上有什么差异?
提出问题:
猜想与假设:
制定计划:
进行实验:
二、 金属与合金性质的差异
资料: 焊锡熔点为183℃,组成它的金属锡的熔点为232℃ 、铅为327℃ 。
铝片VS铝合金 铜片VS黄铜片 锡片VS焊锡
硬度
熔点
合金与金属物理性质比较:
合金一般大于各组分金属
合金一般低于各组分金属
纯铜
铜合金
纯金
K金
合金比纯金属具有更多色彩。
合金 主要成分 性能 用途
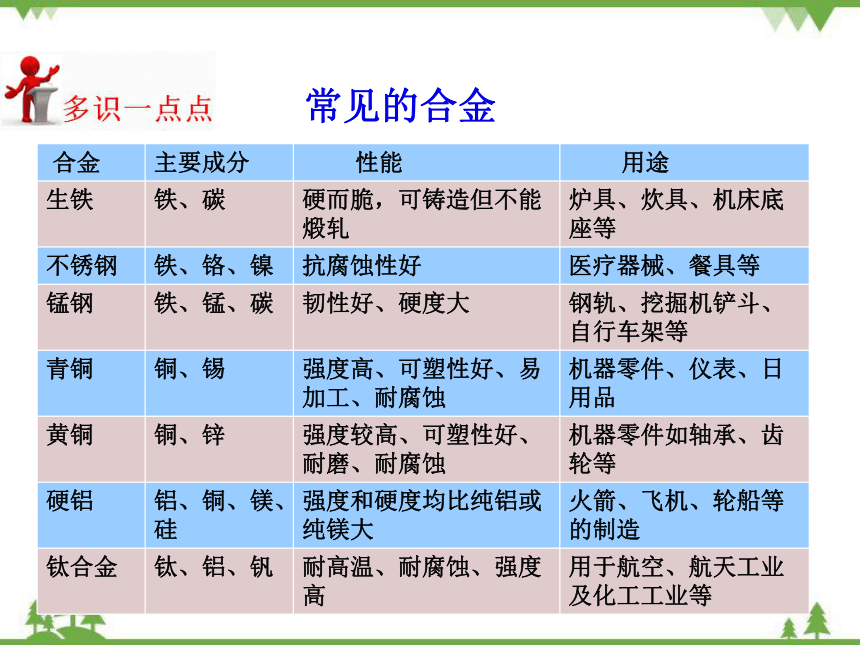
生铁 铁、碳 硬而脆,可铸造但不能煅轧 炉具、炊具、机床底座等
不锈钢 铁、铬、镍 抗腐蚀性好 医疗器械、餐具等
锰钢 铁、锰、碳 韧性好、硬度大 钢轨、挖掘机铲斗、自行车架等
青铜 铜、锡 强度高、可塑性好、易加工、耐腐蚀 机器零件、仪表、日用品
黄铜 铜、锌 强度较高、可塑性好、耐磨、耐腐蚀 机器零件如轴承、齿轮等
硬铝 铝、铜、镁、硅 强度和硬度均比纯铝或纯镁大 火箭、飞机、轮船等的制造
钛合金 钛、铝、钒 耐高温、耐腐蚀、强度高 用于航空、航天工业及化工工业等
常见的合金
N2、O2、木炭和红磷是金属吗?
它们具有的哪些方面的性质可以证明你的答案呢?
石斧
石刀
石器时代
司母戊大方鼎
四羊方尊
青铜器时代
铁犁
铁铲
铁器时代
三、金属矿物及其冶炼
要完成铁的冶炼通常考虑哪些主要方面的问题?
冶炼原料;
冶炼原理;
冶炼装置(设备)等。
常见的几种铁矿石的成分
黄铁矿
主要成分 FeS2
菱铁矿
主要成分FeCO3
磁铁矿
主要成分 Fe3O4
主要成分 Fe2O3
赤铁矿
70%
72%
48%
47%
主要成分中的含铁量
选择冶炼原料时,通常考虑矿石的价格、金属的含量、安全无污染等。
如何从铁矿石中得到铁呢
以赤铁矿(主要成分为Fe2O3)为例。
Fe2O3 Fe
CO
高温
炼铁原理
仪器选择(相同仪器有多件)
①
②
③
⑦
⑥
⑤
温馨提示:常温下,Fe2O3是一种固体, CO是一种有毒的无色气体!
④
A
B
氧化铁
一氧化碳
石灰水
实验设计
实验现象:
红色固体变成黑色;
澄清石灰水变浑浊。
实验装置
A
B
还原反应:含氧化合物中的氧被夺去的反应。
Fe2O3+ 3CO 2Fe + 3CO2
高温
夺取氧的物质叫还原剂。
得氧被氧化,发生氧化反应,作还原剂
失氧被还原,发生还原反应,作氧化剂
在高温条件下,用还原剂(主要是CO)从铁矿石中还原出铁。
炼铁原理
炼铁高炉示意图
1.原料:
3.设备:
高炉
铁矿石
焦炭
石灰石
空气
2.原理:
高温
Fe2O3+3CO 2Fe+3CO2
工业炼铁
炼铁的最终产品是生铁。
含碳2%~4.3%的铁合金。
含碳0.03%~2%的铁合金。
钢
生铁
降低含碳量
A. H2+ CuO Cu+H2O
△
B. Fe2O3+2Al Al2O3+2Fe
判断下列反应中的还原剂。
高温
CO得氧,作还原剂。
Fe3O4失氧,作氧化剂。
4CO+ Fe3O4 3Fe+4CO2
高温
在探究用赤铁矿(主要成分为Fe2O3 )炼铁的主要反应原理时,老师设计的实验装置如图所示,实验中,小明发现一氧化碳被白白烧掉太浪费了,于是对装置又进行了改进。猜一猜小明是怎样改进的?
到目前为止,你学习了哪些制备金属的方法?知道了哪些典型的还原剂?
成语中蕴含了丰富的化学知识,请查阅“沙里淘金”“百炼成钢”的化学寓意。
课后作业
谢谢!
第九单元 金属
第一节 常见的金属材料
1、颜色
2、状态
3、光泽
4、密度
5、硬度
6、导电性
7、导热性
8、熔、沸点
9、延展性
一、金属的物理性质
提出问题:
设计方案:
进行实验:
探究结论:
其他方面的物理性质是怎样的?
金属还具有的物理性质是 。
我已知道:
金属的物理性质有 。
大多数为银白色
常温下一般为固体
金属光泽
一般较大
一般较大
金属共有的物理性质:
优良
优良
一般较高
延展性好
1.颜色
2.状态
3.光泽
4.密度
5.硬度
6.导电性
7.导热性
8.熔、沸点
9.延展性
金属
性质 金
(Au) 银
(Ag) 铜
(Cu) 铁
(Fe) 铝
(Al) 铬
(Cr)
颜色 黄色 银白色 紫红色 银白色 银白色 银白色
密度
(g/cm3) 19.3 10.5 8.92 7.87 2.7 7.2
熔点/℃ 1064 962 1084 1538 660 1857
导电性
(100最好) 74 100 99 17 61
硬度
(10最大) 2.5 2.5 3 4 2.75 8.5
一些金属物理性质的比较:
这些金属各有什么用途
分别利用了它们的什么物理性质?
敢于提问
对于合金你想知道什么?
小资料
一种铝合金的成分配比为:
0.1%~5%的镁、0.1%~3%的锆、
0.1%~15%的铈,75 % ~ 99.7 %的铝。
生产工艺: 1.配制原料;2.真空熔炼;3.锻压;4.热轧;5.粗拉;6.热处理;7.煮洗;8.精拉;9.成品。
性质:有导电性、导热性、延展性等金属性质 。
从资料中你能获得有关合金的哪些信息?
合金 主要成分
生铁 铁、碳
不锈钢 铁、铬、镍
锰钢 铁、锰、碳
青铜 铜、锡
黄铜 铜、锌
硬铝 铝、铜、镁、硅
钛合金 钛、铝、钒
几种合金的组成:
合金——一种金属中加热熔合其他金属(或非金 属),而形成的具有金属特性的物质。
金属与合金在硬度、熔点上有什么差异?
提出问题:
猜想与假设:
制定计划:
进行实验:
二、 金属与合金性质的差异
资料: 焊锡熔点为183℃,组成它的金属锡的熔点为232℃ 、铅为327℃ 。
铝片VS铝合金 铜片VS黄铜片 锡片VS焊锡
硬度
熔点
合金与金属物理性质比较:
合金一般大于各组分金属
合金一般低于各组分金属
纯铜
铜合金
纯金
K金
合金比纯金属具有更多色彩。
合金 主要成分 性能 用途
生铁 铁、碳 硬而脆,可铸造但不能煅轧 炉具、炊具、机床底座等
不锈钢 铁、铬、镍 抗腐蚀性好 医疗器械、餐具等
锰钢 铁、锰、碳 韧性好、硬度大 钢轨、挖掘机铲斗、自行车架等
青铜 铜、锡 强度高、可塑性好、易加工、耐腐蚀 机器零件、仪表、日用品
黄铜 铜、锌 强度较高、可塑性好、耐磨、耐腐蚀 机器零件如轴承、齿轮等
硬铝 铝、铜、镁、硅 强度和硬度均比纯铝或纯镁大 火箭、飞机、轮船等的制造
钛合金 钛、铝、钒 耐高温、耐腐蚀、强度高 用于航空、航天工业及化工工业等
常见的合金
N2、O2、木炭和红磷是金属吗?
它们具有的哪些方面的性质可以证明你的答案呢?
石斧
石刀
石器时代
司母戊大方鼎
四羊方尊
青铜器时代
铁犁
铁铲
铁器时代
三、金属矿物及其冶炼
要完成铁的冶炼通常考虑哪些主要方面的问题?
冶炼原料;
冶炼原理;
冶炼装置(设备)等。
常见的几种铁矿石的成分
黄铁矿
主要成分 FeS2
菱铁矿
主要成分FeCO3
磁铁矿
主要成分 Fe3O4
主要成分 Fe2O3
赤铁矿
70%
72%
48%
47%
主要成分中的含铁量
选择冶炼原料时,通常考虑矿石的价格、金属的含量、安全无污染等。
如何从铁矿石中得到铁呢
以赤铁矿(主要成分为Fe2O3)为例。
Fe2O3 Fe
CO
高温
炼铁原理
仪器选择(相同仪器有多件)
①
②
③
⑦
⑥
⑤
温馨提示:常温下,Fe2O3是一种固体, CO是一种有毒的无色气体!
④
A
B
氧化铁
一氧化碳
石灰水
实验设计
实验现象:
红色固体变成黑色;
澄清石灰水变浑浊。
实验装置
A
B
还原反应:含氧化合物中的氧被夺去的反应。
Fe2O3+ 3CO 2Fe + 3CO2
高温
夺取氧的物质叫还原剂。
得氧被氧化,发生氧化反应,作还原剂
失氧被还原,发生还原反应,作氧化剂
在高温条件下,用还原剂(主要是CO)从铁矿石中还原出铁。
炼铁原理
炼铁高炉示意图
1.原料:
3.设备:
高炉
铁矿石
焦炭
石灰石
空气
2.原理:
高温
Fe2O3+3CO 2Fe+3CO2
工业炼铁
炼铁的最终产品是生铁。
含碳2%~4.3%的铁合金。
含碳0.03%~2%的铁合金。
钢
生铁
降低含碳量
A. H2+ CuO Cu+H2O
△
B. Fe2O3+2Al Al2O3+2Fe
判断下列反应中的还原剂。
高温
CO得氧,作还原剂。
Fe3O4失氧,作氧化剂。
4CO+ Fe3O4 3Fe+4CO2
高温
在探究用赤铁矿(主要成分为Fe2O3 )炼铁的主要反应原理时,老师设计的实验装置如图所示,实验中,小明发现一氧化碳被白白烧掉太浪费了,于是对装置又进行了改进。猜一猜小明是怎样改进的?
到目前为止,你学习了哪些制备金属的方法?知道了哪些典型的还原剂?
成语中蕴含了丰富的化学知识,请查阅“沙里淘金”“百炼成钢”的化学寓意。
课后作业
谢谢!
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
