射阳县高级中学2012年秋学期期末考试选修化学试卷及答案
文档属性
| 名称 | 射阳县高级中学2012年秋学期期末考试选修化学试卷及答案 |

|
|
| 格式 | zip | ||
| 文件大小 | 169.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2013-02-20 00:00:00 | ||
图片预览




文档简介
射阳县高级中学2012年秋学期期末考试试卷
高 二 化 学(选修)
时间:100分钟 总分: 120分 命题人:姚琴
可能用到的相对原子质量:
H—1 C—12 N—14 O—16 Na—23 Mg—24
S—32 Cl—35.5 Fe—56 Cu—64 Zn—65 Ba—137
第Ⅰ卷(选择题,共52分)
选择题(每题只有一个选项符合题意)
1.化学与食品安全和人体健康密切相关,下列做法不利于食品安全的有
①用毛发水解液勾兑“化学酱油",以节约成本
②将地沟油回收再加工为食用油,以减缓水体富营养化
③用工业废水灌溉农田,以提高水资源的利用率
④合理施用微生物肥料,减少化肥施用量,以降低蔬菜产品中硝酸盐含量
⑤推广农作物的生物防治技术,减少农药的使用
⑥邻苯二甲酸酯(塑化剂)能使食品增稠,可用作生产食品的乳化剂
A.①②③⑥ B.①②⑤ C.②⑥ D.③④⑤
2.1999年美国《科学》杂志报道:在40GPa高压下,用激光器加热到1800K,人们成功制得了原子晶体干冰,下列推断中不正确的是
A.原子晶体干冰有很高的熔点、沸点,有很大的硬度
B.原子晶体干冰易气化,可用作制冷材料
C.原子晶体干冰的硬度大,可用作耐磨材料
D.每摩尔原子晶体干冰中含4mol C—O键
3.下列不互为同分异构体的一组物质是
A.葡萄糖和果糖(C6H12O6) B.淀粉和纤维素
C.乙酸和甲酸甲酯 D.蔗糖和麦芽糖
4.含有下列官能团之一的有机物一定会产生银镜反应,此官能团是
A.—OH B.—CH=CH—
C.—CHO D.—COOH
5.下列物质中,与NaOH溶液、Na2CO3、溴水、苯酚钠水溶液和甲醇都能反应的是
A.C6H6 B.CH3CHO
C.CH3COOH D.CH2=CH-COOH
6.下列大气污染物中,能与人体中血红蛋白中Fe2+以配位键结合而引起中毒的气体是
A.SO2 B.CO2 C.NO2 D.CO
7.能区别[Co(NH3)4Cl2]Cl和[Co(NH3)4Cl2]NO3两种溶液的试剂是
A.AgNO3溶液 B.NaOH溶液
C.CCl4 D.浓氨水
8.下列反应中属于取代反应的是
A、2CH4C2H4+2H2 B、2HI+Cl2=I2+2HCl
C、C2H5Cl+Cl2C2H4Cl2+HCl D、CH4+2O2CO2+2H2O
9.下列关于丙烯(CH3—CH =CH2)的说法正确的
A.丙烯分子有8个σ键,1个π键B.丙烯分子中3个碳原子都是sp3杂化
C.丙烯分子不存在非极性键 D.丙烯分子中3个碳原子在同一直线
10.用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.常温下,39g某浓度的乙炔的苯溶液中原子总数为6NA
B.1mol苯乙烯中含有的碳碳双键数为4NA个
C.标准状况下,11.2L的CCl4含有的分子数为0.5NA
D.0.1molC2H6中含有的碳碳单键数为0.6NA
二、不定项选择题(每小题有1~2个选项符合题意)
11.香草醛广泛用于食品、饮料、烟草、酒类、医药、化工和各类化妆用品等, 是一种性能稳定、香味纯正、留香持久的优良香料和食品添加剂。
其结构如右图所示,下列说法不正确的是
A.香草醛的分子式为C7H8O3
B.加FeCl3溶液,溶液不显紫色
C.能与NaOH发生中和反应
D.能发生银镜反应
12.欲除去下列物质中混入的少量杂质(括号内物质为杂质),不能达到目的的是
A.乙酸乙酯(乙酸):加饱和Na2CO3溶液,充分振荡静置后,分液
B.乙醇(水):加入新制生石灰,蒸馏
C. 溴苯(溴):加入NaOH溶液,充分振荡静置后,分液
D.乙酸(乙醇):加入金属钠,蒸馏
13.下列有关化学键与晶体的说法中,正确的是
A.离子晶体的晶格能越大,离子晶体的熔点越高
B.离子化合物中只含有离子键
C.成键原子的原子轨道重叠越多,共价键越牢固
D.共价键的键能越大,分子晶体的熔、沸点越高
14.下列各化合物的命名中正确的是
A.CH2=CH-CH=CH2 1,3—二丁烯 B. 2—甲基丁烷
C. 邻甲基苯酚 D.
15.膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的
杂质中常含有磷化氢。以下关于PH3的叙述不正确的是
A、PH3分子中有未成键的孤电子对 B、PH3是极性分子
C、它的分子构型是三角锥形 D、磷原子采用sp2杂化方式
16.短周期元素A、B、C,原子序数依次递增。已知:A、C同主族,而且三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半。下列叙述中正确的是
A.A、B形成的化合物中含有离子键
B.沸点:A的氢化物高于C的氢化物
C.离子半径:AD.电负性:C>B>A
17.最近发现一种由钛(Ti)原子和碳原子构成的气态团簇分子,分子模型如图所示,其中圆圈表示钛原子,黑点表示碳原子,则它的化学式为:
A.TiC B. C. D.
18.膳食纤维具有的突出保健功能,近年来受到人们的普遍关注,被世界卫生组织称为人体的“第七营养素”。木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构如图所示。下列有关芥子醇的说法正确的是
A.芥子醇的分子式是C11H12O4
B.芥子醇分子中所有碳原子不可能在同一平面
C.芥子醇能与FeCl3溶液发生显色反应
D.1mol芥子醇能与足量溴水反应消耗1molBr2
第Ⅱ卷(非选择题,共68分)
三、填空题
19.下表是元素周期表中短周期的一部分,请用化学式或元素符号等进行填空:
⑴ 下表中元素f的氢化物的电子式是_____________,此氢化物的热稳定性比元素g的氢化物的热稳定性________(填“强”或“弱”),元素e和g的氢化物中沸点较高的是 。
a
b
c
d
e
h
f
g
(2)表中b、c、d三种元素,第一电离能由小到大的顺序是 < < 。
(3)元素h的氧化物的晶体类型为 。
(4)元素b的最高价氧化物分子中,b原子的杂化方式是 ,空间构型为 。
(5)与元素b和c形成的一价阴离子(bc—)互为等电子体的分子有 (写一种)。
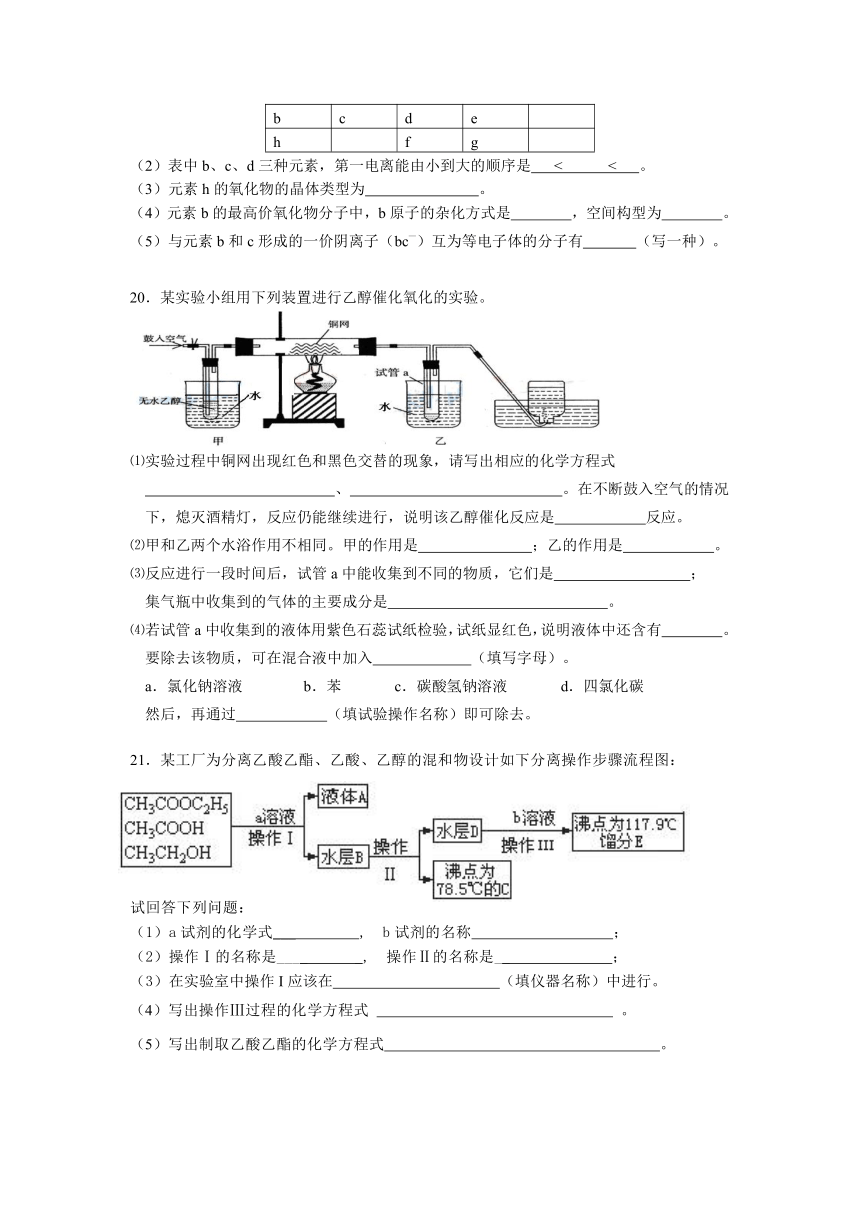
20.某实验小组用下列装置进行乙醇催化氧化的实验。
⑴实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式
、 。在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是 反应。
⑵甲和乙两个水浴作用不相同。甲的作用是 ;乙的作用是 。
⑶反应进行一段时间后,试管a中能收集到不同的物质,它们是 ;
集气瓶中收集到的气体的主要成分是 。
⑷若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有 。
要除去该物质,可在混合液中加入 (填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过 (填试验操作名称)即可除去。
21.某工厂为分离乙酸乙酯、乙酸、乙醇的混和物设计如下分离操作步骤流程图:
试回答下列问题:
(1)a试剂的化学式___ , b试剂的名称 ;
(2)操作Ⅰ的名称是____ _, 操作Ⅱ的名称是__ ;
(3)在实验室中操作I应该在 (填仪器名称)中进行。
(4)写出操作Ⅲ过程的化学方程式 。
(5)写出制取乙酸乙酯的化学方程式 。
22.多巴胺是一种重要的中枢神经传导物质,用来帮助细胞传送脉冲的化学物质,能影响人对事物的欢愉感受。多巴胺可用香兰素与硝基甲烷等为原料按下列路线合成:
(1)香兰素保存不当往往会导致颜色、气味发生明显变化,其原因是
(2)多巴胺中的官能团的名称是 、 ;反应②的反应条件为 、
;反应④的反应类型为 反应。
(3)写出反应③的化学方程式
(4)写出同时满足下列条件的香兰素的一种同分异构体的结构简式:
①能发生水解反应 ②能发生银镜反应 ③能与FeCl3溶液发生显色反应
④有5种不同化学环境的氢原子
23.铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,超细铜粉可应用于导电材料、催化剂等领域中,CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。
⑴超细铜粉的某制备方法如下:
①[Cu(NH3)4]SO4中所含的化学键有 、 、 。
②NH4CuSO3中的金属阳离子的核外电子排布式为: 。
③ NH3分子中N原子的杂化方式为: 。
④SO2分子的空间构型是 。 与SO2互为等电子体的分子有 (写一种)。
⑵氯化亚铜(CuCl)的某制备过程是:向CuCl2溶液中通人一定量SO2,微热,反应一段时间后即生成CuCl白色沉淀。
①CuCl的晶胞结构如下图所示,其中Cl原子的配位数为_________。
②CuCl的熔点比CuO的熔点 (填“高”或“低”) ,原因是 。
2012年秋学期期末考试试卷
高二化学(选修)答题卷
19.⑴ , , 。
(2) < < 。
(3) 。
(4) , 。
(5) 。
20.⑴ ,
,
。
(2) , 。
(3) , 。
(4) , , 。
21.⑴ , 。
(2) 、 。
(3) 。
(4) 。
(5) 。
22.⑴ 。
(2) 、 ,
、 , 。
(3) 。
(4) 。
23.⑴① , , 。
② 。
③ 。
④ , 。
⑵① 。
② , 。
2012年秋学期期末考试试卷
高二化学(选修)答案
1
2
3
4
5
6
7
8
9
10
A
B
B
C
D
D
A
C
A
A
11
12
13
14
15
16
17
18
AB
D
AC
BC
D
AB
D
CD
19.(共10分)⑴ , 弱 , HF 。
(2) C < O < N 。
(3) 原子晶体 。
(4) sp 杂化 , 直线 型 。
(5) N2 或CO 。
20.(共10分)⑴ 2Cu + O2 =2CuO ,
CuO+CH3CH2OH→CH3CHO +Cu +H2O ,
放热 。
(2) 提供乙醇蒸汽 , 冷却生成的乙醛 。
(3) CH3CH2OH CH3COOH H2O , N2 。
(4) CH3COOH , C , 蒸馏 。
21.(共14分)⑴ NaCO3 , 稀硫酸 。
(2) 分液 、 蒸馏 。
(3) 分液漏斗 。
(4) 2CH3COONa + H2SO4 = 2CH3COOH + Na2SO4 。
(5) CH3COOH + C2H5OH → CH3COOCH2CH3 + H2O 。
22.(共14分)⑴ 香兰素被氧化 。
(2) 羟基 、 氨基 ,
浓硫酸 、 加热 , 还原 。
(3) 。
(4) 。
23.(共20分)⑴① 离子键 , 共价键 , 配位键 。
② 【Ar】3d10 。
③ SP3杂化 。
④ V型 , O3 。
⑵① 4 。
② 低 , CuO的晶格能比CuCl的 晶格能大 。
高 二 化 学(选修)
时间:100分钟 总分: 120分 命题人:姚琴
可能用到的相对原子质量:
H—1 C—12 N—14 O—16 Na—23 Mg—24
S—32 Cl—35.5 Fe—56 Cu—64 Zn—65 Ba—137
第Ⅰ卷(选择题,共52分)
选择题(每题只有一个选项符合题意)
1.化学与食品安全和人体健康密切相关,下列做法不利于食品安全的有
①用毛发水解液勾兑“化学酱油",以节约成本
②将地沟油回收再加工为食用油,以减缓水体富营养化
③用工业废水灌溉农田,以提高水资源的利用率
④合理施用微生物肥料,减少化肥施用量,以降低蔬菜产品中硝酸盐含量
⑤推广农作物的生物防治技术,减少农药的使用
⑥邻苯二甲酸酯(塑化剂)能使食品增稠,可用作生产食品的乳化剂
A.①②③⑥ B.①②⑤ C.②⑥ D.③④⑤
2.1999年美国《科学》杂志报道:在40GPa高压下,用激光器加热到1800K,人们成功制得了原子晶体干冰,下列推断中不正确的是
A.原子晶体干冰有很高的熔点、沸点,有很大的硬度
B.原子晶体干冰易气化,可用作制冷材料
C.原子晶体干冰的硬度大,可用作耐磨材料
D.每摩尔原子晶体干冰中含4mol C—O键
3.下列不互为同分异构体的一组物质是
A.葡萄糖和果糖(C6H12O6) B.淀粉和纤维素
C.乙酸和甲酸甲酯 D.蔗糖和麦芽糖
4.含有下列官能团之一的有机物一定会产生银镜反应,此官能团是
A.—OH B.—CH=CH—
C.—CHO D.—COOH
5.下列物质中,与NaOH溶液、Na2CO3、溴水、苯酚钠水溶液和甲醇都能反应的是
A.C6H6 B.CH3CHO
C.CH3COOH D.CH2=CH-COOH
6.下列大气污染物中,能与人体中血红蛋白中Fe2+以配位键结合而引起中毒的气体是
A.SO2 B.CO2 C.NO2 D.CO
7.能区别[Co(NH3)4Cl2]Cl和[Co(NH3)4Cl2]NO3两种溶液的试剂是
A.AgNO3溶液 B.NaOH溶液
C.CCl4 D.浓氨水
8.下列反应中属于取代反应的是
A、2CH4C2H4+2H2 B、2HI+Cl2=I2+2HCl
C、C2H5Cl+Cl2C2H4Cl2+HCl D、CH4+2O2CO2+2H2O
9.下列关于丙烯(CH3—CH =CH2)的说法正确的
A.丙烯分子有8个σ键,1个π键B.丙烯分子中3个碳原子都是sp3杂化
C.丙烯分子不存在非极性键 D.丙烯分子中3个碳原子在同一直线
10.用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.常温下,39g某浓度的乙炔的苯溶液中原子总数为6NA
B.1mol苯乙烯中含有的碳碳双键数为4NA个
C.标准状况下,11.2L的CCl4含有的分子数为0.5NA
D.0.1molC2H6中含有的碳碳单键数为0.6NA
二、不定项选择题(每小题有1~2个选项符合题意)
11.香草醛广泛用于食品、饮料、烟草、酒类、医药、化工和各类化妆用品等, 是一种性能稳定、香味纯正、留香持久的优良香料和食品添加剂。
其结构如右图所示,下列说法不正确的是
A.香草醛的分子式为C7H8O3
B.加FeCl3溶液,溶液不显紫色
C.能与NaOH发生中和反应
D.能发生银镜反应
12.欲除去下列物质中混入的少量杂质(括号内物质为杂质),不能达到目的的是
A.乙酸乙酯(乙酸):加饱和Na2CO3溶液,充分振荡静置后,分液
B.乙醇(水):加入新制生石灰,蒸馏
C. 溴苯(溴):加入NaOH溶液,充分振荡静置后,分液
D.乙酸(乙醇):加入金属钠,蒸馏
13.下列有关化学键与晶体的说法中,正确的是
A.离子晶体的晶格能越大,离子晶体的熔点越高
B.离子化合物中只含有离子键
C.成键原子的原子轨道重叠越多,共价键越牢固
D.共价键的键能越大,分子晶体的熔、沸点越高
14.下列各化合物的命名中正确的是
A.CH2=CH-CH=CH2 1,3—二丁烯 B. 2—甲基丁烷
C. 邻甲基苯酚 D.
15.膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的
杂质中常含有磷化氢。以下关于PH3的叙述不正确的是
A、PH3分子中有未成键的孤电子对 B、PH3是极性分子
C、它的分子构型是三角锥形 D、磷原子采用sp2杂化方式
16.短周期元素A、B、C,原子序数依次递增。已知:A、C同主族,而且三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半。下列叙述中正确的是
A.A、B形成的化合物中含有离子键
B.沸点:A的氢化物高于C的氢化物
C.离子半径:A
17.最近发现一种由钛(Ti)原子和碳原子构成的气态团簇分子,分子模型如图所示,其中圆圈表示钛原子,黑点表示碳原子,则它的化学式为:
A.TiC B. C. D.
18.膳食纤维具有的突出保健功能,近年来受到人们的普遍关注,被世界卫生组织称为人体的“第七营养素”。木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构如图所示。下列有关芥子醇的说法正确的是
A.芥子醇的分子式是C11H12O4
B.芥子醇分子中所有碳原子不可能在同一平面
C.芥子醇能与FeCl3溶液发生显色反应
D.1mol芥子醇能与足量溴水反应消耗1molBr2
第Ⅱ卷(非选择题,共68分)
三、填空题
19.下表是元素周期表中短周期的一部分,请用化学式或元素符号等进行填空:
⑴ 下表中元素f的氢化物的电子式是_____________,此氢化物的热稳定性比元素g的氢化物的热稳定性________(填“强”或“弱”),元素e和g的氢化物中沸点较高的是 。
a
b
c
d
e
h
f
g
(2)表中b、c、d三种元素,第一电离能由小到大的顺序是 < < 。
(3)元素h的氧化物的晶体类型为 。
(4)元素b的最高价氧化物分子中,b原子的杂化方式是 ,空间构型为 。
(5)与元素b和c形成的一价阴离子(bc—)互为等电子体的分子有 (写一种)。
20.某实验小组用下列装置进行乙醇催化氧化的实验。
⑴实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式
、 。在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是 反应。
⑵甲和乙两个水浴作用不相同。甲的作用是 ;乙的作用是 。
⑶反应进行一段时间后,试管a中能收集到不同的物质,它们是 ;
集气瓶中收集到的气体的主要成分是 。
⑷若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有 。
要除去该物质,可在混合液中加入 (填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过 (填试验操作名称)即可除去。
21.某工厂为分离乙酸乙酯、乙酸、乙醇的混和物设计如下分离操作步骤流程图:
试回答下列问题:
(1)a试剂的化学式___ , b试剂的名称 ;
(2)操作Ⅰ的名称是____ _, 操作Ⅱ的名称是__ ;
(3)在实验室中操作I应该在 (填仪器名称)中进行。
(4)写出操作Ⅲ过程的化学方程式 。
(5)写出制取乙酸乙酯的化学方程式 。
22.多巴胺是一种重要的中枢神经传导物质,用来帮助细胞传送脉冲的化学物质,能影响人对事物的欢愉感受。多巴胺可用香兰素与硝基甲烷等为原料按下列路线合成:
(1)香兰素保存不当往往会导致颜色、气味发生明显变化,其原因是
(2)多巴胺中的官能团的名称是 、 ;反应②的反应条件为 、
;反应④的反应类型为 反应。
(3)写出反应③的化学方程式
(4)写出同时满足下列条件的香兰素的一种同分异构体的结构简式:
①能发生水解反应 ②能发生银镜反应 ③能与FeCl3溶液发生显色反应
④有5种不同化学环境的氢原子
23.铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,超细铜粉可应用于导电材料、催化剂等领域中,CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。
⑴超细铜粉的某制备方法如下:
①[Cu(NH3)4]SO4中所含的化学键有 、 、 。
②NH4CuSO3中的金属阳离子的核外电子排布式为: 。
③ NH3分子中N原子的杂化方式为: 。
④SO2分子的空间构型是 。 与SO2互为等电子体的分子有 (写一种)。
⑵氯化亚铜(CuCl)的某制备过程是:向CuCl2溶液中通人一定量SO2,微热,反应一段时间后即生成CuCl白色沉淀。
①CuCl的晶胞结构如下图所示,其中Cl原子的配位数为_________。
②CuCl的熔点比CuO的熔点 (填“高”或“低”) ,原因是 。
2012年秋学期期末考试试卷
高二化学(选修)答题卷
19.⑴ , , 。
(2) < < 。
(3) 。
(4) , 。
(5) 。
20.⑴ ,
,
。
(2) , 。
(3) , 。
(4) , , 。
21.⑴ , 。
(2) 、 。
(3) 。
(4) 。
(5) 。
22.⑴ 。
(2) 、 ,
、 , 。
(3) 。
(4) 。
23.⑴① , , 。
② 。
③ 。
④ , 。
⑵① 。
② , 。
2012年秋学期期末考试试卷
高二化学(选修)答案
1
2
3
4
5
6
7
8
9
10
A
B
B
C
D
D
A
C
A
A
11
12
13
14
15
16
17
18
AB
D
AC
BC
D
AB
D
CD
19.(共10分)⑴ , 弱 , HF 。
(2) C < O < N 。
(3) 原子晶体 。
(4) sp 杂化 , 直线 型 。
(5) N2 或CO 。
20.(共10分)⑴ 2Cu + O2 =2CuO ,
CuO+CH3CH2OH→CH3CHO +Cu +H2O ,
放热 。
(2) 提供乙醇蒸汽 , 冷却生成的乙醛 。
(3) CH3CH2OH CH3COOH H2O , N2 。
(4) CH3COOH , C , 蒸馏 。
21.(共14分)⑴ NaCO3 , 稀硫酸 。
(2) 分液 、 蒸馏 。
(3) 分液漏斗 。
(4) 2CH3COONa + H2SO4 = 2CH3COOH + Na2SO4 。
(5) CH3COOH + C2H5OH → CH3COOCH2CH3 + H2O 。
22.(共14分)⑴ 香兰素被氧化 。
(2) 羟基 、 氨基 ,
浓硫酸 、 加热 , 还原 。
(3) 。
(4) 。
23.(共20分)⑴① 离子键 , 共价键 , 配位键 。
② 【Ar】3d10 。
③ SP3杂化 。
④ V型 , O3 。
⑵① 4 。
② 低 , CuO的晶格能比CuCl的 晶格能大 。
同课章节目录
