化学必修1专题一基础练习(有答案)
图片预览




文档简介
化学必修1专题一基础练习
化学必修一专题1 第一单元练习
姓名∶ 班别∶ 座号∶ 分数∶
题号
1
2
3
4
5
6
7
8
9
10
答案
题号
11
12
13
14
15
16
17
18
19
20
答案
单项选择题,每小题5分,满分共1 0 0分,请把正确答案编号填入上表。
1.自从下列哪项发现或学说开始,化学才开始成为一门科学( )
A.阿伏加德罗提出原子——分子学说 B.拉瓦锡确定空气的组成
C.道尔顿提出近代原子学说 D.汤姆逊发现电子
2.1998年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领域作出的重大贡献。他们的工作使实验和理论能够共同协力探讨分子体系的性质,引起整个化学领域正在经历一场革命性的变化。下列说法正确的是( )
A 化学不再是纯实验科学 B 化学不再需要实验
C 化学不做实验,就什么都不知道 D 未来化学的方向还是经验化
3.(2005年高考上海卷)以下命题,违背化学变化规律的是
A.石墨制成金刚石 B.煤加氢变成人造石油
C.水变成汽油 D.干冰气化
4. 首次将量子化概念应用到原子结构,并解释了原子稳定性的科学家是( )
A. 道尔顿 B. 爱因斯坦 C. 玻尔 D. 普朗克
5. 在饮用水中添加含钙、镁、锌、硒等的矿物质,可以改善人体营养,增强体质。其中的“钙、镁、锌、硒”是指( )
A.分子 B.原子 C.离子 D.元素
6. 下列说法正确的是 ( (
A.原子是不可再分的粒子
B.相对原子质量就是原子的实际质量
C.分子是保持物质性质的最小粒子
D.与元素化学性质关系密切的是原子的最外层电子数
7. 下列说法错误的是 ( )
A.铅笔不含铅 B.水银不含银 C.白金不是金 D.火碱不是碱
8. 下列现象能证明分子在化学变化中可分的是 ( (
A( 100 mL水和100 mL酒精混合后总体积小于200 mL
B( 打开盛装浓盐酸瓶盖,浓盐酸逐渐减少
C( 气态氧在加压降温时变为淡蓝色的液态氧
D( 在1000℃时,甲烷可分解为石墨和氢气
9.下图是表示物质分子的示意图,图中“●”和“○”分别表示两种含有不同质子数的原子,则图中表示单质的是 ( )
A、 B、 C、 D、
10.在原子中,下列关系中一定正确的是 ( (
A( 质子数=核电荷数 B( 相对原子质量=质子数+中子数
C( 质子数≠中子数 D( 相对原子质量=质子数+核外电子数
11. H、D、T、H+可以用来表示( )
A.同一种原子 B.化学性质不同的氢原子
C.氢元素 D.氢的四种核素
12. (2005年高考辽宁文理综合)在下列分子中,电子总数最少的是
A H2S B O2 C CO D NO
13. 电子数相等的微粒叫等电子体,下列各组微粒属于等电子体的是( )
A. N2O4和NO2 B. CH4 和NH4+
C. Al3+ 和 Al D. NO 和CO
14. 已知元素R有某种同位素的氯化物RClX,该氯化物中R微粒核内中子数为Y,核外电子数为Z,该同位素的符号为 ( )
A. B. C. D.
15. (2005年高考辽宁文理综合)关于同一种元素的原子或离子,下列叙述正确的是
A 原子半径比阴离子半径小
B 原子半径比阴离子半径大
C 原子半径比阳离子半径小
D 带正电荷多的阳离子半径比带正电荷少的阳离子半径大
16. (2005年高考上海卷)下列离子中,电子数大于质子数且质子数大于中子数的是
A.D3O+ B.Li+ C.OD— D.OH—
17. 一个12C原子的质量为aKg,一个12C16O2 分子的质量为bkg,若以12C16O2中的一个氧原子质量的1/16作为相对原子质量标准,则 12C16O2 的相对分子质量为∶
A、32b/a-b B、32b/b-a C、16b/b-a D、8b/b-a
18. 钛(Ti)金属常被称为未来钢铁。钛元素的同位素、、、、中,中子数不可能为 ( )
A 30 B 28 C 26 D 24
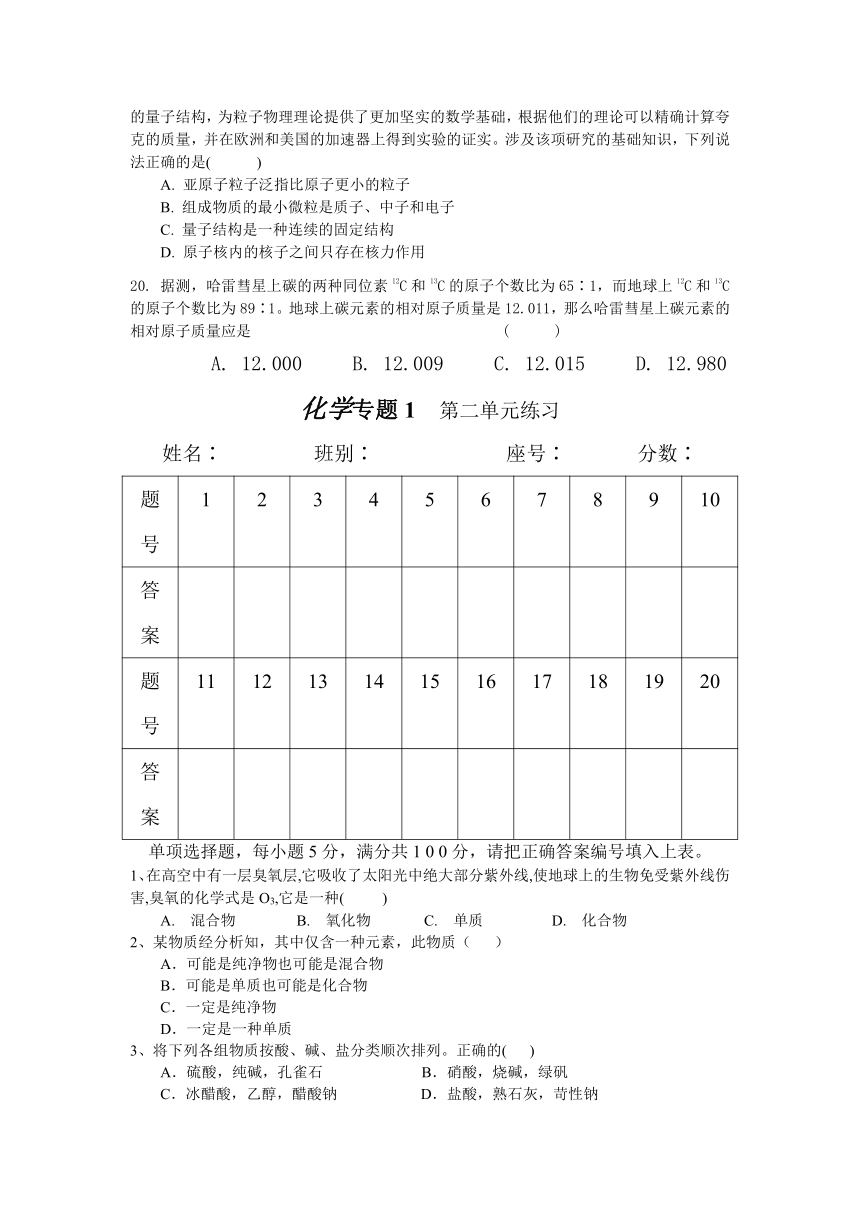
19. 1999年诺贝尔物理学奖授予两位荷兰科学家,他们研究了亚原子粒子之间电弱相互作用的量子结构,为粒子物理理论提供了更加坚实的数学基础,根据他们的理论可以精确计算夸克的质量,并在欧洲和美国的加速器上得到实验的证实。涉及该项研究的基础知识,下列说法正确的是( )
A. 亚原子粒子泛指比原子更小的粒子
B. 组成物质的最小微粒是质子、中子和电子
C. 量子结构是一种连续的固定结构
D. 原子核内的核子之间只存在核力作用
20. 据测,哈雷彗星上碳的两种同位素12C和13C的原子个数比为65∶1,而地球上12C和13C的原子个数比为89∶1。地球上碳元素的相对原子质量是12.011,那么哈雷彗星上碳元素的相对原子质量应是 ( )
A. 12.000 B. 12.009 C. 12.015 D. 12.980
化学专题1 第二单元练习
姓名∶ 班别∶ 座号∶ 分数∶
题号
1
2
3
4
5
6
7
8
9
10
答案
题号
11
12
13
14
15
16
17
18
19
20
答案
单项选择题,每小题5分,满分共1 0 0分,请把正确答案编号填入上表。
1、在高空中有一层臭氧层,它吸收了太阳光中绝大部分紫外线,使地球上的生物免受紫外线伤害,臭氧的化学式是O3,它是一种( )
A. 混合物 B. 氧化物 C. 单质 D. 化合物
2、某物质经分析知,其中仅含一种元素,此物质( )
A.可能是纯净物也可能是混合物
B.可能是单质也可能是化合物
C.一定是纯净物
D.一定是一种单质
3、将下列各组物质按酸、碱、盐分类顺次排列。正确的( )
A.硫酸,纯碱,孔雀石 B.硝酸,烧碱,绿矾
C.冰醋酸,乙醇,醋酸钠 D.盐酸,熟石灰,苛性钠
4、据报道,2003年12月26日,重庆开县发生了天然气矿井“井喷”事件,喷出的气体主要成分是甲烷,还含有硫化氢(H2S),氰化氢(HCN)等多种有毒气体,造成290多人中毒死亡。你认为喷出的气体是 ( )
一种纯净物
全部由无机化合物组成的混合物
全部由有机化合物组成的混合物
由无机化合物和有机化合物组成的混合物
5、中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700℃时制造出纳米级金刚石粉末。该成果发表在世界权威的《科学》杂志上,立刻被科学家们高度评价为“稻草变黄金”。同学们对此有下列一些理解,其中错误的是( )
A、金刚石属于金属单质 B、制造过程中元素种类没有改变
C、CCl4是一种化合物 D、这个反应是置换反应
6.下列叙述中,你认为科学的是( )
A. 某广告语:本饮料纯属天然物质,不含任何化学成分 B、到城乡结合处燃放鞭炮,可避免污染环境 C、水在地球上分布很广,淡水资源取之不尽,用之不竭 D、大气中二氧化碳含量的增多是造成“温室效应”的主要原因
7.下列关于化学反应类型的叙述中,正确的是( )
A. 凡是生成盐和水的反应都是中和反应 B、复分解反应一定没有单质参加
C、生成一种单质和一种化合物的反应一定是置换反应
D、分解反应的生成物一定有单质
8、下列物质中,与0.3moLH2O含相同氢原子数的物质是( )
A、0.3moLHNO3 B、3.612×1023个HNO3分子
C、0.1moLH3PO4 D、0.2moLCH4
9、等质量的下列物质中,所含分子数最少的是( )
A、Cl2 B、 HCl C、Br2 D、 HBr
10、1mol Na转变为Na+时失去的电子数为( )
A、3.01×1023 B、6.02×1023 C、1.204×1023 D、6.02×10—23
11.NA为阿伏加德罗常数,下列叙述正确的是( )
A、80g硝酸铵中含有氮原子数为NA B、0.lmolN5+离子中所含的电子数为34 NA
C、 2mol金属铝与足量的盐酸反应,共失去了4NA个电子
D、16 g氧气和16 g臭氧所含的原子数均为NA
12、相同状况下,下列气体所占体积最大的是( )
A、80g SO2 B、16g O2 C、32g H2S D、3g H2
3、在相同条件下,下列各组气体中,分子数一定相同的是( )
A、14g N2和32g O2 B、34g NH3和4g H2
C、2L CO2和2L H2O D、11.2L O2和0.5mol O2
14.等体积的两容器内,一个盛一氧化氮,另一个盛氮气和氧气的混合气体,若容器内温度、压强相同,则两容器内所盛气体一定具有相同的
A、原子总数 B、质子总数 C、微粒总数 D、质量
15、a mol氢气分子和a mol氦气分子一定具有相同的( )
A、原子数 B、物质的量和质子数 C、质子数和体积 D、体积和核电荷数
16、用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A、含有 NA个氦原子的氦气在标准状况下的体积约为11.2L
B、25℃,1.01×105Pa,64g SO2中含有的原子数为3NA
C、在常温常压下,11.2L Cl2含有的分子数为0.5NA
D、在标准状况下,11.2L H2O含有的分子数为0.5NA
17.用特殊方法把固体物质加工到纳米级(1-100nm,1nm=10-9m)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的微粒直径和这种粒子具有相同数量级的是( )
A.溶液 B.悬浊液 C.胶体 D.乳浊液
18.“摇摇冰”是一种即用即冷的饮料。吸食时将饮料罐隔离层中的化学物质和水混合后摇动即会制冷。该化学物质是 ( )
A.氯化钠 B.固体硝酸铵
C.固体氢氧化钠 D.生石灰
19.下列关于胶体的叙述不正确的是( )
A.胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9 ~ 10-7m之间
B.光线透过胶体时,胶体中可发生丁达尔效应
C.用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同
D.Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的
20.下列现象与胶体无关的是( )
日常生活中看到的烟、云、雾
向豆浆中加入石膏制得可口的豆腐
FeCl3溶液呈现棕黄色
向沸水中逐滴加入FeCl3 稀溶液,得到红褐色透明的分散系
化学专题一复习第三次练习
姓名∶ 班别∶ 座号∶ 分数∶
题号
1
2
3
4
5
6
7
8
9
10
答案
题号
11
12
13
14
15
16
17
18
19
20
答案
选择题∶每小题只有一个选项符合题意,每小题5分,满分100分。
1、下列叙述正确的是 ( )
A、同温同压下,相同体积的物质,其物质的量一定相等
B、任何条件下,等物质的量的甲烷和一氧化碳所含的分子数一定相等
C、1L一氧化碳气体一定比1L氧气的质量小
D、一氧化碳气体和氮气,若体积相等,则质量一定相等
2、下列有关仪器刻度位置的叙述正确的是 ( )
A、容量瓶的体积标线刻在瓶颈上 B、量筒的"0"标线在中间
C、量筒最下端刻有"0"标线 D、托盘天平刻度尺有"0"标线,刻在尺的中间
3、铅笔芯的主要成分是石墨和黏土,这些物质按照不同的比例加以混和、压制,就可以制成铅笔芯。如果铅笔芯质量的一半成分是石墨,且用铅笔写一个字消耗的质量约为1mg。那么一个铅笔字含有的碳原子数约为( )
A、2.5×1019个 B、2.5×1022个 C、5×1019个 D、 5×1022个
4、在强酸性溶液中能大量共存的无色透明离子组是( )
A、K+、Na+、NO3-、Fe3+ B、Mg2+、Na+、Cl-、SO42-
C、K+、Na十、Br-、Cu2+ D、Na十、Ba2+、OH-、SO42-
5、下列贮存化学试剂的方法正确的是( )
A、新制的氯水保存在棕色广口瓶中,并放在阴凉处
B、用做感光片的溴化银贮存在无色试剂瓶中
C、烧碱溶液放在带磨口玻璃塞的试剂瓶中
D、金属钠保存在煤油中
6、能正确表示下列反应的离子方程式是( )
A、Ba(OH)2与稀H2SO4反应 Ba2++OH-+H++SO42-==BaSO4↓+H2O
B、饱和碳酸钠溶液中通入足量CO2 CO32-+H2O+CO2==2HCO3-
C、C12与NaOH溶液反应 Cl2+2OH-==C1-+C1O—+H2O
D、把金属铁放入稀硫酸中 2Fe +6H+==2Fe3++3H2↑
7、在实验室中,对下列事故或药品的处理正确的是( )
A、有大量的氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场
B、金属钠着火燃烧时,用泡沫灭火器灭火
C、少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
D、含硫酸的废液倒入水槽,用水冲入下水道
8 下列各组离子能在同一溶液里大量共存的是 ( )
A.Na+、Al3+、Cl-、AlO2- B.K+、H+、SO42-、AlO2-
C.Na+、Al3+、NO3-、OH- D.K+、Na+、AlO2-、CO32-
9.等体积的AlCl3和NaOH两种溶液混合后,沉淀物中含铝的质量与溶液中含铝的质量相等,则AlCl3和NaOH两种溶液的物质的量浓度之比是 ( )
A.1∶3或2∶7 B.2∶3或2∶7 C.1∶4或.2∶3 D.2∶7或1∶3
10、配置250mL0.5mol/L的NaOH溶液,有下列仪器:①托盘天平、②量筒、③烧杯、④玻璃棒、⑤漏斗、⑥500mL容量瓶、⑦药匙、⑧250mL容量瓶、⑨胶头滴管、⑩坩埚,需要用到的仪器有( )
A、①③④⑥⑨⑩ B、①④⑦⑧⑨⑩ C、①③④⑦⑧⑨ D、①②④⑤⑧⑨
11、在100克浓度为18mol/L、密度为ρ(g/cm3)的浓硫酸中加入一定量的水稀释成9mol/L的硫酸,则加水的体积为(提示:硫酸溶液越浓,其密度越大)( )
A、小于100mL B、等于100mL
C、大于100mL D、等于100/ρmL
12、质量分数为n的NaOH溶液,其物质的量浓度a mol/L为,加热蒸发水使其质量分数变为2n,此时,该溶液中的物质的量浓度为b mol/L,则a与b的关系正确的是( )
A、b=2a B、a=2b C、b﹥2a D、b﹤2a
13.与100mL0.1mol/L(NH4)2SO4溶液中NH4+离子浓度相同的是( )
A..10mL 1mol/L (NH4)2SO4溶液 B.100mL 0.1mol/L NH4Cl溶液
C.10mL0.1mol/L(NH4)2SO4溶液 D.200mL 0.1mol/L NH4NO3溶液
14.将钠、镁、铝各0.3mol 分别放入100mL 1 mol/L 的盐酸中,同温同压下产生的气体体积比是( )
A.1:2:3 B.6:3:2 C.3:1:1 D.1:1:1
15.实验室里需用480mL 0.1mol·L-1的硫酸铜溶液,现选取500mL容量瓶进行配制,以下操作正确的是( )。
A..称取7.68g硫酸铜,加入 500mL水 B..称取12.0g胆矾配成500mL溶液
C..称取8.0g硫酸铜,加入500mL水 D.称取12.5g胆矾配成500mL溶液
16.配制1L1mol/LNaOH溶液,需进行下列操作:①在干燥洁净的滤纸上准确称量40g固体氢氧化钠,并转入洗净的烧杯中;②往烧杯中加入300mL蒸馏水,用玻璃棒搅拌使之完全溶解;③立即将烧杯中的溶液沿玻璃棒注入1000mL容量瓶中;④倒完烧杯中的溶液后,接着将容量瓶振荡混匀,小心加蒸馏水至液面接近刻度1cm~2cm处;⑤用胶头滴管加蒸馏水,使溶液凹液面恰好与刻线相切;⑥塞紧瓶塞,振荡摇匀,静置,此时凹液面低于刻线,再滴加蒸馏水至刻度线。其中正确的是( )。
A. ①②③ B. ④⑥ C. ②④⑤ D. ②⑤
17.下列有关摩尔使用的说法中不正确的是( )
A.1摩尔氧原子 B.1摩尔氧分子 C.1摩尔氧气 D.1摩尔氧
18.下列叙述正确的是( )
A.1 mol H2SO4 的质量为98 g B.H2SO4的摩尔质量为98 g
C.9.8 g H2SO4含有NA个H2SO4分子 D.6.02×1023个H2SO4分子的质量为9.8 g
19.下列说法正确的是( )
A.气体摩尔体积就是22.4L/mol
B.非标准状况下,1mol任何气体的体积不可能为22.4L
C. 22.4L任何气体都含有约6.02×1023个分子
D.1molH2和O2的混合气体在标准状况下的体积约22.4L
20. 下列物质中属于电解质的是( )
A. 铁 B. 氯化氢 C. 五氧化二氮 D. 酒精
化学专题1 第三单元练习
班别∶ 姓名∶ 座号∶ 分数∶
题号
1
2
3
4
5
6
7
8
9
10
答案
题号
11
12
13
14
15
16
17
18
19
20
答案
单项选择题,每小题5分,满分共1 0 0分,请把正确答案编号填入上表。
1.下列分离混合物的操作中,必须加热的是 ( )
A. 过滤 B.升华 C.结晶 D.分液
2.用天然水制取纯度较高的水通常采用的方法是 ( )
A( 煮沸并加入石灰纯碱 B. 加明矾搅拌
C. 进行多次过滤 D( 蒸馏
3.下列各组物质仅用蒸馏水不能鉴别的是 ( )
A.汽油、酒精、硝基苯(不溶于水的液体,ρ>1g·cm-3 )
B.食盐、烧碱、硝酸铵
C.蔗糖、硫酸铜粉末、碳酸钙粉末
D.氧化铜、二氧化锰、活性炭
4.下列各组仪器:①漏斗;②容量瓶;③滴定管;④分液漏斗;⑤天平;⑥量筒;⑦胶头滴管;⑧蒸馏烧瓶。常用于物质分离的是 ( )
A.①③⑦ B.②⑥⑦
C.①④⑧ D.④⑥⑧
5.下列实验操作:① 过滤 ② 分液 ③ 萃取 ④ 蒸馏 ⑤ 分馏。不能用于分离相互混溶的溶液的是 ( )
A( ③和④ B. ①和② C( ③、④和⑤ D. ①、②和③
6.下列除杂质的方法不可行的是( )
A.用NaOH溶液除去CO2中混有的SO2
B.将混合气体通过灼热的铜网除去N2中的少量O2
C.用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水
D.用盐酸除去AgCl中少量的Ag2CO3
7.欲将NaCl中混有的少量碳铵和砂子(SiO2(除去,所进行的必要分离方法是 ( )
A.溶解、过滤、萃取 B.加热、溶解、过滤
C. 升华、萃取、分液 D.盐析、渗析、纸上层析
8.今有下列仪器和用品:铁架台、铁圈、三脚架、烧杯、漏斗、石棉网、酒精灯、玻璃棒、量筒、蒸发皿、滤纸、火柴。从缺乏必要的仪器和用品的角度考虑,不能进行的分离操作是 ( )
A.过滤 B.升华 C. 萃取 D. 蒸发
9.某工厂排出的废液中含有Ba2+、Ag+、Cu2+,用①Na2CO3溶液,②NaOH溶液,③盐酸三种试剂将它们逐一沉淀并加以分离,加入试剂的正确顺序是( )
A.②③① B.③②① C.①②③ D.③①②
10.下列各组物质中不易用物理性质区别的是( )
A.苯和四氯化碳 B.氯化铵和硝酸铵晶体
C.酒精和汽油 D.碘和高锰酸钾固体
11.下列分离提纯物质的操作中,错误的是 ( )
A.用过滤的方法除去食盐中的泥沙
B.用渗析的方法除去淀粉中的氯离子
C.用结晶的方法分离氯化钠和硝酸钾
D.用加热的方法除去碳铵中混有的碘
12.进行焰色反应实验时,通常用来洗涤铂丝的是( )
A.硫酸 B.烧碱溶液 C.稀盐酸 D.蒸馏水
13.可用来鉴别氯化铁溶液和氢氧化铁溶胶的简便方法是( )
A.过滤 B.渗析 C.电泳 D.丁达尔效应
14.某校学生用化学知识解决生活中的问题,下列家庭小实验不合理的是( )
A.用食醋除去暖水瓶中的薄层水垢 B.用米汤检验含碘盐中的碘酸钾(KIO3)
C.用食用碱(Na2CO3)溶液洗涤餐具上的油污
D.用灼烧并闻气味的方法区别纯棉织物和纯毛织物
15.某物质灼烧时,焰色反应为黄色,下列判断中正确的是( )
A.该物质一定是钠的化合物 B.该物质一定含钠元素
C.该物质含有钾元素 D.该物质一定是金属钠
16.下列有关判断中,正确的是 ( )
A.可用澄清石灰水来区分二氧化碳和二氧化硫
B.可用无水硫酸铜检验酒精中是否含少量水
C.通过灼热的CuO,能使固体由黑变红的气体一定是H2
D.用pH试纸来鉴别盐酸和醋酸
17.能把Na2SO4、NH4NO3、KCl、(NH4)2SO4四瓶无色溶液加以区别的一种试剂是(必要时可以加热)( )
A.BaCl2 B.NaOH C.Ba(OH)2 D.AgNO3
18.对于某些离子的检验及结论一定正确的是( )
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32—
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42—
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
19.下列除去杂质的方法正确的是( )
A.除去N2中的少量O2:通过灼热的CuO粉末
B.除去CO2中的少量HCl:通入Na2CO3溶液
C.除去KCl溶液中的少量K2CO3:加入适量的盐酸
D.除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤
20.某气体可能含有CO、CO2、NH3、HCl、H2和水蒸气中的一种或几种,依次通过澄清石灰水(无浑浊现象)、氢氧化钡溶液(有浑浊现象)、浓硫酸、灼热的氧化铜(变红)和无水CuSO4(变蓝),判断该气体中一定有( )
A.HCl、CO2、H2 B.CO、H2、H2O C.CO、H2、NH3 D.HCl、CO、H2O
化学第一次练习参考答案
题号
1
2
3
4
5
6
7
8
9
10
答案
C
A
C
C
D
D
D
D
C
A
题号
11
12
13
14
15
16
17
18
19
20
答案
C
C
B
D
A
D
B
A
A
C
第二次练习参考答案
题号
1
2
3
4
5
6
7
8
9
10
答案
C
A
B
D
A
D
B
B
C
B
题号
11
12
13
14
15
16
17
18
19
20
答案
D
D
B
A
B
B
C
D
C
C
第三次练习参考答案
题号
1
2
3
4
5
6
7
8
9
10
答案
B
A
A
B
D
C
A
D
B
C
题号
11
12
13
14
15
16
17
18
19
20
答案
A
C
C
C
D
D
D
A
D
B
化学第4次练习参考答案
题号
1
2
3
4
5
6
7
8
9
10
答案
B
D
D
C
B
A
B
C
B
B
题号
11
12
13
14
15
16
17
18
19
20
答案
D
C
D
B
B
B
C
C
C
A
化学必修一专题1 第一单元练习
姓名∶ 班别∶ 座号∶ 分数∶
题号
1
2
3
4
5
6
7
8
9
10
答案
题号
11
12
13
14
15
16
17
18
19
20
答案
单项选择题,每小题5分,满分共1 0 0分,请把正确答案编号填入上表。
1.自从下列哪项发现或学说开始,化学才开始成为一门科学( )
A.阿伏加德罗提出原子——分子学说 B.拉瓦锡确定空气的组成
C.道尔顿提出近代原子学说 D.汤姆逊发现电子
2.1998年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领域作出的重大贡献。他们的工作使实验和理论能够共同协力探讨分子体系的性质,引起整个化学领域正在经历一场革命性的变化。下列说法正确的是( )
A 化学不再是纯实验科学 B 化学不再需要实验
C 化学不做实验,就什么都不知道 D 未来化学的方向还是经验化
3.(2005年高考上海卷)以下命题,违背化学变化规律的是
A.石墨制成金刚石 B.煤加氢变成人造石油
C.水变成汽油 D.干冰气化
4. 首次将量子化概念应用到原子结构,并解释了原子稳定性的科学家是( )
A. 道尔顿 B. 爱因斯坦 C. 玻尔 D. 普朗克
5. 在饮用水中添加含钙、镁、锌、硒等的矿物质,可以改善人体营养,增强体质。其中的“钙、镁、锌、硒”是指( )
A.分子 B.原子 C.离子 D.元素
6. 下列说法正确的是 ( (
A.原子是不可再分的粒子
B.相对原子质量就是原子的实际质量
C.分子是保持物质性质的最小粒子
D.与元素化学性质关系密切的是原子的最外层电子数
7. 下列说法错误的是 ( )
A.铅笔不含铅 B.水银不含银 C.白金不是金 D.火碱不是碱
8. 下列现象能证明分子在化学变化中可分的是 ( (
A( 100 mL水和100 mL酒精混合后总体积小于200 mL
B( 打开盛装浓盐酸瓶盖,浓盐酸逐渐减少
C( 气态氧在加压降温时变为淡蓝色的液态氧
D( 在1000℃时,甲烷可分解为石墨和氢气
9.下图是表示物质分子的示意图,图中“●”和“○”分别表示两种含有不同质子数的原子,则图中表示单质的是 ( )
A、 B、 C、 D、
10.在原子中,下列关系中一定正确的是 ( (
A( 质子数=核电荷数 B( 相对原子质量=质子数+中子数
C( 质子数≠中子数 D( 相对原子质量=质子数+核外电子数
11. H、D、T、H+可以用来表示( )
A.同一种原子 B.化学性质不同的氢原子
C.氢元素 D.氢的四种核素
12. (2005年高考辽宁文理综合)在下列分子中,电子总数最少的是
A H2S B O2 C CO D NO
13. 电子数相等的微粒叫等电子体,下列各组微粒属于等电子体的是( )
A. N2O4和NO2 B. CH4 和NH4+
C. Al3+ 和 Al D. NO 和CO
14. 已知元素R有某种同位素的氯化物RClX,该氯化物中R微粒核内中子数为Y,核外电子数为Z,该同位素的符号为 ( )
A. B. C. D.
15. (2005年高考辽宁文理综合)关于同一种元素的原子或离子,下列叙述正确的是
A 原子半径比阴离子半径小
B 原子半径比阴离子半径大
C 原子半径比阳离子半径小
D 带正电荷多的阳离子半径比带正电荷少的阳离子半径大
16. (2005年高考上海卷)下列离子中,电子数大于质子数且质子数大于中子数的是
A.D3O+ B.Li+ C.OD— D.OH—
17. 一个12C原子的质量为aKg,一个12C16O2 分子的质量为bkg,若以12C16O2中的一个氧原子质量的1/16作为相对原子质量标准,则 12C16O2 的相对分子质量为∶
A、32b/a-b B、32b/b-a C、16b/b-a D、8b/b-a
18. 钛(Ti)金属常被称为未来钢铁。钛元素的同位素、、、、中,中子数不可能为 ( )
A 30 B 28 C 26 D 24
19. 1999年诺贝尔物理学奖授予两位荷兰科学家,他们研究了亚原子粒子之间电弱相互作用的量子结构,为粒子物理理论提供了更加坚实的数学基础,根据他们的理论可以精确计算夸克的质量,并在欧洲和美国的加速器上得到实验的证实。涉及该项研究的基础知识,下列说法正确的是( )
A. 亚原子粒子泛指比原子更小的粒子
B. 组成物质的最小微粒是质子、中子和电子
C. 量子结构是一种连续的固定结构
D. 原子核内的核子之间只存在核力作用
20. 据测,哈雷彗星上碳的两种同位素12C和13C的原子个数比为65∶1,而地球上12C和13C的原子个数比为89∶1。地球上碳元素的相对原子质量是12.011,那么哈雷彗星上碳元素的相对原子质量应是 ( )
A. 12.000 B. 12.009 C. 12.015 D. 12.980
化学专题1 第二单元练习
姓名∶ 班别∶ 座号∶ 分数∶
题号
1
2
3
4
5
6
7
8
9
10
答案
题号
11
12
13
14
15
16
17
18
19
20
答案
单项选择题,每小题5分,满分共1 0 0分,请把正确答案编号填入上表。
1、在高空中有一层臭氧层,它吸收了太阳光中绝大部分紫外线,使地球上的生物免受紫外线伤害,臭氧的化学式是O3,它是一种( )
A. 混合物 B. 氧化物 C. 单质 D. 化合物
2、某物质经分析知,其中仅含一种元素,此物质( )
A.可能是纯净物也可能是混合物
B.可能是单质也可能是化合物
C.一定是纯净物
D.一定是一种单质
3、将下列各组物质按酸、碱、盐分类顺次排列。正确的( )
A.硫酸,纯碱,孔雀石 B.硝酸,烧碱,绿矾
C.冰醋酸,乙醇,醋酸钠 D.盐酸,熟石灰,苛性钠
4、据报道,2003年12月26日,重庆开县发生了天然气矿井“井喷”事件,喷出的气体主要成分是甲烷,还含有硫化氢(H2S),氰化氢(HCN)等多种有毒气体,造成290多人中毒死亡。你认为喷出的气体是 ( )
一种纯净物
全部由无机化合物组成的混合物
全部由有机化合物组成的混合物
由无机化合物和有机化合物组成的混合物
5、中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700℃时制造出纳米级金刚石粉末。该成果发表在世界权威的《科学》杂志上,立刻被科学家们高度评价为“稻草变黄金”。同学们对此有下列一些理解,其中错误的是( )
A、金刚石属于金属单质 B、制造过程中元素种类没有改变
C、CCl4是一种化合物 D、这个反应是置换反应
6.下列叙述中,你认为科学的是( )
A. 某广告语:本饮料纯属天然物质,不含任何化学成分 B、到城乡结合处燃放鞭炮,可避免污染环境 C、水在地球上分布很广,淡水资源取之不尽,用之不竭 D、大气中二氧化碳含量的增多是造成“温室效应”的主要原因
7.下列关于化学反应类型的叙述中,正确的是( )
A. 凡是生成盐和水的反应都是中和反应 B、复分解反应一定没有单质参加
C、生成一种单质和一种化合物的反应一定是置换反应
D、分解反应的生成物一定有单质
8、下列物质中,与0.3moLH2O含相同氢原子数的物质是( )
A、0.3moLHNO3 B、3.612×1023个HNO3分子
C、0.1moLH3PO4 D、0.2moLCH4
9、等质量的下列物质中,所含分子数最少的是( )
A、Cl2 B、 HCl C、Br2 D、 HBr
10、1mol Na转变为Na+时失去的电子数为( )
A、3.01×1023 B、6.02×1023 C、1.204×1023 D、6.02×10—23
11.NA为阿伏加德罗常数,下列叙述正确的是( )
A、80g硝酸铵中含有氮原子数为NA B、0.lmolN5+离子中所含的电子数为34 NA
C、 2mol金属铝与足量的盐酸反应,共失去了4NA个电子
D、16 g氧气和16 g臭氧所含的原子数均为NA
12、相同状况下,下列气体所占体积最大的是( )
A、80g SO2 B、16g O2 C、32g H2S D、3g H2
3、在相同条件下,下列各组气体中,分子数一定相同的是( )
A、14g N2和32g O2 B、34g NH3和4g H2
C、2L CO2和2L H2O D、11.2L O2和0.5mol O2
14.等体积的两容器内,一个盛一氧化氮,另一个盛氮气和氧气的混合气体,若容器内温度、压强相同,则两容器内所盛气体一定具有相同的
A、原子总数 B、质子总数 C、微粒总数 D、质量
15、a mol氢气分子和a mol氦气分子一定具有相同的( )
A、原子数 B、物质的量和质子数 C、质子数和体积 D、体积和核电荷数
16、用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A、含有 NA个氦原子的氦气在标准状况下的体积约为11.2L
B、25℃,1.01×105Pa,64g SO2中含有的原子数为3NA
C、在常温常压下,11.2L Cl2含有的分子数为0.5NA
D、在标准状况下,11.2L H2O含有的分子数为0.5NA
17.用特殊方法把固体物质加工到纳米级(1-100nm,1nm=10-9m)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的微粒直径和这种粒子具有相同数量级的是( )
A.溶液 B.悬浊液 C.胶体 D.乳浊液
18.“摇摇冰”是一种即用即冷的饮料。吸食时将饮料罐隔离层中的化学物质和水混合后摇动即会制冷。该化学物质是 ( )
A.氯化钠 B.固体硝酸铵
C.固体氢氧化钠 D.生石灰
19.下列关于胶体的叙述不正确的是( )
A.胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9 ~ 10-7m之间
B.光线透过胶体时,胶体中可发生丁达尔效应
C.用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同
D.Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的
20.下列现象与胶体无关的是( )
日常生活中看到的烟、云、雾
向豆浆中加入石膏制得可口的豆腐
FeCl3溶液呈现棕黄色
向沸水中逐滴加入FeCl3 稀溶液,得到红褐色透明的分散系
化学专题一复习第三次练习
姓名∶ 班别∶ 座号∶ 分数∶
题号
1
2
3
4
5
6
7
8
9
10
答案
题号
11
12
13
14
15
16
17
18
19
20
答案
选择题∶每小题只有一个选项符合题意,每小题5分,满分100分。
1、下列叙述正确的是 ( )
A、同温同压下,相同体积的物质,其物质的量一定相等
B、任何条件下,等物质的量的甲烷和一氧化碳所含的分子数一定相等
C、1L一氧化碳气体一定比1L氧气的质量小
D、一氧化碳气体和氮气,若体积相等,则质量一定相等
2、下列有关仪器刻度位置的叙述正确的是 ( )
A、容量瓶的体积标线刻在瓶颈上 B、量筒的"0"标线在中间
C、量筒最下端刻有"0"标线 D、托盘天平刻度尺有"0"标线,刻在尺的中间
3、铅笔芯的主要成分是石墨和黏土,这些物质按照不同的比例加以混和、压制,就可以制成铅笔芯。如果铅笔芯质量的一半成分是石墨,且用铅笔写一个字消耗的质量约为1mg。那么一个铅笔字含有的碳原子数约为( )
A、2.5×1019个 B、2.5×1022个 C、5×1019个 D、 5×1022个
4、在强酸性溶液中能大量共存的无色透明离子组是( )
A、K+、Na+、NO3-、Fe3+ B、Mg2+、Na+、Cl-、SO42-
C、K+、Na十、Br-、Cu2+ D、Na十、Ba2+、OH-、SO42-
5、下列贮存化学试剂的方法正确的是( )
A、新制的氯水保存在棕色广口瓶中,并放在阴凉处
B、用做感光片的溴化银贮存在无色试剂瓶中
C、烧碱溶液放在带磨口玻璃塞的试剂瓶中
D、金属钠保存在煤油中
6、能正确表示下列反应的离子方程式是( )
A、Ba(OH)2与稀H2SO4反应 Ba2++OH-+H++SO42-==BaSO4↓+H2O
B、饱和碳酸钠溶液中通入足量CO2 CO32-+H2O+CO2==2HCO3-
C、C12与NaOH溶液反应 Cl2+2OH-==C1-+C1O—+H2O
D、把金属铁放入稀硫酸中 2Fe +6H+==2Fe3++3H2↑
7、在实验室中,对下列事故或药品的处理正确的是( )
A、有大量的氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场
B、金属钠着火燃烧时,用泡沫灭火器灭火
C、少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
D、含硫酸的废液倒入水槽,用水冲入下水道
8 下列各组离子能在同一溶液里大量共存的是 ( )
A.Na+、Al3+、Cl-、AlO2- B.K+、H+、SO42-、AlO2-
C.Na+、Al3+、NO3-、OH- D.K+、Na+、AlO2-、CO32-
9.等体积的AlCl3和NaOH两种溶液混合后,沉淀物中含铝的质量与溶液中含铝的质量相等,则AlCl3和NaOH两种溶液的物质的量浓度之比是 ( )
A.1∶3或2∶7 B.2∶3或2∶7 C.1∶4或.2∶3 D.2∶7或1∶3
10、配置250mL0.5mol/L的NaOH溶液,有下列仪器:①托盘天平、②量筒、③烧杯、④玻璃棒、⑤漏斗、⑥500mL容量瓶、⑦药匙、⑧250mL容量瓶、⑨胶头滴管、⑩坩埚,需要用到的仪器有( )
A、①③④⑥⑨⑩ B、①④⑦⑧⑨⑩ C、①③④⑦⑧⑨ D、①②④⑤⑧⑨
11、在100克浓度为18mol/L、密度为ρ(g/cm3)的浓硫酸中加入一定量的水稀释成9mol/L的硫酸,则加水的体积为(提示:硫酸溶液越浓,其密度越大)( )
A、小于100mL B、等于100mL
C、大于100mL D、等于100/ρmL
12、质量分数为n的NaOH溶液,其物质的量浓度a mol/L为,加热蒸发水使其质量分数变为2n,此时,该溶液中的物质的量浓度为b mol/L,则a与b的关系正确的是( )
A、b=2a B、a=2b C、b﹥2a D、b﹤2a
13.与100mL0.1mol/L(NH4)2SO4溶液中NH4+离子浓度相同的是( )
A..10mL 1mol/L (NH4)2SO4溶液 B.100mL 0.1mol/L NH4Cl溶液
C.10mL0.1mol/L(NH4)2SO4溶液 D.200mL 0.1mol/L NH4NO3溶液
14.将钠、镁、铝各0.3mol 分别放入100mL 1 mol/L 的盐酸中,同温同压下产生的气体体积比是( )
A.1:2:3 B.6:3:2 C.3:1:1 D.1:1:1
15.实验室里需用480mL 0.1mol·L-1的硫酸铜溶液,现选取500mL容量瓶进行配制,以下操作正确的是( )。
A..称取7.68g硫酸铜,加入 500mL水 B..称取12.0g胆矾配成500mL溶液
C..称取8.0g硫酸铜,加入500mL水 D.称取12.5g胆矾配成500mL溶液
16.配制1L1mol/LNaOH溶液,需进行下列操作:①在干燥洁净的滤纸上准确称量40g固体氢氧化钠,并转入洗净的烧杯中;②往烧杯中加入300mL蒸馏水,用玻璃棒搅拌使之完全溶解;③立即将烧杯中的溶液沿玻璃棒注入1000mL容量瓶中;④倒完烧杯中的溶液后,接着将容量瓶振荡混匀,小心加蒸馏水至液面接近刻度1cm~2cm处;⑤用胶头滴管加蒸馏水,使溶液凹液面恰好与刻线相切;⑥塞紧瓶塞,振荡摇匀,静置,此时凹液面低于刻线,再滴加蒸馏水至刻度线。其中正确的是( )。
A. ①②③ B. ④⑥ C. ②④⑤ D. ②⑤
17.下列有关摩尔使用的说法中不正确的是( )
A.1摩尔氧原子 B.1摩尔氧分子 C.1摩尔氧气 D.1摩尔氧
18.下列叙述正确的是( )
A.1 mol H2SO4 的质量为98 g B.H2SO4的摩尔质量为98 g
C.9.8 g H2SO4含有NA个H2SO4分子 D.6.02×1023个H2SO4分子的质量为9.8 g
19.下列说法正确的是( )
A.气体摩尔体积就是22.4L/mol
B.非标准状况下,1mol任何气体的体积不可能为22.4L
C. 22.4L任何气体都含有约6.02×1023个分子
D.1molH2和O2的混合气体在标准状况下的体积约22.4L
20. 下列物质中属于电解质的是( )
A. 铁 B. 氯化氢 C. 五氧化二氮 D. 酒精
化学专题1 第三单元练习
班别∶ 姓名∶ 座号∶ 分数∶
题号
1
2
3
4
5
6
7
8
9
10
答案
题号
11
12
13
14
15
16
17
18
19
20
答案
单项选择题,每小题5分,满分共1 0 0分,请把正确答案编号填入上表。
1.下列分离混合物的操作中,必须加热的是 ( )
A. 过滤 B.升华 C.结晶 D.分液
2.用天然水制取纯度较高的水通常采用的方法是 ( )
A( 煮沸并加入石灰纯碱 B. 加明矾搅拌
C. 进行多次过滤 D( 蒸馏
3.下列各组物质仅用蒸馏水不能鉴别的是 ( )
A.汽油、酒精、硝基苯(不溶于水的液体,ρ>1g·cm-3 )
B.食盐、烧碱、硝酸铵
C.蔗糖、硫酸铜粉末、碳酸钙粉末
D.氧化铜、二氧化锰、活性炭
4.下列各组仪器:①漏斗;②容量瓶;③滴定管;④分液漏斗;⑤天平;⑥量筒;⑦胶头滴管;⑧蒸馏烧瓶。常用于物质分离的是 ( )
A.①③⑦ B.②⑥⑦
C.①④⑧ D.④⑥⑧
5.下列实验操作:① 过滤 ② 分液 ③ 萃取 ④ 蒸馏 ⑤ 分馏。不能用于分离相互混溶的溶液的是 ( )
A( ③和④ B. ①和② C( ③、④和⑤ D. ①、②和③
6.下列除杂质的方法不可行的是( )
A.用NaOH溶液除去CO2中混有的SO2
B.将混合气体通过灼热的铜网除去N2中的少量O2
C.用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水
D.用盐酸除去AgCl中少量的Ag2CO3
7.欲将NaCl中混有的少量碳铵和砂子(SiO2(除去,所进行的必要分离方法是 ( )
A.溶解、过滤、萃取 B.加热、溶解、过滤
C. 升华、萃取、分液 D.盐析、渗析、纸上层析
8.今有下列仪器和用品:铁架台、铁圈、三脚架、烧杯、漏斗、石棉网、酒精灯、玻璃棒、量筒、蒸发皿、滤纸、火柴。从缺乏必要的仪器和用品的角度考虑,不能进行的分离操作是 ( )
A.过滤 B.升华 C. 萃取 D. 蒸发
9.某工厂排出的废液中含有Ba2+、Ag+、Cu2+,用①Na2CO3溶液,②NaOH溶液,③盐酸三种试剂将它们逐一沉淀并加以分离,加入试剂的正确顺序是( )
A.②③① B.③②① C.①②③ D.③①②
10.下列各组物质中不易用物理性质区别的是( )
A.苯和四氯化碳 B.氯化铵和硝酸铵晶体
C.酒精和汽油 D.碘和高锰酸钾固体
11.下列分离提纯物质的操作中,错误的是 ( )
A.用过滤的方法除去食盐中的泥沙
B.用渗析的方法除去淀粉中的氯离子
C.用结晶的方法分离氯化钠和硝酸钾
D.用加热的方法除去碳铵中混有的碘
12.进行焰色反应实验时,通常用来洗涤铂丝的是( )
A.硫酸 B.烧碱溶液 C.稀盐酸 D.蒸馏水
13.可用来鉴别氯化铁溶液和氢氧化铁溶胶的简便方法是( )
A.过滤 B.渗析 C.电泳 D.丁达尔效应
14.某校学生用化学知识解决生活中的问题,下列家庭小实验不合理的是( )
A.用食醋除去暖水瓶中的薄层水垢 B.用米汤检验含碘盐中的碘酸钾(KIO3)
C.用食用碱(Na2CO3)溶液洗涤餐具上的油污
D.用灼烧并闻气味的方法区别纯棉织物和纯毛织物
15.某物质灼烧时,焰色反应为黄色,下列判断中正确的是( )
A.该物质一定是钠的化合物 B.该物质一定含钠元素
C.该物质含有钾元素 D.该物质一定是金属钠
16.下列有关判断中,正确的是 ( )
A.可用澄清石灰水来区分二氧化碳和二氧化硫
B.可用无水硫酸铜检验酒精中是否含少量水
C.通过灼热的CuO,能使固体由黑变红的气体一定是H2
D.用pH试纸来鉴别盐酸和醋酸
17.能把Na2SO4、NH4NO3、KCl、(NH4)2SO4四瓶无色溶液加以区别的一种试剂是(必要时可以加热)( )
A.BaCl2 B.NaOH C.Ba(OH)2 D.AgNO3
18.对于某些离子的检验及结论一定正确的是( )
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32—
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42—
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
19.下列除去杂质的方法正确的是( )
A.除去N2中的少量O2:通过灼热的CuO粉末
B.除去CO2中的少量HCl:通入Na2CO3溶液
C.除去KCl溶液中的少量K2CO3:加入适量的盐酸
D.除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤
20.某气体可能含有CO、CO2、NH3、HCl、H2和水蒸气中的一种或几种,依次通过澄清石灰水(无浑浊现象)、氢氧化钡溶液(有浑浊现象)、浓硫酸、灼热的氧化铜(变红)和无水CuSO4(变蓝),判断该气体中一定有( )
A.HCl、CO2、H2 B.CO、H2、H2O C.CO、H2、NH3 D.HCl、CO、H2O
化学第一次练习参考答案
题号
1
2
3
4
5
6
7
8
9
10
答案
C
A
C
C
D
D
D
D
C
A
题号
11
12
13
14
15
16
17
18
19
20
答案
C
C
B
D
A
D
B
A
A
C
第二次练习参考答案
题号
1
2
3
4
5
6
7
8
9
10
答案
C
A
B
D
A
D
B
B
C
B
题号
11
12
13
14
15
16
17
18
19
20
答案
D
D
B
A
B
B
C
D
C
C
第三次练习参考答案
题号
1
2
3
4
5
6
7
8
9
10
答案
B
A
A
B
D
C
A
D
B
C
题号
11
12
13
14
15
16
17
18
19
20
答案
A
C
C
C
D
D
D
A
D
B
化学第4次练习参考答案
题号
1
2
3
4
5
6
7
8
9
10
答案
B
D
D
C
B
A
B
C
B
B
题号
11
12
13
14
15
16
17
18
19
20
答案
D
C
D
B
B
B
C
C
C
A
