影响化学反应速率的因素
图片预览






文档简介
课件17张PPT。研究化学反应速率的现实意义1、对于实际生产和生活有利的反应,尽量加快
如:工业合成氨气、工业炼铁等
2、对于实际生产和生活不利的反应,尽量减慢
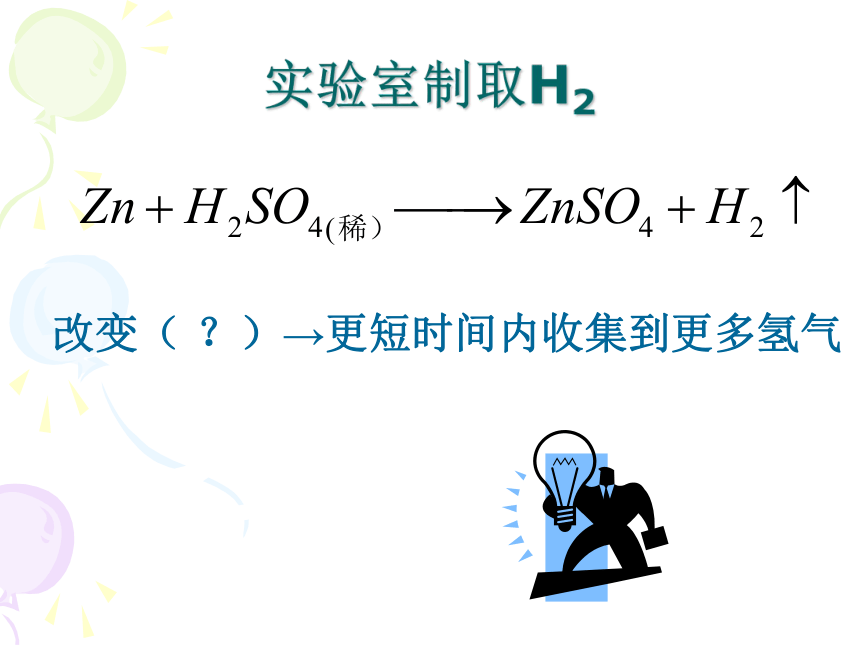
如:食物腐败、钢铁生锈等影响化学反应速率的因素实验室制取H2改变( ?)→更短时间内收集到更多氢气猜测:影响某一特定化学反应快慢的因素压强固体颗粒大小温度其他因素催化剂浓度实验:固体颗粒大小的影响同浓度同体积的盐酸分别与1 g的碳酸钙颗粒和
1 g碳酸钙粉末反应,观察试管上方气球膨胀的快慢(试剂、药品已装入试管和气球)
现象:
粉末状→迅速产生大量气泡→气球迅速膨胀
颗粒状→缓慢产生气泡→气球膨胀较慢 颗粒越小,表面积越大,发生有效碰撞的机会也就越多,反应速率越快。如何解释固体颗粒的影响?Back实验:浓度的影响
Na2S2O3+2HCl→S↓+SO2+2NaCl+H2O
取4个小烧杯中各量取15mL 1mol/L的盐酸
同时将不同浓度的Na2S2O3溶液分别倒入盛有
盐酸的小烧杯中,观察从溶液混合后从澄清到浑
浊的先后加水 A B C D
15mL 10mL 5mL 0mL 5mL 10mL 15mL 20mL
Na2S2O3溶液不同浓度硫代硫酸钠溶液的配制如何解释浓度的影响?在化学上,把能够发生有效碰撞的分子叫活化分子浓度小 浓度大Back压强对反应速率的影响 压强小 压强大Back实验:温度的影响 Na2S2O3+2HCl→S↓+SO2+2NaCl+H2O
同时将同浓度同体积两组溶液在一烧杯中混
合,观察从溶液混合后从澄清到浑浊的先后
温度对反应速率的影响活化分子具有较高的能量,能量不足的分子获取能量后才能变成活化分子温度低 温度高面包保质期:
1月~3月:4天
4月~10月:2天
11月~12月:4天
Back实验:催化剂的影响 同时分别用针筒注入3%的双氧水5mL,观察试
管内现象和针筒活塞的运动不使用催化剂使用
催化剂反应物生成物反应进程能 量Back
如:工业合成氨气、工业炼铁等
2、对于实际生产和生活不利的反应,尽量减慢
如:食物腐败、钢铁生锈等影响化学反应速率的因素实验室制取H2改变( ?)→更短时间内收集到更多氢气猜测:影响某一特定化学反应快慢的因素压强固体颗粒大小温度其他因素催化剂浓度实验:固体颗粒大小的影响同浓度同体积的盐酸分别与1 g的碳酸钙颗粒和
1 g碳酸钙粉末反应,观察试管上方气球膨胀的快慢(试剂、药品已装入试管和气球)
现象:
粉末状→迅速产生大量气泡→气球迅速膨胀
颗粒状→缓慢产生气泡→气球膨胀较慢 颗粒越小,表面积越大,发生有效碰撞的机会也就越多,反应速率越快。如何解释固体颗粒的影响?Back实验:浓度的影响
Na2S2O3+2HCl→S↓+SO2+2NaCl+H2O
取4个小烧杯中各量取15mL 1mol/L的盐酸
同时将不同浓度的Na2S2O3溶液分别倒入盛有
盐酸的小烧杯中,观察从溶液混合后从澄清到浑
浊的先后加水 A B C D
15mL 10mL 5mL 0mL 5mL 10mL 15mL 20mL
Na2S2O3溶液不同浓度硫代硫酸钠溶液的配制如何解释浓度的影响?在化学上,把能够发生有效碰撞的分子叫活化分子浓度小 浓度大Back压强对反应速率的影响 压强小 压强大Back实验:温度的影响 Na2S2O3+2HCl→S↓+SO2+2NaCl+H2O
同时将同浓度同体积两组溶液在一烧杯中混
合,观察从溶液混合后从澄清到浑浊的先后
温度对反应速率的影响活化分子具有较高的能量,能量不足的分子获取能量后才能变成活化分子温度低 温度高面包保质期:
1月~3月:4天
4月~10月:2天
11月~12月:4天
Back实验:催化剂的影响 同时分别用针筒注入3%的双氧水5mL,观察试
管内现象和针筒活塞的运动不使用催化剂使用
催化剂反应物生成物反应进程能 量Back
