人教版化学九年级下册 11.1生活中常见的盐第一课时课件(共14张PPT)
文档属性
| 名称 | 人教版化学九年级下册 11.1生活中常见的盐第一课时课件(共14张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 435.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-14 00:00:00 | ||
图片预览





文档简介
(共14张PPT)
人教版义务教育教科书九年级下册
第十一单元
课题一 生活中常见的盐
(第一课时)
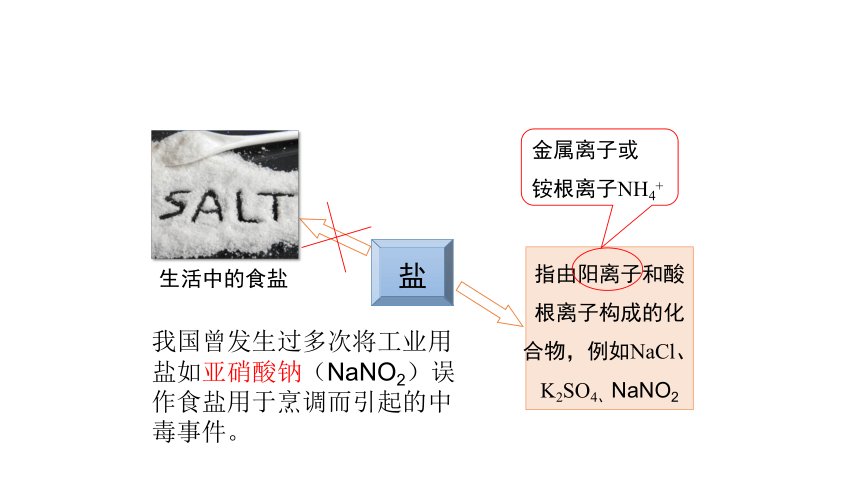
盐
生活中的食盐
指由阳离子和酸根离子构成的化合物,例如NaCl、K2SO4、NaNO2
金属离子或
铵根离子NH4+
我国曾发生过多次将工业用盐如亚硝酸钠(NaNO2)误作食盐用于烹调而引起的中毒事件。
指出下列物质中哪些是酸 哪些是碱 哪些是盐
H2O CaCO3 HCl H2O2 Na2CO3 Ca(OH)2 MnO2 H2SO4 NaOH
酸:HCl H2SO4
碱:NaOH Ca(OH)2
盐:CaCO3 Na2CO3
氧化物:H2O 、MnO2 、 H2O2
自我检测
盐
碱
酸
氧化物
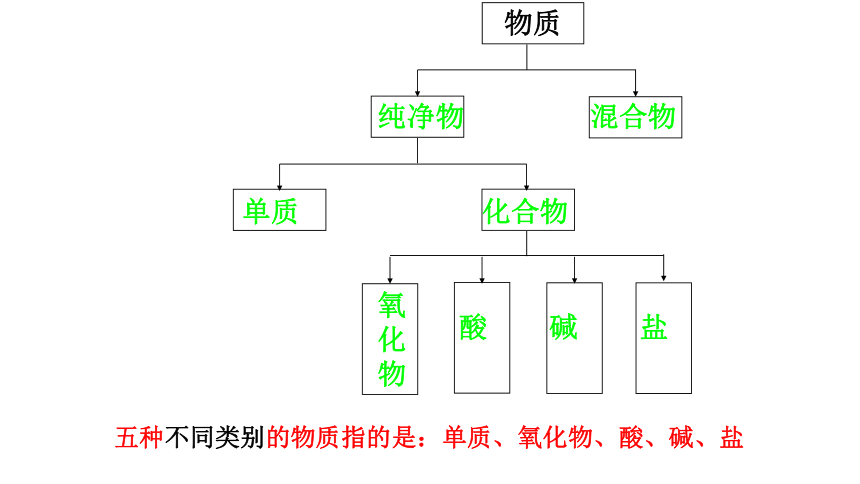
化合物
单质
纯净物
混合物
物质
五种不同类别的物质指的是:单质、氧化物、酸、碱、盐
一、氯化钠(NaCl)
1.物理性质:
NaCl是易溶于水的白色固体,有咸味。它的水溶液呈中性,pH=7.氯化钠的溶解度受温度影响较小。
2.化学性质:
NaCl+AgNO3=NaNO3+AgCl
一、氯化钠
1、用途
①作调味品;
②参与人的正常生理活动;
③医疗上用来配制生理盐水;
④农业上用氯化钠溶液来选种;
⑤工业上用氯化钠来制取碳酸钠、氢氧
化钠、氯气和盐酸等;
⑥腌渍蔬菜、鱼、肉、蛋等;
⑦融雪(降低冰雪的熔点);
3.分布:氯化钠在自然界中的分布很广,除海水
里含有大量的氯化钠外,盐湖、盐井和
盐矿也是氯化钠的来源。
4.制法 :①晾晒海水;
②煮盐湖水;
③煮盐井水;
④从盐矿开采。
一、氯化钠
精盐
1、粗盐提纯的步骤:
称量
溶解
过滤
蒸发
称量
粗盐
计算产率
二、粗盐提纯
=
精盐
溶解的粗盐
×100%
蒸发:倒入蒸发皿里的液体不超过容积的 ,倒入过多的液体,在沸腾时容易迸溅,且不易搅动;当蒸发皿出现较多固体时,应 。玻璃棒的作用 。
停止加热
1/3
注意:蒸发时,蒸发皿不需要垫石棉网。
防止因局部温度过高,造成液滴飞溅
2、具体操作要点:
思考:在溶解 、过滤、蒸发中都用到了玻璃棒,它的作用分别是什么
溶解:搅拌,加速固体的溶解
过滤:引流
蒸发:防止因局部温度过高,造成液滴飞溅
提纯后精盐的质量
溶解粗盐的质量
× 100%
实验后产率偏高或偏低可能是什么原因?
偏低的原因: ①溶解时没有充分溶解
②过滤时有液体洒落
③蒸发时盐粒溅出蒸发皿
④转移固体时氯化钠可能洒出。
偏高的原因: ①蒸发时未蒸干
能力提升
【练习】下列各组物质,能按“溶解、过滤、蒸发”操作顺序
进行分离的是 (填序号)。
①碳酸钙和泥沙 ②KNO3和NaCl
③MnO2和KCl ④CaCl2和CaCO3
溶解 过滤
固体是 ,
溶液是 ,
MnO2
KCl溶液
经过 操作得到KCl晶体
蒸发
自我检测
③④
图为某学生进行粗盐提纯实验中过滤操作的示意图,试回答:
(1)写出标号的仪器名称: ① ,② 。
(2)漏斗中液体的液面应该(填“高”或“低”) 于滤纸的边缘。
烧杯
漏斗
低
防止液体受热不均匀,液滴飞溅
(3)蒸发滤液时,用玻璃棒不断搅拌滤液的目的是 ;等到蒸发皿中出现 时,停止加热,利用蒸发皿的余热使滤液蒸干,移去蒸发皿时应使用的仪器是 。
较多固体
坩埚钳
自我检测
课堂小结
一、物质的分类
五种不同类别的物质:
二、氯化钠
1、物理性质
2、化学性质
3、用途
三、粗盐提纯:步骤:溶解、过滤、蒸发
人教版义务教育教科书九年级下册
第十一单元
课题一 生活中常见的盐
(第一课时)
盐
生活中的食盐
指由阳离子和酸根离子构成的化合物,例如NaCl、K2SO4、NaNO2
金属离子或
铵根离子NH4+
我国曾发生过多次将工业用盐如亚硝酸钠(NaNO2)误作食盐用于烹调而引起的中毒事件。
指出下列物质中哪些是酸 哪些是碱 哪些是盐
H2O CaCO3 HCl H2O2 Na2CO3 Ca(OH)2 MnO2 H2SO4 NaOH
酸:HCl H2SO4
碱:NaOH Ca(OH)2
盐:CaCO3 Na2CO3
氧化物:H2O 、MnO2 、 H2O2
自我检测
盐
碱
酸
氧化物
化合物
单质
纯净物
混合物
物质
五种不同类别的物质指的是:单质、氧化物、酸、碱、盐
一、氯化钠(NaCl)
1.物理性质:
NaCl是易溶于水的白色固体,有咸味。它的水溶液呈中性,pH=7.氯化钠的溶解度受温度影响较小。
2.化学性质:
NaCl+AgNO3=NaNO3+AgCl
一、氯化钠
1、用途
①作调味品;
②参与人的正常生理活动;
③医疗上用来配制生理盐水;
④农业上用氯化钠溶液来选种;
⑤工业上用氯化钠来制取碳酸钠、氢氧
化钠、氯气和盐酸等;
⑥腌渍蔬菜、鱼、肉、蛋等;
⑦融雪(降低冰雪的熔点);
3.分布:氯化钠在自然界中的分布很广,除海水
里含有大量的氯化钠外,盐湖、盐井和
盐矿也是氯化钠的来源。
4.制法 :①晾晒海水;
②煮盐湖水;
③煮盐井水;
④从盐矿开采。
一、氯化钠
精盐
1、粗盐提纯的步骤:
称量
溶解
过滤
蒸发
称量
粗盐
计算产率
二、粗盐提纯
=
精盐
溶解的粗盐
×100%
蒸发:倒入蒸发皿里的液体不超过容积的 ,倒入过多的液体,在沸腾时容易迸溅,且不易搅动;当蒸发皿出现较多固体时,应 。玻璃棒的作用 。
停止加热
1/3
注意:蒸发时,蒸发皿不需要垫石棉网。
防止因局部温度过高,造成液滴飞溅
2、具体操作要点:
思考:在溶解 、过滤、蒸发中都用到了玻璃棒,它的作用分别是什么
溶解:搅拌,加速固体的溶解
过滤:引流
蒸发:防止因局部温度过高,造成液滴飞溅
提纯后精盐的质量
溶解粗盐的质量
× 100%
实验后产率偏高或偏低可能是什么原因?
偏低的原因: ①溶解时没有充分溶解
②过滤时有液体洒落
③蒸发时盐粒溅出蒸发皿
④转移固体时氯化钠可能洒出。
偏高的原因: ①蒸发时未蒸干
能力提升
【练习】下列各组物质,能按“溶解、过滤、蒸发”操作顺序
进行分离的是 (填序号)。
①碳酸钙和泥沙 ②KNO3和NaCl
③MnO2和KCl ④CaCl2和CaCO3
溶解 过滤
固体是 ,
溶液是 ,
MnO2
KCl溶液
经过 操作得到KCl晶体
蒸发
自我检测
③④
图为某学生进行粗盐提纯实验中过滤操作的示意图,试回答:
(1)写出标号的仪器名称: ① ,② 。
(2)漏斗中液体的液面应该(填“高”或“低”) 于滤纸的边缘。
烧杯
漏斗
低
防止液体受热不均匀,液滴飞溅
(3)蒸发滤液时,用玻璃棒不断搅拌滤液的目的是 ;等到蒸发皿中出现 时,停止加热,利用蒸发皿的余热使滤液蒸干,移去蒸发皿时应使用的仪器是 。
较多固体
坩埚钳
自我检测
课堂小结
一、物质的分类
五种不同类别的物质:
二、氯化钠
1、物理性质
2、化学性质
3、用途
三、粗盐提纯:步骤:溶解、过滤、蒸发
同课章节目录
