物质的鉴别与检验专题复习
图片预览




文档简介
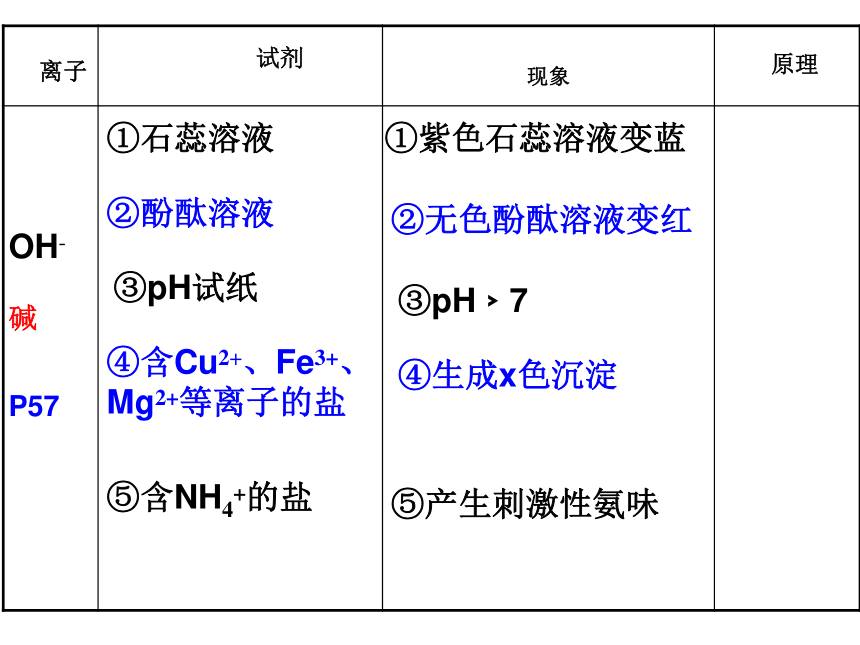
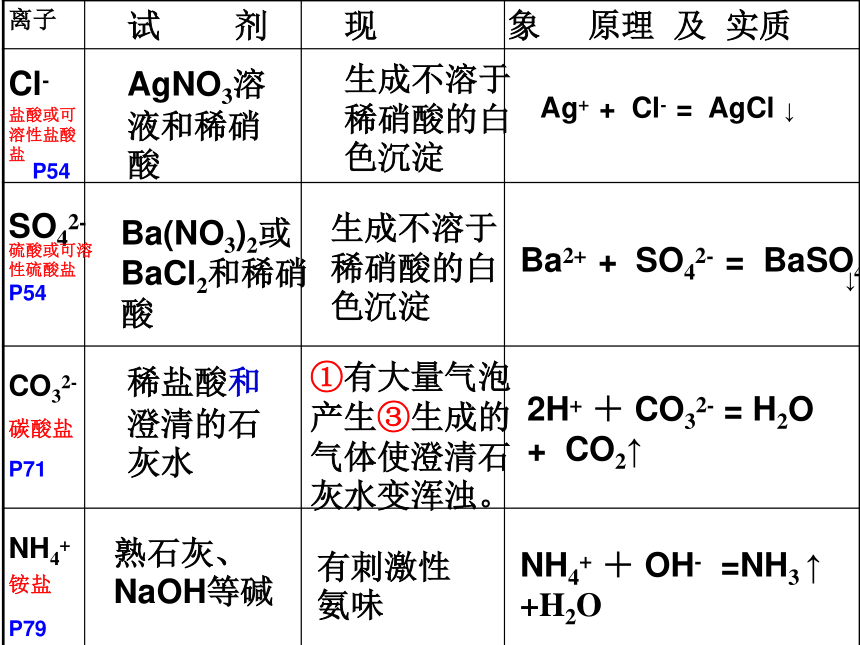
课件18张PPT。物质的鉴别和检验 专题复习鉴别:区别开;检验:判断存不存在一、常见离子的鉴别:①紫色石蕊溶液①紫色石蕊溶液变红②pH试纸②pH﹤7③Zn、Mg等活泼金属③有气泡产生④石灰石、纯碱等碳酸盐④有气泡产生⑤Cu(OH)2 、 Fe(OH)3等不溶碱⑤x色固体逐渐溶解,溶液由x色变为x 色⑥CuO、锈铁钉等金属氧化物⑥ x色固体逐渐溶解,溶液由x色变为x 色离子试剂现象原理OH-碱P57①石蕊溶液②酚酞溶液③pH试纸④含Cu2+、Fe3+、Mg2+等离子的盐⑤含NH4+的盐①紫色石蕊溶液变蓝②无色酚酞溶液变红③pH﹥7④生成x色沉淀⑤产生刺激性氨味离子试 剂现 象原理 及 实质Cl-AgNO3溶液和稀硝酸生成不溶于稀硝酸的白色沉淀盐酸或可溶性盐酸盐Ag+ + Cl- = AgCl↓SO42-硫酸或可溶性硫酸盐Ba(NO3)2或BaCl2和稀硝酸生成不溶于稀硝酸的白色沉淀Ba2+ + SO42- = BaSO4↓CO32-碳酸盐稀盐酸和 澄清的石灰水①有大量气泡产生③生成的气体使澄清石灰水变浑浊。2H+ + CO32- = H2O + CO2↑NH4+铵盐熟石灰、NaOH等碱有刺激性氨味NH4+ + OH- =NH3 ↑ +H2OP54P54P71P79离 子试 剂现 象原理 及 实质Ca2+、Ba2+Na2CO3溶液生成溶于酸的白色沉淀Ca2+ + CO32- = CaCO3Cu2+、Fe3+、Mg2+NaOH等可溶碱有x色沉淀生成Cu2+ + OH- = Cu(OH)2
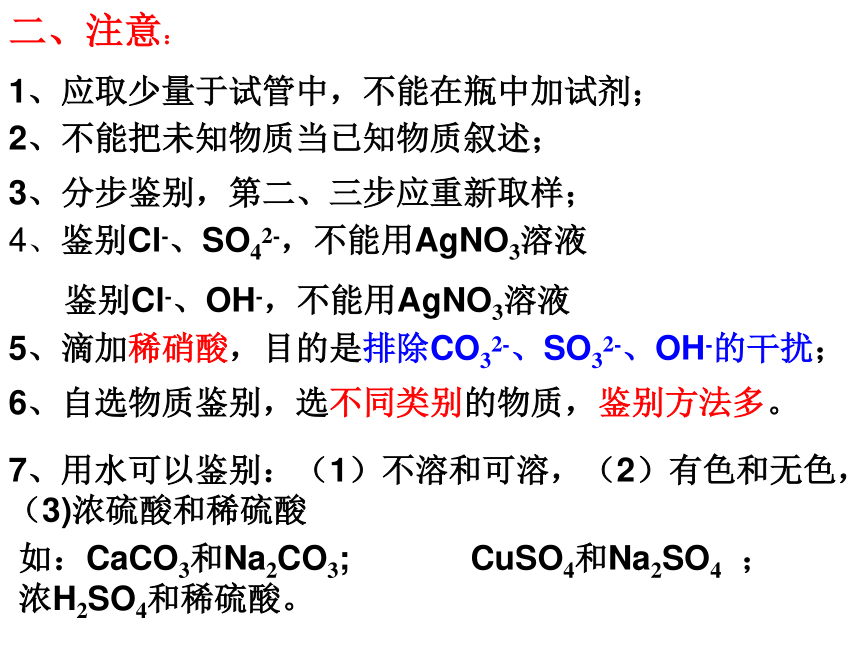
Fe3+ + OH- = Fe(OH)3Ba2+ + CO32- = BaCO3↓↓↓↓↓ 有两瓶失去标签的无色溶液,它们是氢氧化钠溶液和澄清的石灰水,请鉴别。小明:分别向瓶中通入CO2,变浑浊的是澄清的石灰水,没反应的是氢氧化钠溶液小东:取氢氧化钠溶液和澄清的石灰水于2支试管,分别通入CO2,变浑浊的是澄清的石灰水,无现象的是氢氧化钠溶液小伟:各取少量于2支试管,分别通入CO2,石灰水变浑浊,氢氧化钠溶液无现象。小妮:各取少量于2支试管,分别通入CO2,变浑浊的原溶液是澄清的石灰水,无现象的原溶液是氢氧化钠溶液。CO2+2NaOH ==Na2CO3+H2O下面是几位同学的答案,有无错误?大伟:各取少量于2支试管,分别滴加Na2CO3溶液,有白色沉淀生成的原溶液是澄清的石灰水,无现象的原溶液是氢氧化钠溶液。二、注意:1、应取少量于试管中,不能在瓶中加试剂;2、不能把未知物质当已知物质叙述;3、分步鉴别,第二、三步应重新取样;4、鉴别Cl-、SO42-,不能用AgNO3溶液
鉴别Cl-、OH-,不能用AgNO3溶液5、滴加稀硝酸,目的是排除CO32-、SO32-、OH-的干扰;6、自选物质鉴别,选不同类别的物质,鉴别方法多。7、用水可以鉴别:(1)不溶和可溶,(2)有色和无色,(3)浓硫酸和稀硫酸如:CaCO3和Na2CO3; CuSO4和Na2SO4 ; 浓H2SO4和稀硫酸。三、不用其它试剂,组内物质相互鉴别:1、找出有色溶液,(含Cu2+、Fe3+、Fe2+),并用它滴加其它溶液,依次鉴别如:有以下几种溶液:①NaCl、②MgSO4、③NaOH、④CuCl2、⑤Ba(NO3)2,不用外加试剂欲将它们一一鉴别,鉴别的顺序是 。2、用组内物质两两组合反应,产生沉淀、气体。如:下列各组溶液,不用外加试剂,就能一一鉴别的是( )
A、FeCl3、KOH、NaCl B、Na2CO3、BaCl2、HCl
C、CuSO4、HCl、KCl D、K2SO4、KCl、Na2SO4④③②⑤①A、B ⑷ 有时用水、CuSO4、Ba(OH)2等做试剂鉴别。3、三种溶液用一种试剂来检验⑴三种溶液分别呈酸性、碱性、中性时,用紫色石蕊或pH试纸检验。⑶ 三种溶液中有碳酸盐时,可从酸入手; ⑵ 若三种溶液中有酸时,可从Na2CO3入手。BaCl2有含Ag+ 的化合物时用盐酸,有含Ba2+的化合物时用硫酸加以区别。鉴别方法讨论1:
请用化学方法区分HCl、NaCl和Ca(OH)2三种溶液。 1、向烧杯中装入少量NaOH溶液,滴入几滴酚酞溶液,变红,然后逐滴滴加稀H2SO4溶液,至红色刚好褪为无色。此时烧杯中溶液是酸性、还是碱性或中性?请你大胆猜想。
猜想一: ,验证方法 (操作、现象、结论) 。
猜想二: ,验证方法 (操作、现象、结论) 。 2、有两瓶失去标签的无色溶液,它们是澄清石灰水和稀盐酸。
(1)你的第一种鉴别方法是(操作、现象、结论) 。
(2)鉴别它们的另外4种试剂是(不雷同)① 、② 、
③ 、 ④ 。中性酸性取少量于试管,测溶液的pH ,若溶液的pH=7,溶液显中性 。取少量于试管,加入锌粒,若有气泡产生,溶液显酸性 。各取少量于2支试管,分别加入石灰石,有气泡产生的原溶液是稀盐酸,无现象的原原溶液是石灰水。锌粒CuO石蕊溶液CO2酚酞溶液Cu(OH)2 3、实验操作考试结束后,小明同学发现实验台上有一瓶标签破损的试剂,如图:Na2请你大胆猜想,并设计实验验证你的猜想。猜 想操 作现 象结 论猜想1,试剂是 。猜想2,试剂是 。Na2CO3Na2SO4取少量于试管,加入稀盐酸有气泡产生是Na2CO3取少量于试管,加入BaCl2溶液有白色沉淀产生是Na2SO4 4、904班的同学对物质的鉴别开展探究比赛。标准是:方案多的获胜。要求:探究方案不能雷同(即所选物质的类别为一类只能算一种方案)。以下是他们的探究过程:
(一)探究问题:从稀盐酸、氢氧化钠溶液、碳酸钠溶液、氢氧化钙溶液、稀硫酸中任选两种物质来鉴别。用于鉴别的试剂可任选。
(二)探究方案:
(1)小梦同学选取了稀盐酸和稀硫酸来鉴别,他只找到两种试剂来鉴别,这两种试剂是 、 。 (写化学式,下同)
(2)小建同学选取了氢氧化钠溶液和氢氧化钙溶液来鉴别,他找到了以下两种试剂来鉴别,这两种试剂 、 。
(3)小锦同学在鉴别稀盐酸和氢氧化钠溶液时,他选用了以下5种试剂:指示剂、金属锌、氧化铜、 、 。
小锦在上述方案中,没有涉及到氢氧化钠的一条化学性质,写出氢氧化钠与这类物质反应的任一个化学方程式 。
没有选择这类物质的理由是 。
(三)比赛结果:小锦获胜。
(四)我的反思:
(1)用于鉴别物质的依据是:根据这两种物质的 不同,或反应时发生的 , 不同,来进行鉴别。
(2)若我参与类似“物质的鉴别”比赛,我选择这两种物质的特征应该是 ,才有获胜的希望。BaCl2溶液 Ba(OH)2溶液CO2Na2CO3CaCO3Cu(OH)2CO2+2NaOH=Na2CO3+H2O物质的类别不同性质现象反应无现象 5、现有五瓶溶液:盐酸、硫酸、氢氧化钙、氯化钠、碳酸钠,请你从中选两种溶液,用五种不同的化学方法进行鉴别。
要求:所依据的化学性质不能雷同;所用试剂在上述五种溶液之外。
(1)你选的两种溶液是 ,
(2) 鉴别它们的第一种方法是:(包括步骤、现象、结论) 。
(3)鉴别它们的另外4种方法是:(只要求写出试剂) 、 、 、 。
(4)写出(3)中的一个化学方程式 。四、练习:1、只用一种试剂来鉴别Ca(OH)2、NaCl、稀H2SO4三种无色溶液,这种试剂是( )
A 、BaCl2溶液 B、紫色石蕊溶液 C、稀HCl D、稀H2SO42、用水不能鉴别的一组物质是( )
A、Na2SO 4和CuSO4; B、CaCO3和Na2CO3; C、BaCl2和KNO3 D、浓H2SO4和稀H2SO43、只用一种试剂来鉴别Na2CO 3、BaCl2、Mg(NO3)2三种溶液,这种试剂是( )
A、紫色石蕊溶液 B、无色酚酞溶液 C、稀H2SO4 D、稀HClBCC4、有4瓶失去标签的溶液,①NaOH、②CuSO4、③MgCl2、④Na2SO4,不用其它试剂,而要将它们一一鉴别出来,正确顺序为( )
A、 ③ ① ② ④ B、 ② ③ ④ ① C、 ② ① ③ ④ D、 ① ③ ② ④ 5、有两瓶无色溶液食盐水和蒸馏水,请用多种方法鉴别。6、有三瓶无色溶液食盐水、澄清石灰水、稀盐酸,用两种方法鉴别C7、有两瓶失去标签的无色溶液,它们是澄清石灰水和稀盐酸。
(1)你的第一种鉴别方法是(操作、现象、结论) 。
(2)鉴别它们的另外4种试剂是(不能雷同) 、 、 、 。8、向烧杯中加入少量氢氧化钠溶液,滴入几滴酚酞溶液,变红,然后用滴管逐滴滴加稀硫酸,至红色刚好褪为无色。此时,烧杯中的溶液是中性还是酸性或碱性?请你大胆猜想:
猜想1: ,验证方法(操作、现象、结论) 。
猜想2: ,验证方法(操作、现象、结论) 。11、向烧杯中加入少量氢氧化钠溶液,滴入几滴酚酞溶液,变红,然后用滴管逐滴滴加稀硫酸,至红色刚好褪为无色。此时,烧杯中的溶液是中性还是酸性或碱性?请你大胆猜想:
猜想1: ,验证方法(操作、现象、结论) 。
猜想2: ,验证方法(操作、现象、结论) 。
Fe3+ + OH- = Fe(OH)3Ba2+ + CO32- = BaCO3↓↓↓↓↓ 有两瓶失去标签的无色溶液,它们是氢氧化钠溶液和澄清的石灰水,请鉴别。小明:分别向瓶中通入CO2,变浑浊的是澄清的石灰水,没反应的是氢氧化钠溶液小东:取氢氧化钠溶液和澄清的石灰水于2支试管,分别通入CO2,变浑浊的是澄清的石灰水,无现象的是氢氧化钠溶液小伟:各取少量于2支试管,分别通入CO2,石灰水变浑浊,氢氧化钠溶液无现象。小妮:各取少量于2支试管,分别通入CO2,变浑浊的原溶液是澄清的石灰水,无现象的原溶液是氢氧化钠溶液。CO2+2NaOH ==Na2CO3+H2O下面是几位同学的答案,有无错误?大伟:各取少量于2支试管,分别滴加Na2CO3溶液,有白色沉淀生成的原溶液是澄清的石灰水,无现象的原溶液是氢氧化钠溶液。二、注意:1、应取少量于试管中,不能在瓶中加试剂;2、不能把未知物质当已知物质叙述;3、分步鉴别,第二、三步应重新取样;4、鉴别Cl-、SO42-,不能用AgNO3溶液
鉴别Cl-、OH-,不能用AgNO3溶液5、滴加稀硝酸,目的是排除CO32-、SO32-、OH-的干扰;6、自选物质鉴别,选不同类别的物质,鉴别方法多。7、用水可以鉴别:(1)不溶和可溶,(2)有色和无色,(3)浓硫酸和稀硫酸如:CaCO3和Na2CO3; CuSO4和Na2SO4 ; 浓H2SO4和稀硫酸。三、不用其它试剂,组内物质相互鉴别:1、找出有色溶液,(含Cu2+、Fe3+、Fe2+),并用它滴加其它溶液,依次鉴别如:有以下几种溶液:①NaCl、②MgSO4、③NaOH、④CuCl2、⑤Ba(NO3)2,不用外加试剂欲将它们一一鉴别,鉴别的顺序是 。2、用组内物质两两组合反应,产生沉淀、气体。如:下列各组溶液,不用外加试剂,就能一一鉴别的是( )
A、FeCl3、KOH、NaCl B、Na2CO3、BaCl2、HCl
C、CuSO4、HCl、KCl D、K2SO4、KCl、Na2SO4④③②⑤①A、B ⑷ 有时用水、CuSO4、Ba(OH)2等做试剂鉴别。3、三种溶液用一种试剂来检验⑴三种溶液分别呈酸性、碱性、中性时,用紫色石蕊或pH试纸检验。⑶ 三种溶液中有碳酸盐时,可从酸入手; ⑵ 若三种溶液中有酸时,可从Na2CO3入手。BaCl2有含Ag+ 的化合物时用盐酸,有含Ba2+的化合物时用硫酸加以区别。鉴别方法讨论1:
请用化学方法区分HCl、NaCl和Ca(OH)2三种溶液。 1、向烧杯中装入少量NaOH溶液,滴入几滴酚酞溶液,变红,然后逐滴滴加稀H2SO4溶液,至红色刚好褪为无色。此时烧杯中溶液是酸性、还是碱性或中性?请你大胆猜想。
猜想一: ,验证方法 (操作、现象、结论) 。
猜想二: ,验证方法 (操作、现象、结论) 。 2、有两瓶失去标签的无色溶液,它们是澄清石灰水和稀盐酸。
(1)你的第一种鉴别方法是(操作、现象、结论) 。
(2)鉴别它们的另外4种试剂是(不雷同)① 、② 、
③ 、 ④ 。中性酸性取少量于试管,测溶液的pH ,若溶液的pH=7,溶液显中性 。取少量于试管,加入锌粒,若有气泡产生,溶液显酸性 。各取少量于2支试管,分别加入石灰石,有气泡产生的原溶液是稀盐酸,无现象的原原溶液是石灰水。锌粒CuO石蕊溶液CO2酚酞溶液Cu(OH)2 3、实验操作考试结束后,小明同学发现实验台上有一瓶标签破损的试剂,如图:Na2请你大胆猜想,并设计实验验证你的猜想。猜 想操 作现 象结 论猜想1,试剂是 。猜想2,试剂是 。Na2CO3Na2SO4取少量于试管,加入稀盐酸有气泡产生是Na2CO3取少量于试管,加入BaCl2溶液有白色沉淀产生是Na2SO4 4、904班的同学对物质的鉴别开展探究比赛。标准是:方案多的获胜。要求:探究方案不能雷同(即所选物质的类别为一类只能算一种方案)。以下是他们的探究过程:
(一)探究问题:从稀盐酸、氢氧化钠溶液、碳酸钠溶液、氢氧化钙溶液、稀硫酸中任选两种物质来鉴别。用于鉴别的试剂可任选。
(二)探究方案:
(1)小梦同学选取了稀盐酸和稀硫酸来鉴别,他只找到两种试剂来鉴别,这两种试剂是 、 。 (写化学式,下同)
(2)小建同学选取了氢氧化钠溶液和氢氧化钙溶液来鉴别,他找到了以下两种试剂来鉴别,这两种试剂 、 。
(3)小锦同学在鉴别稀盐酸和氢氧化钠溶液时,他选用了以下5种试剂:指示剂、金属锌、氧化铜、 、 。
小锦在上述方案中,没有涉及到氢氧化钠的一条化学性质,写出氢氧化钠与这类物质反应的任一个化学方程式 。
没有选择这类物质的理由是 。
(三)比赛结果:小锦获胜。
(四)我的反思:
(1)用于鉴别物质的依据是:根据这两种物质的 不同,或反应时发生的 , 不同,来进行鉴别。
(2)若我参与类似“物质的鉴别”比赛,我选择这两种物质的特征应该是 ,才有获胜的希望。BaCl2溶液 Ba(OH)2溶液CO2Na2CO3CaCO3Cu(OH)2CO2+2NaOH=Na2CO3+H2O物质的类别不同性质现象反应无现象 5、现有五瓶溶液:盐酸、硫酸、氢氧化钙、氯化钠、碳酸钠,请你从中选两种溶液,用五种不同的化学方法进行鉴别。
要求:所依据的化学性质不能雷同;所用试剂在上述五种溶液之外。
(1)你选的两种溶液是 ,
(2) 鉴别它们的第一种方法是:(包括步骤、现象、结论) 。
(3)鉴别它们的另外4种方法是:(只要求写出试剂) 、 、 、 。
(4)写出(3)中的一个化学方程式 。四、练习:1、只用一种试剂来鉴别Ca(OH)2、NaCl、稀H2SO4三种无色溶液,这种试剂是( )
A 、BaCl2溶液 B、紫色石蕊溶液 C、稀HCl D、稀H2SO42、用水不能鉴别的一组物质是( )
A、Na2SO 4和CuSO4; B、CaCO3和Na2CO3; C、BaCl2和KNO3 D、浓H2SO4和稀H2SO43、只用一种试剂来鉴别Na2CO 3、BaCl2、Mg(NO3)2三种溶液,这种试剂是( )
A、紫色石蕊溶液 B、无色酚酞溶液 C、稀H2SO4 D、稀HClBCC4、有4瓶失去标签的溶液,①NaOH、②CuSO4、③MgCl2、④Na2SO4,不用其它试剂,而要将它们一一鉴别出来,正确顺序为( )
A、 ③ ① ② ④ B、 ② ③ ④ ① C、 ② ① ③ ④ D、 ① ③ ② ④ 5、有两瓶无色溶液食盐水和蒸馏水,请用多种方法鉴别。6、有三瓶无色溶液食盐水、澄清石灰水、稀盐酸,用两种方法鉴别C7、有两瓶失去标签的无色溶液,它们是澄清石灰水和稀盐酸。
(1)你的第一种鉴别方法是(操作、现象、结论) 。
(2)鉴别它们的另外4种试剂是(不能雷同) 、 、 、 。8、向烧杯中加入少量氢氧化钠溶液,滴入几滴酚酞溶液,变红,然后用滴管逐滴滴加稀硫酸,至红色刚好褪为无色。此时,烧杯中的溶液是中性还是酸性或碱性?请你大胆猜想:
猜想1: ,验证方法(操作、现象、结论) 。
猜想2: ,验证方法(操作、现象、结论) 。11、向烧杯中加入少量氢氧化钠溶液,滴入几滴酚酞溶液,变红,然后用滴管逐滴滴加稀硫酸,至红色刚好褪为无色。此时,烧杯中的溶液是中性还是酸性或碱性?请你大胆猜想:
猜想1: ,验证方法(操作、现象、结论) 。
猜想2: ,验证方法(操作、现象、结论) 。
