化学人教版(2019)必修第二册7.1.1认识有机化合物-甲烷(共40张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册7.1.1认识有机化合物-甲烷(共40张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-16 00:00:00 | ||
图片预览






文档简介
(共40张PPT)
第一节 认识有机化合物
青霉素
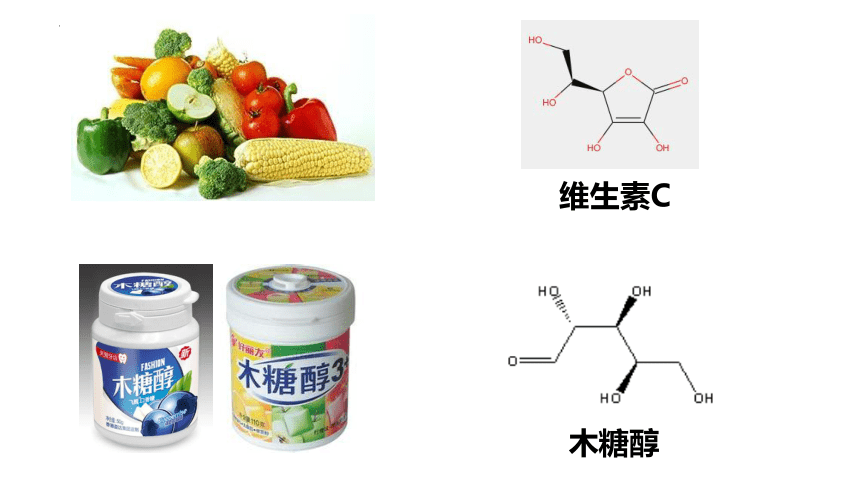
维生素C
木糖醇
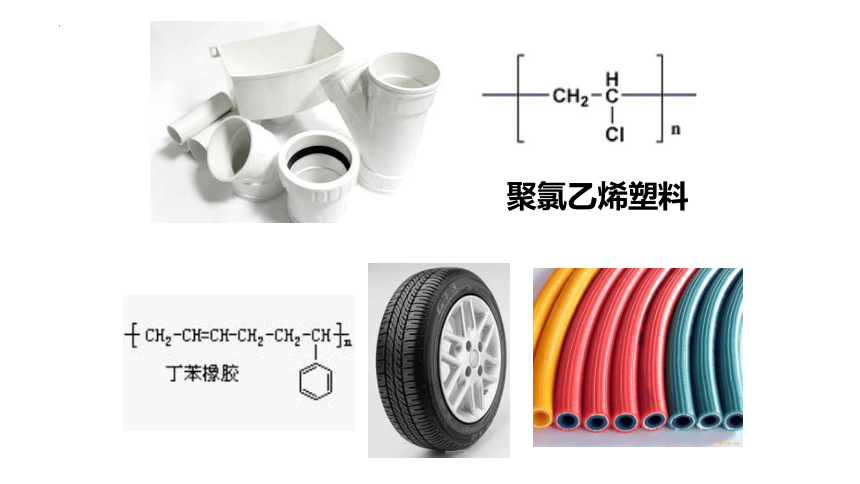
聚氯乙烯塑料
C2H5OH
酒
CH3COOH
醋
蔗糖
C12H22O11
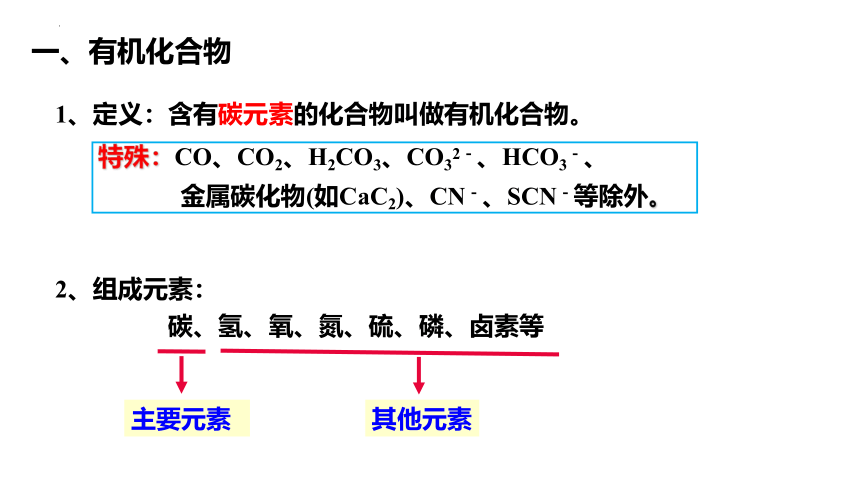
1、定义:含有碳元素的化合物叫做有机化合物。
2、组成元素:
碳、氢、氧、氮、硫、磷、卤素等
主要元素
其他元素
一、有机化合物
特殊:CO、CO2、H2CO3、CO32-、HCO3-、
金属碳化物(如CaC2)、CN-、SCN-等除外。
【练习1】下列物质中属于有机物的是( )
①乙醇 ②食盐 ③石墨 ④甲烷 ⑤蔗糖
⑥水 ⑦一氧化碳 ⑧碳酸钙 ⑨乙酸
A.①②④⑤⑨ B.①④⑤⑨
C.①③④⑤⑦⑧⑨ D.①④⑤⑥
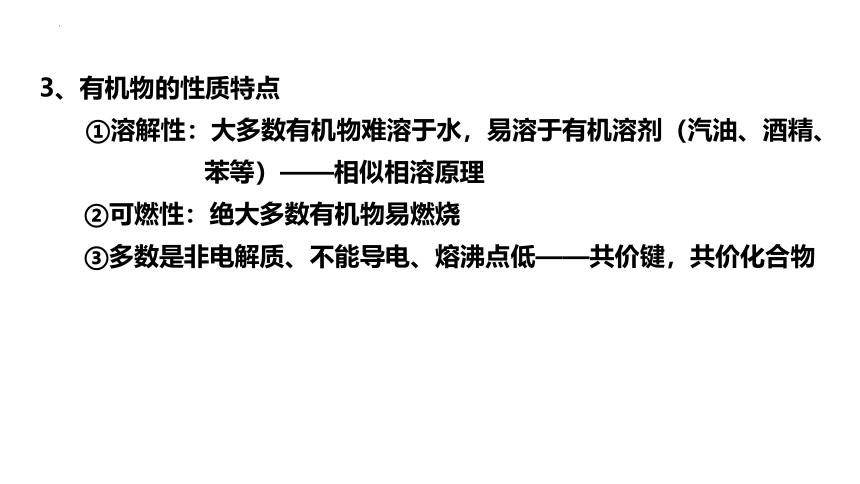
3、有机物的性质特点
①溶解性:大多数有机物难溶于水,易溶于有机溶剂(汽油、酒精、苯等)——相似相溶原理
②可燃性:绝大多数有机物易燃烧
③多数是非电解质、不能导电、熔沸点低——共价键,共价化合物
①成键数目:
②成键方式:
③连接方式:
(P60)
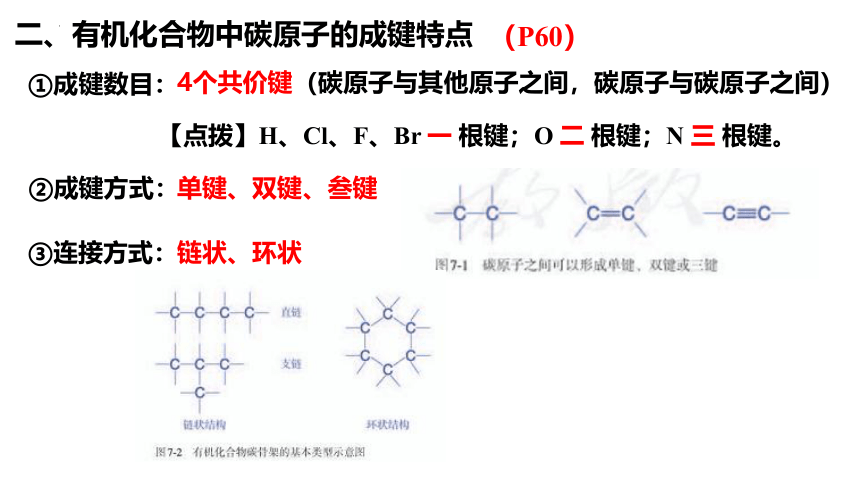
二、有机化合物中碳原子的成键特点
4个共价键(碳原子与其他原子之间,碳原子与碳原子之间)
单键、双键、叁键
链状、环状
【点拨】H、Cl、F、Br 一 根键;O 二 根键;N 三 根键。
P61思考与讨论:有机化合物为什么如此繁多?
1、有机物分子中的碳原子与其他原子的结合方式是( )
A.通过两个共价键 B.通过非极性键
C.形成四对共用电子对 D.通过离子键和共价键
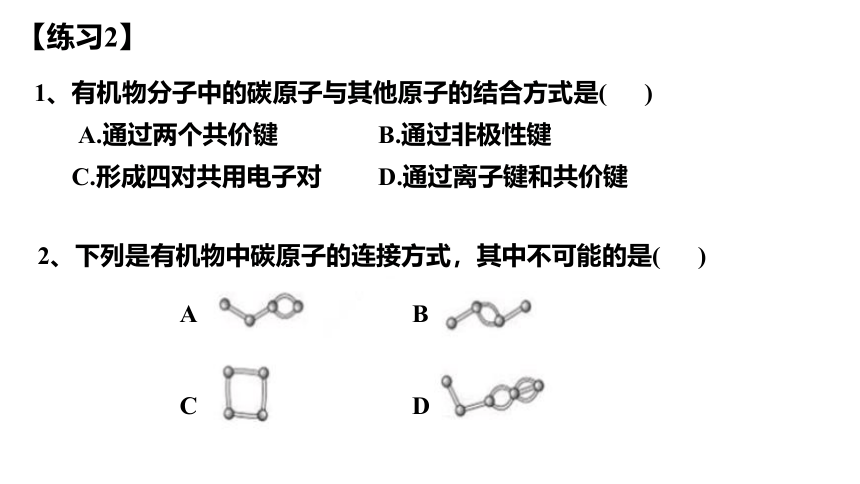
【练习2】
A
B
D
C
2、下列是有机物中碳原子的连接方式,其中不可能的是( )
4、下列说法不正确的是( )
A. 有机物分子中一定含有一个或多个碳原子
B. 有机物分子中的碳原子可以相互连接成链状或环状
C. 有机物分子中的碳原子可以与其它元素的原子连接
D. 分子中含有碳原子的化合物一定是有机物
系统集成 P49
三、甲烷
煤矿坑道气(瓦斯)
沼气(甲烷的俗称)
天然气、油田气
可燃冰
1、存在与用途
沼气
煤矿坑道气
天然气
油田气
可燃冰是天然气(甲烷等)的水合物,它易燃烧,外形似冰,被称为“可燃冰”。“可燃冰”储量较大,可燃冰成为最理想替代能源 P103
千年的希望
“可燃冰”
分子式
CH4
电子式
结构式
球棍模型
空间填充模型
2、甲烷的分子结构
最能反映真实结构
表示方法 含义
分子式 用元素符号表示物质分子组成的式子,可反映一个分子中原子的种类和数目
结构式 ①能反映物质的结构
②表示分子中原子结合或排列顺序的式子,但不表 示空间构型
结构简式 省略了部分短线“—”的结构式
最简式/实验式 表示物质组成的各元素原子最简整数比的式子
球棍模型 小球表示原子,短棍表示价键(单键、双键或三键)
比例/填充模型 用不同体积的小球表示不同大小的原子
系统集成P55
① 甲烷是正四面体结构,最多3原子共面
② 碳原子为中心,4个氢原子为顶点
③ 4 个 C-H 键的长度和强度相同,键角相等
CH4
【思考】 是否说明甲烷分子的真实构型是以碳原子为中心, 四个氢原子为顶点的平面正方形?
由于有机物的立体结构式书写起来比较耗时,为方便起见,一般采用平面的结构式。
1、下列物质的主要成分不是甲烷的是 A.天然气 B.沼气 C.瓦斯 D.水煤气
2、下列关于甲烷分子结构的叙述中,正确的是( )
A. 甲烷分子中碳、氢原子间是离子键
B. 甲烷分子的空间结构是正方体
C. 甲烷的结构式是CH4
D. 甲烷分子中4个碳氢键完全相同
【练习3】
3、下列各图均能表示甲烷的分子结构,其中能反应其真实存在状况的是
球棍模型
比例模型
电子式
结构示意图
A
B
C
D
1、甲烷物理性质
颜色 状态 气味 密度 水溶性
色 体 无味 比空气 , 溶于水
无
气
小
难
向下排气法
收集
排水法
收集
M空气=29g/mol
四、甲烷性质
2、化学性质
通常情况下,甲烷比较稳定,与强酸、强碱和强氧化剂等一般 不发生化学反应。
甲烷不能使酸性高锰酸钾褪色
CH4+2O2 CO2+2H2O
点燃
现象:火焰明亮且呈淡蓝色
【注意】
(1)点燃甲烷前必须验纯,否则会爆炸。
(2)有机反应方程式中用“ → ”不用“=”。
①甲烷的氧化反应
设计实验验证CH4燃烧的产物
在火焰上方罩一个干燥的烧杯,烧杯内壁有水珠出现;把烧杯翻转注入少量澄清石灰水,振荡,澄清石灰水变浑浊证明有CO2生成。
【思考与交流】
CH4
【牢记】检验顺序:先检验H2O后检验CO2
1、甲烷气体在氧气中燃烧生成二氧化碳和水的实验事实说明
A.甲烷的分子式为CH4
B.甲烷气体中含有碳元素和氢元素
C.甲烷气体中只含有碳元素和氢元素
D.甲烷的化学性质比较稳定
2、为验证甲烷分子中含有碳、氢两种元素,可将其燃烧产物通过
①浓硫酸;②澄清石灰水;③无水硫酸铜。正确的顺序是 A.①②③ B.②③ C.②③① D.③②
【练习4】
3、如下图所示,某气体X可能是H2、CO或CH4中的一种,将X气体燃烧后生成的气体通过A、B 两个洗气瓶。试回答下列问题:
(1)若A洗气瓶的质量增加,B洗气瓶的质量不变,则气体X是 。(2)若A洗气瓶的质量不变,B洗气瓶的质量增加,则气体X是 。(3)若A、B两个洗气瓶的质量都增加,则气体X是 。
4、将一定量的甲烷完全燃烧,使所生成的气体依次通过装有足量无水CaCl2和NaOH的玻璃管。结果盛NaOH的玻璃管质量增加了1.1g,则原来甲烷的物质的量为 A.0.1mol B.0.05mol C.0.025mol D.0.0125mol
②与Cl2取代反应
光照下:试管内气体颜色逐渐逐渐变浅;试管内壁出现油状液滴, 试管中有少量白雾,且试管内液面上升;水槽中有固体析出。
Cl
+ HCl
+ Cl2
光照
H
C
H
H
H
C
H
H
H
取代反应
一氯甲烷
简写: CH4 + Cl2 CH3Cl + HCl
光照
有机物分子里的某些原子或原子团被其他原子或
原子团代替的反应。
特征:一下一上,取而代之
(一氯甲烷, 气态)
(二氯甲烷,液态)
(四氯甲烷,液态,又叫四氯化碳,常作溶剂)
CH4 + Cl2 CH3Cl + HCl
光照
CHCl3 + Cl2 CCl4 + HCl
光照
光照
CH3Cl + Cl2 CH2Cl2 + HCl
(三氯甲烷,液态,又叫氯仿,曾用作麻醉剂)
CHCl3 + HCl
光照
CH2Cl2 + Cl2
甲烷与氯气的反应
a.连锁反应,甲烷的氢原子逐步被氯原子取代
b.数量关系:每取代1molH,消耗1molCl2,生成1molHCl
c.CH4与Cl2发生取代反应,生成 5 种产物,得到产物的物质的量最多的是HCl
d.能证明CH4分子是正四面体结构的事实是二氯甲烷只有一种结构。
特别注意
a.光照(不能强光直射);
b.只能用纯净的卤素,如氯气或溴蒸气(液溴),不能用氯水和溴水。
1、取代反应的条件:
2、特点:
【巩固】①写出CH4与Br2反应的反应式
②写出CH3CH3与Cl2反应的反应式
【练习4】
1、在光照条件下,下列物质中能与甲烷反应的是
A.盐酸 B.Cl2 C.NaOH溶液 D.酸性KMnO4溶液
2、(双选)下列物质能和甲烷发生取代反应的是( ) A.Cl2 B.CCl4 C.氯水 D.溴蒸气
3、光照下,甲烷与氯气发生取代反应后,共得产物
A.5种 B.2种 C.3种 D.4种
4、在光照的条件下,将等物质的量的甲烷和氯气混合充分反应后,得到产物的物质的量最多的是
A.CH2Cl2 B.CHCl3 C.CCl4 D.HCl
5、将1molCH4和4molCl2发生取代反应,待反应完全后,测得四种有机取代物的物质的量相等,则消耗Cl2为
A.0.5 mol B.2 mol C.2.5 mol D.4 mol
6、下列反应属于取代反应的是( )
解析:
无机反应中的置换反应不属于取代反应。
取代反应“有上有下”的特点
7、下图是CH4、CCl4、CH3Cl分子的球棍模型图,下列说法正确的是
A.CH4、CCl4和CH3Cl都是正四面体结构
B.CH4、CCl4都是正四面体结构
C.CH4和CCl4中的化学键均为非极性键
D.CH4、CCl4的结构相同,性质也相同
一个碳原子以4个单键与其他原子相结合时:
(1)如果这4个原子相同,则构成正四面体。
(2)如果这4个原子不相同,则构成四面体,但不是正四面体。
(3)无论这4个原子是否相同,最多有3个原子共面。
思维启迪
在隔绝空气并加热至1000℃的高温下,甲烷分解
CH4 C + 2H2
高温
合成氨、汽油的原料
橡胶工业的原料
③甲烷的受热分解
四、甲烷的应用
③甲烷在一定条件下氧化生成一氧化碳、氢气的混合物,
用它们可以合成甲醇
① 气体燃料
② 化工原料:制氯仿和氟利昂
甲烷
化学
性质
总体:
一定条件下
能燃烧
易取代
高温分解
性质较稳定
【归纳总结】
不与强酸、强碱反应
不与强氧化剂
(如高锰酸钾、浓硫酸、浓硝酸等)反应
在光照时与氯气或溴蒸气等反应
第一节 认识有机化合物
青霉素
维生素C
木糖醇
聚氯乙烯塑料
C2H5OH
酒
CH3COOH
醋
蔗糖
C12H22O11
1、定义:含有碳元素的化合物叫做有机化合物。
2、组成元素:
碳、氢、氧、氮、硫、磷、卤素等
主要元素
其他元素
一、有机化合物
特殊:CO、CO2、H2CO3、CO32-、HCO3-、
金属碳化物(如CaC2)、CN-、SCN-等除外。
【练习1】下列物质中属于有机物的是( )
①乙醇 ②食盐 ③石墨 ④甲烷 ⑤蔗糖
⑥水 ⑦一氧化碳 ⑧碳酸钙 ⑨乙酸
A.①②④⑤⑨ B.①④⑤⑨
C.①③④⑤⑦⑧⑨ D.①④⑤⑥
3、有机物的性质特点
①溶解性:大多数有机物难溶于水,易溶于有机溶剂(汽油、酒精、苯等)——相似相溶原理
②可燃性:绝大多数有机物易燃烧
③多数是非电解质、不能导电、熔沸点低——共价键,共价化合物
①成键数目:
②成键方式:
③连接方式:
(P60)
二、有机化合物中碳原子的成键特点
4个共价键(碳原子与其他原子之间,碳原子与碳原子之间)
单键、双键、叁键
链状、环状
【点拨】H、Cl、F、Br 一 根键;O 二 根键;N 三 根键。
P61思考与讨论:有机化合物为什么如此繁多?
1、有机物分子中的碳原子与其他原子的结合方式是( )
A.通过两个共价键 B.通过非极性键
C.形成四对共用电子对 D.通过离子键和共价键
【练习2】
A
B
D
C
2、下列是有机物中碳原子的连接方式,其中不可能的是( )
4、下列说法不正确的是( )
A. 有机物分子中一定含有一个或多个碳原子
B. 有机物分子中的碳原子可以相互连接成链状或环状
C. 有机物分子中的碳原子可以与其它元素的原子连接
D. 分子中含有碳原子的化合物一定是有机物
系统集成 P49
三、甲烷
煤矿坑道气(瓦斯)
沼气(甲烷的俗称)
天然气、油田气
可燃冰
1、存在与用途
沼气
煤矿坑道气
天然气
油田气
可燃冰是天然气(甲烷等)的水合物,它易燃烧,外形似冰,被称为“可燃冰”。“可燃冰”储量较大,可燃冰成为最理想替代能源 P103
千年的希望
“可燃冰”
分子式
CH4
电子式
结构式
球棍模型
空间填充模型
2、甲烷的分子结构
最能反映真实结构
表示方法 含义
分子式 用元素符号表示物质分子组成的式子,可反映一个分子中原子的种类和数目
结构式 ①能反映物质的结构
②表示分子中原子结合或排列顺序的式子,但不表 示空间构型
结构简式 省略了部分短线“—”的结构式
最简式/实验式 表示物质组成的各元素原子最简整数比的式子
球棍模型 小球表示原子,短棍表示价键(单键、双键或三键)
比例/填充模型 用不同体积的小球表示不同大小的原子
系统集成P55
① 甲烷是正四面体结构,最多3原子共面
② 碳原子为中心,4个氢原子为顶点
③ 4 个 C-H 键的长度和强度相同,键角相等
CH4
【思考】 是否说明甲烷分子的真实构型是以碳原子为中心, 四个氢原子为顶点的平面正方形?
由于有机物的立体结构式书写起来比较耗时,为方便起见,一般采用平面的结构式。
1、下列物质的主要成分不是甲烷的是 A.天然气 B.沼气 C.瓦斯 D.水煤气
2、下列关于甲烷分子结构的叙述中,正确的是( )
A. 甲烷分子中碳、氢原子间是离子键
B. 甲烷分子的空间结构是正方体
C. 甲烷的结构式是CH4
D. 甲烷分子中4个碳氢键完全相同
【练习3】
3、下列各图均能表示甲烷的分子结构,其中能反应其真实存在状况的是
球棍模型
比例模型
电子式
结构示意图
A
B
C
D
1、甲烷物理性质
颜色 状态 气味 密度 水溶性
色 体 无味 比空气 , 溶于水
无
气
小
难
向下排气法
收集
排水法
收集
M空气=29g/mol
四、甲烷性质
2、化学性质
通常情况下,甲烷比较稳定,与强酸、强碱和强氧化剂等一般 不发生化学反应。
甲烷不能使酸性高锰酸钾褪色
CH4+2O2 CO2+2H2O
点燃
现象:火焰明亮且呈淡蓝色
【注意】
(1)点燃甲烷前必须验纯,否则会爆炸。
(2)有机反应方程式中用“ → ”不用“=”。
①甲烷的氧化反应
设计实验验证CH4燃烧的产物
在火焰上方罩一个干燥的烧杯,烧杯内壁有水珠出现;把烧杯翻转注入少量澄清石灰水,振荡,澄清石灰水变浑浊证明有CO2生成。
【思考与交流】
CH4
【牢记】检验顺序:先检验H2O后检验CO2
1、甲烷气体在氧气中燃烧生成二氧化碳和水的实验事实说明
A.甲烷的分子式为CH4
B.甲烷气体中含有碳元素和氢元素
C.甲烷气体中只含有碳元素和氢元素
D.甲烷的化学性质比较稳定
2、为验证甲烷分子中含有碳、氢两种元素,可将其燃烧产物通过
①浓硫酸;②澄清石灰水;③无水硫酸铜。正确的顺序是 A.①②③ B.②③ C.②③① D.③②
【练习4】
3、如下图所示,某气体X可能是H2、CO或CH4中的一种,将X气体燃烧后生成的气体通过A、B 两个洗气瓶。试回答下列问题:
(1)若A洗气瓶的质量增加,B洗气瓶的质量不变,则气体X是 。(2)若A洗气瓶的质量不变,B洗气瓶的质量增加,则气体X是 。(3)若A、B两个洗气瓶的质量都增加,则气体X是 。
4、将一定量的甲烷完全燃烧,使所生成的气体依次通过装有足量无水CaCl2和NaOH的玻璃管。结果盛NaOH的玻璃管质量增加了1.1g,则原来甲烷的物质的量为 A.0.1mol B.0.05mol C.0.025mol D.0.0125mol
②与Cl2取代反应
光照下:试管内气体颜色逐渐逐渐变浅;试管内壁出现油状液滴, 试管中有少量白雾,且试管内液面上升;水槽中有固体析出。
Cl
+ HCl
+ Cl2
光照
H
C
H
H
H
C
H
H
H
取代反应
一氯甲烷
简写: CH4 + Cl2 CH3Cl + HCl
光照
有机物分子里的某些原子或原子团被其他原子或
原子团代替的反应。
特征:一下一上,取而代之
(一氯甲烷, 气态)
(二氯甲烷,液态)
(四氯甲烷,液态,又叫四氯化碳,常作溶剂)
CH4 + Cl2 CH3Cl + HCl
光照
CHCl3 + Cl2 CCl4 + HCl
光照
光照
CH3Cl + Cl2 CH2Cl2 + HCl
(三氯甲烷,液态,又叫氯仿,曾用作麻醉剂)
CHCl3 + HCl
光照
CH2Cl2 + Cl2
甲烷与氯气的反应
a.连锁反应,甲烷的氢原子逐步被氯原子取代
b.数量关系:每取代1molH,消耗1molCl2,生成1molHCl
c.CH4与Cl2发生取代反应,生成 5 种产物,得到产物的物质的量最多的是HCl
d.能证明CH4分子是正四面体结构的事实是二氯甲烷只有一种结构。
特别注意
a.光照(不能强光直射);
b.只能用纯净的卤素,如氯气或溴蒸气(液溴),不能用氯水和溴水。
1、取代反应的条件:
2、特点:
【巩固】①写出CH4与Br2反应的反应式
②写出CH3CH3与Cl2反应的反应式
【练习4】
1、在光照条件下,下列物质中能与甲烷反应的是
A.盐酸 B.Cl2 C.NaOH溶液 D.酸性KMnO4溶液
2、(双选)下列物质能和甲烷发生取代反应的是( ) A.Cl2 B.CCl4 C.氯水 D.溴蒸气
3、光照下,甲烷与氯气发生取代反应后,共得产物
A.5种 B.2种 C.3种 D.4种
4、在光照的条件下,将等物质的量的甲烷和氯气混合充分反应后,得到产物的物质的量最多的是
A.CH2Cl2 B.CHCl3 C.CCl4 D.HCl
5、将1molCH4和4molCl2发生取代反应,待反应完全后,测得四种有机取代物的物质的量相等,则消耗Cl2为
A.0.5 mol B.2 mol C.2.5 mol D.4 mol
6、下列反应属于取代反应的是( )
解析:
无机反应中的置换反应不属于取代反应。
取代反应“有上有下”的特点
7、下图是CH4、CCl4、CH3Cl分子的球棍模型图,下列说法正确的是
A.CH4、CCl4和CH3Cl都是正四面体结构
B.CH4、CCl4都是正四面体结构
C.CH4和CCl4中的化学键均为非极性键
D.CH4、CCl4的结构相同,性质也相同
一个碳原子以4个单键与其他原子相结合时:
(1)如果这4个原子相同,则构成正四面体。
(2)如果这4个原子不相同,则构成四面体,但不是正四面体。
(3)无论这4个原子是否相同,最多有3个原子共面。
思维启迪
在隔绝空气并加热至1000℃的高温下,甲烷分解
CH4 C + 2H2
高温
合成氨、汽油的原料
橡胶工业的原料
③甲烷的受热分解
四、甲烷的应用
③甲烷在一定条件下氧化生成一氧化碳、氢气的混合物,
用它们可以合成甲醇
① 气体燃料
② 化工原料:制氯仿和氟利昂
甲烷
化学
性质
总体:
一定条件下
能燃烧
易取代
高温分解
性质较稳定
【归纳总结】
不与强酸、强碱反应
不与强氧化剂
(如高锰酸钾、浓硫酸、浓硝酸等)反应
在光照时与氯气或溴蒸气等反应
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
