第三单元 物质构成的奥秘单元测试(word版有答案)
文档属性
| 名称 | 第三单元 物质构成的奥秘单元测试(word版有答案) |
|
|
| 格式 | doc | ||
| 文件大小 | 746.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-15 00:00:00 | ||
图片预览


文档简介
第三单元 物质构成的奥秘
一、选择题:本大题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.广东多地有天然温泉,温泉水中含有丰富的矿物质,泡温泉具有一定的保健、疗养功效。某地温泉水中含有钙、镁、锌、锰等成分,这里的“钙、镁、锌、锰”指的是( )
A.元素 B.原子 C.离子 D.单质
2.【2021·北京】远古时期火法炼铜的原料是孔雀石[主要成分为Cu2(OH)2CO3],组成Cu2(OH)2CO3的元素种类为( )
A. 3种 B. 4种 C. 5种 D. 6种
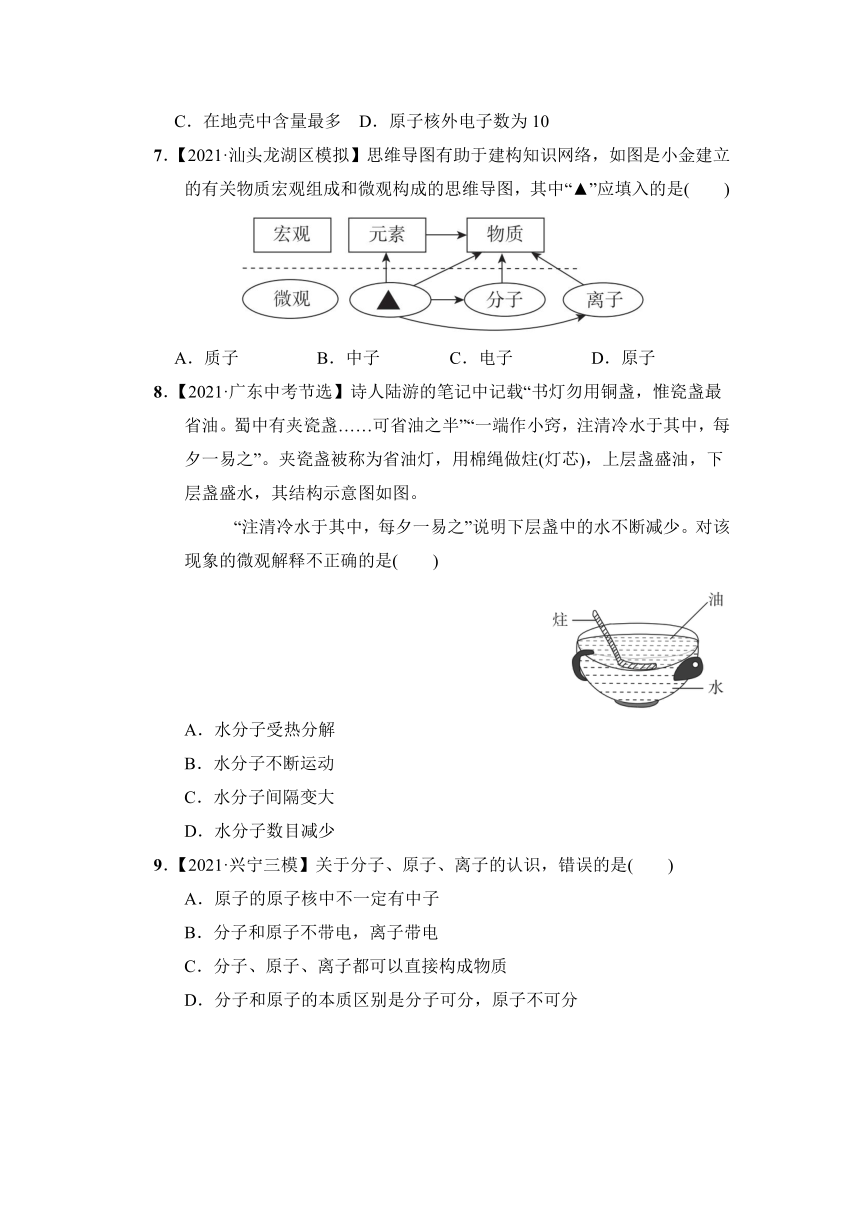
3. 根据某陨石样品中各种元素含量的比例图,请选择以下说法正确的选项( )
A.该陨石含量最多的元素是氧 B.该陨石含量最多的金属元素是硅
C.该陨石只含5种金属元素 D.该陨石一定是纯净物
4.2021年4月,我国科学家首次合成的铀-214,是目前已知质量最小的铀原子。其相对原子质量为214,核外电子数是92。则铀-214原子的中子数为( )
A. 122 B. 92 C. 214 D. 306
5.【2021·汕头龙湖区模拟】移动通信已经进入 5G 时代,铊得到了广泛应用,如图是元素周期表中铊的信息,下列有关铊元素说法不正确的是( )
A.属于金属元素 B.其原子核内有81个质子
C.原子质量是 204.4 D.元素符号为 Tl
6.【2021·安徽】关于原子序数为8的元素,下列说法正确的是( )
A.元素符号为N B.属于金属元素
C.在地壳中含量最多 D.原子核外电子数为10
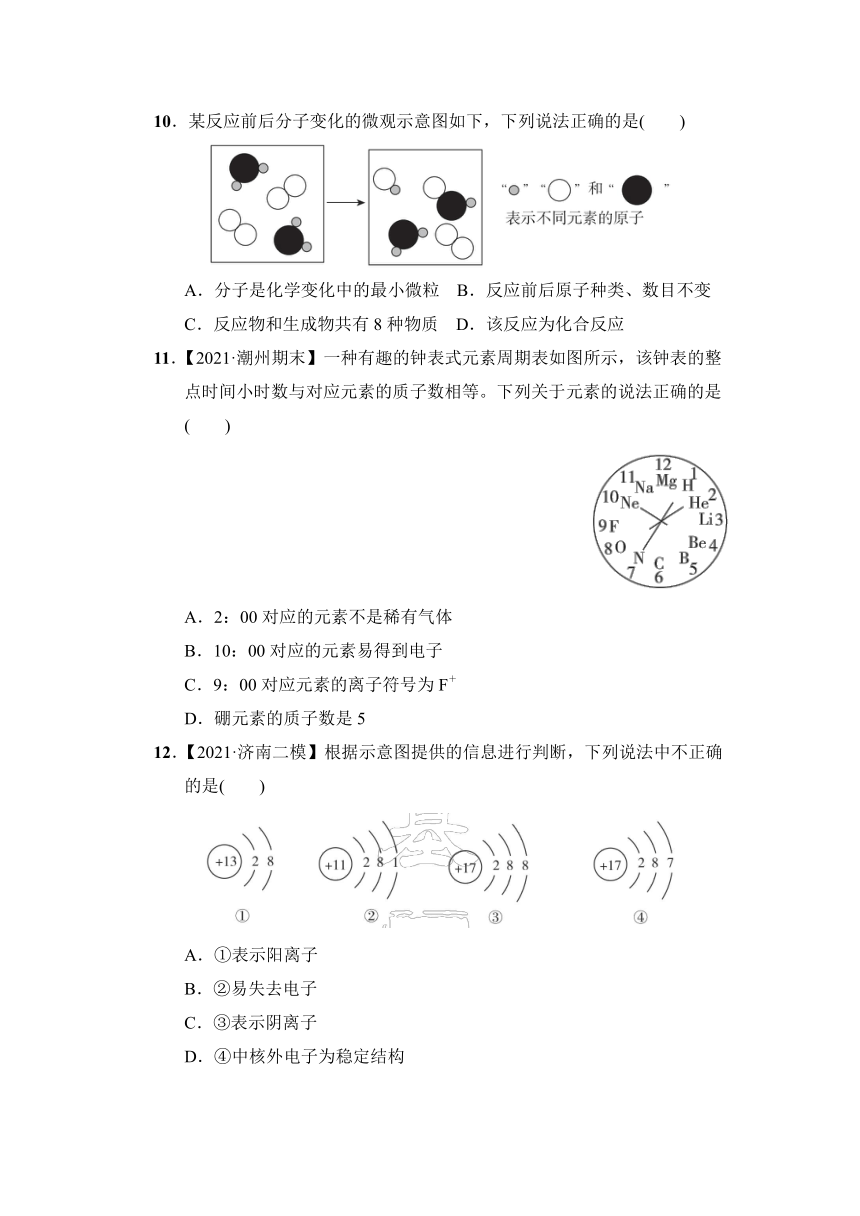
7.【2021·汕头龙湖区模拟】思维导图有助于建构知识网络,如图是小金建立的有关物质宏观组成和微观构成的思维导图,其中“▲”应填入的是( )
A.质子 B.中子 C.电子 D.原子
8.【2021·广东中考节选】诗人陆游的笔记中记载“书灯勿用铜盏,惟瓷盏最省油。蜀中有夹瓷盏……可省油之半”“一端作小窍,注清冷水于其中,每夕一易之”。夹瓷盏被称为省油灯,用棉绳做炷(灯芯),上层盏盛油,下层盏盛水,其结构示意图如图。
“注清冷水于其中,每夕一易之”说明下层盏中的水不断减少。对该现象的微观解释不正确的是( )
A.水分子受热分解
B.水分子不断运动
C.水分子间隔变大
D.水分子数目减少
9.【2021·兴宁三模】关于分子、原子、离子的认识,错误的是( )
A.原子的原子核中不一定有中子
B.分子和原子不带电,离子带电
C.分子、原子、离子都可以直接构成物质
D.分子和原子的本质区别是分子可分,原子不可分
10.某反应前后分子变化的微观示意图如下,下列说法正确的是( )
A.分子是化学变化中的最小微粒 B.反应前后原子种类、数目不变
C.反应物和生成物共有8种物质 D.该反应为化合反应
11.【2021·潮州期末】一种有趣的钟表式元素周期表如图所示,该钟表的整点时间小时数与对应元素的质子数相等。下列关于元素的说法正确的是( )
A.2:00对应的元素不是稀有气体
B.10:00对应的元素易得到电子
C.9:00对应元素的离子符号为F+
D.硼元素的质子数是5
12.【2021·济南二模】根据示意图提供的信息进行判断,下列说法中不正确的是( )
A.①表示阳离子
B.②易失去电子
C.③表示阴离子
D.④中核外电子为稳定结构
13.对下列事实的解释错误的是( )
选项 实例 解释
A 一氧化碳和二氧化碳的化学性质不同 不同种物质的分子性质不同
B 过氧化氢分解,生成水和氧气 化学变化中,分子可分,原子不能再分
C 液氧和氧气的化学性质相同 同种分子性质相同
D 用水银体温计测量体温,水银柱上升 温度升高,分子体积变大
14.【2021·阳西二模】2021年4月13日,日本政府正式决定将东京电力公司福岛第一核电站内储存的核废水排入大海。核废水中含有氚、锶、铯等放射性元素。其中,铯元素的原子结构示意图及其在元素周期表中的信息如图所示,下列关于铯元素的说法错误的是( )
A.铯元素易失去一个电子
B.铯元素的中子数为55
C.铯离子的符号是Cs+
D.铯元素在元素周期表中位于第六周期
15.截止到2021年9月21日,大亚湾核电站已安全运营10 000天,核反应堆中,氧化铕发挥着重要作用。已知某氧原子的实际质量为m g,其相对原子质量为16,铕(Eu)原子的相对原子质量为152,铕(Eu)原子的质量为( )
A. g B. C. g D.
二、非选择题:本大题共6小题,第16小题7分,第17小题8分,第18~21小题各10分,共55分。
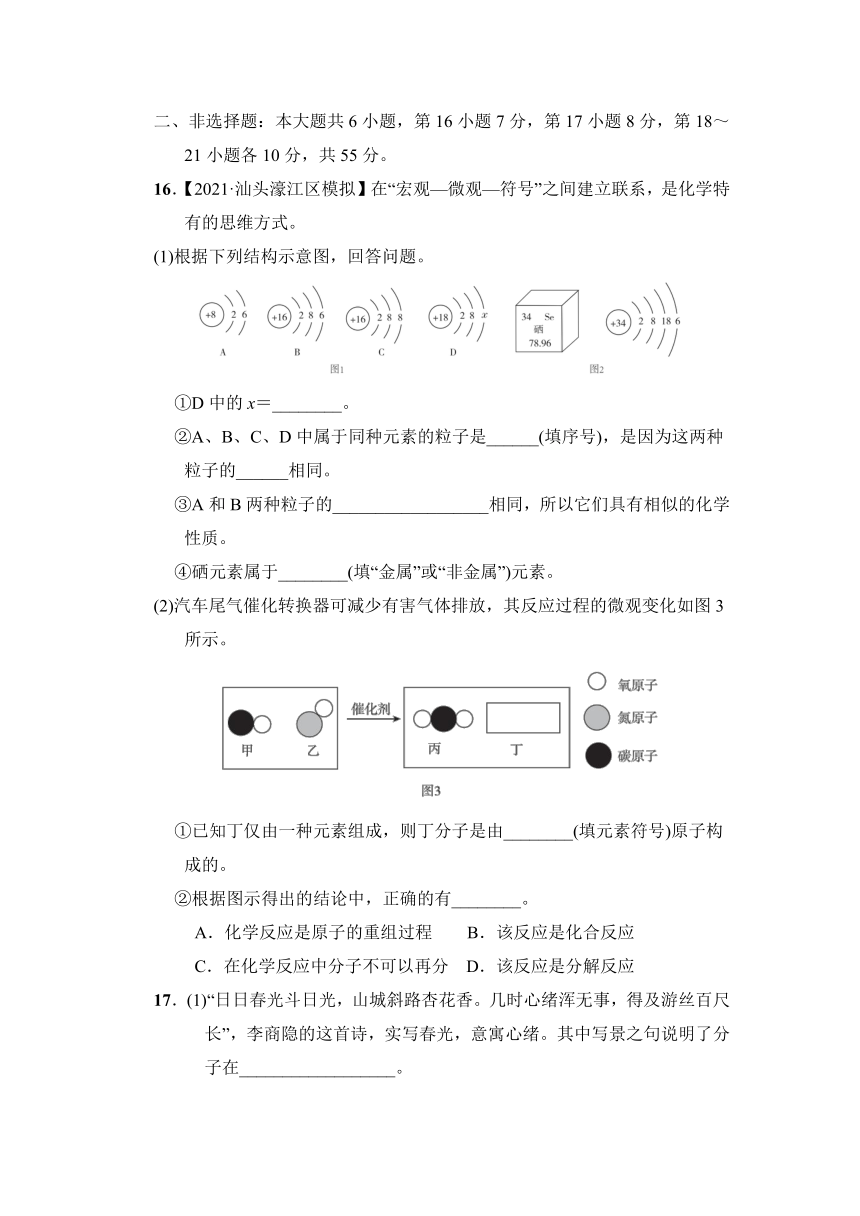
16.【2021·汕头濠江区模拟】在“宏观—微观—符号”之间建立联系,是化学特有的思维方式。
(1)根据下列结构示意图,回答问题。
①D中的x=________。
②A、B、C、D中属于同种元素的粒子是______(填序号),是因为这两种粒子的______相同。
③A和B两种粒子的__________________相同,所以它们具有相似的化学性质。
④硒元素属于________(填“金属”或“非金属”)元素。
(2)汽车尾气催化转换器可减少有害气体排放,其反应过程的微观变化如图3所示。
①已知丁仅由一种元素组成,则丁分子是由________(填元素符号)原子构成的。
②根据图示得出的结论中,正确的有________。
A.化学反应是原子的重组过程 B.该反应是化合反应
C.在化学反应中分子不可以再分 D.该反应是分解反应
17.(1)“日日春光斗日光,山城斜路杏花香。几时心绪浑无事,得及游丝百尺长”,李商隐的这首诗,实写春光,意寓心绪。其中写景之句说明了分子在__________________。
(2)50 mL无水酒精和50 mL水混合后,总体积小于100 mL,说明__________________。
(3)元素周期表是学习化学和研究化学的重要工具。如图所示是元素周期表的部分信息,请认真分析,回答下列问题:
①分析图1规律,可推知图中x=________。
②图2表示的是________(填粒子符号),它的核外电子数为________。
③Al属于________(填“金属”或“非金属”)元素,其原子的核电荷数为________。
④元素周期表中硫元素的有关信息如图3所示,图中“32.06”所表示的含义是______________________________。
18.物质与其构成粒子之间的关系如图。
回答下列问题:
(1)金属铁是由________ (填“原子”“分子”或 “离子”,下同)构成的,二氧化碳是由________构成的。
(2)原子得到或失去电子后形成离子。某粒子的结构示意图为。
①当a=________时,该粒子是原子。
②当a=8时,该粒子是________(填“原子”“阳离子”或“阴离子”)。
③当a=12时,该粒子符号为________。
④上述②③对应的粒子相互作用形成________。
19.根据如图实验,按要求回答问题。
(1)如图1将少量的高锰酸钾固体加入装有水的试管中,实验现象为________________,该现象说明______________________。
(2)图2取两支注射器分别吸入等体积空气和水,再用手指顶住注射器末端的孔,对比感受压缩空气和水的难度差异,水比空气更________(填“难”或“易”)压缩,请从微观的角度解释该实验说明了______________________________。
(3)为了探究分子是否运动,小明设计了如图3所示的实验。
①一段时间后,图3中酚酞的液点由下往上依次变红色,他得出了__________________的结论,但小红觉得小明的实验还不足以证明,她又补充了实验,你觉得没有必要的是______(填序号)。
A.用酒精灯对U形管加热
B.向少量浓氨水中滴加酚酞试液
C.取少量浓氨水放在空气中看是否变色
D.在U形管外放一条相同的酚酞试液纸条
②纸条变色,而棉球没有变色,说明浓氨水和酚酞试液两种物质中________具有挥发性。
③小亮也想探究分子运动,他设计了以下两个实验(图4图5)。
I.图4实验中可观察到________(填“A”或“B”)烧杯中的溶液变为红色。
II.图5实验中可观察________(填“ab”或“bc”)段纱布条先变色。
III.若将图5中装有浓氨水的弯管处浸入冰水中,可观察到纱布条变红的速率变________(填“快”或“慢”)。
20.【2021·广州改编】氢在太阳中的核聚变放出大量光和热(如图所示),是太阳能的来源,掌握可控核聚变技术对人类未来文明发展至关重要。2021年5月,中科院“人造太阳”EAST实验装置创造了氘、氚核聚变在1.2亿摄氏度下运行101秒的新纪录,为世界核聚变研究的发展作出巨大贡献。
氢气是高热值清洁燃料,目前主要通过电解水和天然气重整的方法获取氢气,其中天然气重整制氢的一种原理为甲烷和水在催化剂作用下生成一氧化碳和氢气,一氧化碳和水又在催化剂作用下生成二氧化碳和氢气(甲烷+水一氧化碳+氢气,一氧化碳+水二氧化碳+氢气)。氢氧燃料电池已被用作汽车驱动电源,氢气和氧气在电池内部(含有硫酸等导电物质的溶液)发生反应产生电能。另外,甲烷、乙醇等也可用作燃料电池的燃料,它们在燃料电池中的反应本质上与它们在氧气中的燃烧相同。
原子名称 质子数 中子数 核外电子数
氘(dāo) 1 1 1
氚(chuān) 1 2 1
(1)氘、氚原子的构成如表,它们都属于氢元素的原因是__________相同,它们的化学性质__________(填“相似”或“不相似”)。
(2)上述天然气重整制氢原理的两个反应中,保持不变的粒子是__________________。
(3)燃料电池工作时硫酸(H2SO4)溶液中的离子是________(填化学符号)。
(4)甲烷在氧气中充分燃烧的文字表达式是______________________________________。
21.【2021·揭西期中】已知作为相对原子质量标准的一个碳原子(相对原子质量为12)的质量约为1.993×10-26 kg,一个氧原子的质量约为2.657×10-26 kg。
求:(1)氧原子的相对原子质量(结果保留整数)。
(2)若镁的相对原子质量为24,求一个镁原子的质量。
(3)等质量的金属镁和碳中所含原子的个数比。
答案
一、1.A 2.B 3.A 4.A 5.C 6.C 7.D
8.A 省油灯的原理是油燃烧放热,上层盏内油温升高,下层盏内水吸热,减少油的挥发,以达到省油的目的。下层盏中的水不断减少,是因为水分子不断运动、水分子间隔变大、水分子数目减少。故选A。
9.D 10.B 11.D 12.D 13.D 14.B 15.A
二、16.(1) ① 8 ②B、C ;核电荷数(或质子数)
③最外层电子数 ④非金属
(2) ① N ② A
17.(1)不断地运动 (2)分子之间有间隔
(3)①17 ② Na+ ;10 ③金属;13
④硫的相对原子质量为32.06
18.(1)原子;分子
(2)①10
②阴离子
③Mg2+
④MgO(或氧化镁)
19.(1)试管中的液体变成紫色;构成物质的微粒在不断运动
(2)难;气体分子之间的间隔比较大
(3)①分子在不断运动;A、C ②浓氨水 ③B; ab;慢
点拨:(3)①用酒精灯对U形管加热,如果分子是不断运动的,加热能够加快运动的速率,如果不是不断运动的,加热时分子仍然不运动,A选项没有必要;向少量浓氨水中滴加酚酞试液,观察酚酞试液是否变色,B选项有必要;浓氨水一直与空气接触,C选项没有必要;在U形管外放一条相同的蘸酚酞试液的纸条,进行对比,D选项有必要。
20.(1)核电荷数;相似
(2)碳原子、氢原子、氧原子 (3)H+、SO42-
(4)甲烷+氧气二氧化碳+水
点拨:(4)燃料电池工作时硫酸溶液中起导电作用的离子是氢离子和硫酸根离子,离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。离子符号分别为H+、SO42-。
21.解:(1)已知作为相对原子质量标准的一个碳原子(相对原子质量为12)的质量为1.993×10-26 kg,一个氧原子的质量为2.657×10-26 kg。
氧原子的相对原子质量为≈16
(2)若镁的相对原子质量为24,设一个镁原子的质量为x。
=24
x=3.986×10-26 kg
(3)原子的相对原子质量与原子的实际质量呈正比,镁原子和碳原子的相对原子质量比为24 ∶12=2 ∶1,则镁原子和碳原子的质量比为2 ∶1,故等质量的金属镁和碳中所含原子的个数比为1 ∶2。
答:(1)氧原子的相对原子质量为16;(2)一个镁原子的质量为3.986×10-26 kg;(3)等质量的金属镁和碳中所含原子的个数比为1 ∶2。
一、选择题:本大题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.广东多地有天然温泉,温泉水中含有丰富的矿物质,泡温泉具有一定的保健、疗养功效。某地温泉水中含有钙、镁、锌、锰等成分,这里的“钙、镁、锌、锰”指的是( )
A.元素 B.原子 C.离子 D.单质
2.【2021·北京】远古时期火法炼铜的原料是孔雀石[主要成分为Cu2(OH)2CO3],组成Cu2(OH)2CO3的元素种类为( )
A. 3种 B. 4种 C. 5种 D. 6种
3. 根据某陨石样品中各种元素含量的比例图,请选择以下说法正确的选项( )
A.该陨石含量最多的元素是氧 B.该陨石含量最多的金属元素是硅
C.该陨石只含5种金属元素 D.该陨石一定是纯净物
4.2021年4月,我国科学家首次合成的铀-214,是目前已知质量最小的铀原子。其相对原子质量为214,核外电子数是92。则铀-214原子的中子数为( )
A. 122 B. 92 C. 214 D. 306
5.【2021·汕头龙湖区模拟】移动通信已经进入 5G 时代,铊得到了广泛应用,如图是元素周期表中铊的信息,下列有关铊元素说法不正确的是( )
A.属于金属元素 B.其原子核内有81个质子
C.原子质量是 204.4 D.元素符号为 Tl
6.【2021·安徽】关于原子序数为8的元素,下列说法正确的是( )
A.元素符号为N B.属于金属元素
C.在地壳中含量最多 D.原子核外电子数为10
7.【2021·汕头龙湖区模拟】思维导图有助于建构知识网络,如图是小金建立的有关物质宏观组成和微观构成的思维导图,其中“▲”应填入的是( )
A.质子 B.中子 C.电子 D.原子
8.【2021·广东中考节选】诗人陆游的笔记中记载“书灯勿用铜盏,惟瓷盏最省油。蜀中有夹瓷盏……可省油之半”“一端作小窍,注清冷水于其中,每夕一易之”。夹瓷盏被称为省油灯,用棉绳做炷(灯芯),上层盏盛油,下层盏盛水,其结构示意图如图。
“注清冷水于其中,每夕一易之”说明下层盏中的水不断减少。对该现象的微观解释不正确的是( )
A.水分子受热分解
B.水分子不断运动
C.水分子间隔变大
D.水分子数目减少
9.【2021·兴宁三模】关于分子、原子、离子的认识,错误的是( )
A.原子的原子核中不一定有中子
B.分子和原子不带电,离子带电
C.分子、原子、离子都可以直接构成物质
D.分子和原子的本质区别是分子可分,原子不可分
10.某反应前后分子变化的微观示意图如下,下列说法正确的是( )
A.分子是化学变化中的最小微粒 B.反应前后原子种类、数目不变
C.反应物和生成物共有8种物质 D.该反应为化合反应
11.【2021·潮州期末】一种有趣的钟表式元素周期表如图所示,该钟表的整点时间小时数与对应元素的质子数相等。下列关于元素的说法正确的是( )
A.2:00对应的元素不是稀有气体
B.10:00对应的元素易得到电子
C.9:00对应元素的离子符号为F+
D.硼元素的质子数是5
12.【2021·济南二模】根据示意图提供的信息进行判断,下列说法中不正确的是( )
A.①表示阳离子
B.②易失去电子
C.③表示阴离子
D.④中核外电子为稳定结构
13.对下列事实的解释错误的是( )
选项 实例 解释
A 一氧化碳和二氧化碳的化学性质不同 不同种物质的分子性质不同
B 过氧化氢分解,生成水和氧气 化学变化中,分子可分,原子不能再分
C 液氧和氧气的化学性质相同 同种分子性质相同
D 用水银体温计测量体温,水银柱上升 温度升高,分子体积变大
14.【2021·阳西二模】2021年4月13日,日本政府正式决定将东京电力公司福岛第一核电站内储存的核废水排入大海。核废水中含有氚、锶、铯等放射性元素。其中,铯元素的原子结构示意图及其在元素周期表中的信息如图所示,下列关于铯元素的说法错误的是( )
A.铯元素易失去一个电子
B.铯元素的中子数为55
C.铯离子的符号是Cs+
D.铯元素在元素周期表中位于第六周期
15.截止到2021年9月21日,大亚湾核电站已安全运营10 000天,核反应堆中,氧化铕发挥着重要作用。已知某氧原子的实际质量为m g,其相对原子质量为16,铕(Eu)原子的相对原子质量为152,铕(Eu)原子的质量为( )
A. g B. C. g D.
二、非选择题:本大题共6小题,第16小题7分,第17小题8分,第18~21小题各10分,共55分。
16.【2021·汕头濠江区模拟】在“宏观—微观—符号”之间建立联系,是化学特有的思维方式。
(1)根据下列结构示意图,回答问题。
①D中的x=________。
②A、B、C、D中属于同种元素的粒子是______(填序号),是因为这两种粒子的______相同。
③A和B两种粒子的__________________相同,所以它们具有相似的化学性质。
④硒元素属于________(填“金属”或“非金属”)元素。
(2)汽车尾气催化转换器可减少有害气体排放,其反应过程的微观变化如图3所示。
①已知丁仅由一种元素组成,则丁分子是由________(填元素符号)原子构成的。
②根据图示得出的结论中,正确的有________。
A.化学反应是原子的重组过程 B.该反应是化合反应
C.在化学反应中分子不可以再分 D.该反应是分解反应
17.(1)“日日春光斗日光,山城斜路杏花香。几时心绪浑无事,得及游丝百尺长”,李商隐的这首诗,实写春光,意寓心绪。其中写景之句说明了分子在__________________。
(2)50 mL无水酒精和50 mL水混合后,总体积小于100 mL,说明__________________。
(3)元素周期表是学习化学和研究化学的重要工具。如图所示是元素周期表的部分信息,请认真分析,回答下列问题:
①分析图1规律,可推知图中x=________。
②图2表示的是________(填粒子符号),它的核外电子数为________。
③Al属于________(填“金属”或“非金属”)元素,其原子的核电荷数为________。
④元素周期表中硫元素的有关信息如图3所示,图中“32.06”所表示的含义是______________________________。
18.物质与其构成粒子之间的关系如图。
回答下列问题:
(1)金属铁是由________ (填“原子”“分子”或 “离子”,下同)构成的,二氧化碳是由________构成的。
(2)原子得到或失去电子后形成离子。某粒子的结构示意图为。
①当a=________时,该粒子是原子。
②当a=8时,该粒子是________(填“原子”“阳离子”或“阴离子”)。
③当a=12时,该粒子符号为________。
④上述②③对应的粒子相互作用形成________。
19.根据如图实验,按要求回答问题。
(1)如图1将少量的高锰酸钾固体加入装有水的试管中,实验现象为________________,该现象说明______________________。
(2)图2取两支注射器分别吸入等体积空气和水,再用手指顶住注射器末端的孔,对比感受压缩空气和水的难度差异,水比空气更________(填“难”或“易”)压缩,请从微观的角度解释该实验说明了______________________________。
(3)为了探究分子是否运动,小明设计了如图3所示的实验。
①一段时间后,图3中酚酞的液点由下往上依次变红色,他得出了__________________的结论,但小红觉得小明的实验还不足以证明,她又补充了实验,你觉得没有必要的是______(填序号)。
A.用酒精灯对U形管加热
B.向少量浓氨水中滴加酚酞试液
C.取少量浓氨水放在空气中看是否变色
D.在U形管外放一条相同的酚酞试液纸条
②纸条变色,而棉球没有变色,说明浓氨水和酚酞试液两种物质中________具有挥发性。
③小亮也想探究分子运动,他设计了以下两个实验(图4图5)。
I.图4实验中可观察到________(填“A”或“B”)烧杯中的溶液变为红色。
II.图5实验中可观察________(填“ab”或“bc”)段纱布条先变色。
III.若将图5中装有浓氨水的弯管处浸入冰水中,可观察到纱布条变红的速率变________(填“快”或“慢”)。
20.【2021·广州改编】氢在太阳中的核聚变放出大量光和热(如图所示),是太阳能的来源,掌握可控核聚变技术对人类未来文明发展至关重要。2021年5月,中科院“人造太阳”EAST实验装置创造了氘、氚核聚变在1.2亿摄氏度下运行101秒的新纪录,为世界核聚变研究的发展作出巨大贡献。
氢气是高热值清洁燃料,目前主要通过电解水和天然气重整的方法获取氢气,其中天然气重整制氢的一种原理为甲烷和水在催化剂作用下生成一氧化碳和氢气,一氧化碳和水又在催化剂作用下生成二氧化碳和氢气(甲烷+水一氧化碳+氢气,一氧化碳+水二氧化碳+氢气)。氢氧燃料电池已被用作汽车驱动电源,氢气和氧气在电池内部(含有硫酸等导电物质的溶液)发生反应产生电能。另外,甲烷、乙醇等也可用作燃料电池的燃料,它们在燃料电池中的反应本质上与它们在氧气中的燃烧相同。
原子名称 质子数 中子数 核外电子数
氘(dāo) 1 1 1
氚(chuān) 1 2 1
(1)氘、氚原子的构成如表,它们都属于氢元素的原因是__________相同,它们的化学性质__________(填“相似”或“不相似”)。
(2)上述天然气重整制氢原理的两个反应中,保持不变的粒子是__________________。
(3)燃料电池工作时硫酸(H2SO4)溶液中的离子是________(填化学符号)。
(4)甲烷在氧气中充分燃烧的文字表达式是______________________________________。
21.【2021·揭西期中】已知作为相对原子质量标准的一个碳原子(相对原子质量为12)的质量约为1.993×10-26 kg,一个氧原子的质量约为2.657×10-26 kg。
求:(1)氧原子的相对原子质量(结果保留整数)。
(2)若镁的相对原子质量为24,求一个镁原子的质量。
(3)等质量的金属镁和碳中所含原子的个数比。
答案
一、1.A 2.B 3.A 4.A 5.C 6.C 7.D
8.A 省油灯的原理是油燃烧放热,上层盏内油温升高,下层盏内水吸热,减少油的挥发,以达到省油的目的。下层盏中的水不断减少,是因为水分子不断运动、水分子间隔变大、水分子数目减少。故选A。
9.D 10.B 11.D 12.D 13.D 14.B 15.A
二、16.(1) ① 8 ②B、C ;核电荷数(或质子数)
③最外层电子数 ④非金属
(2) ① N ② A
17.(1)不断地运动 (2)分子之间有间隔
(3)①17 ② Na+ ;10 ③金属;13
④硫的相对原子质量为32.06
18.(1)原子;分子
(2)①10
②阴离子
③Mg2+
④MgO(或氧化镁)
19.(1)试管中的液体变成紫色;构成物质的微粒在不断运动
(2)难;气体分子之间的间隔比较大
(3)①分子在不断运动;A、C ②浓氨水 ③B; ab;慢
点拨:(3)①用酒精灯对U形管加热,如果分子是不断运动的,加热能够加快运动的速率,如果不是不断运动的,加热时分子仍然不运动,A选项没有必要;向少量浓氨水中滴加酚酞试液,观察酚酞试液是否变色,B选项有必要;浓氨水一直与空气接触,C选项没有必要;在U形管外放一条相同的蘸酚酞试液的纸条,进行对比,D选项有必要。
20.(1)核电荷数;相似
(2)碳原子、氢原子、氧原子 (3)H+、SO42-
(4)甲烷+氧气二氧化碳+水
点拨:(4)燃料电池工作时硫酸溶液中起导电作用的离子是氢离子和硫酸根离子,离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。离子符号分别为H+、SO42-。
21.解:(1)已知作为相对原子质量标准的一个碳原子(相对原子质量为12)的质量为1.993×10-26 kg,一个氧原子的质量为2.657×10-26 kg。
氧原子的相对原子质量为≈16
(2)若镁的相对原子质量为24,设一个镁原子的质量为x。
=24
x=3.986×10-26 kg
(3)原子的相对原子质量与原子的实际质量呈正比,镁原子和碳原子的相对原子质量比为24 ∶12=2 ∶1,则镁原子和碳原子的质量比为2 ∶1,故等质量的金属镁和碳中所含原子的个数比为1 ∶2。
答:(1)氧原子的相对原子质量为16;(2)一个镁原子的质量为3.986×10-26 kg;(3)等质量的金属镁和碳中所含原子的个数比为1 ∶2。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
