6.2.2 化学反应中能量变化原因 燃料的选择和氢能的利用 课件(38张PPT)
文档属性
| 名称 | 6.2.2 化学反应中能量变化原因 燃料的选择和氢能的利用 课件(38张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-17 00:00:00 | ||
图片预览









文档简介
(共38张PPT)
专题6 化学反应与能量变化
第二单元 化学反应中的热
第2课时 化学反应中能量变化原因 燃料的选择和氢能的利用
1.能从宏观与微观相结合的角度解释化学反应中的能量变化。
2.能利用化学反应中的能量变化解决生产、生活中的简单问题。
3.能运用化学计量单位定量分析化学变化伴随的能量转化。
学习目标
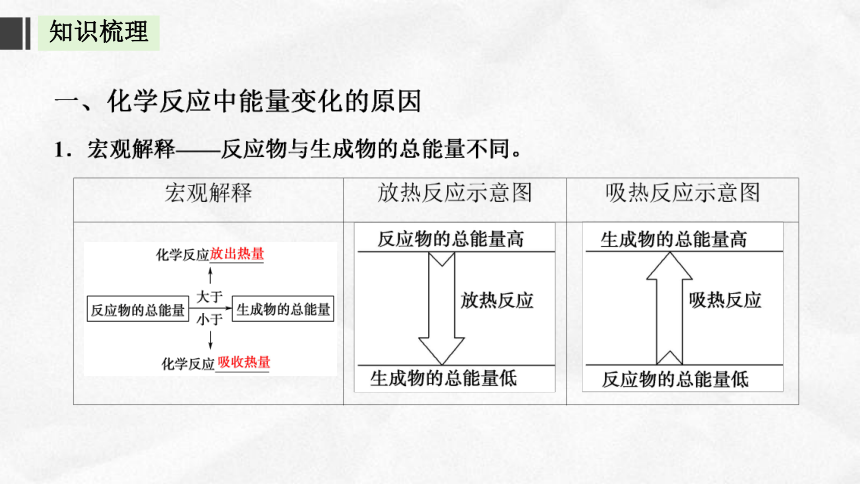
知识梳理
<
>
放出
吸收
热
单位质量
能量
√
×
×
×
探究化学反应中能量变化的原因
能力提升
B
2.已知化学反应N2+3H2
2NH3的能量变化如图所示:
释放
释放
(b-a)
知识应用
当堂检测
D
A B C D
A
A
本节内容结束
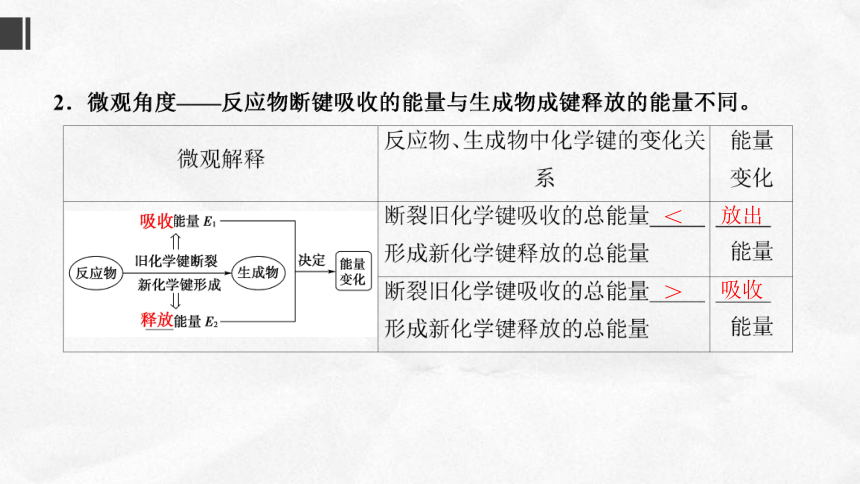
能量E1
旧化学键断裂
决定
生成物
能量
反应物
新化学键形成
变化
能量E2
原料-制取H2的原料是
,资源不受限制
无污染)-H2燃烧的产物是,无污染且可
利用
热值高)--是等质量汽油完全燃烧放出热量的3倍多
电能
N
燃料电池
电解
H20
H2、02化学能
燃烧
热能
太阳能光分解催化剂
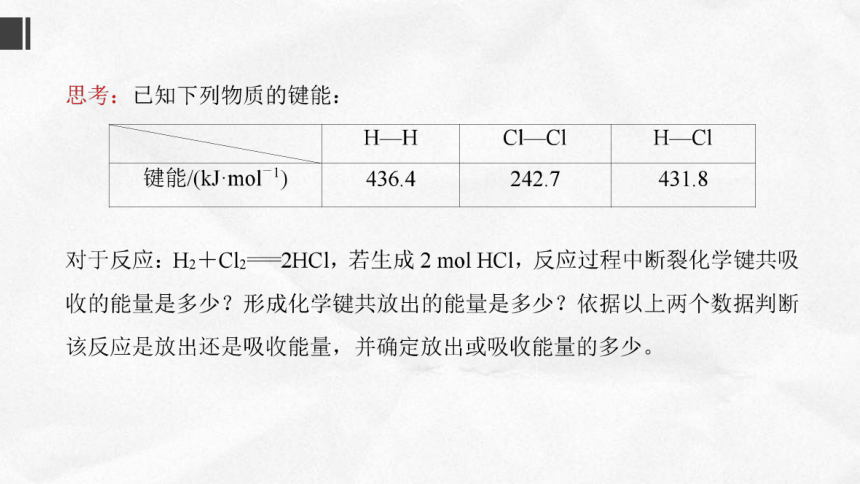
1mol键断裂
吸收
H
436kJ
能量
lmol键断裂
CI
吸收
成
廣
243kJ
能量
放出
放出
431kJ
431kJ
能量
能量
H20流向
能量E增加
1 mol N+3 mol H
△E=akJ
△E=bkJ
mol N(+mol Ha(g)
1 mol NH3(g)↑
△E=ckJ
1 mol NH3(①)
能量
生成物
能量/(kJ-mol-1)
!
浓硫酸
稀盐酸
508
600
d
反应物
N2+3H2
2NH3
反应过程
反应过程
锌粉
专题6 化学反应与能量变化
第二单元 化学反应中的热
第2课时 化学反应中能量变化原因 燃料的选择和氢能的利用
1.能从宏观与微观相结合的角度解释化学反应中的能量变化。
2.能利用化学反应中的能量变化解决生产、生活中的简单问题。
3.能运用化学计量单位定量分析化学变化伴随的能量转化。
学习目标
知识梳理
<
>
放出
吸收
热
单位质量
能量
√
×
×
×
探究化学反应中能量变化的原因
能力提升
B
2.已知化学反应N2+3H2
2NH3的能量变化如图所示:
释放
释放
(b-a)
知识应用
当堂检测
D
A B C D
A
A
本节内容结束
能量E1
旧化学键断裂
决定
生成物
能量
反应物
新化学键形成
变化
能量E2
原料-制取H2的原料是
,资源不受限制
无污染)-H2燃烧的产物是,无污染且可
利用
热值高)--是等质量汽油完全燃烧放出热量的3倍多
电能
N
燃料电池
电解
H20
H2、02化学能
燃烧
热能
太阳能光分解催化剂
1mol键断裂
吸收
H
436kJ
能量
lmol键断裂
CI
吸收
成
廣
243kJ
能量
放出
放出
431kJ
431kJ
能量
能量
H20流向
能量E增加
1 mol N+3 mol H
△E=akJ
△E=bkJ
mol N(+mol Ha(g)
1 mol NH3(g)↑
△E=ckJ
1 mol NH3(①)
能量
生成物
能量/(kJ-mol-1)
!
浓硫酸
稀盐酸
508
600
d
反应物
N2+3H2
2NH3
反应过程
反应过程
锌粉
