2021-2022学年高中化学人教版(2019)选择性必修3-2.1烷烃-课件(18张ppt)
文档属性
| 名称 | 2021-2022学年高中化学人教版(2019)选择性必修3-2.1烷烃-课件(18张ppt) |  | |
| 格式 | pptx | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-17 18:37:42 | ||
图片预览





文档简介
(共18张PPT)
第二章 烃
第一节 烷烃
前 言
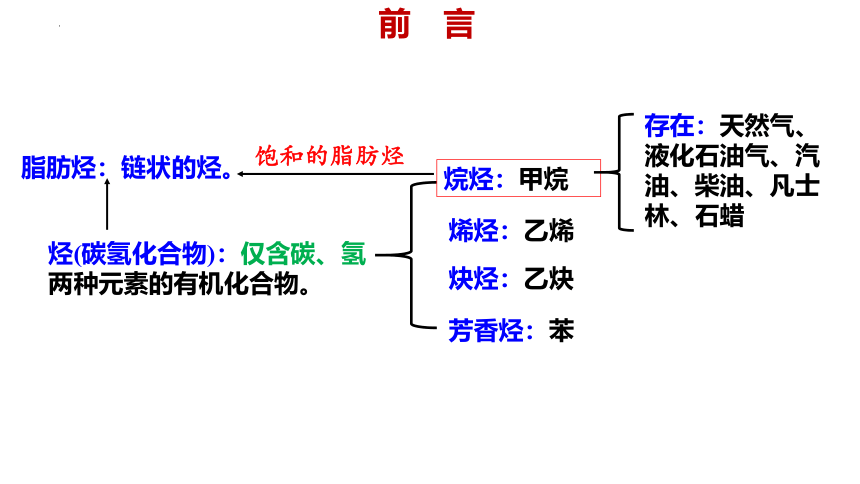
烃(碳氢化合物):仅含碳、氢两种元素的有机化合物。
烷烃:甲烷
烯烃:乙烯
炔烃:乙炔
芳香烃:苯
脂肪烃:链状的烃。
饱和的脂肪烃
存在:天然气、液化石油气、汽油、柴油、凡士林、石蜡
一.烷烃的结构和性质
思考与讨论:请根据图中所示烷烃的分子结构,写出相应的结构简式和分子式,并分析它们在组成和结构上的相似点。
名称 结构简式 分子式 碳原子的 杂化方式 分子中共价键的类型(按原子轨道重叠方式/共用电子对数目)
甲烷
乙烷
丙烷
正丁烷
正戊烷
CH4 CH4 sp3 σ键、单键
CH3CH3 C2H6 sp3 σ键、单键
CH3CH2CH3 C3H8 sp3 σ键、单键
CH3(CH2)2CH3 C4H10 sp3 σ键、单键
CH3(CH2)3CH3 C5H12 sp3 σ键、 单键
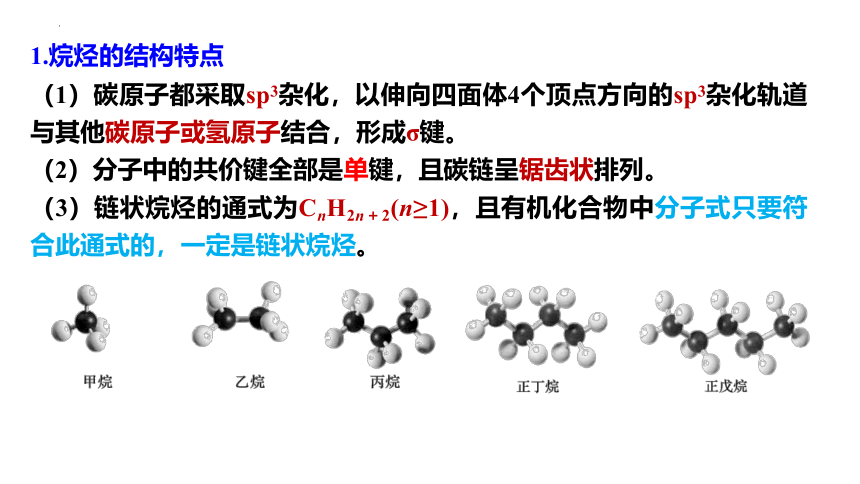
1.烷烃的结构特点
(1)碳原子都采取sp3杂化,以伸向四面体4个顶点方向的sp3杂化轨道与其他碳原子或氢原子结合,形成σ键。
(2)分子中的共价键全部是单键,且碳链呈锯齿状排列。
(3)链状烷烃的通式为CnH2n+2(n≥1),且有机化合物中分子式只要符合此通式的,一定是链状烷烃。
2.烷烃的性质
(1)同系物:
结构相似、分子组成上相差一个或若干个CH2原子团的化合物互称为同系物。
因结构相似,所以化学性质相似;它们的某些物理性质随着相对分子质量的增大而发生规律性的变化。
官能团种类、个数相同
相对分子质量相差14或14的
整数倍
烷烃的物理性质随着分子中碳原子数的递增,有哪些规律性变化?
物理性质 变化规律
状态
熔、沸点
密度
溶解性
(2)物理性质
随碳原子数的增加,常温下存在的状态由气态(≤4)逐渐过渡到液态(5~16)、固态(≥17)。
新戊烷常温下呈气态。
随碳原子数的增加,熔、沸点逐渐升高。
同种烷烃的不同异构体中,支链越多,熔、沸点越低。
都难溶于水,易溶于有机溶剂。
随碳原子数的增加,密度逐渐增大,但比水的小。
(3)甲烷的性质
烷烃的结构决定了其性质与甲烷相似。最简单的烷烃——甲烷是烷烃的代表物。
①物理性质:
纯净的甲烷是无色、无臭的气体,难溶于水,密度比空气小。
②化学性质:
a.甲烷的化学性质比较稳定,常温下不能被酸性高锰酸钾溶液氧化,
也不与强酸、强碱及溴的四氯化碳溶液反应。
b.能在空气中燃烧(可燃性)。
c.能在光照下与氯气发生取代反应。
CH4 + 2O2 CO2 + 2H2O
点燃
产生明亮的蓝色火焰。
连续反应,反应过程不会停留在某一步,所以产物较为复杂,不适合制备物质。
反应生成两种气态物质,三种液态物质。
最多的产物是HCl。
(4)烷烃的化学性质
①烷烃的化学性质比较稳定,常温下不能被酸性高锰酸钾溶液氧化,也不与强酸、强碱及溴的四氯化碳溶液反应。
①氧化反应(可燃性)
链状烷烃燃烧的通式为:
②取代反应
烷烃可与卤素单质在光照下发生取代反应生成卤代烃和卤化氢。
③分解:
烷烃在较高温度下会发生分解。
二.烷烃的命名
1.烃基
丁基:4种 戊基:8种
2.习惯命名法
根据烷烃分子里所含碳原子数目来命名。
(1)碳原子数在十以内的用十大天干来表示:
(2)碳原子数十以上的用数字来表示:
即C原子数目为1~10个的烷烃其对应的名称分别为:甲烷、乙烷、丙烷、丁烷、戊烷、己烷、庚烷、辛烷、壬烷、癸烷。
C原子数目为11 、15、17、20、100等的烷烃其对应的名称分别为:十一烷、十五烷、十七烷、二十烷、一百烷。
(3)没有支链的称“正某烷”,含一个甲基为支链的称“异某烷”,同一碳原子上含两个甲基支链的称“新某烷”。
CH3-CH2-CH2-CH2-CH3
CH3-CH2-CH-CH3
CH3
CH3
CH3-C-CH3
CH3
异戊烷
正戊烷
新戊烷
3、系统命名法
(1)选主链,称“某烷”。
①选定分子中最长的碳链为主链,按主链中碳原子的数目称作“某烷”
CH3—CH—CH2—CH—CH3
CH3 CH2—CH3
己烷
②当出现两条或多条等长的碳链时,
选择含取代基最多的一条作为主链。
CH3—CH—CH2—CH—C—CH3
CH3 C2H5 CH3
选主链原则:碳链最长
取代基最多
己烷
CH3
(2)编序号,定支链
①选主链中离取代基最近的一端为起点,用1、2、3等阿拉伯数字依次给主链上的碳原子编号定位,以确定取代基在主链中的位置。
CH3—CH—CH2—CH—CH3
CH3 CH2—CH3
1 2 3 4
5 6
6 5 4 3
2 1
原则:①起点离支链最近
CH3—CH—CH2—CH—CH—CH3
CH3 C2H5 CH3
②当两个相同取代基分别处于主链两端同等距离,
1 2 3 4 5 6
6 5 4 3 2 1
从离第三个取代基最近的一端开始编号。
CH3—CH2—CH2—CH—CH2—CH3
CH3 C2H5
③当两个不同支链分别处于取代基两端同等距离,
1 2 3 4 5 6
6 5 4 3 2 1
从简单的一端开始编号。
原则:②同样近,简单优先
CH3
CH3—CH—CH2—CH—C—CH3
CH3 C2H5 CH3
④不管从主链的哪端开始,支链的位置都相同,都一样简单(—CH3),
1 2 3 4 5 6
6 5 4 3 2 1
从取代基编号位次之和最小的一端开始。
编序号的原则:最近、最简、最小
原则:③同样近同样简,编号之和最小
(3)写名称
①将取代基的名称写在主链名称的前面,在取代基的前面用阿拉伯数字注明它在主链上的位置,并在数字与名称之间用“—”隔开。
②如果主链上有相同的取代基,将取代基合并起来,用“二、三”等数字表示取代基的个数。表示取代基位置的阿拉伯数字之间用“,”隔开。
③如果主链上有几个不同的取代基,把简单的写在前,复杂的写在后。
1
2
3
4
5
6
CH3—CH — CH — CH2 — CH2 — CH3
CH3
CH3
2,3 — 二 甲基 己烷
主链名称
主链碳原子个数
物质类别
取代基名称
取代基数目
取代基位置
三.烷烃同分异构体的书写——减碳对称法
主链由长到短
支链由整到散
位置由心到边
排布由对、邻、间
用氢补足碳的四价键
书写C6H14的同分异构体
CH3CH2CH2CH2CH2CH3,己烷
,3-甲基戊烷、
,2-甲基戊烷
,2,2-二甲基丁烷、
,2,3-二甲基丁烷
烃基的同分异构体种类数与烃分子中处于不同化学环境的氢原子种类数相同。请写出4种丁基(—C4H9)的结构简式。
—CH2CH2CH2CH3、 、 、
第二章 烃
第一节 烷烃
前 言
烃(碳氢化合物):仅含碳、氢两种元素的有机化合物。
烷烃:甲烷
烯烃:乙烯
炔烃:乙炔
芳香烃:苯
脂肪烃:链状的烃。
饱和的脂肪烃
存在:天然气、液化石油气、汽油、柴油、凡士林、石蜡
一.烷烃的结构和性质
思考与讨论:请根据图中所示烷烃的分子结构,写出相应的结构简式和分子式,并分析它们在组成和结构上的相似点。
名称 结构简式 分子式 碳原子的 杂化方式 分子中共价键的类型(按原子轨道重叠方式/共用电子对数目)
甲烷
乙烷
丙烷
正丁烷
正戊烷
CH4 CH4 sp3 σ键、单键
CH3CH3 C2H6 sp3 σ键、单键
CH3CH2CH3 C3H8 sp3 σ键、单键
CH3(CH2)2CH3 C4H10 sp3 σ键、单键
CH3(CH2)3CH3 C5H12 sp3 σ键、 单键
1.烷烃的结构特点
(1)碳原子都采取sp3杂化,以伸向四面体4个顶点方向的sp3杂化轨道与其他碳原子或氢原子结合,形成σ键。
(2)分子中的共价键全部是单键,且碳链呈锯齿状排列。
(3)链状烷烃的通式为CnH2n+2(n≥1),且有机化合物中分子式只要符合此通式的,一定是链状烷烃。
2.烷烃的性质
(1)同系物:
结构相似、分子组成上相差一个或若干个CH2原子团的化合物互称为同系物。
因结构相似,所以化学性质相似;它们的某些物理性质随着相对分子质量的增大而发生规律性的变化。
官能团种类、个数相同
相对分子质量相差14或14的
整数倍
烷烃的物理性质随着分子中碳原子数的递增,有哪些规律性变化?
物理性质 变化规律
状态
熔、沸点
密度
溶解性
(2)物理性质
随碳原子数的增加,常温下存在的状态由气态(≤4)逐渐过渡到液态(5~16)、固态(≥17)。
新戊烷常温下呈气态。
随碳原子数的增加,熔、沸点逐渐升高。
同种烷烃的不同异构体中,支链越多,熔、沸点越低。
都难溶于水,易溶于有机溶剂。
随碳原子数的增加,密度逐渐增大,但比水的小。
(3)甲烷的性质
烷烃的结构决定了其性质与甲烷相似。最简单的烷烃——甲烷是烷烃的代表物。
①物理性质:
纯净的甲烷是无色、无臭的气体,难溶于水,密度比空气小。
②化学性质:
a.甲烷的化学性质比较稳定,常温下不能被酸性高锰酸钾溶液氧化,
也不与强酸、强碱及溴的四氯化碳溶液反应。
b.能在空气中燃烧(可燃性)。
c.能在光照下与氯气发生取代反应。
CH4 + 2O2 CO2 + 2H2O
点燃
产生明亮的蓝色火焰。
连续反应,反应过程不会停留在某一步,所以产物较为复杂,不适合制备物质。
反应生成两种气态物质,三种液态物质。
最多的产物是HCl。
(4)烷烃的化学性质
①烷烃的化学性质比较稳定,常温下不能被酸性高锰酸钾溶液氧化,也不与强酸、强碱及溴的四氯化碳溶液反应。
①氧化反应(可燃性)
链状烷烃燃烧的通式为:
②取代反应
烷烃可与卤素单质在光照下发生取代反应生成卤代烃和卤化氢。
③分解:
烷烃在较高温度下会发生分解。
二.烷烃的命名
1.烃基
丁基:4种 戊基:8种
2.习惯命名法
根据烷烃分子里所含碳原子数目来命名。
(1)碳原子数在十以内的用十大天干来表示:
(2)碳原子数十以上的用数字来表示:
即C原子数目为1~10个的烷烃其对应的名称分别为:甲烷、乙烷、丙烷、丁烷、戊烷、己烷、庚烷、辛烷、壬烷、癸烷。
C原子数目为11 、15、17、20、100等的烷烃其对应的名称分别为:十一烷、十五烷、十七烷、二十烷、一百烷。
(3)没有支链的称“正某烷”,含一个甲基为支链的称“异某烷”,同一碳原子上含两个甲基支链的称“新某烷”。
CH3-CH2-CH2-CH2-CH3
CH3-CH2-CH-CH3
CH3
CH3
CH3-C-CH3
CH3
异戊烷
正戊烷
新戊烷
3、系统命名法
(1)选主链,称“某烷”。
①选定分子中最长的碳链为主链,按主链中碳原子的数目称作“某烷”
CH3—CH—CH2—CH—CH3
CH3 CH2—CH3
己烷
②当出现两条或多条等长的碳链时,
选择含取代基最多的一条作为主链。
CH3—CH—CH2—CH—C—CH3
CH3 C2H5 CH3
选主链原则:碳链最长
取代基最多
己烷
CH3
(2)编序号,定支链
①选主链中离取代基最近的一端为起点,用1、2、3等阿拉伯数字依次给主链上的碳原子编号定位,以确定取代基在主链中的位置。
CH3—CH—CH2—CH—CH3
CH3 CH2—CH3
1 2 3 4
5 6
6 5 4 3
2 1
原则:①起点离支链最近
CH3—CH—CH2—CH—CH—CH3
CH3 C2H5 CH3
②当两个相同取代基分别处于主链两端同等距离,
1 2 3 4 5 6
6 5 4 3 2 1
从离第三个取代基最近的一端开始编号。
CH3—CH2—CH2—CH—CH2—CH3
CH3 C2H5
③当两个不同支链分别处于取代基两端同等距离,
1 2 3 4 5 6
6 5 4 3 2 1
从简单的一端开始编号。
原则:②同样近,简单优先
CH3
CH3—CH—CH2—CH—C—CH3
CH3 C2H5 CH3
④不管从主链的哪端开始,支链的位置都相同,都一样简单(—CH3),
1 2 3 4 5 6
6 5 4 3 2 1
从取代基编号位次之和最小的一端开始。
编序号的原则:最近、最简、最小
原则:③同样近同样简,编号之和最小
(3)写名称
①将取代基的名称写在主链名称的前面,在取代基的前面用阿拉伯数字注明它在主链上的位置,并在数字与名称之间用“—”隔开。
②如果主链上有相同的取代基,将取代基合并起来,用“二、三”等数字表示取代基的个数。表示取代基位置的阿拉伯数字之间用“,”隔开。
③如果主链上有几个不同的取代基,把简单的写在前,复杂的写在后。
1
2
3
4
5
6
CH3—CH — CH — CH2 — CH2 — CH3
CH3
CH3
2,3 — 二 甲基 己烷
主链名称
主链碳原子个数
物质类别
取代基名称
取代基数目
取代基位置
三.烷烃同分异构体的书写——减碳对称法
主链由长到短
支链由整到散
位置由心到边
排布由对、邻、间
用氢补足碳的四价键
书写C6H14的同分异构体
CH3CH2CH2CH2CH2CH3,己烷
,3-甲基戊烷、
,2-甲基戊烷
,2,2-二甲基丁烷、
,2,3-二甲基丁烷
烃基的同分异构体种类数与烃分子中处于不同化学环境的氢原子种类数相同。请写出4种丁基(—C4H9)的结构简式。
—CH2CH2CH2CH3、 、 、
