8.2.1 乙醇 课件(21张PPT)
文档属性
| 名称 | 8.2.1 乙醇 课件(21张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-18 00:00:00 | ||
图片预览







文档简介
(共21张PPT)
第1课时 乙 醇
第二单元 食品中的有机化合物
专题8 有机化合物的获得与应用
清明时节雨纷纷
路上行人欲断魂
借问酒家何处有
牧童遥指杏花村
清 明
杜牧
情景导入
乙醇俗称酒精,跟我们日常生活密切联系
情景导入
让我
看一看?
想一想?
颜 色 :
气 味 :
状 态:
挥发性:
密 度:
溶解性:
无色透明
特殊香味
液体
比水小
跟水以任意比互溶
能够溶解多种无机物和有机物
易挥发
1.乙醇的物理性质
基础梳理
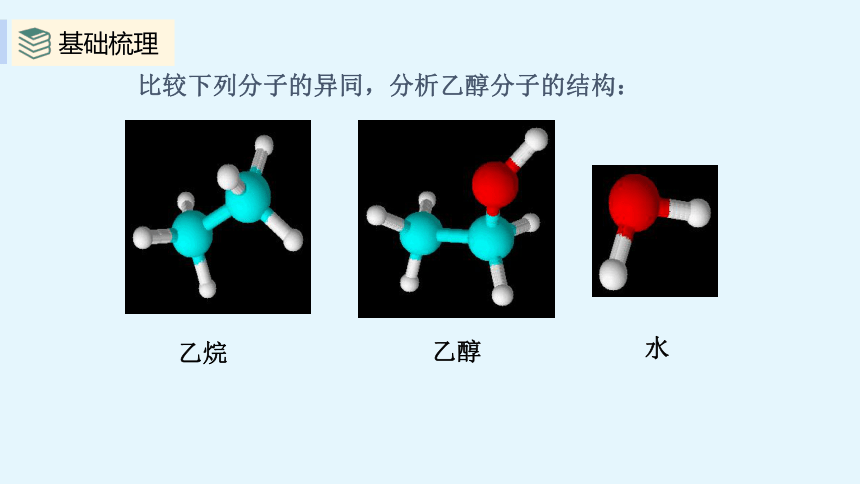
比较下列分子的异同,分析乙醇分子的结构:
乙烷
乙醇
水
基础梳理
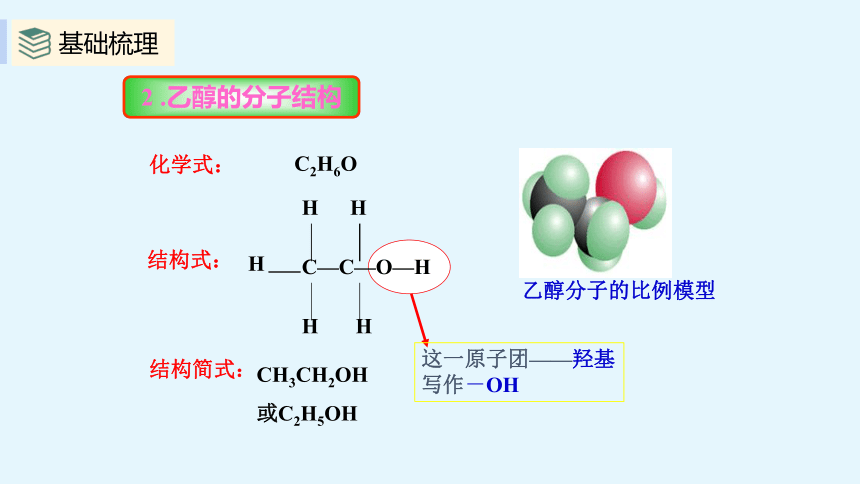
2 .乙醇的分子结构
C—C—O—H
H
H
H
H
H
结构式:
CH3CH2OH
或C2H5OH
这一原子团——羟基
写作-OH
乙醇分子的比例模型
化学式:
C2H6O
结构简式:
基础梳理
比较乙烷和乙醇的结构,下列说法错误的是 。
A.两个碳原子都以单键相连
B.分子里都含有6个相同的氢原子
C. 乙醇可以看成是乙烷分子中的一个氢原子被羟基取代后的产物
B
跟踪练习
分析乙醇分子中存在哪些化学键?推测发生化学反应时,乙醇分子中的哪些化学键可能发生断裂?
思考讨论
[实验]
将两块金属钠分别投入盛有冷水和乙醇的小烧杯中,观察钠与水、与乙醇反应的现象有何异同?哪一个更剧烈? 填写下表:
3 .乙醇的化学性质
(1)乙醇与金属钠反应
基础梳理
项目物质 金属钠的变化 气体燃烧现象 检验产物
水
乙醇
钠浮在水面上,熔
成闪亮的小球,四
处游动,发出“嘶
嘶”响声。钠球迅速变小,最后消失
气体在空
气中燃
烧,发出
淡蓝色火
焰
溶液加酚酞后变红,生成了碱
钠沉于无水酒精
底部,不熔成闪亮
的小球,也不发出
响声,反应缓慢
气体在空
气中燃烧,发出淡蓝色火焰
倒扣在火焰上方的干燥烧杯内壁有水珠,再向烧杯中加入澄清石灰水无明显现象,证明无CO2生成
结论:
①密度:
②羟基上的氢原子与水中氢原子的活泼性:
写出此反应的化学方程式,并判断断键位置。
水>钠>乙醇
水中的H > 羟基中的H
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
其它活泼金属如钾、钙、镁等也可与乙醇反应。
2CH3CH2OH+Mg→(CH3CH2O)2Mg+H2↑
乙醇钠属于离子化合物,易溶于水,在水中易电离。
H—C —C—O—H
H H
H H
—
断开
该反应属于 反应。
置换
练习:写出乙醇与镁反应的化学方程式
①乙醇的燃烧:
CH3CH2OH +3O2 2CO2 + 3H2O
点燃
乙醇与氧气是否只能在点燃的条件下反应呢?
完成 “基础实验”实验2,观察铜丝的变化并闻液体的气味。
(2)乙醇的还原性
实验·探究
②乙醇催化氧化:
催化剂
2CH3CH2OH+O2 2CH3CHO+2H2O
C—C—H
H
H
H
H
O—H
工业上利用此原理生产乙醛
[O]
H2O
Cu或Ag
C2H6O
C—C—H
H
H
H
O
-2H
C2H4O
①与活泼金属反应
②氧化反应——燃烧
——催化氧化
分子结构:
物理性质:
化学性质:
C—C—O—H
H
H
H
H
H
①
②
④
③
①
① ③
全部
乙醇 醇类物质
官能团-OH
反应中乙醇断键位置?
课堂小结
醇氧化机理:
①-③位断键
①
③
R2—C—O—H
R1
H
+ O2
2
生成醛或酮
+ 2H2 O
—C=O
R1
R2
2
Cu
△
原理
②
1.下列有关乙醇的物理性质的应用中不正确的是( )
A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中药的有效成分
C.由于乙醇能够以任意比溶解于水,所以酒厂可以勾兑各种浓度的酒
D.由于乙醇容易挥发,所以才有熟语“酒香不怕巷子深”的说法
A
当堂过关
2.在下列物质中,分别加入金属钠,不能产生氢气的是( )
A. 苯 B .蒸馏水
C .无水酒精 D . 75%的酒精
A
3 .能用来检验酒精中是否含有水的试剂是( )
A . CuSO4·5H2O
C . 浓硫酸
B . CuSO4
D .金属钠
B
4.用工业酒精(95.57%)制备无水乙醇(99.5 % ),可选用的方法是( )
A. 加入足量金属钠,反应完后再蒸馏
B. 加入生石灰再蒸馏
C. 加入浓硫酸,再加热,蒸出乙醇
D. 直接加热蒸馏
B
本节内容结束
第1课时 乙 醇
第二单元 食品中的有机化合物
专题8 有机化合物的获得与应用
清明时节雨纷纷
路上行人欲断魂
借问酒家何处有
牧童遥指杏花村
清 明
杜牧
情景导入
乙醇俗称酒精,跟我们日常生活密切联系
情景导入
让我
看一看?
想一想?
颜 色 :
气 味 :
状 态:
挥发性:
密 度:
溶解性:
无色透明
特殊香味
液体
比水小
跟水以任意比互溶
能够溶解多种无机物和有机物
易挥发
1.乙醇的物理性质
基础梳理
比较下列分子的异同,分析乙醇分子的结构:
乙烷
乙醇
水
基础梳理
2 .乙醇的分子结构
C—C—O—H
H
H
H
H
H
结构式:
CH3CH2OH
或C2H5OH
这一原子团——羟基
写作-OH
乙醇分子的比例模型
化学式:
C2H6O
结构简式:
基础梳理
比较乙烷和乙醇的结构,下列说法错误的是 。
A.两个碳原子都以单键相连
B.分子里都含有6个相同的氢原子
C. 乙醇可以看成是乙烷分子中的一个氢原子被羟基取代后的产物
B
跟踪练习
分析乙醇分子中存在哪些化学键?推测发生化学反应时,乙醇分子中的哪些化学键可能发生断裂?
思考讨论
[实验]
将两块金属钠分别投入盛有冷水和乙醇的小烧杯中,观察钠与水、与乙醇反应的现象有何异同?哪一个更剧烈? 填写下表:
3 .乙醇的化学性质
(1)乙醇与金属钠反应
基础梳理
项目物质 金属钠的变化 气体燃烧现象 检验产物
水
乙醇
钠浮在水面上,熔
成闪亮的小球,四
处游动,发出“嘶
嘶”响声。钠球迅速变小,最后消失
气体在空
气中燃
烧,发出
淡蓝色火
焰
溶液加酚酞后变红,生成了碱
钠沉于无水酒精
底部,不熔成闪亮
的小球,也不发出
响声,反应缓慢
气体在空
气中燃烧,发出淡蓝色火焰
倒扣在火焰上方的干燥烧杯内壁有水珠,再向烧杯中加入澄清石灰水无明显现象,证明无CO2生成
结论:
①密度:
②羟基上的氢原子与水中氢原子的活泼性:
写出此反应的化学方程式,并判断断键位置。
水>钠>乙醇
水中的H > 羟基中的H
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
其它活泼金属如钾、钙、镁等也可与乙醇反应。
2CH3CH2OH+Mg→(CH3CH2O)2Mg+H2↑
乙醇钠属于离子化合物,易溶于水,在水中易电离。
H—C —C—O—H
H H
H H
—
断开
该反应属于 反应。
置换
练习:写出乙醇与镁反应的化学方程式
①乙醇的燃烧:
CH3CH2OH +3O2 2CO2 + 3H2O
点燃
乙醇与氧气是否只能在点燃的条件下反应呢?
完成 “基础实验”实验2,观察铜丝的变化并闻液体的气味。
(2)乙醇的还原性
实验·探究
②乙醇催化氧化:
催化剂
2CH3CH2OH+O2 2CH3CHO+2H2O
C—C—H
H
H
H
H
O—H
工业上利用此原理生产乙醛
[O]
H2O
Cu或Ag
C2H6O
C—C—H
H
H
H
O
-2H
C2H4O
①与活泼金属反应
②氧化反应——燃烧
——催化氧化
分子结构:
物理性质:
化学性质:
C—C—O—H
H
H
H
H
H
①
②
④
③
①
① ③
全部
乙醇 醇类物质
官能团-OH
反应中乙醇断键位置?
课堂小结
醇氧化机理:
①-③位断键
①
③
R2—C—O—H
R1
H
+ O2
2
生成醛或酮
+ 2H2 O
—C=O
R1
R2
2
Cu
△
原理
②
1.下列有关乙醇的物理性质的应用中不正确的是( )
A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中药的有效成分
C.由于乙醇能够以任意比溶解于水,所以酒厂可以勾兑各种浓度的酒
D.由于乙醇容易挥发,所以才有熟语“酒香不怕巷子深”的说法
A
当堂过关
2.在下列物质中,分别加入金属钠,不能产生氢气的是( )
A. 苯 B .蒸馏水
C .无水酒精 D . 75%的酒精
A
3 .能用来检验酒精中是否含有水的试剂是( )
A . CuSO4·5H2O
C . 浓硫酸
B . CuSO4
D .金属钠
B
4.用工业酒精(95.57%)制备无水乙醇(99.5 % ),可选用的方法是( )
A. 加入足量金属钠,反应完后再蒸馏
B. 加入生石灰再蒸馏
C. 加入浓硫酸,再加热,蒸出乙醇
D. 直接加热蒸馏
B
本节内容结束
