8.2.4 糖类 蛋白质和氨基酸 课件(35张PPT)
文档属性
| 名称 | 8.2.4 糖类 蛋白质和氨基酸 课件(35张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 956.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-18 00:00:00 | ||
图片预览










文档简介
(共35张PPT)
第二单元 食品中的有机化合物
第4课时 糖类 蛋白质和氨基酸
专题8 有机化合物的获得与应用
课堂导入
图中是我们常见的一种食物馒头,那么,为什么馒头越嚼越甜呢
肉
蛋
奶
肉、蛋、奶,是我们餐桌上必不可少的食品。它们除了具有美味的口感外,还具有丰富的营养物质。那么,它们都有含有哪些营养物质呢?
学习目标
1.掌握糖类的分类和性质。
2.了解糖类存在和应用。
3.了解蛋白质的组成和主要性质。
4.了解蛋白质在日常生活中的应用。
5.了解氨基酸的结构特点。
学习探究
1.糖类的组成和物理性质
(1)糖类的组成
糖
单糖
二糖
多糖
葡萄糖(带甜味的水果)
果糖(水果中,是甜度最高的糖)
蔗糖
麦芽糖
淀粉
纤维素
(甘蔗 甜菜)
(谷类 豆类 薯类)
(植物的细胞壁 棉花 木材)
一、糖类
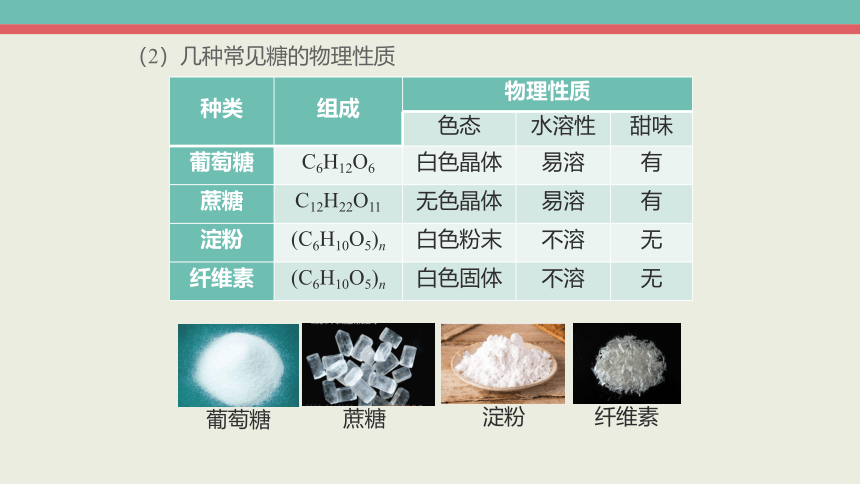
种类 组成 物理性质 色态 水溶性 甜味
葡萄糖 C6H12O6 白色晶体 易溶 有
蔗糖 C12H22O11 无色晶体 易溶 有
淀粉 (C6H10O5)n 白色粉末 不溶 无
纤维素 (C6H10O5)n 白色固体 不溶 无
葡萄糖
蔗糖
淀粉
纤维素
(2)几种常见糖的物理性质
思考
1.糖类物质是否一定有甜味?有甜味的物质是否一定是糖类?
2.为什么人们曾把这些糖类化合物称为“碳水化合物”?
不一定。淀粉、纤维素是没有甜味的。有甜味的物质也不一定是糖类,比如木糖醇,是一种醇类,它也具有甜味
因为葡萄糖、蔗糖、淀粉、纤维素都可以写成Cn(H2O)m,但是并不能认为糖类都能写成Cn(H2O)m
2.糖类的化学性质
(1)麦芽糖、淀粉和纤维素的水解反应
种类 化学方程式
蔗糖 C12H22O11+H2O C6H12O6+C6H12O6
蔗糖 葡萄糖 果糖
淀粉 (C6H10O5)n+nH2O nC6H12O6
淀粉 葡萄糖
纤维素 (C6H10O5)n+nH2O nC6H12O6
纤维素 葡萄糖
(2)葡萄糖的氧化反应
①生理氧化
1 mol葡萄糖缓慢氧化放出2 804 kJ能量,热化学方程式为
C6H12O6(s)+6O2(g) 6CO2(g)+6H2O(l) ΔH=-2 804 kJ·mol-1
②与银氨溶液反应
将葡萄糖溶液滴入盛有银氨溶液的试管并水浴加热,可观察到 。
试管内壁有光亮的银镜产生
实验结论:葡萄糖具有还原性,能够被银氨溶液氧化。
③与新制Cu(OH)2悬浊液反应
将葡萄糖溶液滴入新制Cu(OH)2悬浊液中并加热,可观察到试管内 。
实验结论:葡萄糖具有还原性,能够被新制Cu(OH)2悬浊液氧化。
产生砖红色沉淀
④葡萄糖制造酒精
工业上还可以用葡萄糖造酒精,反应的化学方程式为C6H12O6 2C2H5OH+2CO2↑
(3)淀粉、纤维素有什么异同
属性名称 同 异
淀粉、 纤维素 1.化学式均为(C6H10O5)n 2.本身不显还原性 3.均能水解为葡萄糖 4.均是多糖 5.都是混合物 1.二者分子结构中的n值不同
2.结构不同
3.淀粉能遇碘水变蓝
4.二者既不是同系物,也不是同分异构体
5.纤维素的水解比淀粉难
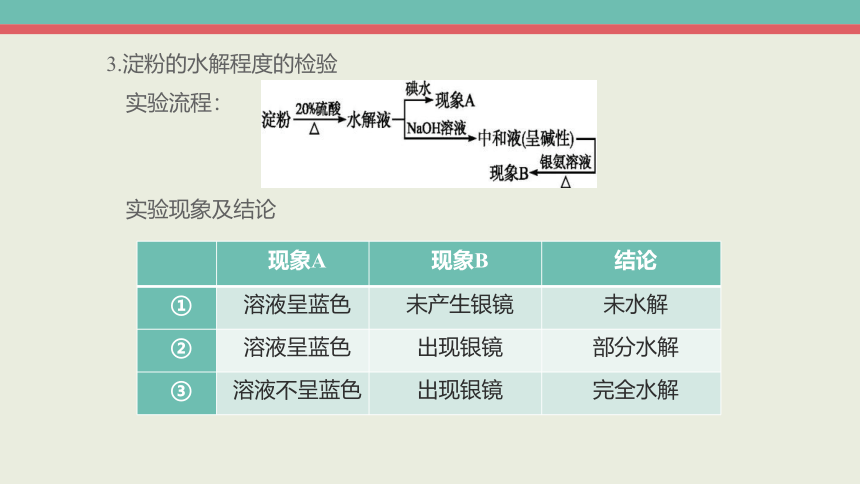
3.淀粉的水解程度的检验
实验流程:
实验现象及结论
现象A 现象B 结论
① 溶液呈蓝色 未产生银镜 未水解
② 溶液呈蓝色 出现银镜 部分水解
③ 溶液不呈蓝色 出现银镜 完全水解
自我检测
将淀粉水解,并用新制的氢氧化铜悬浊液检验其水解产物的实验中,要进行的主要操作是:①加热;②滴入稀硫酸;③加入新制的氢氧化铜悬浊液;④加入足量的氢氧化钠溶液。以上各步操作的先后顺序排列正确的是( )
A.①②③④① B.②①④③①
C.②④①③① D.③④①②①
B
学习探究
二、蛋白质
1.组成
蛋白质中除含有碳、氢、氧外,还含有氮等元素,有的含有硫元素。蛋白质是结构非常复杂的高分子化合物。
蛋白质的四级结构
蛋白质复杂的空间结构
2.性质
探究实验
实验操作 实验现象
蛋白质溶液 加饱和硫酸铵溶液,再加蒸馏水
加稀硫酸,再加蒸馏水
加硫酸铜溶液,再加蒸馏水
加甲醛溶液,再加蒸馏水
加热,再加蒸馏水
有沉淀析出,加水溶解
有沉淀析出,加水不溶解
有沉淀析出,加水不溶解
有沉淀析出,加水不溶解
有沉淀析出,加水不溶解
(1)盐析
蛋白质溶液中加入浓的无机盐溶液,使蛋白质的溶解度降低而析出的现象叫做盐析
特征:
条件:
用途:
(NH4)2SO4等铵盐、Na2SO4等轻金属盐
可逆、物理变化、蛋白质保持活性
分离、提纯蛋白质
(2)变性
蛋白质发生化学变化凝聚成固体物质而析出。
特征:
条件:
用途:
强酸、强碱、重金属盐、酒精、甲醛、加热、紫外线等
不可逆、化学变化、蛋白质失去活性
杀菌消毒、解毒、作动物标本
蛋白质盐析与变性的比较
盐析 变性
涵义
变化条件
变化特征
重要应用
一定条件,溶液中蛋白质凝结为固体析出
在一定条件下,蛋白质失去原有的生理活性、溶解性等性质
浓的轻金属盐
和铵盐溶液
加热/紫外线/X射线/重金属盐/强酸/强碱/甲醛/酒精,等
可逆。蛋白质仍保留原有的生理活性、溶解性等性质
不可逆。蛋白质失去原有的生理活性等性质
分离或提纯蛋白质
消毒、杀菌。保存动物标本,缓解重金属盐中毒
(3)水解
蛋白质在酸、碱或酶的作用下能发生水解,水解的最终产物是多种氨基酸。天然蛋白质水解的产物是多种α-氨基酸。
如:甘氨酸 谷氨酸 苯丙氨酸
4.蛋白质的检验
(1)灼烧
蛋白质灼烧时,产生具有烧焦羽毛的气味
(2)颜色反应
某些蛋白质遇浓硝酸变黄
自我检测
欲将蛋白质从水中析出而又不改变它的性质,应加入 ( )
A.福尔马林
B.18.4 mol·L-1H2SO4溶液
C.饱和Na2SO4溶液
D.1.0 mol·L-1CuSO4溶液
C
三、氨基酸
1.结构特点
官能团:
羧基
氨基
α-氨基酸的结构通式:
H2N— CH—COOH
R
2.化学性质
(1)两性
酸
碱
(2)形成多肽或蛋白质
在一定条件下,氨基酸能发生缩合反应生成多肽,构成蛋白质。
自我检测
一种有机物,其结构简式为 , 下列关于该有机物
酸碱性的叙述正确的是( )
A.既没有酸性,又没有碱性
B.既具有酸性,又具有碱性
C.只有酸性,没有碱性
D.只有碱性,没有酸性
B
糖
单糖
二糖
多糖
葡萄糖(银镜反应、砖红色沉淀)
果糖(甜度最高的糖)
蔗糖
麦芽糖
淀粉
纤维素
(水解产物为葡萄糖和果糖)
(水解产物为葡萄糖,淀粉水解程度的检验)
(水解产物为葡萄糖)
(水解产物为两分子葡萄糖)
课堂小结
α—氨基酸 蛋白质
组成
性质
结构
性质
用途
缩合
水解
1、盐析
2、变性
3、水解
4、检验
当堂检测
1.下列关于葡萄糖的说法中错误的是( )
A.葡萄糖的分子式是C6H12O6
B.葡萄糖属于单糖
C.葡萄糖是碳水化合物,因为它的分子是由6个碳原子和6个水分子组成的
D.葡萄糖能与新制的氢氧化铜悬浊液在加热的条件下发生反应生成砖红色的沉淀
C
2.能说明葡萄糖是一种还原性糖的依据是( )
A.与金属钠反应放出H2
B.能发生银镜反应
C.能与酸发生酯化反应
D.能与H2发生加成反应
B
3.关于蛋白质的下列叙述中,正确的是( )
A.向鸡蛋清中加入稀的(NH4)2SO4溶液,蛋白质会盐析
B.蛋白质是结构复杂的高分子化合物,相对分子质量从几万到几千万
C.向鸡蛋清中加入食盐,会使蛋白质变性
D.天然蛋白质的组成元素仅有碳、氢、氧、氮四种
B
4.下列过程不属于化学变化的是 ( )
A.在蛋白质溶液中,加入饱和硫酸铵溶液,有沉淀析出
B.鸡蛋白溶液受热凝固
C.在蛋白质溶液中,加入硫酸铜溶液,有沉淀析出
D.用稀释的福尔马林溶液(0.1%~0.5%)浸泡植物种子
A
5.下列关于生物体内氨基酸的叙述错误的是( )
A.构成天然蛋白质的氨基酸都是α-氨基酸
B.氨基酸能发生酯化反应
C.氨基酸只有酸性
D.两个氨基酸通过脱水缩合形成二肽
C
6.(1)葡萄糖与银氨溶液的反应。
实验步骤:在 的试管里加入 (制得澄清的银氨溶液),再加入1 mL 10%的葡萄糖溶液,在水浴里加热3~5 min,观察并记录实验现象。
实验现象:试管内壁 。
(2)葡萄糖与新制Cu(OH)2悬浊液的反应。
实验步骤:在洁净的试管里加入2mL 10%的 溶液,滴加4~5滴5%的 溶液,得到含 的氢氧化铜悬浊液。加入2 mL 10%的葡萄糖溶液,加热,观察并记录实验现象。
实验现象:加热至沸腾后,试管中生成了 沉淀。
(3)探究淀粉的水解。
实验步骤:①向两支试管里分别加入4 mL淀粉溶液。
②向其中一支试管里加入碘水,观察溶液颜色的变化。
③向另一支试管里加入少量硫酸,加热4~5 min,待溶液冷却后分装在两支试管中,在一支试管中滴加碘水;将另一支试管中的水解液用氢氧化钠溶液 ,然后加入含氢氧化钠的氢氧化铜悬浊液,并加热至沸腾。
实验现象:向淀粉溶液中加入碘水呈现 色。向淀粉溶液中加入少量硫酸,加热4~5 min,然后再向溶液中加碘水不呈 ,用NaOH溶液中和后再加入新制的Cu(OH)2悬浊液,加热时,有 色沉淀生成。
实验结论:淀粉溶液遇碘单质变为 色,淀粉在硫酸催化作用下水解生成了 。
答案:(1)洁净 2 mL 2%的硝酸银溶液,振荡试管,同时滴加2%的稀氨水,直到析出的沉淀恰好溶解为止 附有光亮的银镜
(2)氢氧化钠 硫酸铜 氢氧化钠 砖红色
(3)中和 蓝 蓝色 砖红 蓝 葡萄糖
本节内容结束
第二单元 食品中的有机化合物
第4课时 糖类 蛋白质和氨基酸
专题8 有机化合物的获得与应用
课堂导入
图中是我们常见的一种食物馒头,那么,为什么馒头越嚼越甜呢
肉
蛋
奶
肉、蛋、奶,是我们餐桌上必不可少的食品。它们除了具有美味的口感外,还具有丰富的营养物质。那么,它们都有含有哪些营养物质呢?
学习目标
1.掌握糖类的分类和性质。
2.了解糖类存在和应用。
3.了解蛋白质的组成和主要性质。
4.了解蛋白质在日常生活中的应用。
5.了解氨基酸的结构特点。
学习探究
1.糖类的组成和物理性质
(1)糖类的组成
糖
单糖
二糖
多糖
葡萄糖(带甜味的水果)
果糖(水果中,是甜度最高的糖)
蔗糖
麦芽糖
淀粉
纤维素
(甘蔗 甜菜)
(谷类 豆类 薯类)
(植物的细胞壁 棉花 木材)
一、糖类
种类 组成 物理性质 色态 水溶性 甜味
葡萄糖 C6H12O6 白色晶体 易溶 有
蔗糖 C12H22O11 无色晶体 易溶 有
淀粉 (C6H10O5)n 白色粉末 不溶 无
纤维素 (C6H10O5)n 白色固体 不溶 无
葡萄糖
蔗糖
淀粉
纤维素
(2)几种常见糖的物理性质
思考
1.糖类物质是否一定有甜味?有甜味的物质是否一定是糖类?
2.为什么人们曾把这些糖类化合物称为“碳水化合物”?
不一定。淀粉、纤维素是没有甜味的。有甜味的物质也不一定是糖类,比如木糖醇,是一种醇类,它也具有甜味
因为葡萄糖、蔗糖、淀粉、纤维素都可以写成Cn(H2O)m,但是并不能认为糖类都能写成Cn(H2O)m
2.糖类的化学性质
(1)麦芽糖、淀粉和纤维素的水解反应
种类 化学方程式
蔗糖 C12H22O11+H2O C6H12O6+C6H12O6
蔗糖 葡萄糖 果糖
淀粉 (C6H10O5)n+nH2O nC6H12O6
淀粉 葡萄糖
纤维素 (C6H10O5)n+nH2O nC6H12O6
纤维素 葡萄糖
(2)葡萄糖的氧化反应
①生理氧化
1 mol葡萄糖缓慢氧化放出2 804 kJ能量,热化学方程式为
C6H12O6(s)+6O2(g) 6CO2(g)+6H2O(l) ΔH=-2 804 kJ·mol-1
②与银氨溶液反应
将葡萄糖溶液滴入盛有银氨溶液的试管并水浴加热,可观察到 。
试管内壁有光亮的银镜产生
实验结论:葡萄糖具有还原性,能够被银氨溶液氧化。
③与新制Cu(OH)2悬浊液反应
将葡萄糖溶液滴入新制Cu(OH)2悬浊液中并加热,可观察到试管内 。
实验结论:葡萄糖具有还原性,能够被新制Cu(OH)2悬浊液氧化。
产生砖红色沉淀
④葡萄糖制造酒精
工业上还可以用葡萄糖造酒精,反应的化学方程式为C6H12O6 2C2H5OH+2CO2↑
(3)淀粉、纤维素有什么异同
属性名称 同 异
淀粉、 纤维素 1.化学式均为(C6H10O5)n 2.本身不显还原性 3.均能水解为葡萄糖 4.均是多糖 5.都是混合物 1.二者分子结构中的n值不同
2.结构不同
3.淀粉能遇碘水变蓝
4.二者既不是同系物,也不是同分异构体
5.纤维素的水解比淀粉难
3.淀粉的水解程度的检验
实验流程:
实验现象及结论
现象A 现象B 结论
① 溶液呈蓝色 未产生银镜 未水解
② 溶液呈蓝色 出现银镜 部分水解
③ 溶液不呈蓝色 出现银镜 完全水解
自我检测
将淀粉水解,并用新制的氢氧化铜悬浊液检验其水解产物的实验中,要进行的主要操作是:①加热;②滴入稀硫酸;③加入新制的氢氧化铜悬浊液;④加入足量的氢氧化钠溶液。以上各步操作的先后顺序排列正确的是( )
A.①②③④① B.②①④③①
C.②④①③① D.③④①②①
B
学习探究
二、蛋白质
1.组成
蛋白质中除含有碳、氢、氧外,还含有氮等元素,有的含有硫元素。蛋白质是结构非常复杂的高分子化合物。
蛋白质的四级结构
蛋白质复杂的空间结构
2.性质
探究实验
实验操作 实验现象
蛋白质溶液 加饱和硫酸铵溶液,再加蒸馏水
加稀硫酸,再加蒸馏水
加硫酸铜溶液,再加蒸馏水
加甲醛溶液,再加蒸馏水
加热,再加蒸馏水
有沉淀析出,加水溶解
有沉淀析出,加水不溶解
有沉淀析出,加水不溶解
有沉淀析出,加水不溶解
有沉淀析出,加水不溶解
(1)盐析
蛋白质溶液中加入浓的无机盐溶液,使蛋白质的溶解度降低而析出的现象叫做盐析
特征:
条件:
用途:
(NH4)2SO4等铵盐、Na2SO4等轻金属盐
可逆、物理变化、蛋白质保持活性
分离、提纯蛋白质
(2)变性
蛋白质发生化学变化凝聚成固体物质而析出。
特征:
条件:
用途:
强酸、强碱、重金属盐、酒精、甲醛、加热、紫外线等
不可逆、化学变化、蛋白质失去活性
杀菌消毒、解毒、作动物标本
蛋白质盐析与变性的比较
盐析 变性
涵义
变化条件
变化特征
重要应用
一定条件,溶液中蛋白质凝结为固体析出
在一定条件下,蛋白质失去原有的生理活性、溶解性等性质
浓的轻金属盐
和铵盐溶液
加热/紫外线/X射线/重金属盐/强酸/强碱/甲醛/酒精,等
可逆。蛋白质仍保留原有的生理活性、溶解性等性质
不可逆。蛋白质失去原有的生理活性等性质
分离或提纯蛋白质
消毒、杀菌。保存动物标本,缓解重金属盐中毒
(3)水解
蛋白质在酸、碱或酶的作用下能发生水解,水解的最终产物是多种氨基酸。天然蛋白质水解的产物是多种α-氨基酸。
如:甘氨酸 谷氨酸 苯丙氨酸
4.蛋白质的检验
(1)灼烧
蛋白质灼烧时,产生具有烧焦羽毛的气味
(2)颜色反应
某些蛋白质遇浓硝酸变黄
自我检测
欲将蛋白质从水中析出而又不改变它的性质,应加入 ( )
A.福尔马林
B.18.4 mol·L-1H2SO4溶液
C.饱和Na2SO4溶液
D.1.0 mol·L-1CuSO4溶液
C
三、氨基酸
1.结构特点
官能团:
羧基
氨基
α-氨基酸的结构通式:
H2N— CH—COOH
R
2.化学性质
(1)两性
酸
碱
(2)形成多肽或蛋白质
在一定条件下,氨基酸能发生缩合反应生成多肽,构成蛋白质。
自我检测
一种有机物,其结构简式为 , 下列关于该有机物
酸碱性的叙述正确的是( )
A.既没有酸性,又没有碱性
B.既具有酸性,又具有碱性
C.只有酸性,没有碱性
D.只有碱性,没有酸性
B
糖
单糖
二糖
多糖
葡萄糖(银镜反应、砖红色沉淀)
果糖(甜度最高的糖)
蔗糖
麦芽糖
淀粉
纤维素
(水解产物为葡萄糖和果糖)
(水解产物为葡萄糖,淀粉水解程度的检验)
(水解产物为葡萄糖)
(水解产物为两分子葡萄糖)
课堂小结
α—氨基酸 蛋白质
组成
性质
结构
性质
用途
缩合
水解
1、盐析
2、变性
3、水解
4、检验
当堂检测
1.下列关于葡萄糖的说法中错误的是( )
A.葡萄糖的分子式是C6H12O6
B.葡萄糖属于单糖
C.葡萄糖是碳水化合物,因为它的分子是由6个碳原子和6个水分子组成的
D.葡萄糖能与新制的氢氧化铜悬浊液在加热的条件下发生反应生成砖红色的沉淀
C
2.能说明葡萄糖是一种还原性糖的依据是( )
A.与金属钠反应放出H2
B.能发生银镜反应
C.能与酸发生酯化反应
D.能与H2发生加成反应
B
3.关于蛋白质的下列叙述中,正确的是( )
A.向鸡蛋清中加入稀的(NH4)2SO4溶液,蛋白质会盐析
B.蛋白质是结构复杂的高分子化合物,相对分子质量从几万到几千万
C.向鸡蛋清中加入食盐,会使蛋白质变性
D.天然蛋白质的组成元素仅有碳、氢、氧、氮四种
B
4.下列过程不属于化学变化的是 ( )
A.在蛋白质溶液中,加入饱和硫酸铵溶液,有沉淀析出
B.鸡蛋白溶液受热凝固
C.在蛋白质溶液中,加入硫酸铜溶液,有沉淀析出
D.用稀释的福尔马林溶液(0.1%~0.5%)浸泡植物种子
A
5.下列关于生物体内氨基酸的叙述错误的是( )
A.构成天然蛋白质的氨基酸都是α-氨基酸
B.氨基酸能发生酯化反应
C.氨基酸只有酸性
D.两个氨基酸通过脱水缩合形成二肽
C
6.(1)葡萄糖与银氨溶液的反应。
实验步骤:在 的试管里加入 (制得澄清的银氨溶液),再加入1 mL 10%的葡萄糖溶液,在水浴里加热3~5 min,观察并记录实验现象。
实验现象:试管内壁 。
(2)葡萄糖与新制Cu(OH)2悬浊液的反应。
实验步骤:在洁净的试管里加入2mL 10%的 溶液,滴加4~5滴5%的 溶液,得到含 的氢氧化铜悬浊液。加入2 mL 10%的葡萄糖溶液,加热,观察并记录实验现象。
实验现象:加热至沸腾后,试管中生成了 沉淀。
(3)探究淀粉的水解。
实验步骤:①向两支试管里分别加入4 mL淀粉溶液。
②向其中一支试管里加入碘水,观察溶液颜色的变化。
③向另一支试管里加入少量硫酸,加热4~5 min,待溶液冷却后分装在两支试管中,在一支试管中滴加碘水;将另一支试管中的水解液用氢氧化钠溶液 ,然后加入含氢氧化钠的氢氧化铜悬浊液,并加热至沸腾。
实验现象:向淀粉溶液中加入碘水呈现 色。向淀粉溶液中加入少量硫酸,加热4~5 min,然后再向溶液中加碘水不呈 ,用NaOH溶液中和后再加入新制的Cu(OH)2悬浊液,加热时,有 色沉淀生成。
实验结论:淀粉溶液遇碘单质变为 色,淀粉在硫酸催化作用下水解生成了 。
答案:(1)洁净 2 mL 2%的硝酸银溶液,振荡试管,同时滴加2%的稀氨水,直到析出的沉淀恰好溶解为止 附有光亮的银镜
(2)氢氧化钠 硫酸铜 氢氧化钠 砖红色
(3)中和 蓝 蓝色 砖红 蓝 葡萄糖
本节内容结束
