2021-2022学年度人教版九年级化学下册课件 9.2.2 溶解度(共21张PPT)
文档属性
| 名称 | 2021-2022学年度人教版九年级化学下册课件 9.2.2 溶解度(共21张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-18 00:00:00 | ||
图片预览






文档简介
(共21张PPT)
九年级化学人教版
第九单元 溶液
课题2 溶解度
第二课时 溶解度
新课引入
NaCl
KNO3
我溶解能力强,20℃时,50g水中最多可溶解18g。
那有什么了不起,我 10 ℃时,100g水中最多可溶解20.9g。
哼!我才用了50g水,你呢!100g…
我比你强!
也不想想你的温度比我高呀!我在60 ℃,50g水中最多溶解55g…
食盐与硝酸钾相比,谁在水中的溶解能力更强……
如何比较NaCl、KNO3的溶解性大小?
新课引入
20℃
40℃
应该在同一温度下
NaCl
KNO3
不行
能否以此来比较KNO3 和NaCl 的溶解性大小呢?
新课引入
溶剂量应该相同
20℃,20g水
20℃,100g水
NaCl
KNO3
不行
能否以此来比较KNO3 和NaCl 的溶解性大小呢?
新课引入
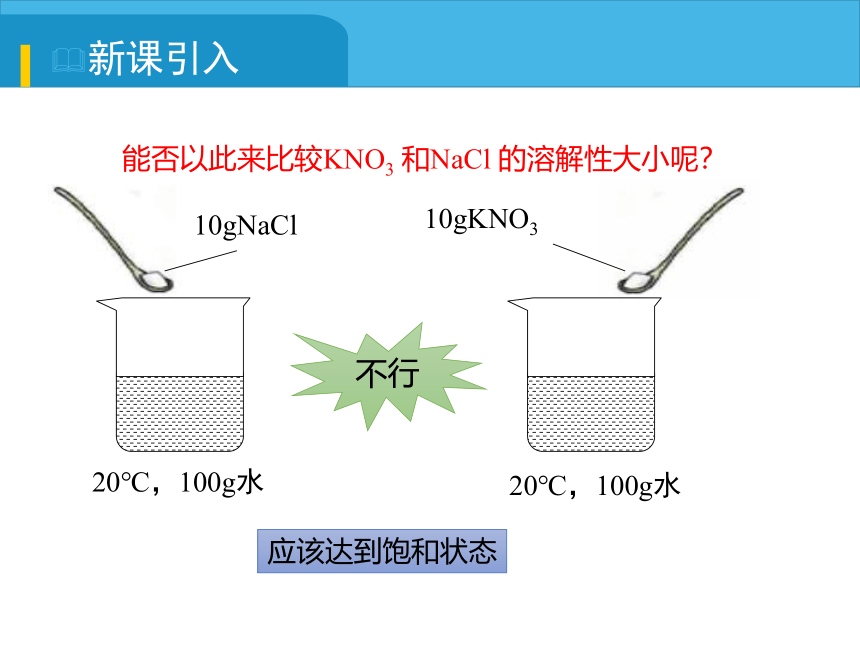
20℃,100g水
20℃,100g水
110gNaCl
10gKNO3
应该达到饱和状态
不行
能否以此来比较KNO3 和NaCl 的溶解性大小呢?
新课引入
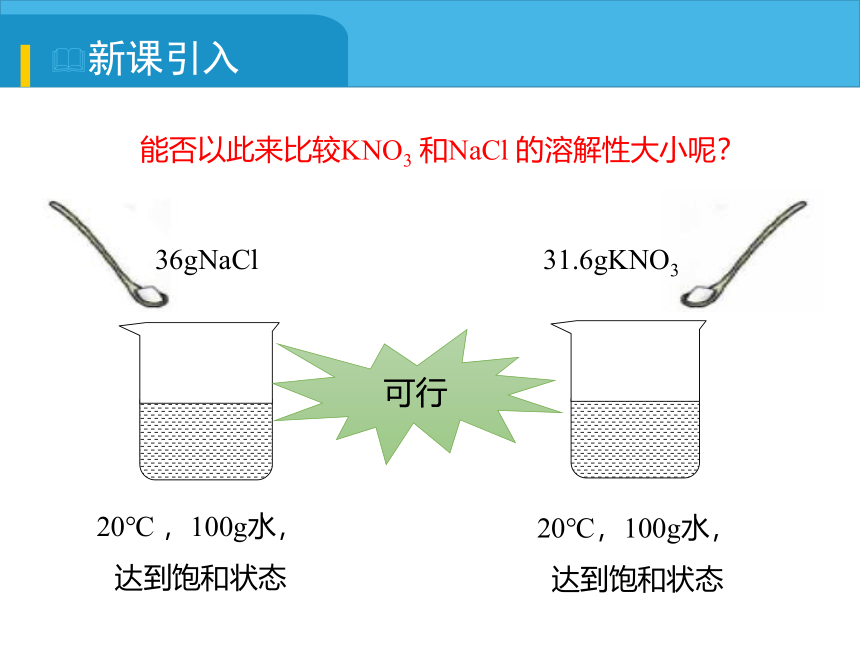
36gNaCl
31.6gKNO3
20℃ ,100g水,
达到饱和状态
20℃,100g水,
达到饱和状态
可行
能否以此来比较KNO3 和NaCl 的溶解性大小呢?
新课讲解
一、固体的溶解度
在一定温度下,某物质在100g溶剂里达到饱和状态时所溶解的质量,叫做这种溶质在这种溶剂里的溶解度。
注意:四个关键词必须同时满足,溶解度才有意义。
(1)条件:在一定温度下;
(2)标准:在100g溶剂里;
(3)状态:达到饱和状态时;
(4)单位:质量常用单位“克”。
在20℃时,NaCl在100g水中达到饱和状态时,所溶解的质量是36g。
在20℃时,100g水中最多能溶解36g NaCl 。
例如,20℃时NaCl的溶解度为36g,其含义是
新课讲解
【辨析】下列说法是否正确?
(1)食盐在水里的溶解度是36g。
(2)20℃时,硝酸钾的溶解度为31.6。
(3)20℃时,50g水中加入18g食盐后溶液恰好饱和,因此,20℃时,食盐在水中的溶解度为18g。
(4)10℃时,100g水里溶解了10g蔗糖,所以10℃时,蔗糖在水中的溶解度为10g。
错误,没有指明温度。
错误,没有单位,溶解度的单位是克。
错误,溶解度是指物质在100g溶剂里所溶解的最大质量,此时食盐的溶解度为36g。
错误,没有指明达到饱和状态,溶解度是指一定温度下,物质在100g溶剂里所溶解的最大质量。
新课讲解
【注意】溶解性和溶解度的比较
☆ 区别:
溶解性:是说明物质溶解能力的定性方法,是物质的一种物理性质。
溶解度:是衡量一定温度下物质在某种溶剂里溶解性大小的尺度,是溶解性的定量表示方法。
☆ 联系:
20℃的溶解度/g <0.01 0.01~1 1~10 >10
溶解性描述 难溶 微溶 可溶 易溶
难溶
微溶
可溶
易溶
0.01
1
10
20℃
g/100g
【巧记】
新课讲解
二、固体溶解度曲线及意义
溶解度曲线是借助数学的方法,用图像将物质的溶解度随温度变化的情况直观地表示出来。
新课讲解
影响固体溶解度的因素
☆内因:溶质、溶剂的性质
☆外因:温度
(1)大多数固体物质的溶解度随温度的升高而升高;
(2)少数物质(如NaCl)的溶解度受温度的影响很小;
(3)极少数物质[如Ca(OH)2]的溶解度随温度的升高而降低。
新课讲解
N
M
温度/℃
溶解度\克
t1
t2
0
●
b
●
●
a
两曲线的交点:
表示两物质在交点所示的温度下的溶解度相等;
表示在交点所示的温度下两物质的饱和溶液质量分数相等。
●
c
曲线下方的点:
不饱和溶液
曲线上方的点:形成饱和溶液并有物质剩余。
10
20
曲线上的点:
表示物质在
该点所示温度
下的溶解度。
新课讲解
【注意】溶解度曲线的应用
1、判断某种物质在不同温度下的溶解度是多少;
2、比较不同物质在同一温度下的溶解度大小;
3、判断物质的溶解度受温度影响变化的趋势——看曲线倾斜度;
4、判断将饱和溶液转化为不饱和溶液的方法:改变温度或改变溶质质量;
5、确定使溶质结晶析出的方法:改变温度或蒸发溶剂;
6、确定混合物分离、提纯的方法。
新课讲解
三、气体溶解度的定义
某气体在压强为101kPa,一定温度时,在1体积水中达到饱和状态时所溶解的体积。
【注意】定义中的几个关键词:
①一定温度下;
②101 kPa;
③1体积水中;
④饱和时的气体体积数。
已知0℃、1个标准大气压时1体积水最多能溶解0.049体积氧气,此时氧气的溶解度为0.049。
新课讲解
【思考】喝汽水的时候,为什么会打开瓶塞汽水会自动喷出来?喝了冰镇汽水以后,为什么常常会打嗝?
汽水中溶解了一定量的二氧化碳气体,当外界条件(如温度、压强)变化时,二氧化碳在水中的溶解度也会发生变化,导致二氧化碳从溶液中逸出。
气体的溶解度随温度的升高而减小,随压强的增大而增大。
归纳小结
1、固体溶解度表示在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量;
2、气体的溶解度通常是指该气体的压强为101kPa和一定温度时,溶解在1体积水里达到饱和状态时的气体体积。
3、物质的溶解度随温度变化的曲线叫做溶解度曲线。利用溶解度曲线,可以获得许多有关物质溶解度的信息。
强化训练
1、60℃时,硝酸钾的溶解度为110g。在60℃时,将70g硝酸钾投入50g水中充分搅拌后得到溶液的质量是( )
A.105g B.110g C.120g D.210g
A
【解析】
60℃时,KNO3的溶解度为110g,在此温度下50g水中最多溶解55gKNO3固体,形成这一温度下的饱和溶液,因此饱和溶液的质量为50g+55g=105g。
强化训练
2、如图是A、B、C三种物质的溶解度曲线。下列说法错误的是( )
A.C的溶解度随温度的升高而减小
B.t2℃时A、B、C的溶解度大小为A=B>C
C.t2℃A、B、C的饱和溶液降温到t1℃时,
A、C两溶液中溶质的质量分数相等
D.t1℃时,A的饱和溶液中溶质质量分数为20%
C
【解析】A、由溶解度曲线图可知:C的溶解度随温度的升高而减小,故正确;
B、t2℃时,A、B、C三种物质的溶解度大小为:A=B>C,故正确;
C、t2℃时,A、B、C三种物质的饱和溶液溶质质量分数由大到小的顺序为:A=B>C;当降温到t1℃,A仍为饱和溶液,C为不饱和溶液,与t2℃时溶液溶质的质量分数相等,在t1℃时A的溶解度大于t2℃时C的溶解度,故降温至t1℃时,A溶液的溶质质量分数大于C溶液的溶质质量分数,故错误;
D、t1℃时,A物质的溶解度为25g,所以饱和溶液中溶质的质量分数是:25g/125g×100%=20%,故正确。
3、家庭生活中烧开水时,会看到有大量气泡从水中冒出,这是因为温度升高时( )
A.水发生了分解反应
B.空气在水中的溶解度减小
C.水与壶发生了化学反应
D.空气在水中的溶解性增强
强化训练
B
【解析】
气体的溶解度随温度的升高而减小,故家庭生活中烧开水时,会看到有大量气泡从水中冒出。
布置作业
在炎热的夏日,特别是闷热的午后,鱼塘需要及时充氧,否则会出现“死鱼”现象,请你说明原因?
【参考答案】夏日闷热的午后,鱼塘中因温度高、气压低,氧气在水中的溶解度明显降低,如果不及时充氧,会因水中氧气含量小,而出现“死鱼”现象。
本课结束
九年级化学人教版
第九单元 溶液
课题2 溶解度
第二课时 溶解度
新课引入
NaCl
KNO3
我溶解能力强,20℃时,50g水中最多可溶解18g。
那有什么了不起,我 10 ℃时,100g水中最多可溶解20.9g。
哼!我才用了50g水,你呢!100g…
我比你强!
也不想想你的温度比我高呀!我在60 ℃,50g水中最多溶解55g…
食盐与硝酸钾相比,谁在水中的溶解能力更强……
如何比较NaCl、KNO3的溶解性大小?
新课引入
20℃
40℃
应该在同一温度下
NaCl
KNO3
不行
能否以此来比较KNO3 和NaCl 的溶解性大小呢?
新课引入
溶剂量应该相同
20℃,20g水
20℃,100g水
NaCl
KNO3
不行
能否以此来比较KNO3 和NaCl 的溶解性大小呢?
新课引入
20℃,100g水
20℃,100g水
110gNaCl
10gKNO3
应该达到饱和状态
不行
能否以此来比较KNO3 和NaCl 的溶解性大小呢?
新课引入
36gNaCl
31.6gKNO3
20℃ ,100g水,
达到饱和状态
20℃,100g水,
达到饱和状态
可行
能否以此来比较KNO3 和NaCl 的溶解性大小呢?
新课讲解
一、固体的溶解度
在一定温度下,某物质在100g溶剂里达到饱和状态时所溶解的质量,叫做这种溶质在这种溶剂里的溶解度。
注意:四个关键词必须同时满足,溶解度才有意义。
(1)条件:在一定温度下;
(2)标准:在100g溶剂里;
(3)状态:达到饱和状态时;
(4)单位:质量常用单位“克”。
在20℃时,NaCl在100g水中达到饱和状态时,所溶解的质量是36g。
在20℃时,100g水中最多能溶解36g NaCl 。
例如,20℃时NaCl的溶解度为36g,其含义是
新课讲解
【辨析】下列说法是否正确?
(1)食盐在水里的溶解度是36g。
(2)20℃时,硝酸钾的溶解度为31.6。
(3)20℃时,50g水中加入18g食盐后溶液恰好饱和,因此,20℃时,食盐在水中的溶解度为18g。
(4)10℃时,100g水里溶解了10g蔗糖,所以10℃时,蔗糖在水中的溶解度为10g。
错误,没有指明温度。
错误,没有单位,溶解度的单位是克。
错误,溶解度是指物质在100g溶剂里所溶解的最大质量,此时食盐的溶解度为36g。
错误,没有指明达到饱和状态,溶解度是指一定温度下,物质在100g溶剂里所溶解的最大质量。
新课讲解
【注意】溶解性和溶解度的比较
☆ 区别:
溶解性:是说明物质溶解能力的定性方法,是物质的一种物理性质。
溶解度:是衡量一定温度下物质在某种溶剂里溶解性大小的尺度,是溶解性的定量表示方法。
☆ 联系:
20℃的溶解度/g <0.01 0.01~1 1~10 >10
溶解性描述 难溶 微溶 可溶 易溶
难溶
微溶
可溶
易溶
0.01
1
10
20℃
g/100g
【巧记】
新课讲解
二、固体溶解度曲线及意义
溶解度曲线是借助数学的方法,用图像将物质的溶解度随温度变化的情况直观地表示出来。
新课讲解
影响固体溶解度的因素
☆内因:溶质、溶剂的性质
☆外因:温度
(1)大多数固体物质的溶解度随温度的升高而升高;
(2)少数物质(如NaCl)的溶解度受温度的影响很小;
(3)极少数物质[如Ca(OH)2]的溶解度随温度的升高而降低。
新课讲解
N
M
温度/℃
溶解度\克
t1
t2
0
●
b
●
●
a
两曲线的交点:
表示两物质在交点所示的温度下的溶解度相等;
表示在交点所示的温度下两物质的饱和溶液质量分数相等。
●
c
曲线下方的点:
不饱和溶液
曲线上方的点:形成饱和溶液并有物质剩余。
10
20
曲线上的点:
表示物质在
该点所示温度
下的溶解度。
新课讲解
【注意】溶解度曲线的应用
1、判断某种物质在不同温度下的溶解度是多少;
2、比较不同物质在同一温度下的溶解度大小;
3、判断物质的溶解度受温度影响变化的趋势——看曲线倾斜度;
4、判断将饱和溶液转化为不饱和溶液的方法:改变温度或改变溶质质量;
5、确定使溶质结晶析出的方法:改变温度或蒸发溶剂;
6、确定混合物分离、提纯的方法。
新课讲解
三、气体溶解度的定义
某气体在压强为101kPa,一定温度时,在1体积水中达到饱和状态时所溶解的体积。
【注意】定义中的几个关键词:
①一定温度下;
②101 kPa;
③1体积水中;
④饱和时的气体体积数。
已知0℃、1个标准大气压时1体积水最多能溶解0.049体积氧气,此时氧气的溶解度为0.049。
新课讲解
【思考】喝汽水的时候,为什么会打开瓶塞汽水会自动喷出来?喝了冰镇汽水以后,为什么常常会打嗝?
汽水中溶解了一定量的二氧化碳气体,当外界条件(如温度、压强)变化时,二氧化碳在水中的溶解度也会发生变化,导致二氧化碳从溶液中逸出。
气体的溶解度随温度的升高而减小,随压强的增大而增大。
归纳小结
1、固体溶解度表示在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量;
2、气体的溶解度通常是指该气体的压强为101kPa和一定温度时,溶解在1体积水里达到饱和状态时的气体体积。
3、物质的溶解度随温度变化的曲线叫做溶解度曲线。利用溶解度曲线,可以获得许多有关物质溶解度的信息。
强化训练
1、60℃时,硝酸钾的溶解度为110g。在60℃时,将70g硝酸钾投入50g水中充分搅拌后得到溶液的质量是( )
A.105g B.110g C.120g D.210g
A
【解析】
60℃时,KNO3的溶解度为110g,在此温度下50g水中最多溶解55gKNO3固体,形成这一温度下的饱和溶液,因此饱和溶液的质量为50g+55g=105g。
强化训练
2、如图是A、B、C三种物质的溶解度曲线。下列说法错误的是( )
A.C的溶解度随温度的升高而减小
B.t2℃时A、B、C的溶解度大小为A=B>C
C.t2℃A、B、C的饱和溶液降温到t1℃时,
A、C两溶液中溶质的质量分数相等
D.t1℃时,A的饱和溶液中溶质质量分数为20%
C
【解析】A、由溶解度曲线图可知:C的溶解度随温度的升高而减小,故正确;
B、t2℃时,A、B、C三种物质的溶解度大小为:A=B>C,故正确;
C、t2℃时,A、B、C三种物质的饱和溶液溶质质量分数由大到小的顺序为:A=B>C;当降温到t1℃,A仍为饱和溶液,C为不饱和溶液,与t2℃时溶液溶质的质量分数相等,在t1℃时A的溶解度大于t2℃时C的溶解度,故降温至t1℃时,A溶液的溶质质量分数大于C溶液的溶质质量分数,故错误;
D、t1℃时,A物质的溶解度为25g,所以饱和溶液中溶质的质量分数是:25g/125g×100%=20%,故正确。
3、家庭生活中烧开水时,会看到有大量气泡从水中冒出,这是因为温度升高时( )
A.水发生了分解反应
B.空气在水中的溶解度减小
C.水与壶发生了化学反应
D.空气在水中的溶解性增强
强化训练
B
【解析】
气体的溶解度随温度的升高而减小,故家庭生活中烧开水时,会看到有大量气泡从水中冒出。
布置作业
在炎热的夏日,特别是闷热的午后,鱼塘需要及时充氧,否则会出现“死鱼”现象,请你说明原因?
【参考答案】夏日闷热的午后,鱼塘中因温度高、气压低,氧气在水中的溶解度明显降低,如果不及时充氧,会因水中氧气含量小,而出现“死鱼”现象。
本课结束
同课章节目录
