人教版化学九年级上册同步课时训练:第6单元 课题2 二氧化碳制取的研究(word版 含答案)
文档属性
| 名称 | 人教版化学九年级上册同步课时训练:第6单元 课题2 二氧化碳制取的研究(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 296.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-19 00:00:00 | ||
图片预览

文档简介
课题2 二氧化碳制取的研究
知识点 1 实验室制取二氧化碳的反应原理
1.(1)实验室制取二氧化碳的试剂是 ,反应的化学方程式是 。
(2)实验室制取二氧化碳一般不选用碳酸钠粉末的原因是 ;一般不选用稀硫酸的原因是 。
2.下列反应都能生成二氧化碳,但实验室制取二氧化碳不能用下列方法,有关原因叙述错误的是 ( )
A.碳在氧气中燃烧,可能生成一氧化碳,使制得的气体不纯
B.高温煅烧石灰石,条件是高温,实验室不易达到
C.石灰石和浓盐酸,反应太慢,收集时间太长
D.碳酸钠与稀盐酸,反应太快,不容易控制
知识点 2 实验室制取二氧化碳的装置及步骤
3.下列不适合作实验室制取二氧化碳的发生装置的是 ( )
4.实验室制取二氧化碳的装置如图图图所示。
(1)请指出图中的两处错误: ; 。
(2)用改正后的装置制取二氧化碳的主要操作如图图图下:①收集气体;②检查装置的气密性;③按要求装配好仪器;④向漏斗里注入酸液;⑤将固体药品加入锥形瓶中。下列操作顺序正确的是 (填字母)。
A.③②⑤④① B.③②④⑤① C.②③⑤④① D.③⑤④②①
(3)将固体药品加入锥形瓶中的正确操作是 。
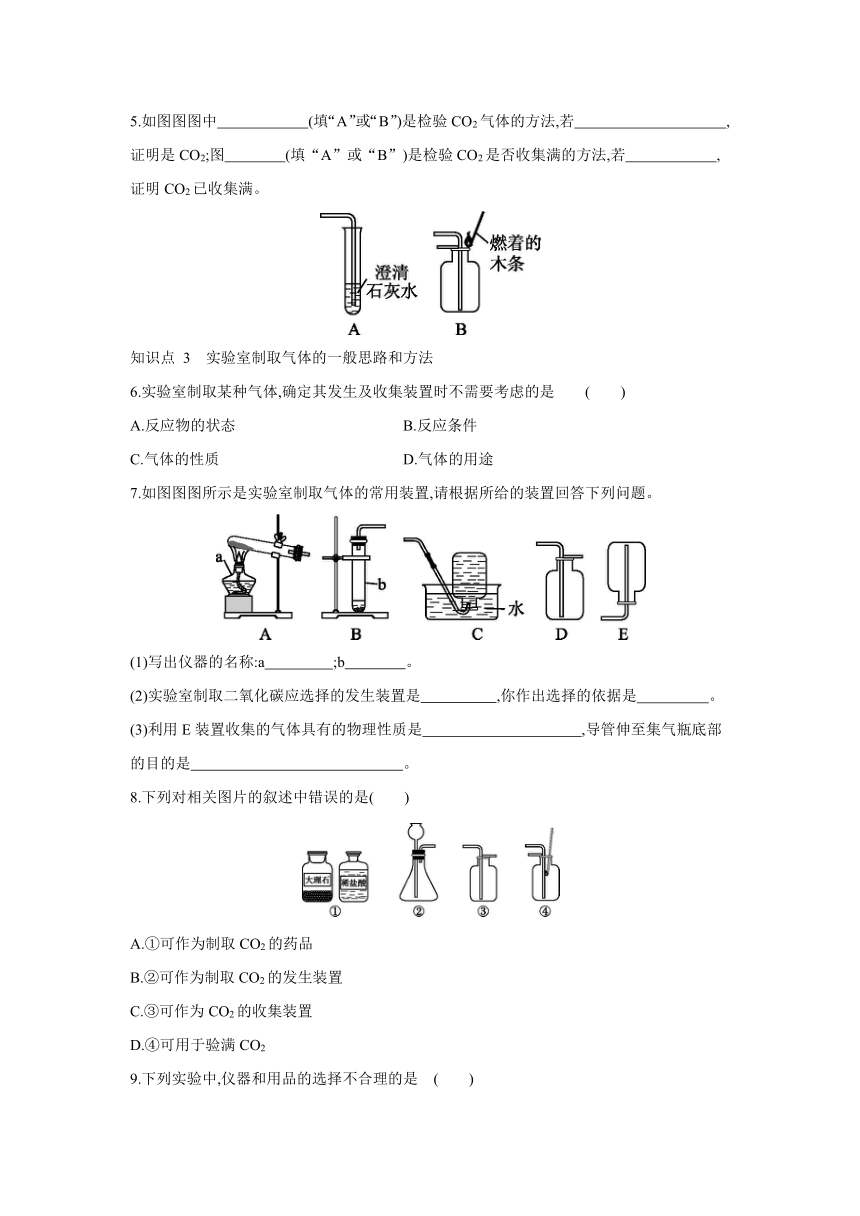
5.如图图图中 (填“A”或“B”)是检验CO2气体的方法,若 ,证明是CO2;图 (填“A”或“B”)是检验CO2是否收集满的方法,若 ,证明CO2已收集满。
知识点 3 实验室制取气体的一般思路和方法
6.实验室制取某种气体,确定其发生及收集装置时不需要考虑的是 ( )
A.反应物的状态 B.反应条件
C.气体的性质 D.气体的用途
7.如图图图所示是实验室制取气体的常用装置,请根据所给的装置回答下列问题。
(1)写出仪器的名称:a ;b 。
(2)实验室制取二氧化碳应选择的发生装置是 ,你作出选择的依据是 。
(3)利用E装置收集的气体具有的物理性质是 ,导管伸至集气瓶底部的目的是 。
8.下列对相关图片的叙述中错误的是( )
A.①可作为制取CO2的药品
B.②可作为制取CO2的发生装置
C.③可作为CO2的收集装置
D.④可用于验满CO2
9.下列实验中,仪器和用品的选择不合理的是 ( )
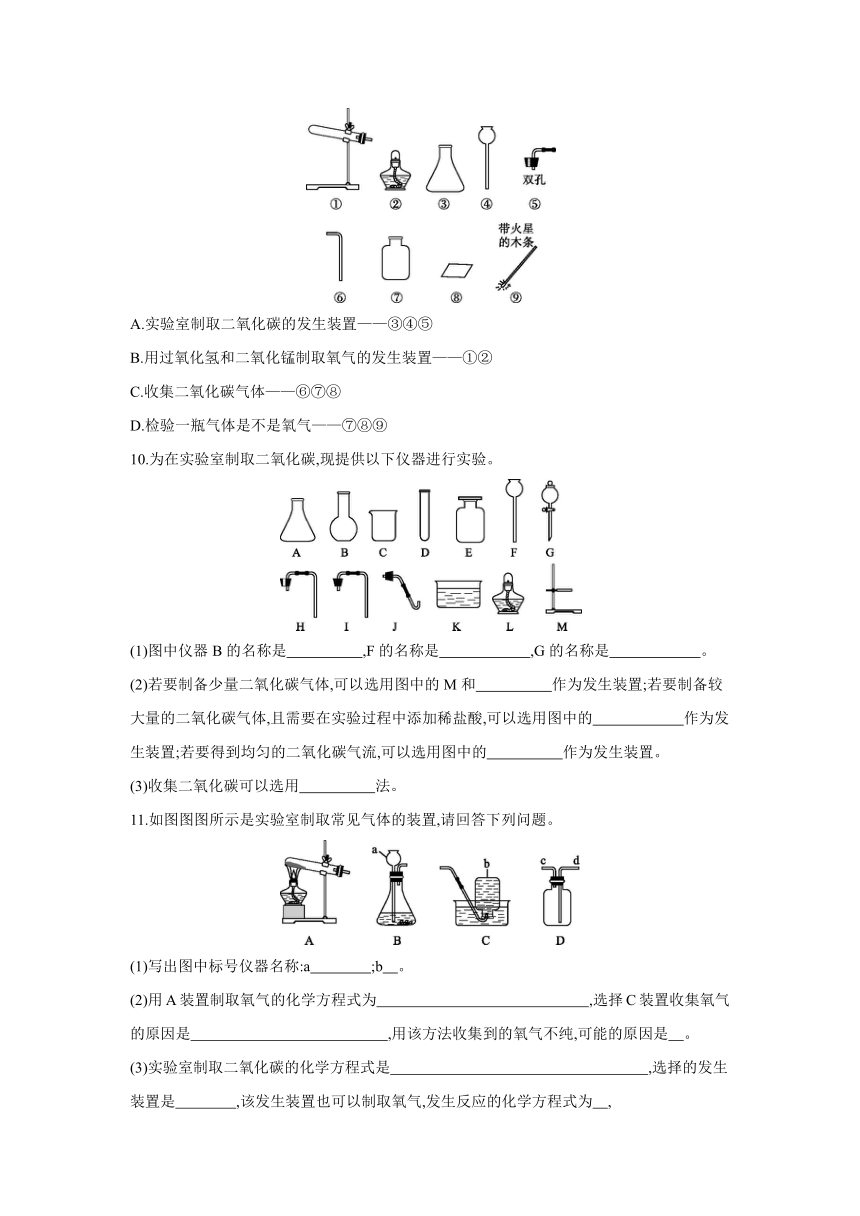
A.实验室制取二氧化碳的发生装置——③④⑤
B.用过氧化氢和二氧化锰制取氧气的发生装置——①②
C.收集二氧化碳气体——⑥⑦⑧
D.检验一瓶气体是不是氧气——⑦⑧⑨
10.为在实验室制取二氧化碳,现提供以下仪器进行实验。
(1)图中仪器B的名称是 ,F的名称是 ,G的名称是 。
(2)若要制备少量二氧化碳气体,可以选用图中的M和 作为发生装置;若要制备较大量的二氧化碳气体,且需要在实验过程中添加稀盐酸,可以选用图中的 作为发生装置;若要得到均匀的二氧化碳气流,可以选用图中的 作为发生装置。
(3)收集二氧化碳可以选用 法。
11.如图图图所示是实验室制取常见气体的装置,请回答下列问题。
(1)写出图中标号仪器名称:a ;b 。
(2)用A装置制取氧气的化学方程式为 ,选择C装置收集氧气的原因是 ,用该方法收集到的氧气不纯,可能的原因是 。
(3)实验室制取二氧化碳的化学方程式是 ,选择的发生装置是 ,该发生装置也可以制取氧气,发生反应的化学方程式为 ,
检查该装置的气密性的方法是 ;检验二氧化碳可选用的试剂是 。
(4)用D装置收集二氧化碳气体,二氧化碳应从D装置的 (填“c”或“d”)端通入。
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下氨气是一种无色、有刺激性气味的气体,极易溶于水。制取氨气,可选用的装置组合是 。
12.某地盛产的石灰石中含碳酸钙80%,现有250 g这种石灰石,若与足量的稀盐酸反应,能生成多少克二氧化碳
考|题|展|示
13.[2020·孝感] 实验室制取某种气体X,X为氢气、氧气或二氧化碳。根据回答下列问题。
(1)若将A和C连接制取气体X,则X为 。
(2)若将A和B或A和D连接都可制取气体X,则分液漏斗中盛装的药品为 。
(3)若在锥形瓶中盛装大理石或石灰石,来制取气体X,则选用的收集装置为 (填字母)。
(4)若用加热氯酸钾和二氧化锰的混合物的方法来制取氧气,除选取图中部分装置外,还需补充大试管、单孔塞、玻璃导管、胶皮管、铁架台(带铁夹)、玻璃片和 (填一种仪器)。
答案
1.(1)大理石(或石灰石)和稀盐酸
CaCO3+2HClCaCl2+CO2↑+H2O
(2)反应太快 会生成微溶于水的硫酸钙,覆盖在大理石(或石灰石)表面阻碍反应继续进行
2.C 浓盐酸具有挥发性,会使制得的气体中含氯化氢气体,所得气体不纯。
3.A A装置中导管太长,导致生成的二氧化碳气体不易排出。
4.(1)长颈漏斗的下端管口没有伸入液面以下 用排水法收集二氧化碳
(2)A
(3)先将锥形瓶横放,用镊子将药品放在锥形瓶口,再将锥形瓶慢慢竖起,使药品缓缓地滑到锥形瓶底部
5.A 澄清石灰水变浑浊 B 木条熄灭
6.D
7.(1)酒精灯 试管
(2)B 大理石(或石灰石)是固体,稀盐酸是液体,反应不需要加热
(3)密度比空气小 更好地排尽空气
8.D
9.B 大理石(或石灰石)和稀盐酸反应不需要加热,可以用锥形瓶、长颈漏斗和带导管的双孔橡胶塞进行实验;过氧化氢在二氧化锰催化作用下制氧气所需装置为固液不加热型装置;二氧化碳密度比空气大,用向上排空气法收集,可以用玻璃导管、集气瓶和玻璃片进行收集;检验气体是不是氧气时,可以用集气瓶、玻璃片和带火星的木条进行实验。
10.(1)平底烧瓶 长颈漏斗 分液漏斗
(2)DI AFH(或BFH)
AGH(或BGH或DGHM)
(3)向上排空气
11.(1)长颈漏斗 集气瓶
(2)2KClO32KCl+3O2↑ 氧气不易溶于水,不与水反应 导管口一有气泡冒出就收集(或收集前集气瓶内没有装满水)
(3)CaCO3+2HClCaCl2+H2O+CO2↑ B 2H2O22H2O+O2↑ 在导管的一端连接胶皮管,用弹簧夹夹紧胶皮管,沿长颈漏斗注入水,至长颈漏斗内形成一段水柱,静置,若观察到长颈漏斗内的液面不变,说明气密性良好(合理即可) 澄清石灰水
(4)d (5)AD
12.解:250 g这种石灰石中碳酸钙的质量为250 g×80%=200 g。
设能生成二氧化碳的质量为x。
CaCO3+2HClCaCl2+CO2↑+H2O
100 44
200 g x
= x=88 g
答:能生成88 g二氧化碳。
13.(1)氢气(或H2)
(2)过氧化氢溶液
(3)B (4)酒精灯
(1)C为向下排空气法收集气体,氧气和二氧化碳密度比空气大,应选用装置B收集,氢气密度比空气小,可选用装置C收集。(2)B为向上排空气法收集气体,D为排水法收集气体,气体X可用这两种装置收集,说明X密度比空气大且不易溶于水,则气体X应为氧气,固液反应制取氧气,用的药品是过氧化氢溶液和二氧化锰,则分液漏斗中盛装的药品是过氧化氢溶液。(3)大理石或石灰石的主要成分是碳酸钙,可与稀盐酸反应制取二氧化碳,二氧化碳密度比空气大,能溶于水,采用向上排空气法收集,选择装置B。(4)加热氯酸钾和二氧化锰的混合物制取氧气,应选用固固加热型发生装置,除了题干所给的装置和仪器外,还需要酒精灯。
知识点 1 实验室制取二氧化碳的反应原理
1.(1)实验室制取二氧化碳的试剂是 ,反应的化学方程式是 。
(2)实验室制取二氧化碳一般不选用碳酸钠粉末的原因是 ;一般不选用稀硫酸的原因是 。
2.下列反应都能生成二氧化碳,但实验室制取二氧化碳不能用下列方法,有关原因叙述错误的是 ( )
A.碳在氧气中燃烧,可能生成一氧化碳,使制得的气体不纯
B.高温煅烧石灰石,条件是高温,实验室不易达到
C.石灰石和浓盐酸,反应太慢,收集时间太长
D.碳酸钠与稀盐酸,反应太快,不容易控制
知识点 2 实验室制取二氧化碳的装置及步骤
3.下列不适合作实验室制取二氧化碳的发生装置的是 ( )
4.实验室制取二氧化碳的装置如图图图所示。
(1)请指出图中的两处错误: ; 。
(2)用改正后的装置制取二氧化碳的主要操作如图图图下:①收集气体;②检查装置的气密性;③按要求装配好仪器;④向漏斗里注入酸液;⑤将固体药品加入锥形瓶中。下列操作顺序正确的是 (填字母)。
A.③②⑤④① B.③②④⑤① C.②③⑤④① D.③⑤④②①
(3)将固体药品加入锥形瓶中的正确操作是 。
5.如图图图中 (填“A”或“B”)是检验CO2气体的方法,若 ,证明是CO2;图 (填“A”或“B”)是检验CO2是否收集满的方法,若 ,证明CO2已收集满。
知识点 3 实验室制取气体的一般思路和方法
6.实验室制取某种气体,确定其发生及收集装置时不需要考虑的是 ( )
A.反应物的状态 B.反应条件
C.气体的性质 D.气体的用途
7.如图图图所示是实验室制取气体的常用装置,请根据所给的装置回答下列问题。
(1)写出仪器的名称:a ;b 。
(2)实验室制取二氧化碳应选择的发生装置是 ,你作出选择的依据是 。
(3)利用E装置收集的气体具有的物理性质是 ,导管伸至集气瓶底部的目的是 。
8.下列对相关图片的叙述中错误的是( )
A.①可作为制取CO2的药品
B.②可作为制取CO2的发生装置
C.③可作为CO2的收集装置
D.④可用于验满CO2
9.下列实验中,仪器和用品的选择不合理的是 ( )
A.实验室制取二氧化碳的发生装置——③④⑤
B.用过氧化氢和二氧化锰制取氧气的发生装置——①②
C.收集二氧化碳气体——⑥⑦⑧
D.检验一瓶气体是不是氧气——⑦⑧⑨
10.为在实验室制取二氧化碳,现提供以下仪器进行实验。
(1)图中仪器B的名称是 ,F的名称是 ,G的名称是 。
(2)若要制备少量二氧化碳气体,可以选用图中的M和 作为发生装置;若要制备较大量的二氧化碳气体,且需要在实验过程中添加稀盐酸,可以选用图中的 作为发生装置;若要得到均匀的二氧化碳气流,可以选用图中的 作为发生装置。
(3)收集二氧化碳可以选用 法。
11.如图图图所示是实验室制取常见气体的装置,请回答下列问题。
(1)写出图中标号仪器名称:a ;b 。
(2)用A装置制取氧气的化学方程式为 ,选择C装置收集氧气的原因是 ,用该方法收集到的氧气不纯,可能的原因是 。
(3)实验室制取二氧化碳的化学方程式是 ,选择的发生装置是 ,该发生装置也可以制取氧气,发生反应的化学方程式为 ,
检查该装置的气密性的方法是 ;检验二氧化碳可选用的试剂是 。
(4)用D装置收集二氧化碳气体,二氧化碳应从D装置的 (填“c”或“d”)端通入。
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下氨气是一种无色、有刺激性气味的气体,极易溶于水。制取氨气,可选用的装置组合是 。
12.某地盛产的石灰石中含碳酸钙80%,现有250 g这种石灰石,若与足量的稀盐酸反应,能生成多少克二氧化碳
考|题|展|示
13.[2020·孝感] 实验室制取某种气体X,X为氢气、氧气或二氧化碳。根据回答下列问题。
(1)若将A和C连接制取气体X,则X为 。
(2)若将A和B或A和D连接都可制取气体X,则分液漏斗中盛装的药品为 。
(3)若在锥形瓶中盛装大理石或石灰石,来制取气体X,则选用的收集装置为 (填字母)。
(4)若用加热氯酸钾和二氧化锰的混合物的方法来制取氧气,除选取图中部分装置外,还需补充大试管、单孔塞、玻璃导管、胶皮管、铁架台(带铁夹)、玻璃片和 (填一种仪器)。
答案
1.(1)大理石(或石灰石)和稀盐酸
CaCO3+2HClCaCl2+CO2↑+H2O
(2)反应太快 会生成微溶于水的硫酸钙,覆盖在大理石(或石灰石)表面阻碍反应继续进行
2.C 浓盐酸具有挥发性,会使制得的气体中含氯化氢气体,所得气体不纯。
3.A A装置中导管太长,导致生成的二氧化碳气体不易排出。
4.(1)长颈漏斗的下端管口没有伸入液面以下 用排水法收集二氧化碳
(2)A
(3)先将锥形瓶横放,用镊子将药品放在锥形瓶口,再将锥形瓶慢慢竖起,使药品缓缓地滑到锥形瓶底部
5.A 澄清石灰水变浑浊 B 木条熄灭
6.D
7.(1)酒精灯 试管
(2)B 大理石(或石灰石)是固体,稀盐酸是液体,反应不需要加热
(3)密度比空气小 更好地排尽空气
8.D
9.B 大理石(或石灰石)和稀盐酸反应不需要加热,可以用锥形瓶、长颈漏斗和带导管的双孔橡胶塞进行实验;过氧化氢在二氧化锰催化作用下制氧气所需装置为固液不加热型装置;二氧化碳密度比空气大,用向上排空气法收集,可以用玻璃导管、集气瓶和玻璃片进行收集;检验气体是不是氧气时,可以用集气瓶、玻璃片和带火星的木条进行实验。
10.(1)平底烧瓶 长颈漏斗 分液漏斗
(2)DI AFH(或BFH)
AGH(或BGH或DGHM)
(3)向上排空气
11.(1)长颈漏斗 集气瓶
(2)2KClO32KCl+3O2↑ 氧气不易溶于水,不与水反应 导管口一有气泡冒出就收集(或收集前集气瓶内没有装满水)
(3)CaCO3+2HClCaCl2+H2O+CO2↑ B 2H2O22H2O+O2↑ 在导管的一端连接胶皮管,用弹簧夹夹紧胶皮管,沿长颈漏斗注入水,至长颈漏斗内形成一段水柱,静置,若观察到长颈漏斗内的液面不变,说明气密性良好(合理即可) 澄清石灰水
(4)d (5)AD
12.解:250 g这种石灰石中碳酸钙的质量为250 g×80%=200 g。
设能生成二氧化碳的质量为x。
CaCO3+2HClCaCl2+CO2↑+H2O
100 44
200 g x
= x=88 g
答:能生成88 g二氧化碳。
13.(1)氢气(或H2)
(2)过氧化氢溶液
(3)B (4)酒精灯
(1)C为向下排空气法收集气体,氧气和二氧化碳密度比空气大,应选用装置B收集,氢气密度比空气小,可选用装置C收集。(2)B为向上排空气法收集气体,D为排水法收集气体,气体X可用这两种装置收集,说明X密度比空气大且不易溶于水,则气体X应为氧气,固液反应制取氧气,用的药品是过氧化氢溶液和二氧化锰,则分液漏斗中盛装的药品是过氧化氢溶液。(3)大理石或石灰石的主要成分是碳酸钙,可与稀盐酸反应制取二氧化碳,二氧化碳密度比空气大,能溶于水,采用向上排空气法收集,选择装置B。(4)加热氯酸钾和二氧化锰的混合物制取氧气,应选用固固加热型发生装置,除了题干所给的装置和仪器外,还需要酒精灯。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
