冲刺2022中考必刷选择题(13)氧气、二氧化碳、酸、碱(含答案)
文档属性
| 名称 | 冲刺2022中考必刷选择题(13)氧气、二氧化碳、酸、碱(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-04-21 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
中考必刷选择题(13)氧气、二氧化碳、酸、碱
一、氧气性质与制取
1.(2021·台州)1774年,法国化学家拉瓦锡在加热氧化汞时,制得并命名了氧气。加热氧化汞发生的化学反应为2HgO=2Hg+O2↑。该反应属于( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
2.(2021·杭州)下列依据实验现象得出的结论错误的是( )
选项 实验操作与现象 实验结论
A 将1g白磷、1g红磷分别放入两支带塞的试管中,再将试管同时浸约80℃的热水里, 只有白磷燃烧 白磷的着火点比红磷低
B 将二氧化碳通入紫色石蕊试液,试液变红 二氧化碳是一种酸
C 在常温常压下,硫在氧气中燃烧比在空气中该条件下, 燃烧更剧烈 氧气的浓度越大硫燃烧得越剧烈
D 将铁粉、硫粉按一定比例混合加热后,所得固体物质不能被磁铁吸引 铁粉已跟硫粉发生了化学反应
A.A B.B C.C D.D
3.(2020·绍兴)与图示微观变化相符的化学反应是( )
A.2CO+O2 2CO2 B.H2+CuO H2O+Cu
C.2H2+O2 2H2O D.H2CO3 H2O+CO2↑
4.(2018·嘉兴)15%的H2O2溶液在二氧化锰催化作用下会剧烈反应产生O2,实验室欲利用15%的H2O2溶液制取O2,则下列装置中,仪器选择和药品放置最合理的是( )
A.B.C.D.
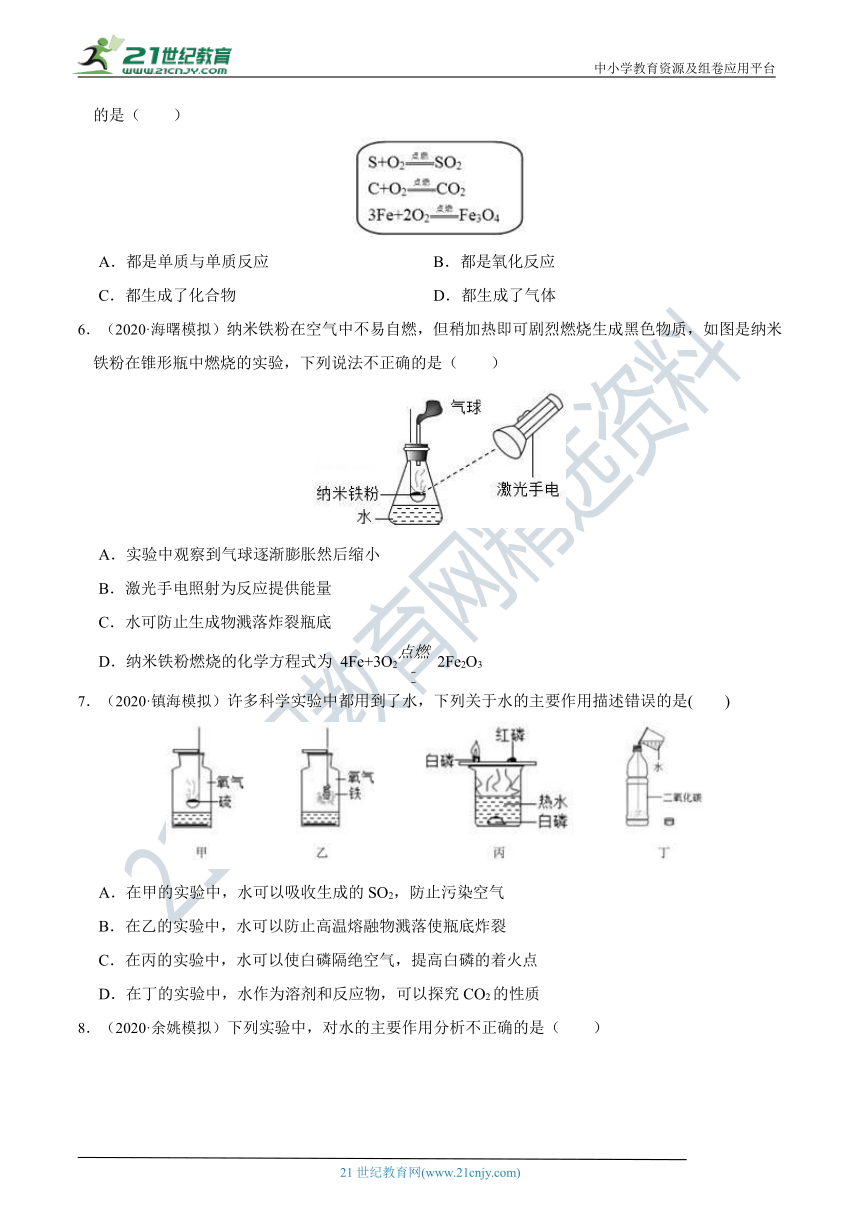
5.(2017·温州)如图是小明整理的与氧气化学性质有关的部分笔记,他归纳了以下四点,其中不合理的是( )
A.都是单质与单质反应 B.都是氧化反应
C.都生成了化合物 D.都生成了气体
6.(2020·海曙模拟)纳米铁粉在空气中不易自燃,但稍加热即可剧烈燃烧生成黑色物质,如图是纳米铁粉在锥形瓶中燃烧的实验,下列说法不正确的是( )
A.实验中观察到气球逐渐膨胀然后缩小
B.激光手电照射为反应提供能量
C.水可防止生成物溅落炸裂瓶底
D.纳米铁粉燃烧的化学方程式为 4Fe+3O2 2Fe2O3
7.(2020·镇海模拟)许多科学实验中都用到了水,下列关于水的主要作用描述错误的是( )
A.在甲的实验中,水可以吸收生成的SO2,防止污染空气
B.在乙的实验中,水可以防止高温熔融物溅落使瓶底炸裂
C.在丙的实验中,水可以使白磷隔绝空气,提高白磷的着火点
D.在丁的实验中,水作为溶剂和反应物,可以探究CO2的性质
8.(2020·余姚模拟)下列实验中,对水的主要作用分析不正确的是( )
A.图甲中的水参与反应,并可观察烧瓶内气压变化
B.图乙中的水只是提供热量
C.图丙中集气瓶里的水排尽空气,并可观察O2的收集情况
D.图丁中的水可防止熔融物炸裂集气瓶
二、二氧化碳性质与制取
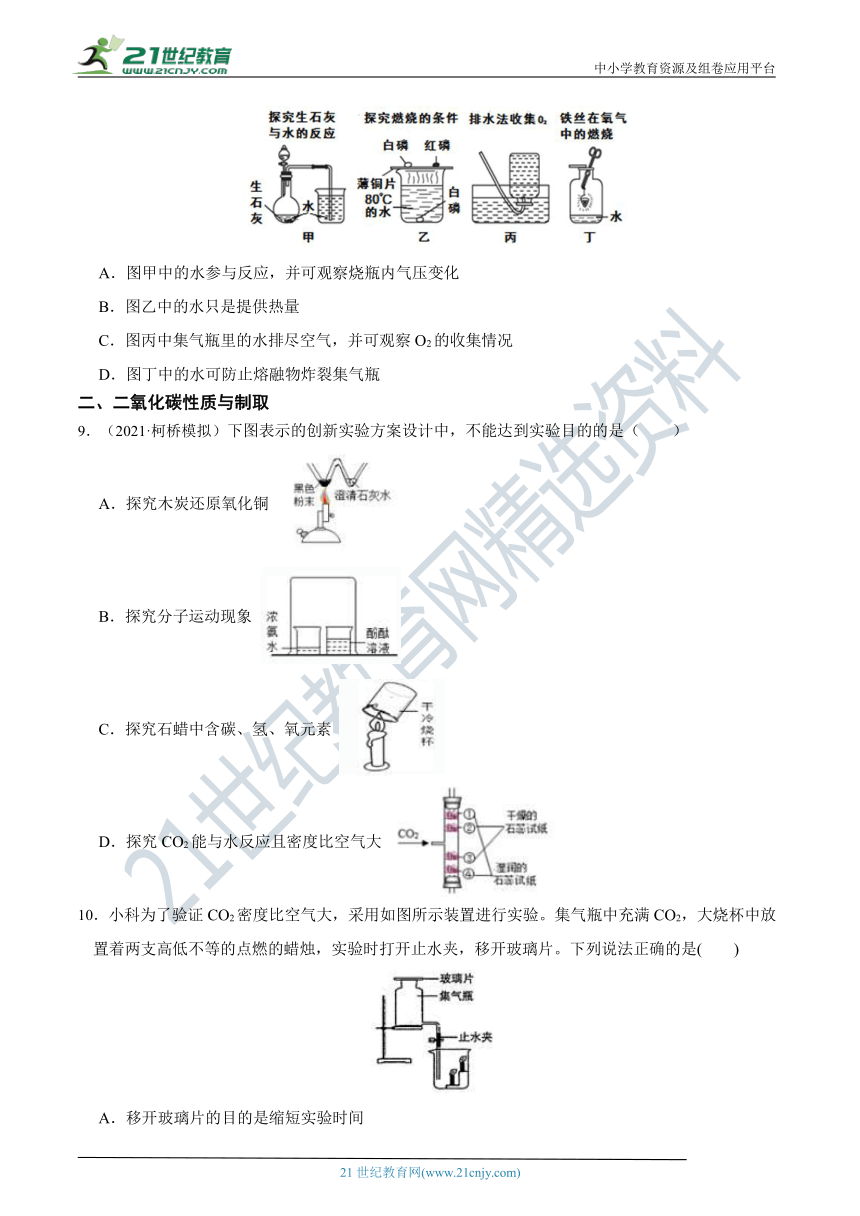
9.(2021·柯桥模拟)下图表示的创新实验方案设计中,不能达到实验目的的是( )
A.探究木炭还原氧化铜
B.探究分子运动现象
C.探究石蜡中含碳、氢、氧元素
D.探究CO2能与水反应且密度比空气大
10.小科为了验证CO2密度比空气大,采用如图所示装置进行实验。集气瓶中充满CO2,大烧杯中放置着两支高低不等的点燃的蜡烛,实验时打开止水夹,移开玻璃片。下列说法正确的是( )
A.移开玻璃片的目的是缩短实验时间
B.观察到高的蜡烛先熄灭,低的蜡烛后熄灭
C.蜡烛会熄灭是因为CO2降低了蜡烛的着火点
D.导管插入到大烧杯底部比插在两蜡烛之间要严谨科学
11.(2021·余杭模拟)金属钛(Ti)抗腐蚀性能好,露置于空气中数年,仍能光亮如初。以金红石(主要成分是TiO2)为原料生产Ti的步骤主要有:①在高温下,向金红石与焦炭(C)的混合物中通入氯气(Cl2),得到TiCl4和一种可燃性气体;②在稀有气体环境和加热条件下,用Mg和TiCl4反应得到Ti和MgCl2。下列说法正确的是( )
A.①中生成的可燃性气体为CO2
B.①中生成的TiCl4中钛元素的化合价为+2价
C.②中发生的化学反应属于置换反应
D.②中生成的Ti在常温下易与O2反应
12.(2011·杭州)把干燥A的蓝色石蕊试纸放在CO2气体中,石蕊试纸不变色。将CO2气体通入滴有石蕊指示剂的水中,溶液变红色。再将该溶液敞口加热一段时间,发现溶液的红色褪去,冷却到原温度后,再次通人CO2,溶液又变红色。上述实验现象不能说明的是( )
A.CO2能和水发生化学反应 B.CO2的水溶液具有酸性
C.加热能使CO2水溶液的酸性减弱 D.CO2具有酸性
13.小松用稀盐酸与石灰石反应制取CO2,尝试直接利用如图所示装置制取并收集,你认为小松( )
A.选择A、B装置,导管a接导管c可收集到一瓶CO2
B.选择B、C装置,导管d接导管b可收集到一瓶CO2
C.选择B、C装置,导管d接导管c可收集到一瓶CO2
D.不可能收集到一瓶CO2,因为CO2可溶于水
14.在锥形瓶甲中放人10 g纯净的块状碳酸钙,在锥形瓶乙中放人10 g纯净的粉末状碳酸钙,分别同时加入足量同浓度的稀盐酸与碳酸钙反应。下列图中对该实验产生气体的质量与反应时间的关系,描述合理的是( )
A.B.C.D.
15.如图所示实验中,①④为用紫色石蕊试液润湿的棉球,②③为用紫色石蕊试液染成紫色的干燥棉球。下列能说明二氧化碳密度大于空气密度且能与水反应的现象是( )
A.①变红,③不变红 B.④变红,③不变红
C.①④变红,②③不变红 D.④比①先变红,②③不变红
16.小兵同学在参考书上发现,镁能在二氧化碳气体中燃烧。于是他做了如下实验:将镁条用砂纸擦亮,点燃后迅速伸入盛有二氧化碳的集气瓶中,发现镁条剧烈燃烧,发出白光,集气瓶变热,产生一种白色粉末(MgO)和一种黑色粉末(C)。你认为下列结论不正确的是( )
A.某些金属的燃烧不能用CO2灭火
B.该反应放出热量
C.该反应的实质是Mg与CO2中混有的O2反应
D.该反应的反应速率很快
17.把干燥的蓝色石蕊试纸放在CO2中,石蕊试纸不变色。将CO2通入滴有石蕊指示剂的水中,溶液变红色,将该溶液敞口加热一段时间,发现溶液的红色褪去,冷却到原温度后,再次通入CO2,溶液又变红色。上述实验现象不能说明的是( )
A.CO2能和水发生化学反应
B.CO2的水溶液具有酸性
C.加热能使二氧化碳水溶液的酸性减弱
D.CO2具有酸性
18.某兴趣小组利用如图所示装置对二氧化碳的性质进行探究(A装置制二氧化碳),下列说法错误的是( )
A.B处现象说明二氧化碳能使紫色石蕊试液变红
B.C处溶液变浑浊,是因为生成了不溶于水的碳酸钙
C.D处的实验现象是下层蜡烛先熄灭,上层蜡烛后熄灭
D.D处现象说明二氧化碳不可燃,不助燃,密度比空气大
19.(2019·德清模拟)如图所示,若关闭Ⅱ阀打开Ⅰ阀,紫色小花(用石蕊溶液染成)变红;若关闭Ⅰ阀打开Ⅱ阀,紫色小花不变红。则甲瓶中所盛的试剂可能是( )
①浓硫酸;②浓氢氧化钠溶液;③饱和氯化钠溶液
A.只有① B.只有② C.①② D.①②③
三、酸的性质
20.(2022九下·杭州月考)小明在探究稀硫酸性质时,下列说法正确的是( )
A.稀H2SO4与紫色石蕊试液反应后,溶液变蓝
B.若能与X反应制取H2,则X是Cu
C.和金属氧化物反应,有盐和水生成
D.若与Y发生中和反应,则Y一定是NaOH
21.(2021·台州)盐酸在生产和生活中的用途很广,能与多种物质发生反应。下列物质与盐酸反应时,能观察到白色沉淀的是( )
A.B.C.D.
22.(2021·南湖模拟)硫酸是一种常见的酸。下列关于硫酸的说法中,正确的是( )
A.组成:硫酸溶液中有H+和SO42-两种微粒,且数目相同
B.性质:能与碱、多种金属和CO2、SO3等非金属氧化物反应
C.用途:可用于清除铁表面的氧化铁和生产化肥硫酸铵
D.检验:滴入氯化钡溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解
23.(2020·江干模拟)下列选项没有体现酸的通性或者碱的通性的是( )
A.实验室制取二氧化碳和氢气
B.利用稀硫酸除去硫酸钠中混有的少量碳酸钠
C.可溶性铜盐或铁盐遇氢氧化钠产生有色沉淀
D.实验室利用硝酸钡鉴别稀硫酸和稀盐酸
24.(2020·上城模拟)为了研究稀硫酸的性质,教材中设计了如图所示实验。分别将过量的稀硫酸滴入盛有锌粒,氧化铁粉末,氧化铜粉末,氢氧化铜和氯化钡溶液的5支试管中。关于实验过程和结论 正确的是( )
A.所有的反应均体现了酸的通性
B.把稀硫酸改成稀盐酸现象都相同
C.氧化铁与硫酸反应生成硫酸亚铁
D.反应后的溶液全部倒进废液缸不再发生新的反应
25.(2018·镇海模拟)向某硫酸和硫酸铜的混合溶液中加入一定浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法正确的是( )
A.a点溶液中含有两种溶质
B.bc段发生反应的类型为置换反应
C.根据图中数据可以计算出氢氧化钠溶液的浓度
D.d点溶液中主要存在的离子为Na+、Cu2+、OH-、SO42-
26.(2022九下·天台开学考)烧杯中盛有盐酸和氯化镁的混合溶液,向其中逐渐加入过量 10%氢氧化钠溶液,下列有关 图像不正确的是( )
A.B.C.D.
四、碱的性质
27.(2021九上·奉化期末)实验室有一瓶敞口放置的氢氧化钠溶液。对于该溶液变质情况的探究,下列实验设计合理且结论正确的是( )
A.取样,在溶液中加入少量的稀盐酸,若无气泡产生,则可证明该溶液没有变质
B.取样,在溶液中滴加酚酞,若溶液呈红色,则可证明该溶液没有变质
C.取样,在溶液中加入过量的稀盐酸,若有气泡产生,则可证明该溶液已变质
D.取样,在溶液中加入过量氯化钡溶液,若产生白色沉淀,则可证明溶液已完全变质
28.某锥形瓶内盛有盐酸和氯化铜的混合溶液100g,向其中加入溶质质量分数为10%的氢氧化钠溶液,锥形瓶内溶液质量m1与加入的氢氧化钠溶液质量m2的变化关系如图所示。下列说法错误的是( )
A.反应至A点时,所加NaOH溶液的质量为40g
B.反应至A点时,溶液中的溶质有CuCl2和NaCl
C.反应至B点时,锥形瓶内溶液的质量为280.4g
D.反应至B点时,锥形瓶内溶液中NaCl的质量为23.4g
29.研究氢氧化钠性质实验中的部分实验及现象记录如下,其中现象不合理的是( )
序号 实 验 现 象
A 将氢氧化钠固体放在表面皿上,放置一会儿 固体受潮,逐渐溶解
B 向盛有氢氧化钠溶液的试管中滴入无色酚酞试液 溶液变红
C 向盛有氢氧化钠溶液的试管中滴加稀盐酸 有氯化钠生成
D 向盛有氢氧化钠溶液的试管中滴加硫酸铜溶液 产生蓝色沉淀
A.A B.B C.C D.D
30.一定质量的氢氧化钡溶液中逐渐加入碳酸钠粉末(不考虑溶液体积变化),直至过量。如图横坐表示加入碳酸钠粉末的质量,根据图像判断,纵坐标可能表示( )
A.生成沉淀的质量 B.溶液中溶剂的质量
C.溶液中溶质的质量 D.溶液的pH
31.在氢氧化钠溶液中加入一定量的稀盐酸后,下列实验能证明两者恰好完全中和的是( )
A.滴入适量FeCl3溶液,溶液变黄,但无沉淀生成
B.滴入几滴酚酞试液,酚酞试液不变色
C.测得反应后溶液中Na+与Cl-的个数比为1:1
D.滴入适量AgNO3溶液和稀硝酸,观察到有白色沉淀
32.小科为研究“碱与盐反应”的规律,设计了如图所示的五组实验,每支试管盛有3毫升溶液,分别向试管中只滴加3滴溶液。除氢氧化钙溶液是饱和外,其余溶液的质量分数都为5%。下列叙述正确的是( )
A.甲组和乙组实验能观察到相同现象
B.乙组和丙组实验均能观察到蓝色沉淀
C.乙组实验产生的沉淀质量比丁组多
D.戊组实验产生的沉淀质量比丙组少
33.(2020·温州模拟)小雅将滴有酚酞的Ba(OH)2溶液平均分成两份,置于甲、乙两个烧杯中,分别往甲、乙两烧杯中滴加稀硫酸、硫酸钠溶液至过量(如图)。下列说法正确的是( )
A.甲烧杯中,溶液的颜色始终为红色
B.甲烧杯中,氢离子的数量一直不变
C.乙烧杯中,溶液的颜色始终为红色
D.乙烧杯中,钠离子的数量一直不变
34.(2019·杭州模拟)小乐按图示操作进行酸和碱反应的实验,下别有关分析正确的是( )
A.①中NaOH溶液易潮解和变质,需密封保存
B.②中酚酞试液变红,其原因是溶液中存在Na+
C.③中反应的实质是H+和OH-结台生成水
D.⑤中浓硫酸的稀释中,甲物质是水
35.(2019·杭州模拟)某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法不正确的是( )
A.a点所示溶液中,含有的溶质是NaCl和NaOH
B.c点所示溶液能使紫色石蕊溶液变蓝
C.b点表示氢氧化钠和稀盐酸恰好完全反应
D.a、b、c所示的溶液中都含有 Na+、Cl-
36.(2019·浙江模拟)为了探究酸碱中和反应是否放热,某同学设计了如图所示的实验装置(夹持等固定装置图略),针对该实验目的,下列评价或改进,错误的是( )
A.若观察到红墨水向右移,则说明该实验一定有放热现象
B.为了使实验现象更明显,可改用氢氧化钠固体
C.在打开活塞a之前应先打开橡皮管上的止水夹
D.为了使实验更具有说服力,可用氢氧化钾溶液再次实验
答案解析部分
1.【答案】B2.【答案】B3.【答案】A4.【答案】D5.【答案】D6.【答案】D
7.【答案】C8.【答案】B9.【答案】C10.【答案】A11.【答案】C
12.【答案】D13.【答案】C14.【答案】C15.【答案】D16.【答案】C17.【答案】D
18.【答案】A19.【答案】C20.【答案】C21.【答案】C22.【答案】C23.【答案】D
24.【答案】D25.【答案】C26.【答案】D27.【答案】C28.【答案】D29.【答案】C
30.【答案】C31.【答案】C32.【答案】D33.【答案】C34.【答案】C35.【答案】A
36.【答案】B
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
中考必刷选择题(13)氧气、二氧化碳、酸、碱
一、氧气性质与制取
1.(2021·台州)1774年,法国化学家拉瓦锡在加热氧化汞时,制得并命名了氧气。加热氧化汞发生的化学反应为2HgO=2Hg+O2↑。该反应属于( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
2.(2021·杭州)下列依据实验现象得出的结论错误的是( )
选项 实验操作与现象 实验结论
A 将1g白磷、1g红磷分别放入两支带塞的试管中,再将试管同时浸约80℃的热水里, 只有白磷燃烧 白磷的着火点比红磷低
B 将二氧化碳通入紫色石蕊试液,试液变红 二氧化碳是一种酸
C 在常温常压下,硫在氧气中燃烧比在空气中该条件下, 燃烧更剧烈 氧气的浓度越大硫燃烧得越剧烈
D 将铁粉、硫粉按一定比例混合加热后,所得固体物质不能被磁铁吸引 铁粉已跟硫粉发生了化学反应
A.A B.B C.C D.D
3.(2020·绍兴)与图示微观变化相符的化学反应是( )
A.2CO+O2 2CO2 B.H2+CuO H2O+Cu
C.2H2+O2 2H2O D.H2CO3 H2O+CO2↑
4.(2018·嘉兴)15%的H2O2溶液在二氧化锰催化作用下会剧烈反应产生O2,实验室欲利用15%的H2O2溶液制取O2,则下列装置中,仪器选择和药品放置最合理的是( )
A.B.C.D.
5.(2017·温州)如图是小明整理的与氧气化学性质有关的部分笔记,他归纳了以下四点,其中不合理的是( )
A.都是单质与单质反应 B.都是氧化反应
C.都生成了化合物 D.都生成了气体
6.(2020·海曙模拟)纳米铁粉在空气中不易自燃,但稍加热即可剧烈燃烧生成黑色物质,如图是纳米铁粉在锥形瓶中燃烧的实验,下列说法不正确的是( )
A.实验中观察到气球逐渐膨胀然后缩小
B.激光手电照射为反应提供能量
C.水可防止生成物溅落炸裂瓶底
D.纳米铁粉燃烧的化学方程式为 4Fe+3O2 2Fe2O3
7.(2020·镇海模拟)许多科学实验中都用到了水,下列关于水的主要作用描述错误的是( )
A.在甲的实验中,水可以吸收生成的SO2,防止污染空气
B.在乙的实验中,水可以防止高温熔融物溅落使瓶底炸裂
C.在丙的实验中,水可以使白磷隔绝空气,提高白磷的着火点
D.在丁的实验中,水作为溶剂和反应物,可以探究CO2的性质
8.(2020·余姚模拟)下列实验中,对水的主要作用分析不正确的是( )
A.图甲中的水参与反应,并可观察烧瓶内气压变化
B.图乙中的水只是提供热量
C.图丙中集气瓶里的水排尽空气,并可观察O2的收集情况
D.图丁中的水可防止熔融物炸裂集气瓶
二、二氧化碳性质与制取
9.(2021·柯桥模拟)下图表示的创新实验方案设计中,不能达到实验目的的是( )
A.探究木炭还原氧化铜
B.探究分子运动现象
C.探究石蜡中含碳、氢、氧元素
D.探究CO2能与水反应且密度比空气大
10.小科为了验证CO2密度比空气大,采用如图所示装置进行实验。集气瓶中充满CO2,大烧杯中放置着两支高低不等的点燃的蜡烛,实验时打开止水夹,移开玻璃片。下列说法正确的是( )
A.移开玻璃片的目的是缩短实验时间
B.观察到高的蜡烛先熄灭,低的蜡烛后熄灭
C.蜡烛会熄灭是因为CO2降低了蜡烛的着火点
D.导管插入到大烧杯底部比插在两蜡烛之间要严谨科学
11.(2021·余杭模拟)金属钛(Ti)抗腐蚀性能好,露置于空气中数年,仍能光亮如初。以金红石(主要成分是TiO2)为原料生产Ti的步骤主要有:①在高温下,向金红石与焦炭(C)的混合物中通入氯气(Cl2),得到TiCl4和一种可燃性气体;②在稀有气体环境和加热条件下,用Mg和TiCl4反应得到Ti和MgCl2。下列说法正确的是( )
A.①中生成的可燃性气体为CO2
B.①中生成的TiCl4中钛元素的化合价为+2价
C.②中发生的化学反应属于置换反应
D.②中生成的Ti在常温下易与O2反应
12.(2011·杭州)把干燥A的蓝色石蕊试纸放在CO2气体中,石蕊试纸不变色。将CO2气体通入滴有石蕊指示剂的水中,溶液变红色。再将该溶液敞口加热一段时间,发现溶液的红色褪去,冷却到原温度后,再次通人CO2,溶液又变红色。上述实验现象不能说明的是( )
A.CO2能和水发生化学反应 B.CO2的水溶液具有酸性
C.加热能使CO2水溶液的酸性减弱 D.CO2具有酸性
13.小松用稀盐酸与石灰石反应制取CO2,尝试直接利用如图所示装置制取并收集,你认为小松( )
A.选择A、B装置,导管a接导管c可收集到一瓶CO2
B.选择B、C装置,导管d接导管b可收集到一瓶CO2
C.选择B、C装置,导管d接导管c可收集到一瓶CO2
D.不可能收集到一瓶CO2,因为CO2可溶于水
14.在锥形瓶甲中放人10 g纯净的块状碳酸钙,在锥形瓶乙中放人10 g纯净的粉末状碳酸钙,分别同时加入足量同浓度的稀盐酸与碳酸钙反应。下列图中对该实验产生气体的质量与反应时间的关系,描述合理的是( )
A.B.C.D.
15.如图所示实验中,①④为用紫色石蕊试液润湿的棉球,②③为用紫色石蕊试液染成紫色的干燥棉球。下列能说明二氧化碳密度大于空气密度且能与水反应的现象是( )
A.①变红,③不变红 B.④变红,③不变红
C.①④变红,②③不变红 D.④比①先变红,②③不变红
16.小兵同学在参考书上发现,镁能在二氧化碳气体中燃烧。于是他做了如下实验:将镁条用砂纸擦亮,点燃后迅速伸入盛有二氧化碳的集气瓶中,发现镁条剧烈燃烧,发出白光,集气瓶变热,产生一种白色粉末(MgO)和一种黑色粉末(C)。你认为下列结论不正确的是( )
A.某些金属的燃烧不能用CO2灭火
B.该反应放出热量
C.该反应的实质是Mg与CO2中混有的O2反应
D.该反应的反应速率很快
17.把干燥的蓝色石蕊试纸放在CO2中,石蕊试纸不变色。将CO2通入滴有石蕊指示剂的水中,溶液变红色,将该溶液敞口加热一段时间,发现溶液的红色褪去,冷却到原温度后,再次通入CO2,溶液又变红色。上述实验现象不能说明的是( )
A.CO2能和水发生化学反应
B.CO2的水溶液具有酸性
C.加热能使二氧化碳水溶液的酸性减弱
D.CO2具有酸性
18.某兴趣小组利用如图所示装置对二氧化碳的性质进行探究(A装置制二氧化碳),下列说法错误的是( )
A.B处现象说明二氧化碳能使紫色石蕊试液变红
B.C处溶液变浑浊,是因为生成了不溶于水的碳酸钙
C.D处的实验现象是下层蜡烛先熄灭,上层蜡烛后熄灭
D.D处现象说明二氧化碳不可燃,不助燃,密度比空气大
19.(2019·德清模拟)如图所示,若关闭Ⅱ阀打开Ⅰ阀,紫色小花(用石蕊溶液染成)变红;若关闭Ⅰ阀打开Ⅱ阀,紫色小花不变红。则甲瓶中所盛的试剂可能是( )
①浓硫酸;②浓氢氧化钠溶液;③饱和氯化钠溶液
A.只有① B.只有② C.①② D.①②③
三、酸的性质
20.(2022九下·杭州月考)小明在探究稀硫酸性质时,下列说法正确的是( )
A.稀H2SO4与紫色石蕊试液反应后,溶液变蓝
B.若能与X反应制取H2,则X是Cu
C.和金属氧化物反应,有盐和水生成
D.若与Y发生中和反应,则Y一定是NaOH
21.(2021·台州)盐酸在生产和生活中的用途很广,能与多种物质发生反应。下列物质与盐酸反应时,能观察到白色沉淀的是( )
A.B.C.D.
22.(2021·南湖模拟)硫酸是一种常见的酸。下列关于硫酸的说法中,正确的是( )
A.组成:硫酸溶液中有H+和SO42-两种微粒,且数目相同
B.性质:能与碱、多种金属和CO2、SO3等非金属氧化物反应
C.用途:可用于清除铁表面的氧化铁和生产化肥硫酸铵
D.检验:滴入氯化钡溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解
23.(2020·江干模拟)下列选项没有体现酸的通性或者碱的通性的是( )
A.实验室制取二氧化碳和氢气
B.利用稀硫酸除去硫酸钠中混有的少量碳酸钠
C.可溶性铜盐或铁盐遇氢氧化钠产生有色沉淀
D.实验室利用硝酸钡鉴别稀硫酸和稀盐酸
24.(2020·上城模拟)为了研究稀硫酸的性质,教材中设计了如图所示实验。分别将过量的稀硫酸滴入盛有锌粒,氧化铁粉末,氧化铜粉末,氢氧化铜和氯化钡溶液的5支试管中。关于实验过程和结论 正确的是( )
A.所有的反应均体现了酸的通性
B.把稀硫酸改成稀盐酸现象都相同
C.氧化铁与硫酸反应生成硫酸亚铁
D.反应后的溶液全部倒进废液缸不再发生新的反应
25.(2018·镇海模拟)向某硫酸和硫酸铜的混合溶液中加入一定浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法正确的是( )
A.a点溶液中含有两种溶质
B.bc段发生反应的类型为置换反应
C.根据图中数据可以计算出氢氧化钠溶液的浓度
D.d点溶液中主要存在的离子为Na+、Cu2+、OH-、SO42-
26.(2022九下·天台开学考)烧杯中盛有盐酸和氯化镁的混合溶液,向其中逐渐加入过量 10%氢氧化钠溶液,下列有关 图像不正确的是( )
A.B.C.D.
四、碱的性质
27.(2021九上·奉化期末)实验室有一瓶敞口放置的氢氧化钠溶液。对于该溶液变质情况的探究,下列实验设计合理且结论正确的是( )
A.取样,在溶液中加入少量的稀盐酸,若无气泡产生,则可证明该溶液没有变质
B.取样,在溶液中滴加酚酞,若溶液呈红色,则可证明该溶液没有变质
C.取样,在溶液中加入过量的稀盐酸,若有气泡产生,则可证明该溶液已变质
D.取样,在溶液中加入过量氯化钡溶液,若产生白色沉淀,则可证明溶液已完全变质
28.某锥形瓶内盛有盐酸和氯化铜的混合溶液100g,向其中加入溶质质量分数为10%的氢氧化钠溶液,锥形瓶内溶液质量m1与加入的氢氧化钠溶液质量m2的变化关系如图所示。下列说法错误的是( )
A.反应至A点时,所加NaOH溶液的质量为40g
B.反应至A点时,溶液中的溶质有CuCl2和NaCl
C.反应至B点时,锥形瓶内溶液的质量为280.4g
D.反应至B点时,锥形瓶内溶液中NaCl的质量为23.4g
29.研究氢氧化钠性质实验中的部分实验及现象记录如下,其中现象不合理的是( )
序号 实 验 现 象
A 将氢氧化钠固体放在表面皿上,放置一会儿 固体受潮,逐渐溶解
B 向盛有氢氧化钠溶液的试管中滴入无色酚酞试液 溶液变红
C 向盛有氢氧化钠溶液的试管中滴加稀盐酸 有氯化钠生成
D 向盛有氢氧化钠溶液的试管中滴加硫酸铜溶液 产生蓝色沉淀
A.A B.B C.C D.D
30.一定质量的氢氧化钡溶液中逐渐加入碳酸钠粉末(不考虑溶液体积变化),直至过量。如图横坐表示加入碳酸钠粉末的质量,根据图像判断,纵坐标可能表示( )
A.生成沉淀的质量 B.溶液中溶剂的质量
C.溶液中溶质的质量 D.溶液的pH
31.在氢氧化钠溶液中加入一定量的稀盐酸后,下列实验能证明两者恰好完全中和的是( )
A.滴入适量FeCl3溶液,溶液变黄,但无沉淀生成
B.滴入几滴酚酞试液,酚酞试液不变色
C.测得反应后溶液中Na+与Cl-的个数比为1:1
D.滴入适量AgNO3溶液和稀硝酸,观察到有白色沉淀
32.小科为研究“碱与盐反应”的规律,设计了如图所示的五组实验,每支试管盛有3毫升溶液,分别向试管中只滴加3滴溶液。除氢氧化钙溶液是饱和外,其余溶液的质量分数都为5%。下列叙述正确的是( )
A.甲组和乙组实验能观察到相同现象
B.乙组和丙组实验均能观察到蓝色沉淀
C.乙组实验产生的沉淀质量比丁组多
D.戊组实验产生的沉淀质量比丙组少
33.(2020·温州模拟)小雅将滴有酚酞的Ba(OH)2溶液平均分成两份,置于甲、乙两个烧杯中,分别往甲、乙两烧杯中滴加稀硫酸、硫酸钠溶液至过量(如图)。下列说法正确的是( )
A.甲烧杯中,溶液的颜色始终为红色
B.甲烧杯中,氢离子的数量一直不变
C.乙烧杯中,溶液的颜色始终为红色
D.乙烧杯中,钠离子的数量一直不变
34.(2019·杭州模拟)小乐按图示操作进行酸和碱反应的实验,下别有关分析正确的是( )
A.①中NaOH溶液易潮解和变质,需密封保存
B.②中酚酞试液变红,其原因是溶液中存在Na+
C.③中反应的实质是H+和OH-结台生成水
D.⑤中浓硫酸的稀释中,甲物质是水
35.(2019·杭州模拟)某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法不正确的是( )
A.a点所示溶液中,含有的溶质是NaCl和NaOH
B.c点所示溶液能使紫色石蕊溶液变蓝
C.b点表示氢氧化钠和稀盐酸恰好完全反应
D.a、b、c所示的溶液中都含有 Na+、Cl-
36.(2019·浙江模拟)为了探究酸碱中和反应是否放热,某同学设计了如图所示的实验装置(夹持等固定装置图略),针对该实验目的,下列评价或改进,错误的是( )
A.若观察到红墨水向右移,则说明该实验一定有放热现象
B.为了使实验现象更明显,可改用氢氧化钠固体
C.在打开活塞a之前应先打开橡皮管上的止水夹
D.为了使实验更具有说服力,可用氢氧化钾溶液再次实验
答案解析部分
1.【答案】B2.【答案】B3.【答案】A4.【答案】D5.【答案】D6.【答案】D
7.【答案】C8.【答案】B9.【答案】C10.【答案】A11.【答案】C
12.【答案】D13.【答案】C14.【答案】C15.【答案】D16.【答案】C17.【答案】D
18.【答案】A19.【答案】C20.【答案】C21.【答案】C22.【答案】C23.【答案】D
24.【答案】D25.【答案】C26.【答案】D27.【答案】C28.【答案】D29.【答案】C
30.【答案】C31.【答案】C32.【答案】D33.【答案】C34.【答案】C35.【答案】A
36.【答案】B
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
