九年级化学京改版(2013)下册 第11章酸与碱随堂练习题(word版 含答案)
文档属性
| 名称 | 九年级化学京改版(2013)下册 第11章酸与碱随堂练习题(word版 含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 121.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-22 00:00:00 | ||
图片预览


文档简介
第11章酸与碱随堂练习题—2021-2022学年九年级化学京改版(2013)下册
一、单选题
1.某同学在化学晚会上用毛笔蘸取一种无色液体在一张白纸上书写了“化学魔术”四个字,然后再喷上另一种无色液体,白纸上立即出现了红色的“化学魔术”四个字。该同学所用的两种无色液体可能是
A.NaOH溶液、酚酞溶液
B.白醋、酚酞溶液
C.紫色石蕊溶液、酚酞溶液
D.“雪碧”饮料、酚酞溶液
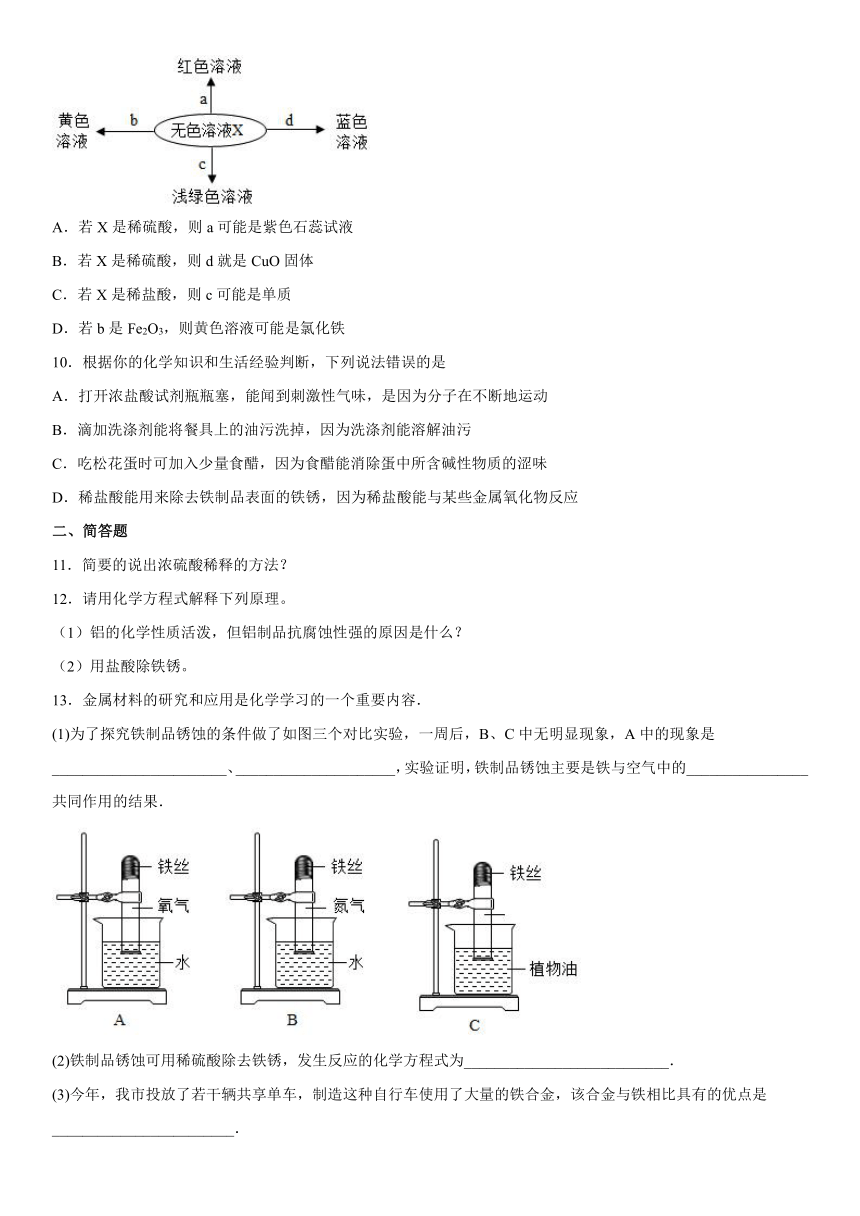
2.下列实验操作正确的是
A. 滴加液体 B. 取用固体
C. 测溶液pH D. 过滤
3.分别向甲、乙、丙三种无色溶液中滴加紫色石蕊试液,观察到甲溶液变红色,乙溶液变蓝色,丙溶液变紫色。则它们的pH由小到大的排列是( )
A.甲、乙、丙 B.甲、丙、乙 C.乙、甲、丙 D.丙、甲、乙
4.下列物质间不能发生反应的是( )
A.稀盐酸和镁条
B.稀盐酸和铜丝
C.稀盐酸和氢氧化镁
D.稀盐酸和氢氧化铜
5.小华将一张滤纸在某指示剂 X 中浸泡后晾干,用蘸有氢氧化钠溶液的玻璃棒在上面写“化学”两字,立刻显红色。再将其悬挂于铁架台上,并在滤纸的下方(如图)放置一个盛有某溶液 Y 的烧杯,过一会儿,发现红色的字消失,则滤纸上的指示剂 X 和烧杯中的溶液 Y 分别是( )
A B C D
指示剂 X 酚酞溶液 酚酞溶液 石蕊溶液 石蕊溶液
溶液 Y 浓氨水 浓盐酸 浓氨水 浓盐酸
A.A B.B C.C D.D
6.逻辑推理是一种重要的化学思维方法,以下推理合理的是( )
A.因为酸性的溶液能使石蕊变红,所以酸溶液一定能使石蕊变红
B.因为酸和碱中和反应生成盐和水,所以生成盐和水一定是中和反应
C.因为金属能和酸反应产生氢气,所以能和酸产生气体的一定是金属
D.酸性氧化物是非金属氧化物,所以非金属氧化物一定是酸性氧化物
7.某校化学小组在利用硫酸和氢氧化钾两溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图像如图所示。下列说法正确的是
A.图中c点所示溶液呈碱性
B.图中a点所示溶液中,含有的溶质是K2SO4和H2SO4
C.该实验是将氢氧化钾溶液逐滴滴入到盛有硫酸溶液的烧杯中
D.由c点到d点的变化过程中没有发生化学反应
8.推理是一种重要的化学思维方法,以下推理合理的是
A.元素的种类是由质子数决定的,则质子数相同的原子属于同种元素
B.溶液是均一、稳定的,所以均一、稳定的物质一定是溶液
C.洗涤剂去油污是利用了乳化作用,则汽油去油污也是利用了乳化作用
D.中和反应一定有盐和水生成,所以有盐和水生成的反应一定是中和反应
9.如图表示化学反应中溶液的颜色变化,下列叙述错误的是( )
A.若X是稀硫酸,则a可能是紫色石蕊试液
B.若X是稀硫酸,则d就是CuO固体
C.若X是稀盐酸,则c可能是单质
D.若b是Fe2O3,则黄色溶液可能是氯化铁
10.根据你的化学知识和生活经验判断,下列说法错误的是
A.打开浓盐酸试剂瓶瓶塞,能闻到刺激性气味,是因为分子在不断地运动
B.滴加洗涤剂能将餐具上的油污洗掉,因为洗涤剂能溶解油污
C.吃松花蛋时可加入少量食醋,因为食醋能消除蛋中所含碱性物质的涩味
D.稀盐酸能用来除去铁制品表面的铁锈,因为稀盐酸能与某些金属氧化物反应
二、简答题
11.简要的说出浓硫酸稀释的方法?
12.请用化学方程式解释下列原理。
(1)铝的化学性质活泼,但铝制品抗腐蚀性强的原因是什么?
(2)用盐酸除铁锈。
13.金属材料的研究和应用是化学学习的一个重要内容.
(1)为了探究铁制品锈蚀的条件做了如图三个对比实验,一周后,B、C中无明显现象,A中的现象是_______________________、_____________________,实验证明,铁制品锈蚀主要是铁与空气中的________________共同作用的结果.
(2)铁制品锈蚀可用稀硫酸除去铁锈,发生反应的化学方程式为___________________________.
(3)今年,我市投放了若干辆共享单车,制造这种自行车使用了大量的铁合金,该合金与铁相比具有的优点是________________________.
三、推断题
14.A~F是初中化学常见物质,已知在常温下A和F均为气体,B常用于制肥皂,C可用于精炼石油,D、E均为黑色粉末。用“一”表示两种物质可以发生化学反应,用“→”表示一种物质能转化为另一种物质。它们之间的部分关系如图所示。请回答下列问题:
(1)请写出下列物质(或主要成分)的化学式:B_________
(2)请写出C与D生成蓝色溶液的化学方程式___________________
(3)请写出F与D生成A时,二者发生反应的装置内观察到的现象为_______________
15.A-F是初中化学常见的物质,且均含有同一种元素,它们相互间的关系如图所示,已知A、B、C、D、E是不同类别的物质,其中C可用于玻璃、造纸、纺织、石油精炼、洗涤剂生产等领域,F是相对分子质量最小的氧化物(注:图中反应条件及部分反应物生成物已省略,“-”表示反应关系,“→”表示转化关系),请回答:
(1)写出下列物质C的化学式_______。
(2)写出D与E反应的化学方程式_______。
四、实验题
16.下列有两组实验,请根据实验中的问题写出化学反应方程式。
(1)写出实验一试管中液面上升“更高”的化学反应方程式:____________。
(2)写出实验二反应“更快”的化学方程式:_______________。
17.以下是实验室制取、干燥收集氧气的实验装置。按要求回答下列问题:
(1)仪器①的名称是_____。
(2)小李用A装置制取O2,写出发生反应的化学方程式_____,实验时发现始终收集不满氧气,请你解释原因_____。
(3)用B装置收集氧气时,气体应该从_____(填字母序号)端通入。
(4)浓硫酸具有吸水性,可以干燥氧气。兴趣小组的同学用湿度传感器测出经过C装置后收集到的氧气湿度为35. 5% ,说明实验中使用浓硫酸作干燥剂_____( 填“能”或“不能”)完全除去氧气中的水蒸气。
18.室温下,将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,利用温度计测出烧杯中溶液的温度,溶液温度随加入盐酸的质量而变化的曲线如图所示:
(1)由如图可知,盐酸与氢氧化钠溶液中和反应是__(填“吸热”或“放热”或“无热量变化”)反应。
(2)在A处溶液中加入石蕊,溶液呈__色。
(3)B处溶液的溶质是__(填化学式)。
(4)B到C的过程中溶液的pH逐渐__(填“增大”或“减小”或“无变化”)。
(5)在C点溶液中加入碳酸钙,现象为__,化学方程式为__。
五、计算题
19.(1)配制200g质量分数为5%的氢氧化钠溶液,需要需要水______mL.配制时用到玻璃仪器有______、烧杯、玻璃棒和胶头滴管。(水的密度近似看作1g/cm3)
(2)用配得氢氧化钠溶液与某硫酸溶液反应,如图是利用数字化传感器得到的溶液pH变化图象。
①根据图中曲线,判断进行的操作是______(填字母)。
A 将硫酸溶液逐滴滴加到氢氧化钠溶液中
B 将氢氧化钠溶液逐滴滴加到硫酸溶液中
②从微观角度分析,该反应实质为______。
③b点对应的溶液中的溶质为______(写化学式)。
④若80g 5%的氢氧化钠溶液能恰好中和50g硫酸溶液,试计算该硫酸溶液的溶质质量分数_____。(请写出计算过程)。
20.实验室常用石灰石和稀盐酸制取二氧化碳,现取含碳酸钙80%的石灰石12.5g和73g稀盐酸恰好完全反应(石灰石中的杂质不溶于水,也不与稀盐酸反应)。求:该稀盐酸的溶质质量分数。
21.向盛有100g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示。
(1)反应生成沉淀的质量为_____克。
(2)镁粉完全溶解后所得溶液中的溶质成分为_____。
(3)计算氢氧化钠溶液的溶质质量分数_____(要求写出计算过程)。
22.实验室中有一瓶标签被腐蚀的盐酸,小丽为了测定溶液中溶质的质量分数,在烧杯中配制了8克10%的氢氧化钠溶液,然后往烧杯中滴加该盐酸,反应过程中溶液的pH与滴入盐酸的质量关系如图所示。请回答下列问题:
(1)配制8克10%的氢氧化钠溶液,需要水的质量为______g;
(2)计算该盐酸的溶质质量分数;__________(写出计算过程)
(3)当滴入4克盐酸时,烧杯内溶液中钠元素的质量为_______g。
参考答案:
1.A
2.C
3.B
4.B
5.B
6.A
7.D
8.A
9.B
10.B
11.稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌.
12.(1)4Al+3O2=2Al2O3;
(2)6HCl+Fe2O3=2FeCl3+3H2O。
13. 铁丝生锈 试管内液面上升 氧气和水蒸气 Fe2O3+3H2SO4═Fe2(SO4)3+3H2O 硬度大,耐腐蚀等
14. NaOH H2SO4 C CO 黑色固体变成紫红色。
15. Na2CO3 Ca(OH)2+H2SO4=CaSO4+2H2O
16. 2NaOH+CO2=Na2CO3+H2O; 2HCl+Mg=MgCl2+H2↑;
17. 锥形瓶 装置的气密性不好(或药品量不足) a 不能
18. 放热 蓝 NaCl 减小 有气泡产生 CaCO3+2HCl═CaCl2+H2O+CO2↑
19. 190, 量筒 B 氢离子和氢氧根离子结合成水分子 Na2SO4、NaOH 9.8%
20.10%
21.(1)8.7(2)H2SO4、MgSO4(3)30%
22.(1)7.2;(2)7.3%;(3)0.46
一、单选题
1.某同学在化学晚会上用毛笔蘸取一种无色液体在一张白纸上书写了“化学魔术”四个字,然后再喷上另一种无色液体,白纸上立即出现了红色的“化学魔术”四个字。该同学所用的两种无色液体可能是
A.NaOH溶液、酚酞溶液
B.白醋、酚酞溶液
C.紫色石蕊溶液、酚酞溶液
D.“雪碧”饮料、酚酞溶液
2.下列实验操作正确的是
A. 滴加液体 B. 取用固体
C. 测溶液pH D. 过滤
3.分别向甲、乙、丙三种无色溶液中滴加紫色石蕊试液,观察到甲溶液变红色,乙溶液变蓝色,丙溶液变紫色。则它们的pH由小到大的排列是( )
A.甲、乙、丙 B.甲、丙、乙 C.乙、甲、丙 D.丙、甲、乙
4.下列物质间不能发生反应的是( )
A.稀盐酸和镁条
B.稀盐酸和铜丝
C.稀盐酸和氢氧化镁
D.稀盐酸和氢氧化铜
5.小华将一张滤纸在某指示剂 X 中浸泡后晾干,用蘸有氢氧化钠溶液的玻璃棒在上面写“化学”两字,立刻显红色。再将其悬挂于铁架台上,并在滤纸的下方(如图)放置一个盛有某溶液 Y 的烧杯,过一会儿,发现红色的字消失,则滤纸上的指示剂 X 和烧杯中的溶液 Y 分别是( )
A B C D
指示剂 X 酚酞溶液 酚酞溶液 石蕊溶液 石蕊溶液
溶液 Y 浓氨水 浓盐酸 浓氨水 浓盐酸
A.A B.B C.C D.D
6.逻辑推理是一种重要的化学思维方法,以下推理合理的是( )
A.因为酸性的溶液能使石蕊变红,所以酸溶液一定能使石蕊变红
B.因为酸和碱中和反应生成盐和水,所以生成盐和水一定是中和反应
C.因为金属能和酸反应产生氢气,所以能和酸产生气体的一定是金属
D.酸性氧化物是非金属氧化物,所以非金属氧化物一定是酸性氧化物
7.某校化学小组在利用硫酸和氢氧化钾两溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图像如图所示。下列说法正确的是
A.图中c点所示溶液呈碱性
B.图中a点所示溶液中,含有的溶质是K2SO4和H2SO4
C.该实验是将氢氧化钾溶液逐滴滴入到盛有硫酸溶液的烧杯中
D.由c点到d点的变化过程中没有发生化学反应
8.推理是一种重要的化学思维方法,以下推理合理的是
A.元素的种类是由质子数决定的,则质子数相同的原子属于同种元素
B.溶液是均一、稳定的,所以均一、稳定的物质一定是溶液
C.洗涤剂去油污是利用了乳化作用,则汽油去油污也是利用了乳化作用
D.中和反应一定有盐和水生成,所以有盐和水生成的反应一定是中和反应
9.如图表示化学反应中溶液的颜色变化,下列叙述错误的是( )
A.若X是稀硫酸,则a可能是紫色石蕊试液
B.若X是稀硫酸,则d就是CuO固体
C.若X是稀盐酸,则c可能是单质
D.若b是Fe2O3,则黄色溶液可能是氯化铁
10.根据你的化学知识和生活经验判断,下列说法错误的是
A.打开浓盐酸试剂瓶瓶塞,能闻到刺激性气味,是因为分子在不断地运动
B.滴加洗涤剂能将餐具上的油污洗掉,因为洗涤剂能溶解油污
C.吃松花蛋时可加入少量食醋,因为食醋能消除蛋中所含碱性物质的涩味
D.稀盐酸能用来除去铁制品表面的铁锈,因为稀盐酸能与某些金属氧化物反应
二、简答题
11.简要的说出浓硫酸稀释的方法?
12.请用化学方程式解释下列原理。
(1)铝的化学性质活泼,但铝制品抗腐蚀性强的原因是什么?
(2)用盐酸除铁锈。
13.金属材料的研究和应用是化学学习的一个重要内容.
(1)为了探究铁制品锈蚀的条件做了如图三个对比实验,一周后,B、C中无明显现象,A中的现象是_______________________、_____________________,实验证明,铁制品锈蚀主要是铁与空气中的________________共同作用的结果.
(2)铁制品锈蚀可用稀硫酸除去铁锈,发生反应的化学方程式为___________________________.
(3)今年,我市投放了若干辆共享单车,制造这种自行车使用了大量的铁合金,该合金与铁相比具有的优点是________________________.
三、推断题
14.A~F是初中化学常见物质,已知在常温下A和F均为气体,B常用于制肥皂,C可用于精炼石油,D、E均为黑色粉末。用“一”表示两种物质可以发生化学反应,用“→”表示一种物质能转化为另一种物质。它们之间的部分关系如图所示。请回答下列问题:
(1)请写出下列物质(或主要成分)的化学式:B_________
(2)请写出C与D生成蓝色溶液的化学方程式___________________
(3)请写出F与D生成A时,二者发生反应的装置内观察到的现象为_______________
15.A-F是初中化学常见的物质,且均含有同一种元素,它们相互间的关系如图所示,已知A、B、C、D、E是不同类别的物质,其中C可用于玻璃、造纸、纺织、石油精炼、洗涤剂生产等领域,F是相对分子质量最小的氧化物(注:图中反应条件及部分反应物生成物已省略,“-”表示反应关系,“→”表示转化关系),请回答:
(1)写出下列物质C的化学式_______。
(2)写出D与E反应的化学方程式_______。
四、实验题
16.下列有两组实验,请根据实验中的问题写出化学反应方程式。
(1)写出实验一试管中液面上升“更高”的化学反应方程式:____________。
(2)写出实验二反应“更快”的化学方程式:_______________。
17.以下是实验室制取、干燥收集氧气的实验装置。按要求回答下列问题:
(1)仪器①的名称是_____。
(2)小李用A装置制取O2,写出发生反应的化学方程式_____,实验时发现始终收集不满氧气,请你解释原因_____。
(3)用B装置收集氧气时,气体应该从_____(填字母序号)端通入。
(4)浓硫酸具有吸水性,可以干燥氧气。兴趣小组的同学用湿度传感器测出经过C装置后收集到的氧气湿度为35. 5% ,说明实验中使用浓硫酸作干燥剂_____( 填“能”或“不能”)完全除去氧气中的水蒸气。
18.室温下,将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,利用温度计测出烧杯中溶液的温度,溶液温度随加入盐酸的质量而变化的曲线如图所示:
(1)由如图可知,盐酸与氢氧化钠溶液中和反应是__(填“吸热”或“放热”或“无热量变化”)反应。
(2)在A处溶液中加入石蕊,溶液呈__色。
(3)B处溶液的溶质是__(填化学式)。
(4)B到C的过程中溶液的pH逐渐__(填“增大”或“减小”或“无变化”)。
(5)在C点溶液中加入碳酸钙,现象为__,化学方程式为__。
五、计算题
19.(1)配制200g质量分数为5%的氢氧化钠溶液,需要需要水______mL.配制时用到玻璃仪器有______、烧杯、玻璃棒和胶头滴管。(水的密度近似看作1g/cm3)
(2)用配得氢氧化钠溶液与某硫酸溶液反应,如图是利用数字化传感器得到的溶液pH变化图象。
①根据图中曲线,判断进行的操作是______(填字母)。
A 将硫酸溶液逐滴滴加到氢氧化钠溶液中
B 将氢氧化钠溶液逐滴滴加到硫酸溶液中
②从微观角度分析,该反应实质为______。
③b点对应的溶液中的溶质为______(写化学式)。
④若80g 5%的氢氧化钠溶液能恰好中和50g硫酸溶液,试计算该硫酸溶液的溶质质量分数_____。(请写出计算过程)。
20.实验室常用石灰石和稀盐酸制取二氧化碳,现取含碳酸钙80%的石灰石12.5g和73g稀盐酸恰好完全反应(石灰石中的杂质不溶于水,也不与稀盐酸反应)。求:该稀盐酸的溶质质量分数。
21.向盛有100g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示。
(1)反应生成沉淀的质量为_____克。
(2)镁粉完全溶解后所得溶液中的溶质成分为_____。
(3)计算氢氧化钠溶液的溶质质量分数_____(要求写出计算过程)。
22.实验室中有一瓶标签被腐蚀的盐酸,小丽为了测定溶液中溶质的质量分数,在烧杯中配制了8克10%的氢氧化钠溶液,然后往烧杯中滴加该盐酸,反应过程中溶液的pH与滴入盐酸的质量关系如图所示。请回答下列问题:
(1)配制8克10%的氢氧化钠溶液,需要水的质量为______g;
(2)计算该盐酸的溶质质量分数;__________(写出计算过程)
(3)当滴入4克盐酸时,烧杯内溶液中钠元素的质量为_______g。
参考答案:
1.A
2.C
3.B
4.B
5.B
6.A
7.D
8.A
9.B
10.B
11.稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌.
12.(1)4Al+3O2=2Al2O3;
(2)6HCl+Fe2O3=2FeCl3+3H2O。
13. 铁丝生锈 试管内液面上升 氧气和水蒸气 Fe2O3+3H2SO4═Fe2(SO4)3+3H2O 硬度大,耐腐蚀等
14. NaOH H2SO4 C CO 黑色固体变成紫红色。
15. Na2CO3 Ca(OH)2+H2SO4=CaSO4+2H2O
16. 2NaOH+CO2=Na2CO3+H2O; 2HCl+Mg=MgCl2+H2↑;
17. 锥形瓶 装置的气密性不好(或药品量不足) a 不能
18. 放热 蓝 NaCl 减小 有气泡产生 CaCO3+2HCl═CaCl2+H2O+CO2↑
19. 190, 量筒 B 氢离子和氢氧根离子结合成水分子 Na2SO4、NaOH 9.8%
20.10%
21.(1)8.7(2)H2SO4、MgSO4(3)30%
22.(1)7.2;(2)7.3%;(3)0.46
