人教版化学九年级下册 第十一单元 盐 化肥 课 题2化学肥料第2课 时-课件(共15张PPT)
文档属性
| 名称 | 人教版化学九年级下册 第十一单元 盐 化肥 课 题2化学肥料第2课 时-课件(共15张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-22 00:00:00 | ||
图片预览





文档简介
(共15张PPT)
课 题 2 化学肥料
第 2 课 时
第十一单元 盐 化肥
第十一单元 盐 化肥
1.了解各种化肥的物理性质,能从外观上区分各类化肥。
2.知道什么是铵态氮肥,知道铵根离子的检验方法。
3.能说出常见铵态氮肥使用的注意事项。
4.能根据化肥的化学性质鉴别各种常见化肥。
学 习 目 标
自 主 探 究
Ca3(PO4)2
NH4HCO3
K2SO4
CO(NH2)2
思考:你能从外观上区分以下化肥吗?
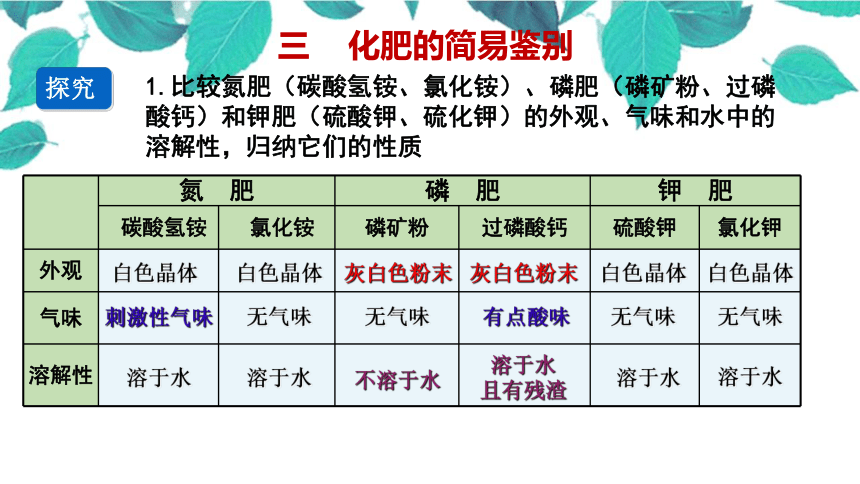
三 化肥的简易鉴别
探究
氮 肥 磷 肥 钾 肥
碳酸氢铵 氯化铵 磷矿粉 过磷酸钙 硫酸钾 氯化钾
外观
气味
溶解性
1.比较氮肥(碳酸氢铵、氯化铵)、磷肥(磷矿粉、过磷酸钙)和钾肥(硫酸钾、硫化钾)的外观、气味和水中的溶解性,归纳它们的性质
白色晶体
白色晶体
灰白色粉末
灰白色粉末
白色晶体
白色晶体
刺激性气味
无气味
无气味
无气味
无气味
有点酸味
溶于水
溶于水
不溶于水
溶于水
溶于水
溶于水
且有残渣
探究
2.取下列化肥各少量,分别加入少量熟石灰粉末,混合、研磨,能否嗅到气味?
氮肥 钾肥
硫酸铵 氯化铵 硫酸钾 氯化钾
加熟石灰研磨
氨气的气味
有刺激性气味
有刺激性气味
无气味
无气味
看外观:氮肥、钾肥都是白色晶体;磷肥是灰白色粉末。
加水:氮肥、钾肥都溶于水;磷肥大多不溶于水或部分溶于水。
总结
初步区分氮肥、磷肥和钾肥的步骤和方法
加熟石灰:铵态氮肥(铵盐)能放出具有刺激性气味的氨气。
液态
刺激性气味
区别于其他氮肥
尿素【CO(NH2)2】
硫酸铵【(NH4)2SO4】
硝酸铵【NH4NO3】
氯化铵【NH4Cl】
碳酸氢铵【NH4HCO3】
氨水【NH3·H2O】
常见氮肥
NH4+
铵态氮肥
铵根离子(NH4+)的检验
检验原理:铵盐能与碱反应,放出氨气,氨气能使湿润的红色石蕊试纸变蓝。
NH4+
铵态氮肥
OH-
NH3
刺激性气味
铵态氮肥不能与碱性物质混合使用!
操作方法
加熟石灰混合研磨或者加入氢氧化钠溶液加热
放出有刺激性气味的气体,用湿润的红色石蕊试纸检验放出的气体,如果湿润的红色石蕊试纸变蓝,含有铵根离子
无明显现象,不含铵根离子
鉴别(NH4)2SO4、 NH4Cl、 NH4NO3、 CO(NH2)2
(NH4)2SO4、 NH4Cl、 NH4NO3、 CO(NH2)2
加熟石灰研磨或者加入氢氧化钠溶液加热
(NH4)2SO4、 NH4Cl、 NH4NO3
CO(NH2)2
有氨味
无氨味
Ba2+ +SO42-→BaSO4↓
Ag+ +Cl- → AgCl↓
加硝酸钡溶液和稀硝酸
无沉淀
有白色沉淀
(NH4)2SO4
NH4Cl、 NH4NO3
加硝酸银溶液和稀硝酸
无沉淀
有白色沉淀
NH4Cl
NH4NO3
课 堂 达 标
2.下列化肥中,从外观即可与其他化肥相区别的是( )
A.硫酸钾 B.硝酸铵 C.磷矿粉 D.氯化钾
1.硝酸铵(俗称硝铵)是一种常见的氮肥,易溶于水易潮解而结块,受热易分解,遇碱放出氨气,在高温或受猛烈撞击时易爆炸。贮存或使用硝铵时正确的是 ( )
A.露天敞口贮存 B.在阴凉处密封贮存
C.结块时用铁锤砸碎 D.与熟石灰混合施用
B
C
D
3.实验室有失去标签的三种化肥,只知道是硫酸铵、硝酸铵、氯化钾,现各取少许进行鉴别,下列物质中能将上述肥料一次性区别开来的一种试剂是( )
A.熟石灰 B.水
C.稀盐酸 D.氢氧化钡溶液
4.下列鉴别化肥的方法不合理的是( )
A.用观察法可鉴别氮肥和磷矿粉
B.用闻气味的方法可鉴别碳酸氢铵和氯化铵
C.用加硝酸银溶液的方法可鉴别硝酸钾和氯化钾
D.用加入熟石灰研磨的方法可鉴别硫酸铵和氯化铵
D
5.某KNO3 化肥中可能混进了NH4 Cl、(NH4 )2 SO4 、K2 CO3 三种物质中的一种或几种,同学们对该化肥开展了以下探究活动。
(1)【探究一】取少量化肥样品与熟石灰在研钵中混合研磨,有刺激性气味的气体产生,该气体的化学式为 ,它能使湿润的红色石蕊试纸变 色。
(2)【探究二】另取少量化肥样品溶于水得到溶液A,按如图所示进行实验,请你回答下列问题:
①白色沉淀E是 。
NH3
蓝
BaSO4
②小明认为由探究二可以确定该化肥中一定混进了NH4 Cl和(NH4 )2 SO4 、一定没有K2 CO3 ,小强认为这个结论不正确,他的理由是 ,为了使小明的结论正确,小强对上述实验进行了改动,他的做法是 。
(3)探究二最终的溶液D中一定存在的溶质是__________________ (写化学式),该废液 (填“能”或“不能”)直接排放。
步骤一加入盐酸引入了氯离子,干扰后续NH4 Cl的检验
将步骤一中的稀盐酸改为稀硝酸
KNO3、NH4NO3、HNO3
不能
课 题 2 化学肥料
第 2 课 时
第十一单元 盐 化肥
第十一单元 盐 化肥
1.了解各种化肥的物理性质,能从外观上区分各类化肥。
2.知道什么是铵态氮肥,知道铵根离子的检验方法。
3.能说出常见铵态氮肥使用的注意事项。
4.能根据化肥的化学性质鉴别各种常见化肥。
学 习 目 标
自 主 探 究
Ca3(PO4)2
NH4HCO3
K2SO4
CO(NH2)2
思考:你能从外观上区分以下化肥吗?
三 化肥的简易鉴别
探究
氮 肥 磷 肥 钾 肥
碳酸氢铵 氯化铵 磷矿粉 过磷酸钙 硫酸钾 氯化钾
外观
气味
溶解性
1.比较氮肥(碳酸氢铵、氯化铵)、磷肥(磷矿粉、过磷酸钙)和钾肥(硫酸钾、硫化钾)的外观、气味和水中的溶解性,归纳它们的性质
白色晶体
白色晶体
灰白色粉末
灰白色粉末
白色晶体
白色晶体
刺激性气味
无气味
无气味
无气味
无气味
有点酸味
溶于水
溶于水
不溶于水
溶于水
溶于水
溶于水
且有残渣
探究
2.取下列化肥各少量,分别加入少量熟石灰粉末,混合、研磨,能否嗅到气味?
氮肥 钾肥
硫酸铵 氯化铵 硫酸钾 氯化钾
加熟石灰研磨
氨气的气味
有刺激性气味
有刺激性气味
无气味
无气味
看外观:氮肥、钾肥都是白色晶体;磷肥是灰白色粉末。
加水:氮肥、钾肥都溶于水;磷肥大多不溶于水或部分溶于水。
总结
初步区分氮肥、磷肥和钾肥的步骤和方法
加熟石灰:铵态氮肥(铵盐)能放出具有刺激性气味的氨气。
液态
刺激性气味
区别于其他氮肥
尿素【CO(NH2)2】
硫酸铵【(NH4)2SO4】
硝酸铵【NH4NO3】
氯化铵【NH4Cl】
碳酸氢铵【NH4HCO3】
氨水【NH3·H2O】
常见氮肥
NH4+
铵态氮肥
铵根离子(NH4+)的检验
检验原理:铵盐能与碱反应,放出氨气,氨气能使湿润的红色石蕊试纸变蓝。
NH4+
铵态氮肥
OH-
NH3
刺激性气味
铵态氮肥不能与碱性物质混合使用!
操作方法
加熟石灰混合研磨或者加入氢氧化钠溶液加热
放出有刺激性气味的气体,用湿润的红色石蕊试纸检验放出的气体,如果湿润的红色石蕊试纸变蓝,含有铵根离子
无明显现象,不含铵根离子
鉴别(NH4)2SO4、 NH4Cl、 NH4NO3、 CO(NH2)2
(NH4)2SO4、 NH4Cl、 NH4NO3、 CO(NH2)2
加熟石灰研磨或者加入氢氧化钠溶液加热
(NH4)2SO4、 NH4Cl、 NH4NO3
CO(NH2)2
有氨味
无氨味
Ba2+ +SO42-→BaSO4↓
Ag+ +Cl- → AgCl↓
加硝酸钡溶液和稀硝酸
无沉淀
有白色沉淀
(NH4)2SO4
NH4Cl、 NH4NO3
加硝酸银溶液和稀硝酸
无沉淀
有白色沉淀
NH4Cl
NH4NO3
课 堂 达 标
2.下列化肥中,从外观即可与其他化肥相区别的是( )
A.硫酸钾 B.硝酸铵 C.磷矿粉 D.氯化钾
1.硝酸铵(俗称硝铵)是一种常见的氮肥,易溶于水易潮解而结块,受热易分解,遇碱放出氨气,在高温或受猛烈撞击时易爆炸。贮存或使用硝铵时正确的是 ( )
A.露天敞口贮存 B.在阴凉处密封贮存
C.结块时用铁锤砸碎 D.与熟石灰混合施用
B
C
D
3.实验室有失去标签的三种化肥,只知道是硫酸铵、硝酸铵、氯化钾,现各取少许进行鉴别,下列物质中能将上述肥料一次性区别开来的一种试剂是( )
A.熟石灰 B.水
C.稀盐酸 D.氢氧化钡溶液
4.下列鉴别化肥的方法不合理的是( )
A.用观察法可鉴别氮肥和磷矿粉
B.用闻气味的方法可鉴别碳酸氢铵和氯化铵
C.用加硝酸银溶液的方法可鉴别硝酸钾和氯化钾
D.用加入熟石灰研磨的方法可鉴别硫酸铵和氯化铵
D
5.某KNO3 化肥中可能混进了NH4 Cl、(NH4 )2 SO4 、K2 CO3 三种物质中的一种或几种,同学们对该化肥开展了以下探究活动。
(1)【探究一】取少量化肥样品与熟石灰在研钵中混合研磨,有刺激性气味的气体产生,该气体的化学式为 ,它能使湿润的红色石蕊试纸变 色。
(2)【探究二】另取少量化肥样品溶于水得到溶液A,按如图所示进行实验,请你回答下列问题:
①白色沉淀E是 。
NH3
蓝
BaSO4
②小明认为由探究二可以确定该化肥中一定混进了NH4 Cl和(NH4 )2 SO4 、一定没有K2 CO3 ,小强认为这个结论不正确,他的理由是 ,为了使小明的结论正确,小强对上述实验进行了改动,他的做法是 。
(3)探究二最终的溶液D中一定存在的溶质是__________________ (写化学式),该废液 (填“能”或“不能”)直接排放。
步骤一加入盐酸引入了氯离子,干扰后续NH4 Cl的检验
将步骤一中的稀盐酸改为稀硝酸
KNO3、NH4NO3、HNO3
不能
同课章节目录
