2022年化学中考备考复习专题突破 《 物质的检验与鉴别、除杂与分离》精讲课件(三)(课件47页)
文档属性
| 名称 | 2022年化学中考备考复习专题突破 《 物质的检验与鉴别、除杂与分离》精讲课件(三)(课件47页) |

|
|
| 格式 | zip | ||
| 文件大小 | 520.7KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-25 00:00:00 | ||
图片预览









文档简介
(共47张PPT)
2022年化学中考备考复习专题突破
《 物质的检验与鉴别、除杂与分离》精讲课件(三)
真题·练讲克重点
2
1
立足教材“过”考点
一、物质的检验
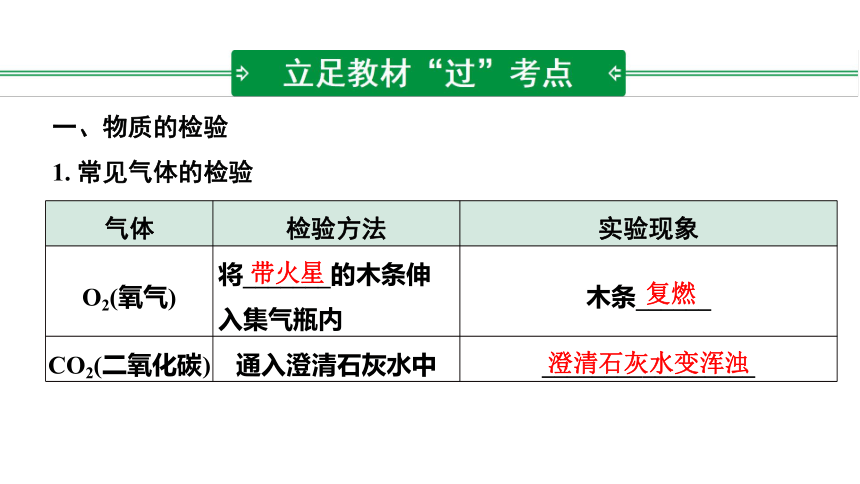
1. 常见气体的检验
气体 检验方法 实验现象
O2(氧气) 将_______的木条伸入集气瓶内 木条______
CO2(二氧化碳) 通入澄清石灰水中 _________________
带火星
复燃
澄清石灰水变浑浊
气体 检验方法 实验现象
H2(氢气) 点燃,在火焰上方罩一干冷的烧杯,迅速倒转后,注入少量澄清石灰水 产生蓝色火焰,烧杯内壁有水珠,澄清石灰水__________
CH4(甲烷) 产生蓝色火焰,烧杯内壁有水珠,澄清石灰水________
CO(一氧化碳) 产生蓝色火焰,烧杯内壁没有水珠,澄清石灰水_______
NH3(氨气) 将湿润的红色石蕊试纸放在试管口 红色石蕊试纸变____
不变浑浊
变浑浊
变浑浊
蓝
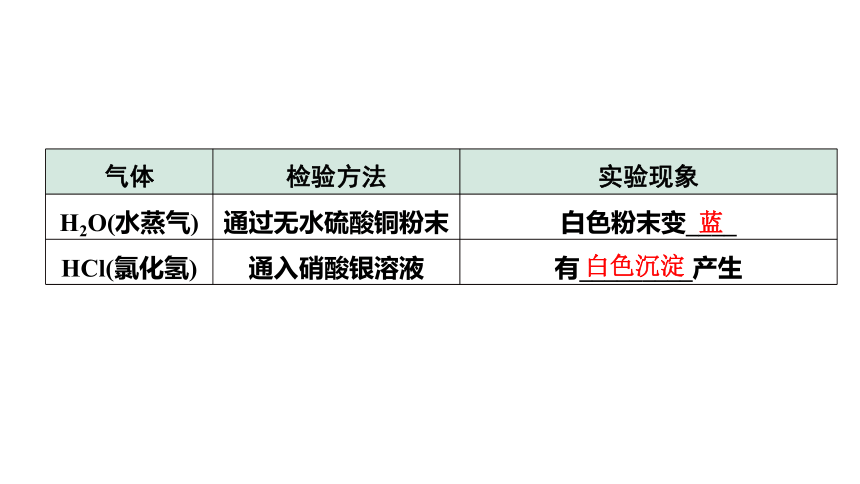
气体 检验方法 实验现象
H2O(水蒸气) 通过无水硫酸铜粉末 白色粉末变____
HCl(氯化氢) 通入硝酸银溶液 有_________产生
蓝
白色沉淀
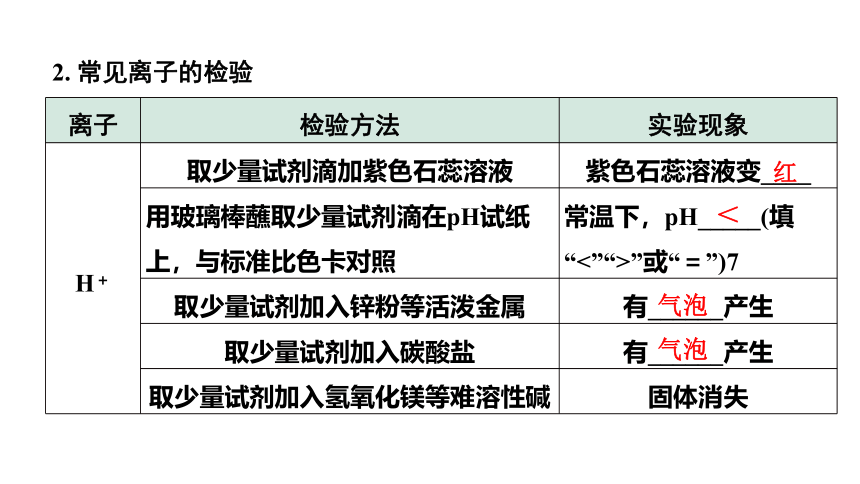
2. 常见离子的检验
离子 检验方法 实验现象
H+ 取少量试剂滴加紫色石蕊溶液 紫色石蕊溶液变____
用玻璃棒蘸取少量试剂滴在pH试纸上,与标准比色卡对照 常温下,pH_____(填“<”“>”或“=”)7
取少量试剂加入锌粉等活泼金属 有______产生
取少量试剂加入碳酸盐 有______产生
取少量试剂加入氢氧化镁等难溶性碱 固体消失
红
<
气泡
气泡
离子 检验方法 实验现象
H+ 取少量试剂加入氧化铁或氧化铜等金属氧化物 固体消失,溶液变为黄色或蓝色
OH- 取少量试剂滴加紫色石蕊溶液 紫色石蕊溶液变____
取少量试剂滴加无色酚酞溶液 无色酚酞溶液变____
用玻璃棒蘸取少量试剂滴在pH试纸上,与标准比色卡对照 常温下,pH____(填“>”“<”或“=”)7
取少量试剂加入含Cu2+或Fe3+或Mg2+的盐溶液 有____________________
_____生成
蓝
红
>
蓝色或红褐色或白色
沉淀
离子 检验方法 实验现象
Cl- 取少量试剂滴加少量___________和稀HNO3 有_________生成
(硫酸盐) 先滴加稀盐酸酸化,再滴加BaCl2溶液 酸化无现象,滴入BaCl2溶液_______________
(碳酸盐) 取少量试剂滴加________,并将产生的气体通入澄清石灰水中 有气泡产生,澄清石灰水变浑浊
(铵盐) 取少量试剂加入可溶性碱,加热,将湿润的红色石蕊试纸放在试管口 产生有刺激性气味的气体,红色石蕊试纸变____
AgNO3溶液
白色沉淀
有白色沉淀生成
稀盐酸
蓝
离子 检验方法 实验现象
Fe3+ 滴加NaOH溶液 ________________
Cu2+ 插入铁片 ____________________________________
滴加NaOH溶液 ______________
产生红褐色沉淀
铁片上有红色固体析出,溶液蓝色变浅
产生蓝色沉淀
二、物质的鉴别
1. 鉴别方法
(1)物理方法
颜色 溶液:如CuSO4溶液呈____色;FeCl3溶液呈____色;FeCl2溶液呈______色
固体:Cu为紫红色;Fe2O3为红棕色;CuO、炭粉、MnO2、铁粉为____色
气味 如SO2、NH3、HCl有刺激性气味
蓝
黄
浅绿
黑
溶解性 如CaCO3不溶于水,NaCl易溶于水,故可用水鉴别CaCO3和NaCl
溶解时的吸放热现象 如NaOH固体溶于水,溶液温度______;NH4NO3固体溶于水,溶液温度______,故可用水鉴别NaOH和NH4NO3固体
升高
降低
(2)化学方法
Ⅰ.加试剂鉴别:选择一种或多种试剂,分别加入到待测物质中根据不同的现象鉴别。
【即时练习】
a.鉴别稀盐酸、CaCl2溶液与NaOH溶液可分别加入紫色石蕊溶液,观察到__________的是稀盐酸,____________的是CaCl2溶液,_________的是NaOH溶液。
溶液变红
溶液不变色
溶液变蓝
b.鉴别稀盐酸、CaCl2溶液与NaOH溶液可分别加入碳酸钠溶液,观察到____________的是稀盐酸,_______________的是CaCl2溶液,________
_____的是NaOH溶液。
c.鉴别Na2CO3溶液、NaCl溶液和AgNO3溶液可分别加入稀盐酸,观察到____________的是Na2CO3溶液,____________的是NaCl溶液,____
_____________的是AgNO3溶液。
有气泡产生
有白色沉淀产生
现象
有气泡产生
无明显现象
白色沉淀产生
无明显
有
Ⅱ.无试剂鉴别
①特征现象法:首先鉴别出有颜色或有气味的物质,再利用已经鉴别出来的物质去鉴别其他物质,以此类推,从而将各物质一一鉴别出来。
如鉴别CuSO4、NaOH、NH4NO3固体:加水溶解,观察发现,只有CuSO4溶液为蓝色,其余均为无色,然后以CuSO4溶液为已知试剂来鉴别另外两种物质,鉴别顺序为CuSO4→ NaOH→ NH4NO3。
②两两混合法:当无法从物理性质入手时,采用两两混合的方法,根据与组内其他物质反应产生各种现象的不同组合,从而将四种物质鉴别出来。
如Na2SO4、Na2CO3、BaCl2、HCl,用两两混合反应的方法分析,可采用列表的方法统计现象,见下表:
(注:-表示不反应,↓表示有沉淀生成,↑表示有气体生成)
Na2SO4 Na2CO3 BaCl2 HCl
Na2SO4 - ↓ -
Na2CO3 - ↓ ↑
BaCl2 ↓ ↓ -
HCl - ↑ -
2. 常见物质的鉴别
物质 鉴别方法
面粉和蔗糖 用水区分:蔗糖能溶于水,面粉不能溶于水
黄金和假黄金(铜锌合金) 加入盐酸:有气泡冒出的是_______,反之为______灼烧:有黑色物质生成的是________,反之为______
纯金属及其 合金 相互刻画:有明显划痕的为_______,反之为______
假黄金
黄金
假黄金
黄金
纯金属
合金
物质 鉴别方法
软水和硬水 加肥皂水,振荡:产生泡沫多、浮渣少的是____水,反之为____水
天然纤维和合成纤维 点燃闻气味:有烧焦羽毛气味且燃烧后的灰烬为黑褐色小球,易碎的是丝或毛;有烧纸气味,灰烬为灰色,细而软的是棉或麻;有特殊气味,灰烬为黑色或褐色硬块,且捏不碎的是合成纤维
化肥 观察颜色:灰白色的是_____;加熟石灰研磨:有刺激性气味的气体放出的是_________
软
硬
磷肥
铵态氮肥
三、物质的除杂
1. 除杂的一般原则
主不减 被提纯的物质不能和加入的试剂反应
杂不增 不能引入新的杂质
易分离 使被提纯的物质和杂质转化为不同状态(固、液、气),易于分离
2. 气体和固体除杂
(1)常见的气体除杂
物质(杂质) 除杂试剂和方法
O2(H2O) 通过浓硫酸
CO(CO2) 先通过_________溶液,再通过浓硫酸
CO2(CO) 通过灼热的氧化铜
CO2(O2) 通过灼热的铜网
CO2(H2) 先通过灼热的______,再通过_______
CO2(HCl) 先通过______________溶液,再通过_______
N2(O2) 通过灼热的铜网
氢氧化钠
CuO
浓硫酸
饱和碳酸氢钠
浓硫酸
(2)常见的固体除杂
物质(杂质) 除杂试剂和方法
Cu(Fe) 加入足量_________________,过滤、洗涤、干燥;或用磁铁吸引
Cu(CuO) 加入足量________________,过滤、洗涤、干燥
CuO(Cu) 通入足量______并加热
CaCO3(CaO) 加入足量的____,过滤、洗涤、干燥
CaO(CaCO3) __________
Ca(OH)2(CaO) 加入足量____,蒸发
稀盐酸(或稀硫酸)
稀硫酸(或稀盐酸)
氧气
水
高温煅烧
水
物质(杂质) 除杂试剂和方法
KCl(KClO3) 加少量_________,充分加热,再加水溶解、过滤、蒸发结晶
MnO2(KCl) 加足量的____溶解、过滤、洗涤、干燥
NaCl(泥沙) 加入足量的____溶解、过滤、蒸发结晶
二氧化锰
水
水
3. 溶液除杂(1)除杂方法
步骤 举例
第一步:对比,找出杂质离子和非杂质离子; 第二步:找出与杂质离子不共存且不引入新杂质的离子,确定除杂 试剂 如:除去NaCl中的Na2CO3
(2)常见的溶液除杂
物质(杂质) 杂质离子 除杂试剂(写化学式)
NaOH溶液(Na2CO3) ______ ____________________
NaCl溶液(Na2SO4) ______ _______
NaCl溶液(NaOH) ______ ______
NaOH溶液[Ca(OH)2] ______ ________
CaCl2溶液(HCl) ______ ________
NaNO3溶液(CuSO4) ___________ _________
FeSO4溶液(CuSO4) ______ ____
Ca(OH)2[或Ba(OH)2]
BaCl2
OH-
HCl
Ca2+
Na2CO3
H+
CaCO3
Cu2+ 、
Ba(OH)2
Cu2+
Fe
四、物质的分离
原理 运用物理或化学方法把混合物里的几种物质分开,并使其恢复原状态
分离方法 物理方法 过滤法:分离不溶于水的固体和液体或可溶性固体与不溶性固体组成的混合物,如分离二氧化锰和氯酸钾的固体混合物,操作如下:
分离方法 物理方法 蒸馏法:分离沸点相差较大的液体混合物,如石油的分馏
磁铁吸引法:分离具有铁磁性和不具有铁磁性的物质,如分离碳粉和铁粉
分离方法 化学方法 针对使用物理方法不能分离的物质,可利用化学反应进行分离,如分离MgCl2固体和NaCl固体,操作如下:
1.下列鉴别氧气、空气、二氧化碳、纯净氢气的方法中最简便易行的是
( )
A. 闻气味 B. 用燃着的木条
C. 用带火星的木条 D. 用澄清的石灰水
B
2.检验溶液中存在的物质,下列判断正确的是( )
A. 向溶液中加入AgNO3溶液有白色沉淀生成,证明溶液中一定有Cl-
B. 向溶液中加入氢氧化铜,固体消失,溶液变为蓝色,说明溶液中一定有H+
C. 向溶液中加入BaCl2溶液有白色沉淀生成,再加稀硝酸,沉淀不溶解,证明溶液中一定有
D. 向溶液中加入MgSO4溶液有白色沉淀生成,证明溶液中一定有OH-
B
3.(2021哈尔滨改编)鉴别下列各组物质的方法正确的是( )
选项 需区分的物质 方法
A 硝酸铵和硝酸钾 加水搅拌,看是否溶解
B 氯化铵和氯化钾 加入氢氧化钙研磨闻气味
C 硬水和软水 尝味道
D 二氧化锰粉末和木炭粉 观察颜色
B
4. 下列除杂方法中,不正确的是( )
选项 物质(括号内为杂质) 除杂方法
A N2(O2) 通过灼热的铜网
B CaO(CaCO3) 高温煅烧
C NaCl溶液(Na2CO3) 加入过量稀盐酸
D CO2(水蒸气) 通过浓硫酸
C
5. 为了除去物质内的杂质,需选用适当的试剂,其中正确的是( )
选项 物质(括号内为杂质) 选用试剂
A C(Zn) 盐酸
B CaCl2溶液(HCl) Ba(OH)2溶液
C CO2(CO) NaOH溶液
D NaOH溶液[Ca(OH)2] K2CO3溶液
A
6.下面关于物质的分离方法不正确的是_____(填字母序号)。
A. 分离糖水中的糖可以用蒸发水的方法
B. 依次用水溶解、过滤、洗涤、蒸发、烘干,可分离MnO2和KCl
C. 依次通过溶解、过滤、蒸发,可分离硝酸钠和碳酸钾
C
考向1 物质的检验与鉴别
1. 下列各组物质用稀硫酸不能完全区分开的是( )
A. 镁粉、氧化铜粉、木炭粉
B. NaOH溶液、Ba(OH)2溶液、KOH溶液
C. Na2CO3溶液、NaCl溶液、BaCl2溶液
D. 铝片、铁片、银片
B
2.区分下列同类物质的两种方案均正确的是
( )
选项 样品物质 方案一 方案二
A 铝片与锌片 加稀盐酸 观察颜色
B 稀盐酸与稀硫酸 加酚酞溶液 加BaCl2溶液
C NaCl与NH4NO3 加水溶解后测溶液温度 加熟石灰混合研磨
D Ca(OH)2溶液与Ba(OH)2溶液 通入CO2 加K2CO3溶液
C
3.按如图所示装置,持续通入气态物质X,可以看到玻璃管中有红色物质生成,无水CuSO4变蓝,澄清石灰水变浑浊,则X不可能是
( )
A
A. 氢气和水蒸气
B. 氢气和二氧化碳
C. 一氧化碳和氢气
D. 一氧化碳和水蒸气
(提示:无水CuSO4遇水变蓝色)
4.(2021铁一中一模)下列各组物质需要借助其它试剂才可以鉴别的是
( )
A. Na2CO3溶液、 CaCl2溶液、稀盐酸
B. Ca(OH)2溶液、稀盐酸、NaCl溶液
C. CuSO4溶液、NaOH溶液、NaCl溶液
D. (NH4)2CO3溶液、Ca(OH)2溶液、稀盐酸
B
5.(2021天津)现有A~F六瓶失去标签的溶液,分别为澄清石灰水、硫酸铁溶液、碳酸钠溶液、稀盐酸、溶质质量分数为10%的氢氧化钠溶液和10%的氢氧化钾溶液。已知硫酸钠、硫酸钾溶液呈中性。
某同学进行实验如下:
(1)从外观上观察,F呈黄色,则F为____________。
(2)从剩余的五瓶溶液中各取少量溶液两两混合,可以观察到:A+D→白色沉淀,C+D→无色气体,其余无明显现象。则这五种溶液两两混合可发生_______个反应,C为_______,A与D反应的化学方程式为_____________________________________。
硫酸铁溶液
5(或五)
稀盐酸
Na2CO3+Ca(OH)2===CaCO3↓+2NaOH
(3)取未鉴别出的B、E溶液各20 g于两个烧杯中,分别滴加两滴酚酞溶液,再分别加入10%的稀硫酸17.5 g(如图所示),并不断搅拌。观察到B溶液由红色变为无色,E溶液仍为红色。则E为_______(填化学式)溶液。
(4)将六瓶溶液贴上标签。
NaOH
考向2 物质的除杂与分离
6.(2021梧州)下列除杂质的方法正确的是( )
选项 物质 杂质(少量) 除杂质的方法
A N2 CO 通入足量的水中
B Al粉 Ag粉 加入适量稀H2SO4,充分反应后过滤
C CaCO3 KCl 加水溶解、过滤、洗涤、干燥
D FeCl2 FeCl3 加入适量KOH溶液,充分反应后过滤
C
7.下列实验方案设计不合理的是( )
A. 从高锰酸钾制氧气的残余物中分离出MnO2,加水溶解、过滤、洗涤、干燥
B. 除去FeCl2溶液中混有的少量CuCl2,加过量铁粉,过滤
C. 除去铁钉表面的铁锈,加入过量稀盐酸
D. 除去水中的色素可以用活性炭吸附
C
8.下图是将潮湿空气中的氧气、二氧化碳、水蒸气分别除去的流程图:
请根据你所确定的除杂方案,将使用的试剂名称填写在横线上:
A为______________;B为_________;C为_____。
氢氧化钠溶液
浓硫酸
铜粉
综合类
9. 下列实验方案能达到实验目的的是( )
选项 实验目的 实验方案
A 除去CO2中少量的CO 通入O2并点燃
B 检验甲烷中含有碳、氢元素 点燃后在火焰上方罩内壁涂有澄清石灰水的烧杯
C 鉴别二氧化锰和活性炭粉 取样,加入过氧化氢溶液
D 分离硝酸钾和氯化钠的固体混合物 加水溶解后,蒸发结晶
C
10. 依据下列各组实验现象,得出的结论正确的是( )
选项 实验现象 实验结论
A 向某无色溶液中加入Ba(NO3)2溶液和稀盐酸,产生白色沉淀 无色溶液中一定含有SO
B 将燃着的木条分别伸入三瓶无色气体中 木条熄灭的是二氧化碳,燃烧更剧烈的是氧气,无明显变化的是空气
选项 实验现象 实验结论
C 将表面积相同的甲、乙两种金属片分别放入质量分数相同的稀盐酸中,甲表面生成气泡的速率比乙快 金属活动性顺序:甲>乙
D 将某固体与熟石灰混合后研磨,产生有刺激性气味的气体 该固体一定是NH4Cl
答案:C
11.(2021盐城)下列实验方案能达到实验目的的是( )
选项 实验目的 实验方案
A 检验酒精中是否含有氧元素 在空气中点燃,检验生成物
B 除去KCl溶液中的MgCl2 滴加适量Ba(OH)2溶液
C 鉴别固体NaOH与NH4NO3 取样,分别溶于水中,观察溶液温度变化
D 分离Cu粉和Fe粉的混合物 加入足量的稀硫酸,过滤、洗涤、干燥
C
12. (2021宁夏改编)下列实验操作能达到实验目的的是(括号内为杂质)
( )
选项 物质 目的 主要实验操作
A CH4、CO、N2 检验 将燃着的木条分别伸入集气瓶中
B 稀H2SO4、Ca(OH)2溶液、NaNO3溶液 鉴别 取样,滴加碳酸钠溶液
C NaNO3、NaCl 分离 取样,加水溶解,蒸发结晶
D Fe(Fe2O3) 除杂 取样,加入稀盐酸,过滤
B
13.(2021广东)鉴别、除杂是重要的实验技能。下列实验设计能达到实验目的的是( )
选项 实验目的 实验设计
A 去除铁粉中的碳粉 在足量的氧气中灼烧
B 鉴别CO与H2 分别点燃,观察火焰颜色
C 去除粗盐中难溶性杂质 溶解、过滤、蒸发
D 鉴别BaCl2溶液与Ba(NO3)2溶液 分别滴加稀硫酸
C
2022年化学中考备考复习专题突破
《 物质的检验与鉴别、除杂与分离》精讲课件(三)
真题·练讲克重点
2
1
立足教材“过”考点
一、物质的检验
1. 常见气体的检验
气体 检验方法 实验现象
O2(氧气) 将_______的木条伸入集气瓶内 木条______
CO2(二氧化碳) 通入澄清石灰水中 _________________
带火星
复燃
澄清石灰水变浑浊
气体 检验方法 实验现象
H2(氢气) 点燃,在火焰上方罩一干冷的烧杯,迅速倒转后,注入少量澄清石灰水 产生蓝色火焰,烧杯内壁有水珠,澄清石灰水__________
CH4(甲烷) 产生蓝色火焰,烧杯内壁有水珠,澄清石灰水________
CO(一氧化碳) 产生蓝色火焰,烧杯内壁没有水珠,澄清石灰水_______
NH3(氨气) 将湿润的红色石蕊试纸放在试管口 红色石蕊试纸变____
不变浑浊
变浑浊
变浑浊
蓝
气体 检验方法 实验现象
H2O(水蒸气) 通过无水硫酸铜粉末 白色粉末变____
HCl(氯化氢) 通入硝酸银溶液 有_________产生
蓝
白色沉淀
2. 常见离子的检验
离子 检验方法 实验现象
H+ 取少量试剂滴加紫色石蕊溶液 紫色石蕊溶液变____
用玻璃棒蘸取少量试剂滴在pH试纸上,与标准比色卡对照 常温下,pH_____(填“<”“>”或“=”)7
取少量试剂加入锌粉等活泼金属 有______产生
取少量试剂加入碳酸盐 有______产生
取少量试剂加入氢氧化镁等难溶性碱 固体消失
红
<
气泡
气泡
离子 检验方法 实验现象
H+ 取少量试剂加入氧化铁或氧化铜等金属氧化物 固体消失,溶液变为黄色或蓝色
OH- 取少量试剂滴加紫色石蕊溶液 紫色石蕊溶液变____
取少量试剂滴加无色酚酞溶液 无色酚酞溶液变____
用玻璃棒蘸取少量试剂滴在pH试纸上,与标准比色卡对照 常温下,pH____(填“>”“<”或“=”)7
取少量试剂加入含Cu2+或Fe3+或Mg2+的盐溶液 有____________________
_____生成
蓝
红
>
蓝色或红褐色或白色
沉淀
离子 检验方法 实验现象
Cl- 取少量试剂滴加少量___________和稀HNO3 有_________生成
(硫酸盐) 先滴加稀盐酸酸化,再滴加BaCl2溶液 酸化无现象,滴入BaCl2溶液_______________
(碳酸盐) 取少量试剂滴加________,并将产生的气体通入澄清石灰水中 有气泡产生,澄清石灰水变浑浊
(铵盐) 取少量试剂加入可溶性碱,加热,将湿润的红色石蕊试纸放在试管口 产生有刺激性气味的气体,红色石蕊试纸变____
AgNO3溶液
白色沉淀
有白色沉淀生成
稀盐酸
蓝
离子 检验方法 实验现象
Fe3+ 滴加NaOH溶液 ________________
Cu2+ 插入铁片 ____________________________________
滴加NaOH溶液 ______________
产生红褐色沉淀
铁片上有红色固体析出,溶液蓝色变浅
产生蓝色沉淀
二、物质的鉴别
1. 鉴别方法
(1)物理方法
颜色 溶液:如CuSO4溶液呈____色;FeCl3溶液呈____色;FeCl2溶液呈______色
固体:Cu为紫红色;Fe2O3为红棕色;CuO、炭粉、MnO2、铁粉为____色
气味 如SO2、NH3、HCl有刺激性气味
蓝
黄
浅绿
黑
溶解性 如CaCO3不溶于水,NaCl易溶于水,故可用水鉴别CaCO3和NaCl
溶解时的吸放热现象 如NaOH固体溶于水,溶液温度______;NH4NO3固体溶于水,溶液温度______,故可用水鉴别NaOH和NH4NO3固体
升高
降低
(2)化学方法
Ⅰ.加试剂鉴别:选择一种或多种试剂,分别加入到待测物质中根据不同的现象鉴别。
【即时练习】
a.鉴别稀盐酸、CaCl2溶液与NaOH溶液可分别加入紫色石蕊溶液,观察到__________的是稀盐酸,____________的是CaCl2溶液,_________的是NaOH溶液。
溶液变红
溶液不变色
溶液变蓝
b.鉴别稀盐酸、CaCl2溶液与NaOH溶液可分别加入碳酸钠溶液,观察到____________的是稀盐酸,_______________的是CaCl2溶液,________
_____的是NaOH溶液。
c.鉴别Na2CO3溶液、NaCl溶液和AgNO3溶液可分别加入稀盐酸,观察到____________的是Na2CO3溶液,____________的是NaCl溶液,____
_____________的是AgNO3溶液。
有气泡产生
有白色沉淀产生
现象
有气泡产生
无明显现象
白色沉淀产生
无明显
有
Ⅱ.无试剂鉴别
①特征现象法:首先鉴别出有颜色或有气味的物质,再利用已经鉴别出来的物质去鉴别其他物质,以此类推,从而将各物质一一鉴别出来。
如鉴别CuSO4、NaOH、NH4NO3固体:加水溶解,观察发现,只有CuSO4溶液为蓝色,其余均为无色,然后以CuSO4溶液为已知试剂来鉴别另外两种物质,鉴别顺序为CuSO4→ NaOH→ NH4NO3。
②两两混合法:当无法从物理性质入手时,采用两两混合的方法,根据与组内其他物质反应产生各种现象的不同组合,从而将四种物质鉴别出来。
如Na2SO4、Na2CO3、BaCl2、HCl,用两两混合反应的方法分析,可采用列表的方法统计现象,见下表:
(注:-表示不反应,↓表示有沉淀生成,↑表示有气体生成)
Na2SO4 Na2CO3 BaCl2 HCl
Na2SO4 - ↓ -
Na2CO3 - ↓ ↑
BaCl2 ↓ ↓ -
HCl - ↑ -
2. 常见物质的鉴别
物质 鉴别方法
面粉和蔗糖 用水区分:蔗糖能溶于水,面粉不能溶于水
黄金和假黄金(铜锌合金) 加入盐酸:有气泡冒出的是_______,反之为______灼烧:有黑色物质生成的是________,反之为______
纯金属及其 合金 相互刻画:有明显划痕的为_______,反之为______
假黄金
黄金
假黄金
黄金
纯金属
合金
物质 鉴别方法
软水和硬水 加肥皂水,振荡:产生泡沫多、浮渣少的是____水,反之为____水
天然纤维和合成纤维 点燃闻气味:有烧焦羽毛气味且燃烧后的灰烬为黑褐色小球,易碎的是丝或毛;有烧纸气味,灰烬为灰色,细而软的是棉或麻;有特殊气味,灰烬为黑色或褐色硬块,且捏不碎的是合成纤维
化肥 观察颜色:灰白色的是_____;加熟石灰研磨:有刺激性气味的气体放出的是_________
软
硬
磷肥
铵态氮肥
三、物质的除杂
1. 除杂的一般原则
主不减 被提纯的物质不能和加入的试剂反应
杂不增 不能引入新的杂质
易分离 使被提纯的物质和杂质转化为不同状态(固、液、气),易于分离
2. 气体和固体除杂
(1)常见的气体除杂
物质(杂质) 除杂试剂和方法
O2(H2O) 通过浓硫酸
CO(CO2) 先通过_________溶液,再通过浓硫酸
CO2(CO) 通过灼热的氧化铜
CO2(O2) 通过灼热的铜网
CO2(H2) 先通过灼热的______,再通过_______
CO2(HCl) 先通过______________溶液,再通过_______
N2(O2) 通过灼热的铜网
氢氧化钠
CuO
浓硫酸
饱和碳酸氢钠
浓硫酸
(2)常见的固体除杂
物质(杂质) 除杂试剂和方法
Cu(Fe) 加入足量_________________,过滤、洗涤、干燥;或用磁铁吸引
Cu(CuO) 加入足量________________,过滤、洗涤、干燥
CuO(Cu) 通入足量______并加热
CaCO3(CaO) 加入足量的____,过滤、洗涤、干燥
CaO(CaCO3) __________
Ca(OH)2(CaO) 加入足量____,蒸发
稀盐酸(或稀硫酸)
稀硫酸(或稀盐酸)
氧气
水
高温煅烧
水
物质(杂质) 除杂试剂和方法
KCl(KClO3) 加少量_________,充分加热,再加水溶解、过滤、蒸发结晶
MnO2(KCl) 加足量的____溶解、过滤、洗涤、干燥
NaCl(泥沙) 加入足量的____溶解、过滤、蒸发结晶
二氧化锰
水
水
3. 溶液除杂(1)除杂方法
步骤 举例
第一步:对比,找出杂质离子和非杂质离子; 第二步:找出与杂质离子不共存且不引入新杂质的离子,确定除杂 试剂 如:除去NaCl中的Na2CO3
(2)常见的溶液除杂
物质(杂质) 杂质离子 除杂试剂(写化学式)
NaOH溶液(Na2CO3) ______ ____________________
NaCl溶液(Na2SO4) ______ _______
NaCl溶液(NaOH) ______ ______
NaOH溶液[Ca(OH)2] ______ ________
CaCl2溶液(HCl) ______ ________
NaNO3溶液(CuSO4) ___________ _________
FeSO4溶液(CuSO4) ______ ____
Ca(OH)2[或Ba(OH)2]
BaCl2
OH-
HCl
Ca2+
Na2CO3
H+
CaCO3
Cu2+ 、
Ba(OH)2
Cu2+
Fe
四、物质的分离
原理 运用物理或化学方法把混合物里的几种物质分开,并使其恢复原状态
分离方法 物理方法 过滤法:分离不溶于水的固体和液体或可溶性固体与不溶性固体组成的混合物,如分离二氧化锰和氯酸钾的固体混合物,操作如下:
分离方法 物理方法 蒸馏法:分离沸点相差较大的液体混合物,如石油的分馏
磁铁吸引法:分离具有铁磁性和不具有铁磁性的物质,如分离碳粉和铁粉
分离方法 化学方法 针对使用物理方法不能分离的物质,可利用化学反应进行分离,如分离MgCl2固体和NaCl固体,操作如下:
1.下列鉴别氧气、空气、二氧化碳、纯净氢气的方法中最简便易行的是
( )
A. 闻气味 B. 用燃着的木条
C. 用带火星的木条 D. 用澄清的石灰水
B
2.检验溶液中存在的物质,下列判断正确的是( )
A. 向溶液中加入AgNO3溶液有白色沉淀生成,证明溶液中一定有Cl-
B. 向溶液中加入氢氧化铜,固体消失,溶液变为蓝色,说明溶液中一定有H+
C. 向溶液中加入BaCl2溶液有白色沉淀生成,再加稀硝酸,沉淀不溶解,证明溶液中一定有
D. 向溶液中加入MgSO4溶液有白色沉淀生成,证明溶液中一定有OH-
B
3.(2021哈尔滨改编)鉴别下列各组物质的方法正确的是( )
选项 需区分的物质 方法
A 硝酸铵和硝酸钾 加水搅拌,看是否溶解
B 氯化铵和氯化钾 加入氢氧化钙研磨闻气味
C 硬水和软水 尝味道
D 二氧化锰粉末和木炭粉 观察颜色
B
4. 下列除杂方法中,不正确的是( )
选项 物质(括号内为杂质) 除杂方法
A N2(O2) 通过灼热的铜网
B CaO(CaCO3) 高温煅烧
C NaCl溶液(Na2CO3) 加入过量稀盐酸
D CO2(水蒸气) 通过浓硫酸
C
5. 为了除去物质内的杂质,需选用适当的试剂,其中正确的是( )
选项 物质(括号内为杂质) 选用试剂
A C(Zn) 盐酸
B CaCl2溶液(HCl) Ba(OH)2溶液
C CO2(CO) NaOH溶液
D NaOH溶液[Ca(OH)2] K2CO3溶液
A
6.下面关于物质的分离方法不正确的是_____(填字母序号)。
A. 分离糖水中的糖可以用蒸发水的方法
B. 依次用水溶解、过滤、洗涤、蒸发、烘干,可分离MnO2和KCl
C. 依次通过溶解、过滤、蒸发,可分离硝酸钠和碳酸钾
C
考向1 物质的检验与鉴别
1. 下列各组物质用稀硫酸不能完全区分开的是( )
A. 镁粉、氧化铜粉、木炭粉
B. NaOH溶液、Ba(OH)2溶液、KOH溶液
C. Na2CO3溶液、NaCl溶液、BaCl2溶液
D. 铝片、铁片、银片
B
2.区分下列同类物质的两种方案均正确的是
( )
选项 样品物质 方案一 方案二
A 铝片与锌片 加稀盐酸 观察颜色
B 稀盐酸与稀硫酸 加酚酞溶液 加BaCl2溶液
C NaCl与NH4NO3 加水溶解后测溶液温度 加熟石灰混合研磨
D Ca(OH)2溶液与Ba(OH)2溶液 通入CO2 加K2CO3溶液
C
3.按如图所示装置,持续通入气态物质X,可以看到玻璃管中有红色物质生成,无水CuSO4变蓝,澄清石灰水变浑浊,则X不可能是
( )
A
A. 氢气和水蒸气
B. 氢气和二氧化碳
C. 一氧化碳和氢气
D. 一氧化碳和水蒸气
(提示:无水CuSO4遇水变蓝色)
4.(2021铁一中一模)下列各组物质需要借助其它试剂才可以鉴别的是
( )
A. Na2CO3溶液、 CaCl2溶液、稀盐酸
B. Ca(OH)2溶液、稀盐酸、NaCl溶液
C. CuSO4溶液、NaOH溶液、NaCl溶液
D. (NH4)2CO3溶液、Ca(OH)2溶液、稀盐酸
B
5.(2021天津)现有A~F六瓶失去标签的溶液,分别为澄清石灰水、硫酸铁溶液、碳酸钠溶液、稀盐酸、溶质质量分数为10%的氢氧化钠溶液和10%的氢氧化钾溶液。已知硫酸钠、硫酸钾溶液呈中性。
某同学进行实验如下:
(1)从外观上观察,F呈黄色,则F为____________。
(2)从剩余的五瓶溶液中各取少量溶液两两混合,可以观察到:A+D→白色沉淀,C+D→无色气体,其余无明显现象。则这五种溶液两两混合可发生_______个反应,C为_______,A与D反应的化学方程式为_____________________________________。
硫酸铁溶液
5(或五)
稀盐酸
Na2CO3+Ca(OH)2===CaCO3↓+2NaOH
(3)取未鉴别出的B、E溶液各20 g于两个烧杯中,分别滴加两滴酚酞溶液,再分别加入10%的稀硫酸17.5 g(如图所示),并不断搅拌。观察到B溶液由红色变为无色,E溶液仍为红色。则E为_______(填化学式)溶液。
(4)将六瓶溶液贴上标签。
NaOH
考向2 物质的除杂与分离
6.(2021梧州)下列除杂质的方法正确的是( )
选项 物质 杂质(少量) 除杂质的方法
A N2 CO 通入足量的水中
B Al粉 Ag粉 加入适量稀H2SO4,充分反应后过滤
C CaCO3 KCl 加水溶解、过滤、洗涤、干燥
D FeCl2 FeCl3 加入适量KOH溶液,充分反应后过滤
C
7.下列实验方案设计不合理的是( )
A. 从高锰酸钾制氧气的残余物中分离出MnO2,加水溶解、过滤、洗涤、干燥
B. 除去FeCl2溶液中混有的少量CuCl2,加过量铁粉,过滤
C. 除去铁钉表面的铁锈,加入过量稀盐酸
D. 除去水中的色素可以用活性炭吸附
C
8.下图是将潮湿空气中的氧气、二氧化碳、水蒸气分别除去的流程图:
请根据你所确定的除杂方案,将使用的试剂名称填写在横线上:
A为______________;B为_________;C为_____。
氢氧化钠溶液
浓硫酸
铜粉
综合类
9. 下列实验方案能达到实验目的的是( )
选项 实验目的 实验方案
A 除去CO2中少量的CO 通入O2并点燃
B 检验甲烷中含有碳、氢元素 点燃后在火焰上方罩内壁涂有澄清石灰水的烧杯
C 鉴别二氧化锰和活性炭粉 取样,加入过氧化氢溶液
D 分离硝酸钾和氯化钠的固体混合物 加水溶解后,蒸发结晶
C
10. 依据下列各组实验现象,得出的结论正确的是( )
选项 实验现象 实验结论
A 向某无色溶液中加入Ba(NO3)2溶液和稀盐酸,产生白色沉淀 无色溶液中一定含有SO
B 将燃着的木条分别伸入三瓶无色气体中 木条熄灭的是二氧化碳,燃烧更剧烈的是氧气,无明显变化的是空气
选项 实验现象 实验结论
C 将表面积相同的甲、乙两种金属片分别放入质量分数相同的稀盐酸中,甲表面生成气泡的速率比乙快 金属活动性顺序:甲>乙
D 将某固体与熟石灰混合后研磨,产生有刺激性气味的气体 该固体一定是NH4Cl
答案:C
11.(2021盐城)下列实验方案能达到实验目的的是( )
选项 实验目的 实验方案
A 检验酒精中是否含有氧元素 在空气中点燃,检验生成物
B 除去KCl溶液中的MgCl2 滴加适量Ba(OH)2溶液
C 鉴别固体NaOH与NH4NO3 取样,分别溶于水中,观察溶液温度变化
D 分离Cu粉和Fe粉的混合物 加入足量的稀硫酸,过滤、洗涤、干燥
C
12. (2021宁夏改编)下列实验操作能达到实验目的的是(括号内为杂质)
( )
选项 物质 目的 主要实验操作
A CH4、CO、N2 检验 将燃着的木条分别伸入集气瓶中
B 稀H2SO4、Ca(OH)2溶液、NaNO3溶液 鉴别 取样,滴加碳酸钠溶液
C NaNO3、NaCl 分离 取样,加水溶解,蒸发结晶
D Fe(Fe2O3) 除杂 取样,加入稀盐酸,过滤
B
13.(2021广东)鉴别、除杂是重要的实验技能。下列实验设计能达到实验目的的是( )
选项 实验目的 实验设计
A 去除铁粉中的碳粉 在足量的氧气中灼烧
B 鉴别CO与H2 分别点燃,观察火焰颜色
C 去除粗盐中难溶性杂质 溶解、过滤、蒸发
D 鉴别BaCl2溶液与Ba(NO3)2溶液 分别滴加稀硫酸
C
同课章节目录
