2022年化学中考备考复习专题突破 《 物质的检验与鉴别、除杂与分离》精讲课件(五)(课件41页)
文档属性
| 名称 | 2022年化学中考备考复习专题突破 《 物质的检验与鉴别、除杂与分离》精讲课件(五)(课件41页) |  | |
| 格式 | zip | ||
| 文件大小 | 470.6KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-25 11:16:26 | ||
图片预览







文档简介
(共41张PPT)
2022年化学中考备考复习专题突破
《 物质的检验与鉴别、除杂与分离》
精讲课件(五)
一、物质的检验
1.常见气体的检验
离子 方法 现象
H+ 滴加酸碱指示剂,如__________ _____ 溶液变红
用pH试纸测其pH pH<7
加入较活泼金属,如___________ 有气泡产生
加入碳酸盐如碳酸钠 有气泡产生
加入金属氧化物,如氧化铜 ____________________
锌(合理即可)
固体溶解,溶液变蓝
紫色石蕊溶液
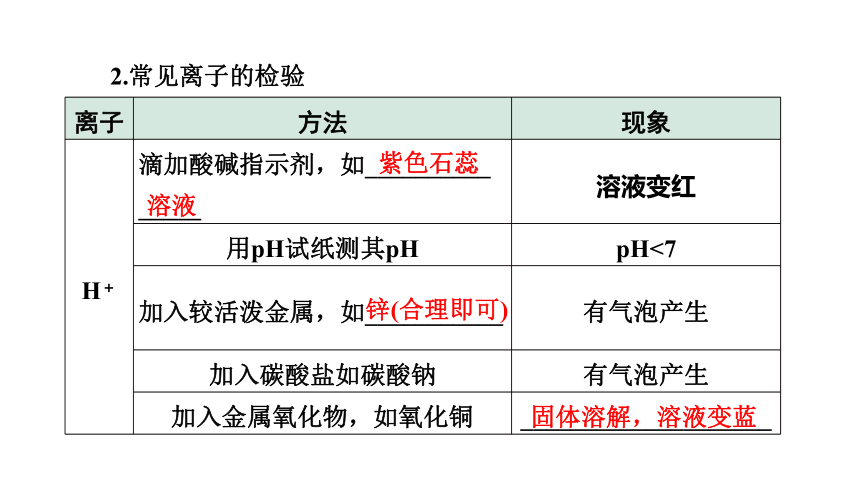
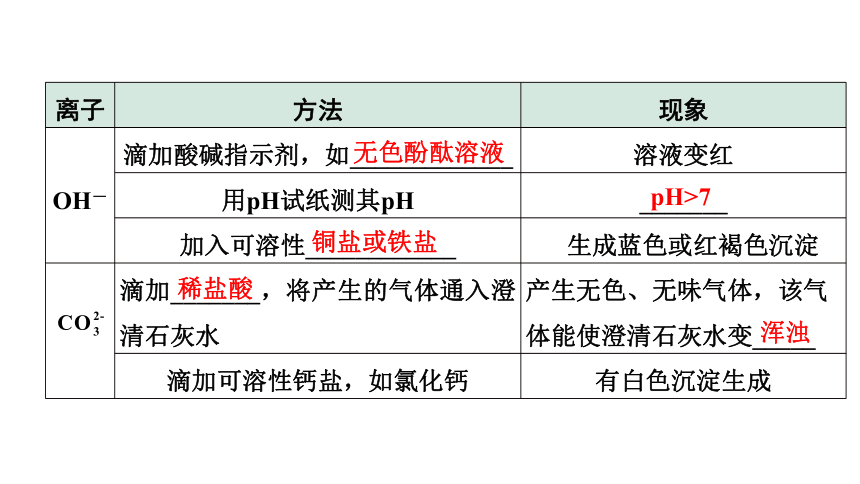
2.常见离子的检验
离子 方法 现象
OH- 滴加酸碱指示剂,如_____________ 溶液变红
用pH试纸测其pH _______
加入可溶性____________ 生成蓝色或红褐色沉淀
滴加_______,将产生的气体通入澄清石灰水 产生无色、无味气体,该气体能使澄清石灰水变_____
滴加可溶性钙盐,如氯化钙 有白色沉淀生成
无色酚酞溶液
pH>7
铜盐或铁盐
稀盐酸
浑浊
离子 方法 现象
铵盐与______研磨 产生有刺激性气味的气体
加入强碱溶液,加热,用湿润的红色石蕊试纸检验产生的气体 产生有刺激性气味的气体,试纸_____
若是碳酸氢铵固体,直接加热,用湿润的酚酞试纸检验产生的气体 固体减少,酚酞试纸变红
熟石灰
变蓝
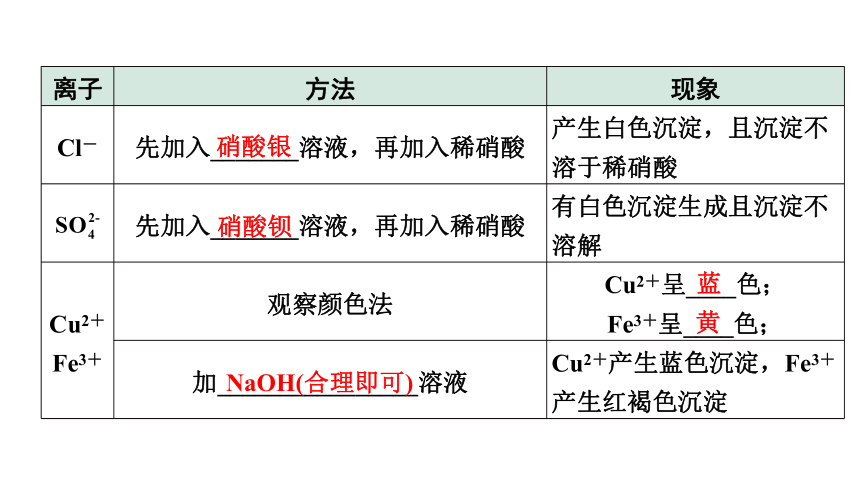
离子 方法 现象
Cl- 先加入_______溶液,再加入稀硝酸 产生白色沉淀,且沉淀不溶于稀硝酸
先加入_______溶液,再加入稀硝酸 有白色沉淀生成且沉淀不溶解
Cu2+ Fe3+ 观察颜色法 Cu2+呈____色;
Fe3+呈____色;
加________________溶液 Cu2+产生蓝色沉淀,Fe3+产生红褐色沉淀
硝酸银
硝酸钡
NaOH(合理即可)
蓝
黄
1. 下列检验气体的方法正确的是( )
A. 检验二氧化碳气体可以用燃着的木条
B. 检验氧气是否集满,将带火星的木条放在集气瓶瓶口
C. 检验一氧化碳时,只需通过灼热的氧化铜固体
D. 检验甲烷中含有碳、氢元素,可以将气体点燃,在火焰上方罩内壁附着澄清石灰水的烧杯
B
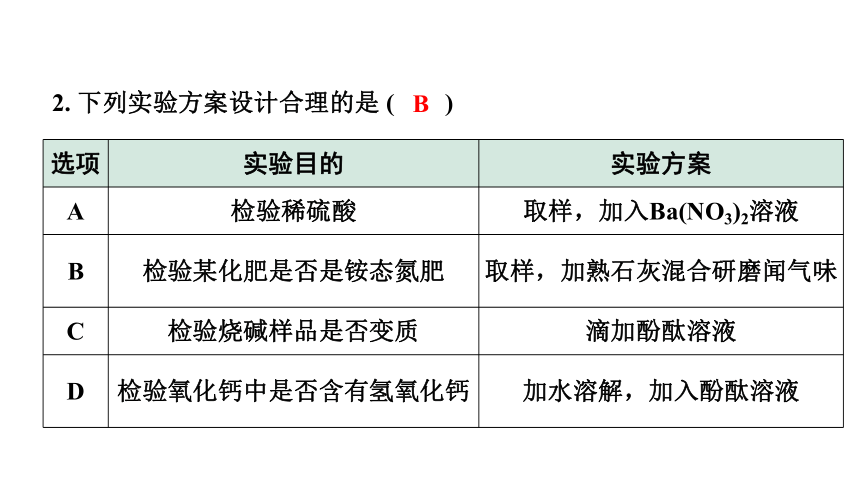
2. 下列实验方案设计合理的是 ( )
选项 实验目的 实验方案
A 检验稀硫酸 取样,加入Ba(NO3)2溶液
B 检验某化肥是否是铵态氮肥 取样,加熟石灰混合研磨闻气味
C 检验烧碱样品是否变质 滴加酚酞溶液
D 检验氧化钙中是否含有氢氧化钙 加水溶解,加入酚酞溶液
B
二、物质的鉴别
考向1 用物理方法区分
方法指导
依据特殊的物理性质(如颜色、气味、溶解现象、磁性等)进行观察分析、区分物质。
3.下列各组物质的鉴别方法错误的是( )
A. CaCl2、CaCO3:加水,观察能否被水溶解
B. CaO、NH4NO3:向分别装有两种药品的烧杯中加水,用手触摸烧杯外壁
C. 浓H2SO4、 稀H2SO4:打开瓶盖,观察是否有白雾
D. 铁粉、石墨粉:分别用磁铁吸引
C
考向2 用化学方法区分
通过化学反应,观察反应现象(如燃烧、产生气泡、沉淀、放热、变色等),根据现象分析得出结论。
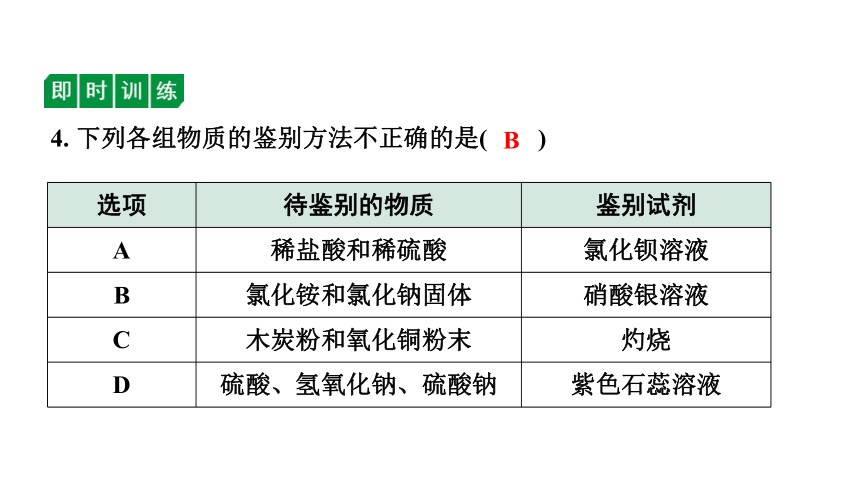
4. 下列各组物质的鉴别方法不正确的是( )
选项 待鉴别的物质 鉴别试剂
A 稀盐酸和稀硫酸 氯化钡溶液
B 氯化铵和氯化钠固体 硝酸银溶液
C 木炭粉和氧化铜粉末 灼烧
D 硫酸、氢氧化钠、硫酸钠 紫色石蕊溶液
B
考向3 几种常见物质鉴别(自选试剂)
选择试剂时,实验现象要明显、实验方法要简便(优先物理方法、后化学方法),通过是否有特殊现象来区分。
5. 请选择试剂鉴别下列物质,并简述其鉴别方法(现象、结论)。
(1)硬水和软水:选择试剂_______;现象及结论_____________________
___________________________________________。
(2)黄铜和纯铜:选择试剂或方法________;现象及结论______________
_________________。
(3)羊毛、棉花和合成纤维:选择方法_____________;现象及结论____________________________________________________________________________________________。
肥皂水
产生泡沫较多、浮渣较
少的是软水,产生泡沫较少、浮渣较多的是硬水
相互刻画
有明显划痕的为
纯铜,反之为黄铜
灼烧,闻气味
有烧焦羽毛气味的是羊毛;有烧纸气味的是棉花;有特殊气味,产物是黑色硬球且捏不碎的是合成纤维
(4)二氧化锰和氧化铜:选择试剂________________;现象及结论_________________________________________________________。
(5)白醋和白酒:选择方法_______;现象及结论______________________
________________。
(6) 氮肥、钾肥和磷肥:
①看外观:现象及结论_______________________________________;
②加水溶解,磷肥大多不溶于水或部分溶于水,氮肥和钾肥全部溶于水;
③加_______研磨,现象及结论______________________________。
闻气味
有刺激性气味的是白醋,
有醇香味的是白酒
氮肥、钾肥都是白色晶体;磷肥是灰白色粉
熟石灰
有刺激性气味放出的是铵态氮肥
稀盐酸(合理即可)
无明显现象的是二氧化锰;固体溶解、溶液变为蓝色的是氧化铜
1. (河南真题组合)下列区分物质的方法或试剂不正确的是( )
A. 用带火星的木条区分氧气和氮气(2018河南10A)
B. 用肥皂水区分硬水、软水(2019河南12B)
C. 用酚酞溶液区分硫酸和硫酸钠溶液(2018河南10C)
D. 用水区分硝酸铵、氢氧化钠(2019河南12D)
C
2. 有三瓶无色溶液分别是盐酸、石灰水、水,用下列试剂能把它们区分开的是( )
A. 酚酞溶液 B. 镁条 C. CuO粉末 D. 石蕊溶液
3. 下列鉴别物质所用的方法中,不正确的是( )
A. 水和过氧化氢溶液——加二氧化锰
B. 区分纯金属与其组成的合金——相互刻画
C. 硫酸和硫酸钠溶液——加硝酸钡溶液
D. 一氧化碳和二氧化碳——通入紫色石蕊溶液中
D
C
4. (2021成都)为区分硫酸钾、氯化铵、硫酸铵、磷矿粉四种固体物质,以下方案及结论有误的是( )
A. 观察固体颜色能区分出磷矿粉
B. 取样,加熟石灰研磨闻到氨味的物质有两种
C. 取样,溶解后加硝酸钡溶液能区分出硫酸铵
D. 用水和氢氧化钡溶液能区分出四种物质
C
5. 下列各组物质分别用括号内物质进行鉴别,不能一次性鉴别出来的是
( )
A. NaOH、CaCO3、NaCl三种固体(水)
B. CO2、O2、空气三种气体(带火星的木条)
C. MnO2、铁粉、CuO三种黑色固体(稀硫酸)
D. CuSO4、NaNO3、K2CO3三种溶液(澄清石灰水)
B
6. (2021湖州)某科学兴趣小组在课余时间做了“开门大吉”的游戏,其规则是:每把钥匙代表一种试剂,每扇门代表需要鉴别的两种溶液,见下图。如果钥匙代表的试剂能够鉴别出门上代表的两种溶液,钥匙就能把门打开(每把钥匙只能使用一次),下列能够依次将四扇门打开的钥匙顺序是( )
B
A. ①②③④ B. ④②③① C. ④③②① D. ①③②④
7. (2021郑州一检)有三瓶无色、无味的气体,它们分别是甲烷、氢气和一氧化碳。请设计实验加以鉴别。
答:点燃三种气体,分别用干燥的冷烧杯罩在火焰上方,烧杯壁上没有水珠的是一氧化碳;向烧杯壁上有水珠的两个集气瓶中,分别注入澄清的石灰水,振荡,石灰水变浑浊的是甲烷,不变浑浊的是氢气。(合理即可)
8. (2021眉山改编)化学实验室有失去标签的硝酸钡、碳酸钠、氢氧化钾、稀硫酸、氢氧化钙五瓶无色溶液,现将其任意编号A、B、C、D、E,然后两两混合进行实验,其部分现象如下表(微溶物视为可溶物)。
实验 A+E A+B B+C B+E
现象 产生沉淀 产生沉淀 产生沉淀 产生气体
(1)碳酸钠俗称纯碱,属于___类(填字母)。
A. 酸 B. 碱 C. 盐
(2)写出溶液B中溶质的化学式________。
(3)写出溶液A与E反应的化学方程式。
C
Na2CO3
答:Ba(NO3)2+H2SO4=== BaSO4↓+2HNO3
\
物质的除杂
一、除杂原则
1.主不减:被提纯的物质不能和加入的试剂反应。
2.杂不增:不能引入新的杂质。
3.易分离:使被提纯的物质和杂质转化为不同状态(固、液、气),固体和液体的分离法为过滤。
二、常见物质的除杂
1. 气体的除杂
2. 固体的除杂
(1)当被提纯物质与杂质中只有一种可溶于水或杂质能与水反应时,可选择用水溶解、过滤的方法除杂。
(2)若被提纯物质与杂质均溶于水,可通过加水将其转化为液体除杂,最终通过蒸发结晶或降温结晶得到要提纯物质。
(3)当两种物质都难溶于水时,可根据物质的性质差异选用气体或液体除杂试剂。
常见固体除杂举例:
物质 杂质 试剂、方法
Cu Fe __________________________,过滤、
洗涤、干燥;或用磁铁吸引
Cu CuO 加足量的稀硫酸(或稀盐酸),过滤、洗涤、干燥
KCl MnO2 溶解、过滤、蒸发结晶
NaCl KNO3 溶解、蒸发结晶
CaO CaCO3 __________
加入足量的稀硫酸(或稀盐酸)
高温煅烧
3. 液体的除杂
第一步:对比,找出杂质离子和非杂质离子;
第二步:找出与杂质离子不共存且不引入新杂质的离子,确定除杂试剂。
如:除去NaCl溶液中的Na2CO3如图所示:
【特别提醒】除杂试剂应适量。
物质(杂质) 杂质离子 除杂试剂(写化学式)
NaOH溶液(Na2CO3) ______ ___________________
NaCl溶液(Na2SO4) _____ ______
NaCl溶液(NaOH) _____ ______________
NaOH溶液[Ca(OH)2] _____ _________
CaCl2溶液(HCl) _____ _________
FeSO4溶液(CuSO4) ______ ___
NaNO3溶液(CuSO4) __________ ________
Ca(OH)2[或Ba(OH)2]
BaCl2
OH-
MgCl2(合理即可)
Ca2+
Na2CO3
H+
CaCO3
Cu2+
Fe
Ba(OH)2
Cu2+、
1. 除去下列物质中混有的少量杂质(括号内为杂质),实验方案不可行的是( )
A. CuO粉末(C):在空气中灼烧
B. FeCl2溶液(CuCl2):加过量的铁粉,过滤
C. KOH溶液(K2CO3):加入适量氢氧化钙溶液,过滤
D. H2(HCl):依次通过足量的NaHCO3溶液和浓硫酸
D
2. (2021德阳)在化工生产中通过除杂得到较纯净的产品。以下除杂的实验设计不合理的是( )
选项 物质 杂质 实验设计
A N2 O2 通过灼热的足量铜网,充分反应
B CaO CaCl2 加水充分溶解,过滤,洗涤,干燥
C 硝酸 H2SO4 加入适量 Ba(NO3)2溶液,充分反应后过滤
D NaCl MgCl2 溶于水,加入稍过量的NaOH溶液,充分反应后过滤,向滤液中加入适量稀盐酸,蒸发结晶
B
3. (2021平顶山一模改编)下列除去杂质(括号内为杂质)的方法正确的是( )
A. CaCO3(CaO)——加热固体混合物
B. CO2(H2O) ——将气体通入盛有生石灰的干燥管
C. KNO3固体(NaCl固体)——充分溶解后蒸发结晶
D. Cu(CuO) ——向固体中加入足量稀盐酸,过滤
D
4. 下列除去杂质的试剂和方法可行的是( )
选项 物质(括号内为杂质) 除杂试剂和方法
A Mg(NO3)2溶液(AgNO3) 加入过量铁粉,过滤
B NaCl溶液(Na2SO4) 加入适量BaCl2溶液,过滤
C CO2(CO) 通过足量澄清石灰水
D Na2SO4溶液(Na2CO3) 加入过量的稀硫酸
B
5. (2021解析与检测改编)下列除去物质中杂质(括号内为杂质)的方法,不正确的是( )
选项 物质(杂质) 除杂方法
A MnO2(KCl) 将物质加水溶解,然后过滤、洗涤、干燥
B CO(CO2) 将混合气体依次通过足量的氢氧化钠溶液和浓硫酸
C KCl(K2CO3) 加足量稀盐酸,蒸发结晶
D NaNO3(NaOH) 滴加适量稀盐酸
D
6. (2021衡阳)下列除杂方法(括号内是杂质)错误的是( )
选项 物质 选用的试剂及操作方法
A KCl溶液(K2SO4) 加入适量的Ba(NO3)2溶液,过滤
B O2(CO2) 依次通过足量NaOH溶液和浓硫酸
C CaO(CaCO3) 高温煅烧
D MnO2( K2MnO4) 加水溶解,过滤,洗涤,干燥
A
7. 除去下列物质中的少量杂质,所选用的试剂及操作方法正确的是( )
选项 物质 杂质 所用试剂及操作方法
A 铁粉 木炭粉 加入足量稀硫酸,过滤、洗涤、干燥
B 氯化钠 碳酸钠 加入适量稀盐酸,蒸发结晶
C 氧化铜 铜 加入足量稀硫酸,过滤、洗涤、干燥
D 硫酸亚铁 硫酸铜 加水溶解后加入足量金属锌,过滤、蒸发结晶
B
8. 某同学为除去食盐水中的Na2SO4杂质,进行了以下实验:
下列有关说法错误的是( )
A. X为BaCl2溶液 B. Y为Na2CO3溶液
C. Z为稀盐酸 D. 步骤③与④可交换
D
9. 下图是将潮湿空气中的氧气、二氧化碳、水蒸气分别除去的流程图:
请根据你所确定的除杂方案,将使用的试剂名称填写在下面的横线上:A为_________________;
B为_________________;
C为____。
氢氧化钠溶液
浓硫酸(或氧化钙)
铜
10. (2021安徽)某燃煤电厂产生的固体废弃物粉煤灰中含有较多的氧化铝。从粉煤灰中提取氧化铝的工艺流程如下。
(1)“酸浸”中使用的酸是___(填字母序号)。
A. HCl B. H2SO4 C. Na2SO4
(2)流程中涉及到的氧化物有_________________________________(写出1种即可)。
B
Al2O3(或H2O,填化学式或名称均可)
(3)“煅烧”过程发生反应的化学方程式为___________________________,反应类型是__________。
(4)该工艺的价值在于____________________________。
废物再利用(其他合理答案均可)
分解反应
2Al(OH)3===== Al2O3+3H2O
高温
11. 某氯化钾样品中含有杂质氯化钙和氯化镁,设计提纯的流程图如下:
(1)写出加入Y溶液时发生反应的化学方程式。
答:K2CO3+CaCl2===CaCO3↓+2KCl
(2)设计实验证明滤液中是否存在KOH。(简要写出操作步骤、现象和结论)
(3 )加入过量盐酸的目的是____________________________。
(4)蒸发操作的目的是除去___________。(填化学式)
答:取少量滤液于试管中,加入足量的氯化钙(或氯化钡等)溶液,产生白色沉淀,静置,取上层清液向其中加入几滴酚酞溶液,若溶液变红,则滤液中有氢氧化钾,反之则不存在。
除去过量的氢氧化钾和碳酸钾
H2O、HCl
2022年化学中考备考复习专题突破
《 物质的检验与鉴别、除杂与分离》
精讲课件(五)
一、物质的检验
1.常见气体的检验
离子 方法 现象
H+ 滴加酸碱指示剂,如__________ _____ 溶液变红
用pH试纸测其pH pH<7
加入较活泼金属,如___________ 有气泡产生
加入碳酸盐如碳酸钠 有气泡产生
加入金属氧化物,如氧化铜 ____________________
锌(合理即可)
固体溶解,溶液变蓝
紫色石蕊溶液
2.常见离子的检验
离子 方法 现象
OH- 滴加酸碱指示剂,如_____________ 溶液变红
用pH试纸测其pH _______
加入可溶性____________ 生成蓝色或红褐色沉淀
滴加_______,将产生的气体通入澄清石灰水 产生无色、无味气体,该气体能使澄清石灰水变_____
滴加可溶性钙盐,如氯化钙 有白色沉淀生成
无色酚酞溶液
pH>7
铜盐或铁盐
稀盐酸
浑浊
离子 方法 现象
铵盐与______研磨 产生有刺激性气味的气体
加入强碱溶液,加热,用湿润的红色石蕊试纸检验产生的气体 产生有刺激性气味的气体,试纸_____
若是碳酸氢铵固体,直接加热,用湿润的酚酞试纸检验产生的气体 固体减少,酚酞试纸变红
熟石灰
变蓝
离子 方法 现象
Cl- 先加入_______溶液,再加入稀硝酸 产生白色沉淀,且沉淀不溶于稀硝酸
先加入_______溶液,再加入稀硝酸 有白色沉淀生成且沉淀不溶解
Cu2+ Fe3+ 观察颜色法 Cu2+呈____色;
Fe3+呈____色;
加________________溶液 Cu2+产生蓝色沉淀,Fe3+产生红褐色沉淀
硝酸银
硝酸钡
NaOH(合理即可)
蓝
黄
1. 下列检验气体的方法正确的是( )
A. 检验二氧化碳气体可以用燃着的木条
B. 检验氧气是否集满,将带火星的木条放在集气瓶瓶口
C. 检验一氧化碳时,只需通过灼热的氧化铜固体
D. 检验甲烷中含有碳、氢元素,可以将气体点燃,在火焰上方罩内壁附着澄清石灰水的烧杯
B
2. 下列实验方案设计合理的是 ( )
选项 实验目的 实验方案
A 检验稀硫酸 取样,加入Ba(NO3)2溶液
B 检验某化肥是否是铵态氮肥 取样,加熟石灰混合研磨闻气味
C 检验烧碱样品是否变质 滴加酚酞溶液
D 检验氧化钙中是否含有氢氧化钙 加水溶解,加入酚酞溶液
B
二、物质的鉴别
考向1 用物理方法区分
方法指导
依据特殊的物理性质(如颜色、气味、溶解现象、磁性等)进行观察分析、区分物质。
3.下列各组物质的鉴别方法错误的是( )
A. CaCl2、CaCO3:加水,观察能否被水溶解
B. CaO、NH4NO3:向分别装有两种药品的烧杯中加水,用手触摸烧杯外壁
C. 浓H2SO4、 稀H2SO4:打开瓶盖,观察是否有白雾
D. 铁粉、石墨粉:分别用磁铁吸引
C
考向2 用化学方法区分
通过化学反应,观察反应现象(如燃烧、产生气泡、沉淀、放热、变色等),根据现象分析得出结论。
4. 下列各组物质的鉴别方法不正确的是( )
选项 待鉴别的物质 鉴别试剂
A 稀盐酸和稀硫酸 氯化钡溶液
B 氯化铵和氯化钠固体 硝酸银溶液
C 木炭粉和氧化铜粉末 灼烧
D 硫酸、氢氧化钠、硫酸钠 紫色石蕊溶液
B
考向3 几种常见物质鉴别(自选试剂)
选择试剂时,实验现象要明显、实验方法要简便(优先物理方法、后化学方法),通过是否有特殊现象来区分。
5. 请选择试剂鉴别下列物质,并简述其鉴别方法(现象、结论)。
(1)硬水和软水:选择试剂_______;现象及结论_____________________
___________________________________________。
(2)黄铜和纯铜:选择试剂或方法________;现象及结论______________
_________________。
(3)羊毛、棉花和合成纤维:选择方法_____________;现象及结论____________________________________________________________________________________________。
肥皂水
产生泡沫较多、浮渣较
少的是软水,产生泡沫较少、浮渣较多的是硬水
相互刻画
有明显划痕的为
纯铜,反之为黄铜
灼烧,闻气味
有烧焦羽毛气味的是羊毛;有烧纸气味的是棉花;有特殊气味,产物是黑色硬球且捏不碎的是合成纤维
(4)二氧化锰和氧化铜:选择试剂________________;现象及结论_________________________________________________________。
(5)白醋和白酒:选择方法_______;现象及结论______________________
________________。
(6) 氮肥、钾肥和磷肥:
①看外观:现象及结论_______________________________________;
②加水溶解,磷肥大多不溶于水或部分溶于水,氮肥和钾肥全部溶于水;
③加_______研磨,现象及结论______________________________。
闻气味
有刺激性气味的是白醋,
有醇香味的是白酒
氮肥、钾肥都是白色晶体;磷肥是灰白色粉
熟石灰
有刺激性气味放出的是铵态氮肥
稀盐酸(合理即可)
无明显现象的是二氧化锰;固体溶解、溶液变为蓝色的是氧化铜
1. (河南真题组合)下列区分物质的方法或试剂不正确的是( )
A. 用带火星的木条区分氧气和氮气(2018河南10A)
B. 用肥皂水区分硬水、软水(2019河南12B)
C. 用酚酞溶液区分硫酸和硫酸钠溶液(2018河南10C)
D. 用水区分硝酸铵、氢氧化钠(2019河南12D)
C
2. 有三瓶无色溶液分别是盐酸、石灰水、水,用下列试剂能把它们区分开的是( )
A. 酚酞溶液 B. 镁条 C. CuO粉末 D. 石蕊溶液
3. 下列鉴别物质所用的方法中,不正确的是( )
A. 水和过氧化氢溶液——加二氧化锰
B. 区分纯金属与其组成的合金——相互刻画
C. 硫酸和硫酸钠溶液——加硝酸钡溶液
D. 一氧化碳和二氧化碳——通入紫色石蕊溶液中
D
C
4. (2021成都)为区分硫酸钾、氯化铵、硫酸铵、磷矿粉四种固体物质,以下方案及结论有误的是( )
A. 观察固体颜色能区分出磷矿粉
B. 取样,加熟石灰研磨闻到氨味的物质有两种
C. 取样,溶解后加硝酸钡溶液能区分出硫酸铵
D. 用水和氢氧化钡溶液能区分出四种物质
C
5. 下列各组物质分别用括号内物质进行鉴别,不能一次性鉴别出来的是
( )
A. NaOH、CaCO3、NaCl三种固体(水)
B. CO2、O2、空气三种气体(带火星的木条)
C. MnO2、铁粉、CuO三种黑色固体(稀硫酸)
D. CuSO4、NaNO3、K2CO3三种溶液(澄清石灰水)
B
6. (2021湖州)某科学兴趣小组在课余时间做了“开门大吉”的游戏,其规则是:每把钥匙代表一种试剂,每扇门代表需要鉴别的两种溶液,见下图。如果钥匙代表的试剂能够鉴别出门上代表的两种溶液,钥匙就能把门打开(每把钥匙只能使用一次),下列能够依次将四扇门打开的钥匙顺序是( )
B
A. ①②③④ B. ④②③① C. ④③②① D. ①③②④
7. (2021郑州一检)有三瓶无色、无味的气体,它们分别是甲烷、氢气和一氧化碳。请设计实验加以鉴别。
答:点燃三种气体,分别用干燥的冷烧杯罩在火焰上方,烧杯壁上没有水珠的是一氧化碳;向烧杯壁上有水珠的两个集气瓶中,分别注入澄清的石灰水,振荡,石灰水变浑浊的是甲烷,不变浑浊的是氢气。(合理即可)
8. (2021眉山改编)化学实验室有失去标签的硝酸钡、碳酸钠、氢氧化钾、稀硫酸、氢氧化钙五瓶无色溶液,现将其任意编号A、B、C、D、E,然后两两混合进行实验,其部分现象如下表(微溶物视为可溶物)。
实验 A+E A+B B+C B+E
现象 产生沉淀 产生沉淀 产生沉淀 产生气体
(1)碳酸钠俗称纯碱,属于___类(填字母)。
A. 酸 B. 碱 C. 盐
(2)写出溶液B中溶质的化学式________。
(3)写出溶液A与E反应的化学方程式。
C
Na2CO3
答:Ba(NO3)2+H2SO4=== BaSO4↓+2HNO3
\
物质的除杂
一、除杂原则
1.主不减:被提纯的物质不能和加入的试剂反应。
2.杂不增:不能引入新的杂质。
3.易分离:使被提纯的物质和杂质转化为不同状态(固、液、气),固体和液体的分离法为过滤。
二、常见物质的除杂
1. 气体的除杂
2. 固体的除杂
(1)当被提纯物质与杂质中只有一种可溶于水或杂质能与水反应时,可选择用水溶解、过滤的方法除杂。
(2)若被提纯物质与杂质均溶于水,可通过加水将其转化为液体除杂,最终通过蒸发结晶或降温结晶得到要提纯物质。
(3)当两种物质都难溶于水时,可根据物质的性质差异选用气体或液体除杂试剂。
常见固体除杂举例:
物质 杂质 试剂、方法
Cu Fe __________________________,过滤、
洗涤、干燥;或用磁铁吸引
Cu CuO 加足量的稀硫酸(或稀盐酸),过滤、洗涤、干燥
KCl MnO2 溶解、过滤、蒸发结晶
NaCl KNO3 溶解、蒸发结晶
CaO CaCO3 __________
加入足量的稀硫酸(或稀盐酸)
高温煅烧
3. 液体的除杂
第一步:对比,找出杂质离子和非杂质离子;
第二步:找出与杂质离子不共存且不引入新杂质的离子,确定除杂试剂。
如:除去NaCl溶液中的Na2CO3如图所示:
【特别提醒】除杂试剂应适量。
物质(杂质) 杂质离子 除杂试剂(写化学式)
NaOH溶液(Na2CO3) ______ ___________________
NaCl溶液(Na2SO4) _____ ______
NaCl溶液(NaOH) _____ ______________
NaOH溶液[Ca(OH)2] _____ _________
CaCl2溶液(HCl) _____ _________
FeSO4溶液(CuSO4) ______ ___
NaNO3溶液(CuSO4) __________ ________
Ca(OH)2[或Ba(OH)2]
BaCl2
OH-
MgCl2(合理即可)
Ca2+
Na2CO3
H+
CaCO3
Cu2+
Fe
Ba(OH)2
Cu2+、
1. 除去下列物质中混有的少量杂质(括号内为杂质),实验方案不可行的是( )
A. CuO粉末(C):在空气中灼烧
B. FeCl2溶液(CuCl2):加过量的铁粉,过滤
C. KOH溶液(K2CO3):加入适量氢氧化钙溶液,过滤
D. H2(HCl):依次通过足量的NaHCO3溶液和浓硫酸
D
2. (2021德阳)在化工生产中通过除杂得到较纯净的产品。以下除杂的实验设计不合理的是( )
选项 物质 杂质 实验设计
A N2 O2 通过灼热的足量铜网,充分反应
B CaO CaCl2 加水充分溶解,过滤,洗涤,干燥
C 硝酸 H2SO4 加入适量 Ba(NO3)2溶液,充分反应后过滤
D NaCl MgCl2 溶于水,加入稍过量的NaOH溶液,充分反应后过滤,向滤液中加入适量稀盐酸,蒸发结晶
B
3. (2021平顶山一模改编)下列除去杂质(括号内为杂质)的方法正确的是( )
A. CaCO3(CaO)——加热固体混合物
B. CO2(H2O) ——将气体通入盛有生石灰的干燥管
C. KNO3固体(NaCl固体)——充分溶解后蒸发结晶
D. Cu(CuO) ——向固体中加入足量稀盐酸,过滤
D
4. 下列除去杂质的试剂和方法可行的是( )
选项 物质(括号内为杂质) 除杂试剂和方法
A Mg(NO3)2溶液(AgNO3) 加入过量铁粉,过滤
B NaCl溶液(Na2SO4) 加入适量BaCl2溶液,过滤
C CO2(CO) 通过足量澄清石灰水
D Na2SO4溶液(Na2CO3) 加入过量的稀硫酸
B
5. (2021解析与检测改编)下列除去物质中杂质(括号内为杂质)的方法,不正确的是( )
选项 物质(杂质) 除杂方法
A MnO2(KCl) 将物质加水溶解,然后过滤、洗涤、干燥
B CO(CO2) 将混合气体依次通过足量的氢氧化钠溶液和浓硫酸
C KCl(K2CO3) 加足量稀盐酸,蒸发结晶
D NaNO3(NaOH) 滴加适量稀盐酸
D
6. (2021衡阳)下列除杂方法(括号内是杂质)错误的是( )
选项 物质 选用的试剂及操作方法
A KCl溶液(K2SO4) 加入适量的Ba(NO3)2溶液,过滤
B O2(CO2) 依次通过足量NaOH溶液和浓硫酸
C CaO(CaCO3) 高温煅烧
D MnO2( K2MnO4) 加水溶解,过滤,洗涤,干燥
A
7. 除去下列物质中的少量杂质,所选用的试剂及操作方法正确的是( )
选项 物质 杂质 所用试剂及操作方法
A 铁粉 木炭粉 加入足量稀硫酸,过滤、洗涤、干燥
B 氯化钠 碳酸钠 加入适量稀盐酸,蒸发结晶
C 氧化铜 铜 加入足量稀硫酸,过滤、洗涤、干燥
D 硫酸亚铁 硫酸铜 加水溶解后加入足量金属锌,过滤、蒸发结晶
B
8. 某同学为除去食盐水中的Na2SO4杂质,进行了以下实验:
下列有关说法错误的是( )
A. X为BaCl2溶液 B. Y为Na2CO3溶液
C. Z为稀盐酸 D. 步骤③与④可交换
D
9. 下图是将潮湿空气中的氧气、二氧化碳、水蒸气分别除去的流程图:
请根据你所确定的除杂方案,将使用的试剂名称填写在下面的横线上:A为_________________;
B为_________________;
C为____。
氢氧化钠溶液
浓硫酸(或氧化钙)
铜
10. (2021安徽)某燃煤电厂产生的固体废弃物粉煤灰中含有较多的氧化铝。从粉煤灰中提取氧化铝的工艺流程如下。
(1)“酸浸”中使用的酸是___(填字母序号)。
A. HCl B. H2SO4 C. Na2SO4
(2)流程中涉及到的氧化物有_________________________________(写出1种即可)。
B
Al2O3(或H2O,填化学式或名称均可)
(3)“煅烧”过程发生反应的化学方程式为___________________________,反应类型是__________。
(4)该工艺的价值在于____________________________。
废物再利用(其他合理答案均可)
分解反应
2Al(OH)3===== Al2O3+3H2O
高温
11. 某氯化钾样品中含有杂质氯化钙和氯化镁,设计提纯的流程图如下:
(1)写出加入Y溶液时发生反应的化学方程式。
答:K2CO3+CaCl2===CaCO3↓+2KCl
(2)设计实验证明滤液中是否存在KOH。(简要写出操作步骤、现象和结论)
(3 )加入过量盐酸的目的是____________________________。
(4)蒸发操作的目的是除去___________。(填化学式)
答:取少量滤液于试管中,加入足量的氯化钙(或氯化钡等)溶液,产生白色沉淀,静置,取上层清液向其中加入几滴酚酞溶液,若溶液变红,则滤液中有氢氧化钾,反之则不存在。
除去过量的氢氧化钾和碳酸钾
H2O、HCl
同课章节目录
