金属和酸反应专题复习课件(课件 35张ppt)
文档属性
| 名称 | 金属和酸反应专题复习课件(课件 35张ppt) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-04-24 00:00:00 | ||
图片预览







文档简介
(共35张PPT)
金属和酸反应专题复习
金属活动性顺序:
k Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
1.在金属活动性顺序中,金属的位置越靠前,它的活动性越强。
2.在金属活动性顺序中,位于氢元素前面的金属能置换出盐酸、稀硫酸中的氢元素!
3.在金属活动性顺序中,位于前面的金属能把位于后面的金属从它们盐溶液里置换出来。
这是重点吆!
(双选)下列化合物不能用金属与相应的酸直接反应制取的是( )
A.FeSO4 B.ZnSO4 C.CuCl2 D. FeCl3 E.AlCl3
C、D
铁与酸反应时,生成的化合物中,铁元素显+2价,
且该物质的溶液均为浅绿色!
金属与酸(仅指稀盐酸、稀硫酸)反应属于
置换反应!
铝与酸反应时,生成的化合物中,铝元素显+3价!
补充知识1:
将相同质量铁、锌、镁、铝分别投入到足量的稀盐酸中,(如图),
则产生气体质量由多到少的顺序是 ________;
产生氢气的速率由快到慢的顺序是_________。
Mg > Al > Zn > Fe
Al > Mg > Fe > Zn
常见金属与酸反应
规律、等质量等价态(+2价)的金属与足量的酸反应,金属的相对原子质量越小,产生的氢气质量越多。
通过曲线的斜率来判断金属的活动性,
斜率越大,反应的速率越快,则金属的活动性越强。
从图像上看生成氢气的多少,只须看“水平线高、线低”,“水平线越高”表示生成氢气越多,“水平线越低”表示生成氢气越少。
规律:
1、要制得1克氢气,需要活泼的金属质量等于相对原子质量/它的化合价
所以等质量等价态(+2价)的金属与足量的酸反应,金属的相对原子质量越小,产生的氢气质量越多。所以水平线越高相对原子质量越小。
2、相同质量的活泼金属与足量的相同酸反
应,产生的氢气由多到少(制氢的本领)依次为 : Al>Mg>Na>Fe>Zn
3、相同质量的同种酸与足量的活泼金属反应,产生的氢气一样多。
4、产生氢气多少看水平线高低。产生氢气快慢看斜率大小。金属活动性强弱也看斜率。
(双选)下列化合物能由金属与酸发生置换反应直接制取的是( )
A.FeCl3 B.ZnCl2 C.FeCl2 D.CuSO4
B、C
小明同学用6.5 g不纯的锌粉与足量盐酸完全反应,收集到H2的质量0.205 g。已知其中只含有另一种金属杂质。这种金属杂质不可能是下列物质中的
A.铁 B.铝 C.铜 D.镁
C
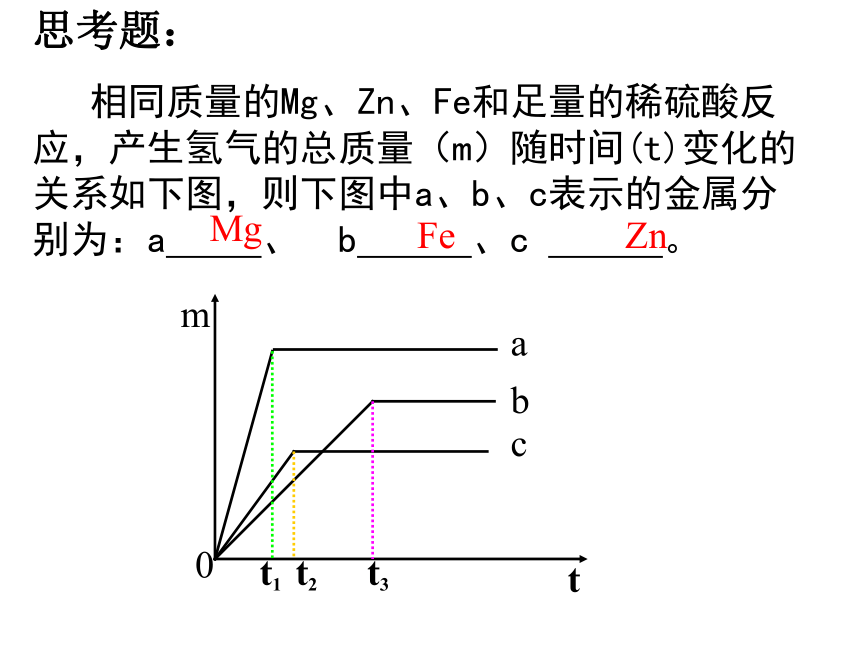
思考题:
相同质量的Mg、Zn、Fe和足量的稀硫酸反应,产生氢气的总质量(m)随时间(t)变化的关系如下图,则下图中a、b、c表示的金属分别为:a 、 b 、c 。
m
t
a
b
c
0
Mg
Fe
Zn
t2
t1
t3
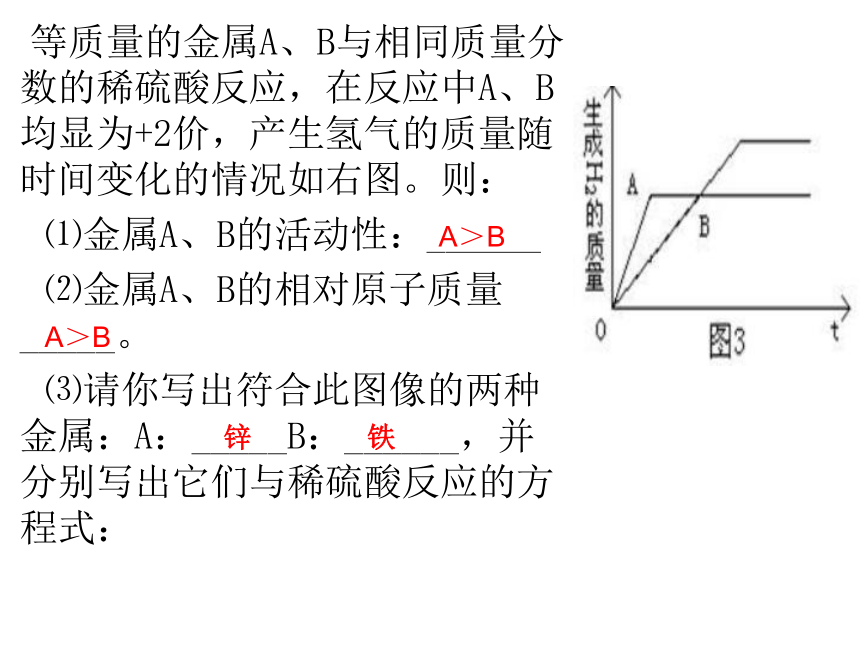
等质量的金属A、B与相同质量分数的稀硫酸反应,在反应中A、B均显为+2价,产生氢气的质量随时间变化的情况如右图。则:
⑴金属A、B的活动性:______
⑵金属A、B的相对原子质量_____。
⑶请你写出符合此图像的两种金属:A:_____B:______,并分别写出它们与稀硫酸反应的方程式:
A>B
A>B
锌
铁
将一瓶盐酸分成两等份,并分别放入两个烧杯中,再将两个烧杯中分别加入等质量的镁、锌两种金属,等反应结束后,两种金属都有剩余。若镁、锌分别与盐酸反应生成的氢气的质量用a、b表示,则a、b两者的大小关系是 :a___b 。你能以时间为横坐标,氢气的质量为纵坐标,画出反应图么?
=
t
m(H2)
Mg
Zn
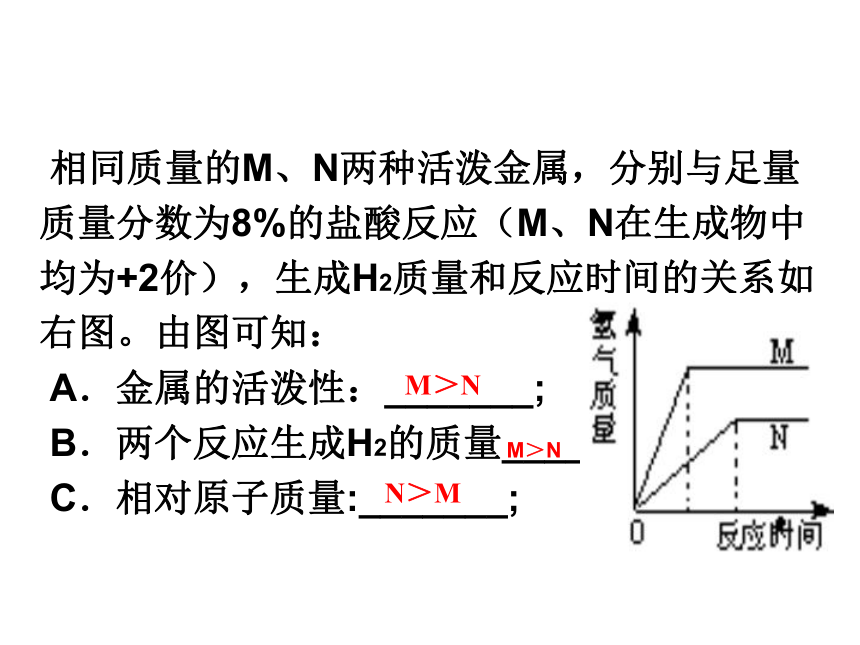
相同质量的M、N两种活泼金属,分别与足量质量分数为8%的盐酸反应(M、N在生成物中均为+2价),生成H2质量和反应时间的关系如右图。由图可知:
A.金属的活泼性:_______;
B.两个反应生成H2的质量_____;
C.相对原子质量:_______;
N>M
M>N
M>N
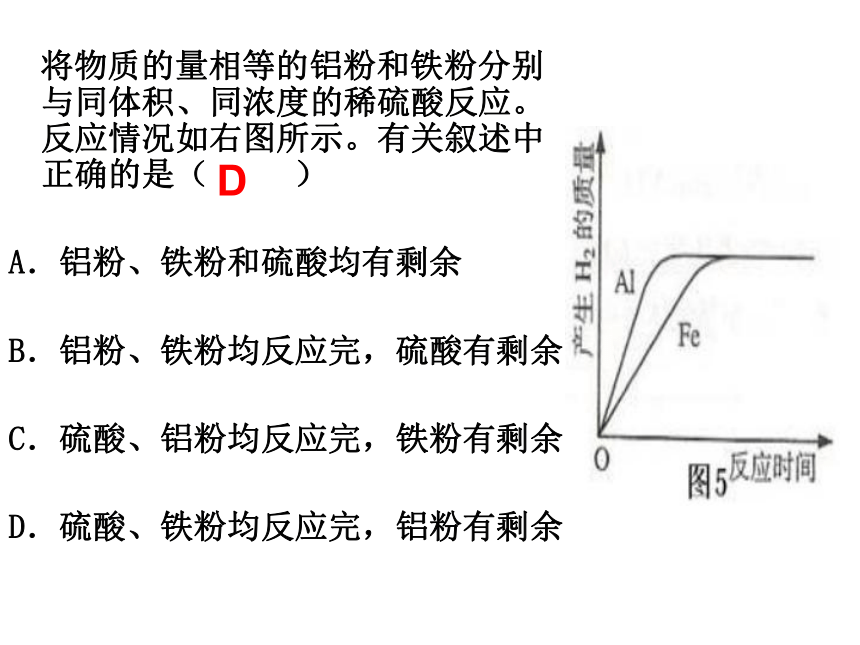
将物质的量相等的铝粉和铁粉分别与同体积、同浓度的稀硫酸反应。反应情况如右图所示。有关叙述中正确的是( )
A.铝粉、铁粉和硫酸均有剩余
B.铝粉、铁粉均反应完,硫酸有剩余
C.硫酸、铝粉均反应完,铁粉有剩余
D.硫酸、铁粉均反应完,铝粉有剩余
D
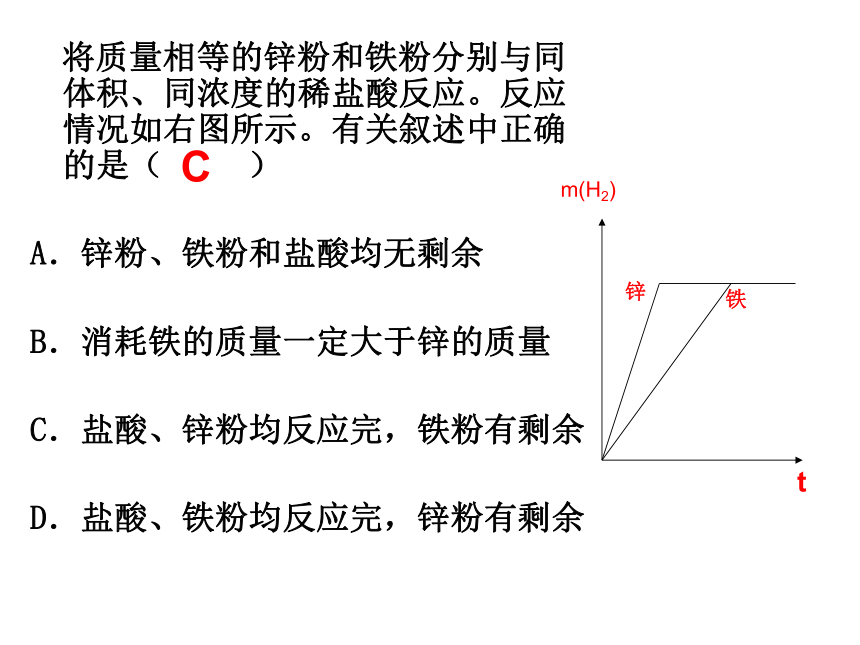
将质量相等的锌粉和铁粉分别与同体积、同浓度的稀盐酸反应。反应情况如右图所示。有关叙述中正确的是( )
A.锌粉、铁粉和盐酸均无剩余
B.消耗铁的质量一定大于锌的质量
C.盐酸、锌粉均反应完,铁粉有剩余
D.盐酸、铁粉均反应完,锌粉有剩余
C
m(H2)
t
锌
铁
在托盘天平两盘烧杯中,各放入质量浓度都相同的稀硫酸,调至天平平衡,分别向两烧杯中各放入5g镁和5g铁,金属全部反应消失后,天平指针将 :
A、向镁一边偏 B、偏向加铁一边
C、仍平衡 D、不能确定
补充知识2:天平是否平衡的问题
B
解答此题的关键就是确定等质量的铁、镁放出的氢气量
谁多谁少!由于“金属全部反应”,所以酸的量是足够的!
又由于金属是等质量,产生氢气的量决定金属的制氢本领。
(铝、镁、钠、铁、锌)所以镁放出的氢气量大于铁。因
此指针偏向铁的一边!
【练习1】:在托盘天平两盘烧杯中,各放入质量浓度都相同的稀盐酸,调至天平平衡,在左、右两个烧杯中分别放入等质量了两种金属(保持盐酸过剩),反应完全后发现左杯升高、右杯下降,则左右两个烧杯中分别放入的金属可能是:
A.镁和铝 B.锌和镁 C.锌和铜 D.铜和铁
补充知识2:天平是否平衡的问题
【练习2】:在托盘天平的左右两盘上,各放一只盛有相同
浓度、相同质量的稀硫酸。天平平衡,在左杯中放入
m g铁粉,在右杯中放入m g锌粉,充分反应后,两杯中
都有金属剩余,此时天平指针( )
A、偏右 B、指在中央 C、偏左 D、无法确定
C
B
【练习3】在托盘天平两盘烧杯中,各放入质量浓度都相同的稀硫酸,调至天平平衡,分别向两烧杯中各放入等质量的锌和铁,则从反应开始到金属完全反应的过程中,天平指针将 :
A、向锌一边偏 B、向铁一边偏
C、先偏向锌后偏向铁 D、先偏向铁后偏向锌
补充知识2:天平是否平衡的问题
D
5.6 g含杂质的铁片加到足量的稀硫酸中,共收集到0.195 g氢气,该铁片中可能含有的杂质
A.铝 B.镁 C.锌 D.镁和铝
分析:用假设极限法,设5.6克全是铁
Fe + H2SO4===== FeSO4+ H2 ↑
56 2
5.6g m
m=0.2g
而实际上是0.195克,也就是说,等质量的另一种金属杂质放出的
氢气要<0.195克两者混合在一起才可能放出0.195克氢气!
由于,制氢本领(铝、镁、钠、铁、锌)所以选C!
C
补充知识3:
小明同学用2.4 g不纯的镁粉与足量盐酸完全反应,收集到H2的质量为0.205 g。已知其中只含有另一种金属杂质。这种金属杂质可能是下列物质中的
A.铁 B.铝 C.铜 D.镁
B
金属活动性顺序:
k Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
1.在金属活动性顺序中,金属的位置越靠前,它的活动性越强。
2.在金属活动性顺序中,位于氢元素前面的金属能置换出盐酸、稀硫酸中的氢元素!
3.在金属活动性顺序中,位于前面的金属能把位于后面的金属从它们盐溶液里置换出来。
这是重点吆!
注意事项:
1、“酸”指的是稀盐酸、稀硫酸!
2、Fe与酸溶液或金属化合物溶液反应都生成+2价的亚铁化合物!且它们的溶液均为浅绿色!
3、金属K、Ca、Na活动性太强,将它们投入酸或金属化合物溶液中之后,它们先于水反应生成相应的氢氧化物,氢氧化物再与酸或金属化合物溶液反应。因此, K、Ca、Na不能置换出氢气或金属!
4、金属与盐溶液反应的先后次序问题:
反应物的金属与盐中的金属在金属活动顺序中相隔越远,越先反应。
⑴ 当多种金属都能与某盐溶液发生反应时,最活泼的先发生反应,然后依次进行。
⑵ 当多种盐溶液都能与某金属发生反应时,一定是最不活泼的金属先置换出来,然后依次进行。
例如:锌、铁、铜组成的混合物投入到硝酸银溶液中,谁先与硝酸银反应?
例如:锌投入到硝酸银和硝酸铜混合溶液中,与谁先反应?
锌
硝酸银
1、有X Y Z三种金属,如果把X和Y分别放入
稀硫酸中, X 溶解并产生氢气,Y不反应;如果
把Y和Z分别放入硝酸银溶液中,过一会儿,在Y
的表面有银析出,而Z无变化.根据以上事实,判
断X Y Z的金属活动顺序.
解答: 金属活动性顺序 X>Y>Z
题型一、金属活动性顺序的应用
课题2的相关题型
3.小忻同学按如下步骤对金属X, Y, Z进行探究:
(1)取样,分别加入到CuSO4溶液中,发现X、 Z表面出现红色物质,而Y没有 ;
(2)取大小相等的X. Z颗粒,分别加入到浓度相等的稀H2SO4中,发现X表面产生气泡的速率比Z快。则X, Y, Z的金属活动性由强到弱的顺序是________________。
X>Z>Y
2、某学生取X、Y、Z三种不同的金属,分别与硫酸铜溶液、稀硫酸反应,实验记录如下表(表中“+”表示能反应,“—”表示不能反应)
X Y Z
硫酸铜溶液 — + +
稀硫酸 — + —
则X、Y、Z、H、Cu五种元素活动性由弱到强
的顺序是:___________________.
X< H< Cu< Z< Y
题型二、金属活动性顺序的实验验证方法
1、两种金属的验证方法
方法1、将两种金属分别与稀盐酸或稀硫酸反应,通过观察两种与酸的反应难易程度或剧烈程度来判断。
方法2、将两种金属中的一种金属伸入另一种金属化合物溶液中,观察两者能否反应来判断
练习1:用实验证明Zn、Cu这两种金属的活动性顺序!
练习2:用实验证明Zn、Mg这两种金属的活动性顺序!
2、三种金属的验证方法
先将三种金属的活动顺序排出来(心中进行),
方法1:将两头的金属放入中间金属的盐溶液中,
通过实验现象得到结论。
方法2: 将中间金属分别放入两边金属的盐溶液中,
通过实验现象得到结论。
注意:关于铁,只能选择+2价的亚铁化合物溶液!
实验设计:
你能否设计实验证明Zn、Cu、Ag三种金属的活动性顺序。(只写出试剂名称那个即可)
方案一:用Zn、Ag和CuSO4溶液
方案二:用Cu、Zn(NO3)2溶液和AgNO3溶液
某化学兴趣小组为测定Ag 、Fe、Cu 三种金属的活动性顺序设四种方案,每种方案所用试剂如下,其中你认为不可行的是( )
A. 溶液、 AgNO3溶液
B. 溶液
C. 、稀盐酸、 AgNO3溶液
D. 溶液
练习:用实验证明Zn、Cu、Mg这三种金属的活动性顺序,选用的试剂有:_____________________.
题型三:鉴别题:
1、有两包黑色粉末,分别是铁粉和木炭粉,请你设计多种实验方案加以鉴别,并填写下列实验报告。
步骤 现象和结论
方案一
方案二
方案三
用磁铁吸引
能被磁铁吸引的是铁
分别在空气中灼烧
能红热且质量减少的是碳
分别放入酸中
能生成气体的是铁
黄铜(铜锌合金)与黄金的外观很相似,一些不法商贩就会利用这一点,以次充好,贩卖假黄金(实际就是黄铜)。我们有什么简单的化学方法来识别真金和假金呢?
步骤 现象和结论
方案一
方案二
方案三
方案四
测密度
加稀盐酸
加热
加硝酸银溶液
能产生气泡说明是黄铜,
变黑的是黄铜。
表面有银白色金属产生的是黄铜
题型三:鉴别题:
题型四、除杂:
要除去铜粉中混有的少量铁粉,下列物质不合适的是( )
A.稀硫酸 B.稀盐酸 C.CuSO4溶液 D.H2O
D
在CuCl2和NaCl的混合溶液中加入过量的Zn粉,充分反应后过滤,留在滤纸上的固体( ) A、只有Zn B、只有Cu C、有Cu和Na D、有Cu和Zn
题型五、判断反应后固体和液体的成分
D
分析:此题主要考查了金属活动顺序表的应用,先准确判断出Zn能与CuCl2反应而不与NaCl反应,又因为题中指出Zn粉“过量”,所以滤纸上有Cu和Zn。
在FeCl2和MgCl2的混合溶液中加入过量的Al粉,充分反应后过滤,留在滤纸上的固体有________,滤液中除了水,还有哪些物质?
Fe和Al
MgCl2和AlCl3
分析:先准确判断出Al能与FeCl2反应而不与MgCl2反应,又因为题中指出Al粉“过量”,所以滤纸上有Al和Fe。由于Al粉将FeCl2反应完了,所以滤液中不再含此物质,而因为Al粉和FeCl2反应时生成了AlCl3 , MgCl2又至始至终都在,所以滤液中含MgCl2、AlCl3 。
变形:
在CuCl2和MgCl2的混合溶液中加入一定量的Al粉,充分反应后过滤,往滤渣中滴加适量稀盐酸,
⑴若滤渣中无气泡产生,则留在滤纸上的固体一定有________,滤液中除了水,一定还有________。
⑵若滤渣中有气泡产生,则留在滤纸上的固体一定有________,滤液中除了水,一定还有________。
MgCl2和AlCl3
AlCl3
Cu
Cu和Al
分析:此题的突破点在于:先要根据“滤渣中有无气泡” 准确判断出Al粉是否“过量”。
题型六、判断反应前后溶液质量变化:
将锌片投入下列溶液中,反应一段时间后,溶液质量减轻的是 ( )
A、硝酸银溶液 B、稀硫酸
C、硫酸铜溶液 D、硫酸钠溶液
金属和酸反应专题复习
金属活动性顺序:
k Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
1.在金属活动性顺序中,金属的位置越靠前,它的活动性越强。
2.在金属活动性顺序中,位于氢元素前面的金属能置换出盐酸、稀硫酸中的氢元素!
3.在金属活动性顺序中,位于前面的金属能把位于后面的金属从它们盐溶液里置换出来。
这是重点吆!
(双选)下列化合物不能用金属与相应的酸直接反应制取的是( )
A.FeSO4 B.ZnSO4 C.CuCl2 D. FeCl3 E.AlCl3
C、D
铁与酸反应时,生成的化合物中,铁元素显+2价,
且该物质的溶液均为浅绿色!
金属与酸(仅指稀盐酸、稀硫酸)反应属于
置换反应!
铝与酸反应时,生成的化合物中,铝元素显+3价!
补充知识1:
将相同质量铁、锌、镁、铝分别投入到足量的稀盐酸中,(如图),
则产生气体质量由多到少的顺序是 ________;
产生氢气的速率由快到慢的顺序是_________。
Mg > Al > Zn > Fe
Al > Mg > Fe > Zn
常见金属与酸反应
规律、等质量等价态(+2价)的金属与足量的酸反应,金属的相对原子质量越小,产生的氢气质量越多。
通过曲线的斜率来判断金属的活动性,
斜率越大,反应的速率越快,则金属的活动性越强。
从图像上看生成氢气的多少,只须看“水平线高、线低”,“水平线越高”表示生成氢气越多,“水平线越低”表示生成氢气越少。
规律:
1、要制得1克氢气,需要活泼的金属质量等于相对原子质量/它的化合价
所以等质量等价态(+2价)的金属与足量的酸反应,金属的相对原子质量越小,产生的氢气质量越多。所以水平线越高相对原子质量越小。
2、相同质量的活泼金属与足量的相同酸反
应,产生的氢气由多到少(制氢的本领)依次为 : Al>Mg>Na>Fe>Zn
3、相同质量的同种酸与足量的活泼金属反应,产生的氢气一样多。
4、产生氢气多少看水平线高低。产生氢气快慢看斜率大小。金属活动性强弱也看斜率。
(双选)下列化合物能由金属与酸发生置换反应直接制取的是( )
A.FeCl3 B.ZnCl2 C.FeCl2 D.CuSO4
B、C
小明同学用6.5 g不纯的锌粉与足量盐酸完全反应,收集到H2的质量0.205 g。已知其中只含有另一种金属杂质。这种金属杂质不可能是下列物质中的
A.铁 B.铝 C.铜 D.镁
C
思考题:
相同质量的Mg、Zn、Fe和足量的稀硫酸反应,产生氢气的总质量(m)随时间(t)变化的关系如下图,则下图中a、b、c表示的金属分别为:a 、 b 、c 。
m
t
a
b
c
0
Mg
Fe
Zn
t2
t1
t3
等质量的金属A、B与相同质量分数的稀硫酸反应,在反应中A、B均显为+2价,产生氢气的质量随时间变化的情况如右图。则:
⑴金属A、B的活动性:______
⑵金属A、B的相对原子质量_____。
⑶请你写出符合此图像的两种金属:A:_____B:______,并分别写出它们与稀硫酸反应的方程式:
A>B
A>B
锌
铁
将一瓶盐酸分成两等份,并分别放入两个烧杯中,再将两个烧杯中分别加入等质量的镁、锌两种金属,等反应结束后,两种金属都有剩余。若镁、锌分别与盐酸反应生成的氢气的质量用a、b表示,则a、b两者的大小关系是 :a___b 。你能以时间为横坐标,氢气的质量为纵坐标,画出反应图么?
=
t
m(H2)
Mg
Zn
相同质量的M、N两种活泼金属,分别与足量质量分数为8%的盐酸反应(M、N在生成物中均为+2价),生成H2质量和反应时间的关系如右图。由图可知:
A.金属的活泼性:_______;
B.两个反应生成H2的质量_____;
C.相对原子质量:_______;
N>M
M>N
M>N
将物质的量相等的铝粉和铁粉分别与同体积、同浓度的稀硫酸反应。反应情况如右图所示。有关叙述中正确的是( )
A.铝粉、铁粉和硫酸均有剩余
B.铝粉、铁粉均反应完,硫酸有剩余
C.硫酸、铝粉均反应完,铁粉有剩余
D.硫酸、铁粉均反应完,铝粉有剩余
D
将质量相等的锌粉和铁粉分别与同体积、同浓度的稀盐酸反应。反应情况如右图所示。有关叙述中正确的是( )
A.锌粉、铁粉和盐酸均无剩余
B.消耗铁的质量一定大于锌的质量
C.盐酸、锌粉均反应完,铁粉有剩余
D.盐酸、铁粉均反应完,锌粉有剩余
C
m(H2)
t
锌
铁
在托盘天平两盘烧杯中,各放入质量浓度都相同的稀硫酸,调至天平平衡,分别向两烧杯中各放入5g镁和5g铁,金属全部反应消失后,天平指针将 :
A、向镁一边偏 B、偏向加铁一边
C、仍平衡 D、不能确定
补充知识2:天平是否平衡的问题
B
解答此题的关键就是确定等质量的铁、镁放出的氢气量
谁多谁少!由于“金属全部反应”,所以酸的量是足够的!
又由于金属是等质量,产生氢气的量决定金属的制氢本领。
(铝、镁、钠、铁、锌)所以镁放出的氢气量大于铁。因
此指针偏向铁的一边!
【练习1】:在托盘天平两盘烧杯中,各放入质量浓度都相同的稀盐酸,调至天平平衡,在左、右两个烧杯中分别放入等质量了两种金属(保持盐酸过剩),反应完全后发现左杯升高、右杯下降,则左右两个烧杯中分别放入的金属可能是:
A.镁和铝 B.锌和镁 C.锌和铜 D.铜和铁
补充知识2:天平是否平衡的问题
【练习2】:在托盘天平的左右两盘上,各放一只盛有相同
浓度、相同质量的稀硫酸。天平平衡,在左杯中放入
m g铁粉,在右杯中放入m g锌粉,充分反应后,两杯中
都有金属剩余,此时天平指针( )
A、偏右 B、指在中央 C、偏左 D、无法确定
C
B
【练习3】在托盘天平两盘烧杯中,各放入质量浓度都相同的稀硫酸,调至天平平衡,分别向两烧杯中各放入等质量的锌和铁,则从反应开始到金属完全反应的过程中,天平指针将 :
A、向锌一边偏 B、向铁一边偏
C、先偏向锌后偏向铁 D、先偏向铁后偏向锌
补充知识2:天平是否平衡的问题
D
5.6 g含杂质的铁片加到足量的稀硫酸中,共收集到0.195 g氢气,该铁片中可能含有的杂质
A.铝 B.镁 C.锌 D.镁和铝
分析:用假设极限法,设5.6克全是铁
Fe + H2SO4===== FeSO4+ H2 ↑
56 2
5.6g m
m=0.2g
而实际上是0.195克,也就是说,等质量的另一种金属杂质放出的
氢气要<0.195克两者混合在一起才可能放出0.195克氢气!
由于,制氢本领(铝、镁、钠、铁、锌)所以选C!
C
补充知识3:
小明同学用2.4 g不纯的镁粉与足量盐酸完全反应,收集到H2的质量为0.205 g。已知其中只含有另一种金属杂质。这种金属杂质可能是下列物质中的
A.铁 B.铝 C.铜 D.镁
B
金属活动性顺序:
k Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
1.在金属活动性顺序中,金属的位置越靠前,它的活动性越强。
2.在金属活动性顺序中,位于氢元素前面的金属能置换出盐酸、稀硫酸中的氢元素!
3.在金属活动性顺序中,位于前面的金属能把位于后面的金属从它们盐溶液里置换出来。
这是重点吆!
注意事项:
1、“酸”指的是稀盐酸、稀硫酸!
2、Fe与酸溶液或金属化合物溶液反应都生成+2价的亚铁化合物!且它们的溶液均为浅绿色!
3、金属K、Ca、Na活动性太强,将它们投入酸或金属化合物溶液中之后,它们先于水反应生成相应的氢氧化物,氢氧化物再与酸或金属化合物溶液反应。因此, K、Ca、Na不能置换出氢气或金属!
4、金属与盐溶液反应的先后次序问题:
反应物的金属与盐中的金属在金属活动顺序中相隔越远,越先反应。
⑴ 当多种金属都能与某盐溶液发生反应时,最活泼的先发生反应,然后依次进行。
⑵ 当多种盐溶液都能与某金属发生反应时,一定是最不活泼的金属先置换出来,然后依次进行。
例如:锌、铁、铜组成的混合物投入到硝酸银溶液中,谁先与硝酸银反应?
例如:锌投入到硝酸银和硝酸铜混合溶液中,与谁先反应?
锌
硝酸银
1、有X Y Z三种金属,如果把X和Y分别放入
稀硫酸中, X 溶解并产生氢气,Y不反应;如果
把Y和Z分别放入硝酸银溶液中,过一会儿,在Y
的表面有银析出,而Z无变化.根据以上事实,判
断X Y Z的金属活动顺序.
解答: 金属活动性顺序 X>Y>Z
题型一、金属活动性顺序的应用
课题2的相关题型
3.小忻同学按如下步骤对金属X, Y, Z进行探究:
(1)取样,分别加入到CuSO4溶液中,发现X、 Z表面出现红色物质,而Y没有 ;
(2)取大小相等的X. Z颗粒,分别加入到浓度相等的稀H2SO4中,发现X表面产生气泡的速率比Z快。则X, Y, Z的金属活动性由强到弱的顺序是________________。
X>Z>Y
2、某学生取X、Y、Z三种不同的金属,分别与硫酸铜溶液、稀硫酸反应,实验记录如下表(表中“+”表示能反应,“—”表示不能反应)
X Y Z
硫酸铜溶液 — + +
稀硫酸 — + —
则X、Y、Z、H、Cu五种元素活动性由弱到强
的顺序是:___________________.
X< H< Cu< Z< Y
题型二、金属活动性顺序的实验验证方法
1、两种金属的验证方法
方法1、将两种金属分别与稀盐酸或稀硫酸反应,通过观察两种与酸的反应难易程度或剧烈程度来判断。
方法2、将两种金属中的一种金属伸入另一种金属化合物溶液中,观察两者能否反应来判断
练习1:用实验证明Zn、Cu这两种金属的活动性顺序!
练习2:用实验证明Zn、Mg这两种金属的活动性顺序!
2、三种金属的验证方法
先将三种金属的活动顺序排出来(心中进行),
方法1:将两头的金属放入中间金属的盐溶液中,
通过实验现象得到结论。
方法2: 将中间金属分别放入两边金属的盐溶液中,
通过实验现象得到结论。
注意:关于铁,只能选择+2价的亚铁化合物溶液!
实验设计:
你能否设计实验证明Zn、Cu、Ag三种金属的活动性顺序。(只写出试剂名称那个即可)
方案一:用Zn、Ag和CuSO4溶液
方案二:用Cu、Zn(NO3)2溶液和AgNO3溶液
某化学兴趣小组为测定Ag 、Fe、Cu 三种金属的活动性顺序设四种方案,每种方案所用试剂如下,其中你认为不可行的是( )
A. 溶液、 AgNO3溶液
B. 溶液
C. 、稀盐酸、 AgNO3溶液
D. 溶液
练习:用实验证明Zn、Cu、Mg这三种金属的活动性顺序,选用的试剂有:_____________________.
题型三:鉴别题:
1、有两包黑色粉末,分别是铁粉和木炭粉,请你设计多种实验方案加以鉴别,并填写下列实验报告。
步骤 现象和结论
方案一
方案二
方案三
用磁铁吸引
能被磁铁吸引的是铁
分别在空气中灼烧
能红热且质量减少的是碳
分别放入酸中
能生成气体的是铁
黄铜(铜锌合金)与黄金的外观很相似,一些不法商贩就会利用这一点,以次充好,贩卖假黄金(实际就是黄铜)。我们有什么简单的化学方法来识别真金和假金呢?
步骤 现象和结论
方案一
方案二
方案三
方案四
测密度
加稀盐酸
加热
加硝酸银溶液
能产生气泡说明是黄铜,
变黑的是黄铜。
表面有银白色金属产生的是黄铜
题型三:鉴别题:
题型四、除杂:
要除去铜粉中混有的少量铁粉,下列物质不合适的是( )
A.稀硫酸 B.稀盐酸 C.CuSO4溶液 D.H2O
D
在CuCl2和NaCl的混合溶液中加入过量的Zn粉,充分反应后过滤,留在滤纸上的固体( ) A、只有Zn B、只有Cu C、有Cu和Na D、有Cu和Zn
题型五、判断反应后固体和液体的成分
D
分析:此题主要考查了金属活动顺序表的应用,先准确判断出Zn能与CuCl2反应而不与NaCl反应,又因为题中指出Zn粉“过量”,所以滤纸上有Cu和Zn。
在FeCl2和MgCl2的混合溶液中加入过量的Al粉,充分反应后过滤,留在滤纸上的固体有________,滤液中除了水,还有哪些物质?
Fe和Al
MgCl2和AlCl3
分析:先准确判断出Al能与FeCl2反应而不与MgCl2反应,又因为题中指出Al粉“过量”,所以滤纸上有Al和Fe。由于Al粉将FeCl2反应完了,所以滤液中不再含此物质,而因为Al粉和FeCl2反应时生成了AlCl3 , MgCl2又至始至终都在,所以滤液中含MgCl2、AlCl3 。
变形:
在CuCl2和MgCl2的混合溶液中加入一定量的Al粉,充分反应后过滤,往滤渣中滴加适量稀盐酸,
⑴若滤渣中无气泡产生,则留在滤纸上的固体一定有________,滤液中除了水,一定还有________。
⑵若滤渣中有气泡产生,则留在滤纸上的固体一定有________,滤液中除了水,一定还有________。
MgCl2和AlCl3
AlCl3
Cu
Cu和Al
分析:此题的突破点在于:先要根据“滤渣中有无气泡” 准确判断出Al粉是否“过量”。
题型六、判断反应前后溶液质量变化:
将锌片投入下列溶液中,反应一段时间后,溶液质量减轻的是 ( )
A、硝酸银溶液 B、稀硫酸
C、硫酸铜溶液 D、硫酸钠溶液
