5.2 放射性元素的衰变(共19张PPT)
文档属性
| 名称 | 5.2 放射性元素的衰变(共19张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 4.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 物理 | ||
| 更新时间 | 2022-04-25 15:37:30 | ||
图片预览




文档简介
(共19张PPT)
5.2 放射性元素的衰变
问题:
在古代,不论是东方还是西方,都有
一批人追求“点石成金”之术,他们试图
利用化学方法将一些普通的矿石变成黄金。当然,这些炼金术士的希望都破灭了。
那么,有没有“让一种元素变成另
一种元素”的过程呢?
类似于“点石成金”的事一直就在自然界中进行着,这就是
伴随着天然放射现象发生的原子核“衰变”过程
原子核的衰变
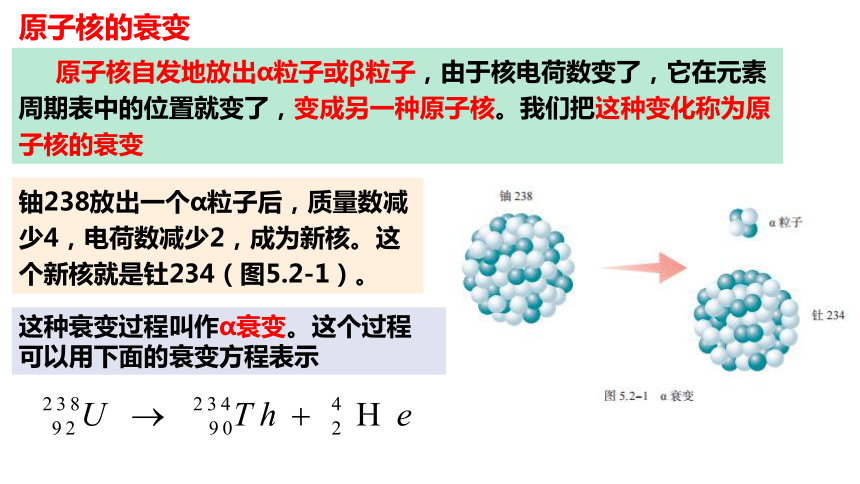
原子核自发地放出α粒子或β粒子,由于核电荷数变了,它在元素周期表中的位置就变了,变成另一种原子核。我们把这种变化称为原子核的衰变
铀238放出一个α粒子后,质量数减少4,电荷数减少2,成为新核。这个新核就是钍234(图5.2-1)。
这种衰变过程叫作α衰变。这个过程
可以用下面的衰变方程表示
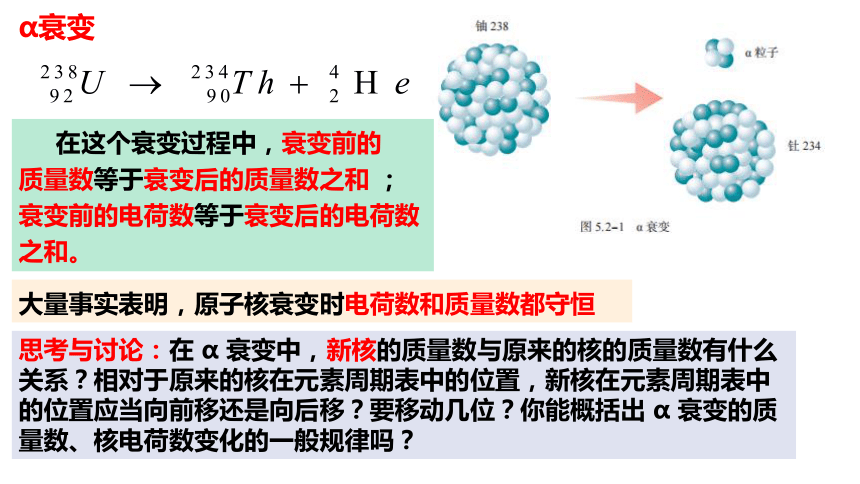
α衰变
在这个衰变过程中,衰变前的
质量数等于衰变后的质量数之和 ;
衰变前的电荷数等于衰变后的电荷数之和。
大量事实表明,原子核衰变时电荷数和质量数都守恒
思考与讨论:在 α 衰变中,新核的质量数与原来的核的质量数有什么关系?相对于原来的核在元素周期表中的位置,新核在元素周期表中的位置应当向前移还是向后移?要移动几位?你能概括出 α 衰变的质量数、核电荷数变化的一般规律吗?
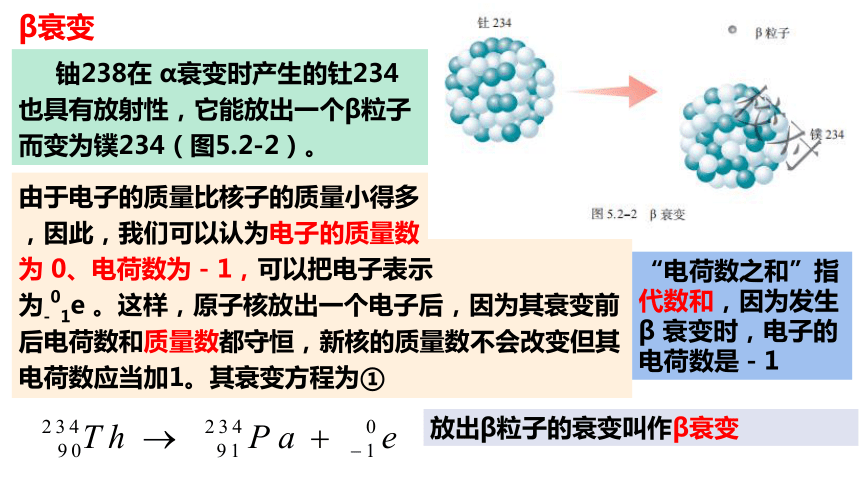
β衰变
铀238在 α衰变时产生的钍234 也具有放射性,它能放出一个β粒子而变为镤234(图5.2-2)。
由于电子的质量比核子的质量小得多
,因此,我们可以认为电子的质量数
为 0、电荷数为-1,可以把电子表示
为-01e 。这样,原子核放出一个电子后,因为其衰变前后电荷数和质量数都守恒,新核的质量数不会改变但其电荷数应当加1。其衰变方程为①
放出β粒子的衰变叫作β衰变
“电荷数之和”指代数和,因为发生 β 衰变时,电子的电荷数是-1
β衰变
思考与讨论:在 β 衰变中,质量数、
核电荷数有什么变化规律?原子核里没有电子,β 衰变中的电子来自哪里
进一步的研究发现,β衰变的实质在于核内的中子转化成了一个质子和一个电子(图5.2-3),其转化方程是:
这种转化产生的电子发射到核外,就是β 粒子
与此同时,新核少了一个中子,却增加了一个质子。所以,新核质量数不变,而电荷数增加1
研究还表明,在一定的条件下,原子核中的两个中子和两个质子会结合起来形成α粒子,并被释放出来,此时原子核就发生了α衰变
原子核发生α衰变时放出α射线,原子核发生β衰变时放出β射线,那么,放射源铀、钋、镭天然放射现象中为什么还有γ射线呢?
γ射线的产生原因
原子核的能量也跟原子的能量一样,其变化是不连续的,也只能取一系列不连续的数值,因此,也存在着能级,同样是能级越低越稳定。
放射性的原子核在发生α衰变、β衰变时产生的新核处于高能级,这时它要向低能级跃迁,并放出γ光子。因此,γ射线经常是伴随α射线和β射线产生的。当放射性物质连续衰变时,原子核中有的发生α衰变,有的发生β衰变,同时伴随着γ射线辐射。这时,放射性物质发出的射线中就会同时具有α、β、γ三种射线
半衰期
放射性同位素衰变的快慢有一定的规律。例如氡222 经过α衰变成为钋218。如图5.2-4,横坐标表示时间,纵坐标表示任意时刻氡的质量m与t = 0时的质量m0 的比值。如果隔一段时间测量一次剩余氡的数量就会发现,每过3.8 d就有一半的氡发生了衰变。也就是说,经过第一个3.8 d,剩有一半的氡;经过第二个3.8 d,剩有 1/ 4的氡;再经过3.8 d,剩有 1/8 的氡……因此,我们可以用“半衰期”来表示放射性元素衰变的快慢。
半衰期
放射性元素的原子核有半数发生衰变所需的时间,叫作这种元素的半衰期。
对于一个特定的氡原子,我们只知道它发生衰变的概率,而不知道它将何时发生衰变。一个特定的氡核可能在下1 s就衰变,也可能在10 min之内衰变,也可能在200万年之后再衰变。
然而,量子理论可以对大量原子核的行为作出统计预测。例如,对于大量氡核,可以准确地预言在1 s后、10 min后,或200万年后,各会剩下百分之几没有衰变。放射性元素的半衰期,描述的就是这样的统计规律
半衰期
不同的放射性元素,半衰期不同,甚至差别非常大。例如,氡222衰变为钋218的半衰期是3.8 d,镭226衰变为氡222的半衰期是1 620年,铀238衰变为钍234的半衰期竟长达4.5×109 年
放射性元素衰变的快慢是由核内部自身的因素决定的,跟原子所处的化学状态和外部条件没有关系。例如,一种放射性元素,不管它是以单质的形式存在,还是与其他元素形成化合物,或者对它施加压力、提高温度,都不能改变它的半衰期。这是因为压力、温度或与其他元素的化合
等,都不会影响原子核的结构
核反应
衰变是原子核的自发变化,科学家更希望人工控制原子核的变化。当初卢瑟福用α粒子轰击氮原子核,产生了氧的一种同位素——氧17和一个质子,即:
这是人类第一次实现的原子核的人工转变。
不仅用α粒子,用质子、中子甚至用γ光子去轰击一些原子核,都可以实现原子核的转变,通过这种方式可以研究原子核的结构,还可以发现和制造新元素
原子核在其他粒子的轰击下产生新原子核的过程,称为核反应。
与衰变过程一样,在核反应中,质量数守恒、电荷数守恒。
放射性同位素及其应用
很多元素都存在一些具有放射性的同位素,它们被称为放射性同位素。
天然放射性同位素不过40多种,而今天通过核反应生成的人工放射性同位素已达1 000多种,每种元素都有了自己的放射性同位素。丰富的放射性同位素资源在国民经济和科学研究的各个领域中得到了广泛的应用
与天然放射性物质相比,人工放射性同位素的放射强度容易控制,半衰
期比较短,因此放射性废料容易处理,获得了广泛的应用。
放射性同位素及其应用
射线测厚仪 工业部门可以使用放射性同位素发出的射线来测厚度。
例如,轧钢厂的热轧机上可以安装射线测厚仪(图5.2-5),让γ射线穿过钢板,仪器探测到的γ射线强度与钢板的厚度有关,轧出的钢板越厚,透过的射线越弱。因此,将射线测厚仪接收到的信号输入计算机,就可
以对钢板的厚度进行自动控制。
放射性同位素及其应用
放射治疗 在医疗方面,患了癌症的病人可以接受钴60的放射治疗(图5.2-6)。为什么射线能够用于治疗癌症呢?原来人体组织对射线的耐受能力是不同的,细胞分裂越快的组织,它对射线的耐受能力就越弱。像癌细胞那样,不断迅速繁殖的、无法控制的细胞组织,在射线照射
下破坏得比健康细胞快。
放射性同位素及其应用
培优、保鲜 利用γ射线照射种子,会使种子的遗传基因发生变异,经过筛选,可以培育出新品种。用γ射线照射食品可以杀死使食物腐败的细菌,抑制蔬菜发芽,延长保存期(图5.2-7)。
放射性同位素及其应用
示踪原子 一种放射性元素的原子核,跟这种元素其他同位素的原子核具有相同数量的质子,因此,核外电子的数量也相同。由此可知,一种元素的各种同位素都有相同的化学性质。这样,我们可以用放射性同位素代替非放射性的同位素来制成各种化合物,这种化合物的原子跟通常的化合物一样参与所有化学反应,但却带有“放射性标记”,可以用仪器探测出来。这种原子就是示踪原子。
棉花在开花、结桃的时候需要较多的磷肥,把磷肥喷在棉花叶子上,磷肥也能被吸收。但是,什么时候的吸收率最高、磷在作物内能存留多长时间、磷在作物体内的分布情况等,用通常的方法很难研究。如果用磷的放射性同位素制成肥料喷在棉花的叶面上,然后每隔一定时间用探测器测量棉株各部位的放射性强度,上面的问题就解决了。
放射性同位素及其应用
示踪原子 人体甲状腺的工作需要碘,碘被吸收后聚集在甲状腺内。如图5.2-8,给人注射碘的放射性同位素碘131,在颈部底部的甲状腺(红色,部分被遮蔽),被放射性示踪剂碘131高亮着色。定时用探测器测量甲状腺及邻近组织的放射强度,有助于诊断甲状腺的疾病。
辐射与安全
人类一直生活在放射性的环境中。例如,地球上的每个角落都有来自宇宙的射线,我们周围的岩石,其中也有放射性物质。我们的食物和日常用品中,有的也具有放射性,例如,食盐和有些水晶眼镜片中含有钾40,香烟中含有钋210,这些也是放射性同位素,不过它们辐射的强度都
在安全剂量之内。
然而过量的射线对人体组织有破坏作用,这些破坏往
往是对细胞核的破坏,有时不会马上察觉。因此,在使用放射性同位素时,必须严格遵守操作规程,注意人身安全,同时,要防止放射性物质对空气、水源、用具等的污染。存在射线危险的地方,常能看到如图5.2-9所示的标志。
5.2 放射性元素的衰变
问题:
在古代,不论是东方还是西方,都有
一批人追求“点石成金”之术,他们试图
利用化学方法将一些普通的矿石变成黄金。当然,这些炼金术士的希望都破灭了。
那么,有没有“让一种元素变成另
一种元素”的过程呢?
类似于“点石成金”的事一直就在自然界中进行着,这就是
伴随着天然放射现象发生的原子核“衰变”过程
原子核的衰变
原子核自发地放出α粒子或β粒子,由于核电荷数变了,它在元素周期表中的位置就变了,变成另一种原子核。我们把这种变化称为原子核的衰变
铀238放出一个α粒子后,质量数减少4,电荷数减少2,成为新核。这个新核就是钍234(图5.2-1)。
这种衰变过程叫作α衰变。这个过程
可以用下面的衰变方程表示
α衰变
在这个衰变过程中,衰变前的
质量数等于衰变后的质量数之和 ;
衰变前的电荷数等于衰变后的电荷数之和。
大量事实表明,原子核衰变时电荷数和质量数都守恒
思考与讨论:在 α 衰变中,新核的质量数与原来的核的质量数有什么关系?相对于原来的核在元素周期表中的位置,新核在元素周期表中的位置应当向前移还是向后移?要移动几位?你能概括出 α 衰变的质量数、核电荷数变化的一般规律吗?
β衰变
铀238在 α衰变时产生的钍234 也具有放射性,它能放出一个β粒子而变为镤234(图5.2-2)。
由于电子的质量比核子的质量小得多
,因此,我们可以认为电子的质量数
为 0、电荷数为-1,可以把电子表示
为-01e 。这样,原子核放出一个电子后,因为其衰变前后电荷数和质量数都守恒,新核的质量数不会改变但其电荷数应当加1。其衰变方程为①
放出β粒子的衰变叫作β衰变
“电荷数之和”指代数和,因为发生 β 衰变时,电子的电荷数是-1
β衰变
思考与讨论:在 β 衰变中,质量数、
核电荷数有什么变化规律?原子核里没有电子,β 衰变中的电子来自哪里
进一步的研究发现,β衰变的实质在于核内的中子转化成了一个质子和一个电子(图5.2-3),其转化方程是:
这种转化产生的电子发射到核外,就是β 粒子
与此同时,新核少了一个中子,却增加了一个质子。所以,新核质量数不变,而电荷数增加1
研究还表明,在一定的条件下,原子核中的两个中子和两个质子会结合起来形成α粒子,并被释放出来,此时原子核就发生了α衰变
原子核发生α衰变时放出α射线,原子核发生β衰变时放出β射线,那么,放射源铀、钋、镭天然放射现象中为什么还有γ射线呢?
γ射线的产生原因
原子核的能量也跟原子的能量一样,其变化是不连续的,也只能取一系列不连续的数值,因此,也存在着能级,同样是能级越低越稳定。
放射性的原子核在发生α衰变、β衰变时产生的新核处于高能级,这时它要向低能级跃迁,并放出γ光子。因此,γ射线经常是伴随α射线和β射线产生的。当放射性物质连续衰变时,原子核中有的发生α衰变,有的发生β衰变,同时伴随着γ射线辐射。这时,放射性物质发出的射线中就会同时具有α、β、γ三种射线
半衰期
放射性同位素衰变的快慢有一定的规律。例如氡222 经过α衰变成为钋218。如图5.2-4,横坐标表示时间,纵坐标表示任意时刻氡的质量m与t = 0时的质量m0 的比值。如果隔一段时间测量一次剩余氡的数量就会发现,每过3.8 d就有一半的氡发生了衰变。也就是说,经过第一个3.8 d,剩有一半的氡;经过第二个3.8 d,剩有 1/ 4的氡;再经过3.8 d,剩有 1/8 的氡……因此,我们可以用“半衰期”来表示放射性元素衰变的快慢。
半衰期
放射性元素的原子核有半数发生衰变所需的时间,叫作这种元素的半衰期。
对于一个特定的氡原子,我们只知道它发生衰变的概率,而不知道它将何时发生衰变。一个特定的氡核可能在下1 s就衰变,也可能在10 min之内衰变,也可能在200万年之后再衰变。
然而,量子理论可以对大量原子核的行为作出统计预测。例如,对于大量氡核,可以准确地预言在1 s后、10 min后,或200万年后,各会剩下百分之几没有衰变。放射性元素的半衰期,描述的就是这样的统计规律
半衰期
不同的放射性元素,半衰期不同,甚至差别非常大。例如,氡222衰变为钋218的半衰期是3.8 d,镭226衰变为氡222的半衰期是1 620年,铀238衰变为钍234的半衰期竟长达4.5×109 年
放射性元素衰变的快慢是由核内部自身的因素决定的,跟原子所处的化学状态和外部条件没有关系。例如,一种放射性元素,不管它是以单质的形式存在,还是与其他元素形成化合物,或者对它施加压力、提高温度,都不能改变它的半衰期。这是因为压力、温度或与其他元素的化合
等,都不会影响原子核的结构
核反应
衰变是原子核的自发变化,科学家更希望人工控制原子核的变化。当初卢瑟福用α粒子轰击氮原子核,产生了氧的一种同位素——氧17和一个质子,即:
这是人类第一次实现的原子核的人工转变。
不仅用α粒子,用质子、中子甚至用γ光子去轰击一些原子核,都可以实现原子核的转变,通过这种方式可以研究原子核的结构,还可以发现和制造新元素
原子核在其他粒子的轰击下产生新原子核的过程,称为核反应。
与衰变过程一样,在核反应中,质量数守恒、电荷数守恒。
放射性同位素及其应用
很多元素都存在一些具有放射性的同位素,它们被称为放射性同位素。
天然放射性同位素不过40多种,而今天通过核反应生成的人工放射性同位素已达1 000多种,每种元素都有了自己的放射性同位素。丰富的放射性同位素资源在国民经济和科学研究的各个领域中得到了广泛的应用
与天然放射性物质相比,人工放射性同位素的放射强度容易控制,半衰
期比较短,因此放射性废料容易处理,获得了广泛的应用。
放射性同位素及其应用
射线测厚仪 工业部门可以使用放射性同位素发出的射线来测厚度。
例如,轧钢厂的热轧机上可以安装射线测厚仪(图5.2-5),让γ射线穿过钢板,仪器探测到的γ射线强度与钢板的厚度有关,轧出的钢板越厚,透过的射线越弱。因此,将射线测厚仪接收到的信号输入计算机,就可
以对钢板的厚度进行自动控制。
放射性同位素及其应用
放射治疗 在医疗方面,患了癌症的病人可以接受钴60的放射治疗(图5.2-6)。为什么射线能够用于治疗癌症呢?原来人体组织对射线的耐受能力是不同的,细胞分裂越快的组织,它对射线的耐受能力就越弱。像癌细胞那样,不断迅速繁殖的、无法控制的细胞组织,在射线照射
下破坏得比健康细胞快。
放射性同位素及其应用
培优、保鲜 利用γ射线照射种子,会使种子的遗传基因发生变异,经过筛选,可以培育出新品种。用γ射线照射食品可以杀死使食物腐败的细菌,抑制蔬菜发芽,延长保存期(图5.2-7)。
放射性同位素及其应用
示踪原子 一种放射性元素的原子核,跟这种元素其他同位素的原子核具有相同数量的质子,因此,核外电子的数量也相同。由此可知,一种元素的各种同位素都有相同的化学性质。这样,我们可以用放射性同位素代替非放射性的同位素来制成各种化合物,这种化合物的原子跟通常的化合物一样参与所有化学反应,但却带有“放射性标记”,可以用仪器探测出来。这种原子就是示踪原子。
棉花在开花、结桃的时候需要较多的磷肥,把磷肥喷在棉花叶子上,磷肥也能被吸收。但是,什么时候的吸收率最高、磷在作物内能存留多长时间、磷在作物体内的分布情况等,用通常的方法很难研究。如果用磷的放射性同位素制成肥料喷在棉花的叶面上,然后每隔一定时间用探测器测量棉株各部位的放射性强度,上面的问题就解决了。
放射性同位素及其应用
示踪原子 人体甲状腺的工作需要碘,碘被吸收后聚集在甲状腺内。如图5.2-8,给人注射碘的放射性同位素碘131,在颈部底部的甲状腺(红色,部分被遮蔽),被放射性示踪剂碘131高亮着色。定时用探测器测量甲状腺及邻近组织的放射强度,有助于诊断甲状腺的疾病。
辐射与安全
人类一直生活在放射性的环境中。例如,地球上的每个角落都有来自宇宙的射线,我们周围的岩石,其中也有放射性物质。我们的食物和日常用品中,有的也具有放射性,例如,食盐和有些水晶眼镜片中含有钾40,香烟中含有钋210,这些也是放射性同位素,不过它们辐射的强度都
在安全剂量之内。
然而过量的射线对人体组织有破坏作用,这些破坏往
往是对细胞核的破坏,有时不会马上察觉。因此,在使用放射性同位素时,必须严格遵守操作规程,注意人身安全,同时,要防止放射性物质对空气、水源、用具等的污染。存在射线危险的地方,常能看到如图5.2-9所示的标志。
同课章节目录
- 第一章 分子动理论
- 1 分子动理论的基本内容
- 2 实验:用油膜法估测油酸分子的大小
- 3 分子运动速率分布规律
- 4 分子动能和分子势能
- 第二章 气体、固体和液体
- 1 温度和温标
- 2 气体的等温变化
- 3 气体的等压变化和等容变化
- 4 固体
- 5 液体
- 第三章 热力学定律
- 1 功、热和内能的改变
- 2 热力学第一定律
- 3 能量守恒定律
- 4 热力学第二定律
- 第四章 原子结构和波粒二象性
- 1 普朗克黑体辐射理论
- 2 光电效应
- 3 原子的核式结构模型
- 4 氢原子光谱和玻尔的原子模型
- 5 粒子的波动性和量子力学的建立
- 第五章 原子核
- 1 原子核的组成
- 2 放射性元素的衰变
- 3 核力与结合能
- 4 核裂变与核聚变
- 5 “基本”粒子
