化学人教版(2019)必修第二册第七章第3节第1课时乙醇乙醇的性质(共27张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册第七章第3节第1课时乙醇乙醇的性质(共27张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 42.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-04-27 00:00:00 | ||
图片预览








文档简介
(共27张PPT)
第七章 有机化合物
第 1 课时 乙醇
第 3 节 乙醇与乙酸
课程学习目标
掌握乙醇参加化学反应的断键机理
3
认识烃的衍生物、官能团等概念
2
认识乙醇的物理性质、分子组成和结构
1
核心素养
1、变化观念与平衡思想:通过对乙醇的分子结构和化学性
质的了解,理解烃的衍生物、官能团等概念。
2、证据推理与模型认知:通过对乙醇的结构及其主要性质
与应用的研究,认识有机物中羟基与其性质的关系。
3、科学探究与创新意识:通过完成乙醇与金属钠反应,乙
醇的催化氧化实验,了解科学探究的基本方法,培养学
生实验动手能力和探究水平。
导入
何以解忧,唯有杜康
酒的历史非常悠久,最早可以追溯到7000多年前的新石器时代,我国是最早掌握酿酒技术的国家之一。
酒的主要成分是什么?
乙醇
新课展示
乙醇
俗称:酒精
一、物理性质
乙醇是一种无色、有特殊香味的液体;
密度比水小,易挥发,与水以任意比互溶;
乙醇是一中有机溶剂,能够溶解多种有机物和无机物。
汽油,苯
I2 等
工业制备无水乙醇:加生石灰(CaO)蒸馏
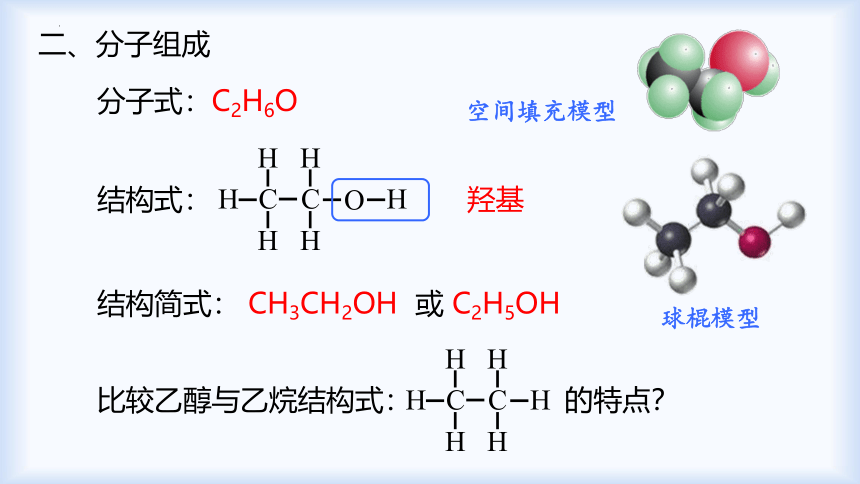
二、分子组成
分子式:C2H6O
结构式:
C
O
H
H
H
C
H
H
H
结构简式:
CH3CH2OH 或 C2H5OH
羟基
空间填充模型
球棍模型
比较乙醇与乙烷结构式: 的特点?
C
H
H
H
C
H
H
H
我们把烃中的氢原子被羟基取代而成的化合物,叫做醇;被卤素原子取代而成的化合物,叫做卤代烃;
比如:一氯甲烷、1,2-二溴乙烷等卤代烃都属于烃的衍生物
乙醇可以看成是乙烷分子中的一个氢原子被羟基取代后的产物
像这样,烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物称为 烃的衍生物。
烃的衍生物
烃的衍生物和烃具有不同的性质
三、化学性质
【实验7-4】
在盛有少量无水乙醇的试管中,加入一小块新切的用滤纸吸干表面煤油的钠,在试管口迅速塞上带尖嘴导管的橡胶塞。用小试管收集气体并检验其纯度,然后点燃(如图7-19),再将干燥的小烧杯罩在火焰上,待烧杯壁上出现液滴后,迅速倒转烧杯,向其中加入少量澄清石灰水,观察现象,并与前面做过的水与钠反应的实验现象进行比较。
1、乙醇与钠反应
实验现象
乙醇与钠反应
① 钠沉入试管底部
② 钠仍为块状
③ 没有声音
④ 产生气泡,速率缓慢
反应
不剧烈
产生的气体可在空气中安静地燃烧,烧壁上有水滴生成,烧杯中
加入澄清的石灰水不变浑浊。
实验结论
说明产生的气体是 H2
ρ钠 > ρ乙醇
实验原理
2CH3CH2OH +2Na → 2CH3CH2ONa + H2↑
乙醇与钠反应
乙醇钠
断键机理:脱去羟基上的氢原子
反应类型: 置换反应 或者 取代反应
应用:此反应可检验—OH的存在,或者用来计算分子中—OH的数目
例如:某 1 mol 有机物分子与足量钠反应可产生 2 mol H2,求此有机
物分子中羟基的数目?
4 个
钠与乙醇、水反应的比较
钠与乙醇反应 钠与水反应
钠的位置
钠的形状
有无声音
有无气泡
剧烈程度
钠沉入乙醇底部
钠浮在水面上
钠仍为块状
钠溶化成小球
没有声音
发出嘶嘶的响声
有气泡产生
有气泡产生
反应剧烈
反应缓慢
为什么钠与乙醇反应缓慢
氢原子活泼性:酸>水>醇
官能团
思考:乙醇和乙烷性质相同吗?
有机化学反应主要发生在官能团上,官能团对有机物的性质起决定作用;即,具有相同的官能团,就具有相同的性质。
不相同,烃的衍生物和烃具有不同的性质
从分子结构分析,是因为取代氢原子的羟基对乙醇性质产生了影响,
像这样决定有机化合物特性的原子或原子团叫做 官能团 。
C
O
H
H
H
C
H
H
H
常见官能团:
碳碳双键
C
C
碳碳三键
C
C
卤素原子
Cl
新课展示
2CO2 +3H2O
C2H5OH + 3O2
点燃
1)乙醇在空气中燃烧
现象:产生淡蓝色火焰,同时放出大量热。
2、氧化反应
想一想:哪些物质燃烧时会产生淡蓝色火焰
H2
CH4
2)乙醇的催化氧化
【实验7-5】
向试管中加入少量乙醇,取一根铜丝,下端绕成螺旋状,在酒精灯上灼烧后插入乙醇,反复几次,注意观察反应现象,小心地闻试管中液体产生的气味。
在一定条件下,乙醇还能被氧化为其他产物
实验展示
实验现象
① 铜丝由红变黑再变红
② 产生有刺激性气味
实验分析
① 铜丝 红 → 黑 → 红
Cu
O2
CuO
Cu
乙醇
② 产生有刺激性气味,说明产生了新物质 乙醛
实验思考
铜丝在此反应中的作用是什么?
作催化剂
实验原理
2CH3CH2OH + O2 2CH3CHO + 2H2O
Cu / Ag
此反应中,说明乙醇具有 还原性
断键机理:脱去羟基上的氢原子和与羟基相连的碳原子上的一个氢
C
O
H
H
H
C
H
H
H
C
O
H
H
H
C
H
变化
思考:若与羟基相连的碳原子上没有氢,能不能发生催化氧化?
乙醛
C
O
H
H
H
C
H
分子式:C2H4O
结构式:
结构简式: CH3CHO
乙醛 分子中的 —CHO 叫做 醛基,是醛类物质的官能团。
在适当的条件下,乙醛可以继续被氧气氧化,最终生成乙酸。
2CH3CHO + O2 2CH3COOH
催化剂
3)乙醇还可以与酸性高锰酸钾溶液和酸性重铬酸钾溶液反应
乙酸遇到强氧化剂会被直接氧化成乙酸
如:
结论:乙醇能使酸性高锰酸钾溶液褪色;
使酸性重铬酸钾溶液由橙红色变为蓝绿色
CH3CH2OH CH3COOH
酸性高锰酸钾溶液
酸性重铬酸钾溶液
K2Cr2O7
Cr2(SO4)3
(橙红色)
(蓝绿色)
乙醇
交警常用此原理检测司机是否酒后驾车
四、乙醇的用途
乙醇可以用作燃料,还可用于生产医药、香料、化妆品、涂料等,医疗上常用 75% 的乙醇溶液作消毒剂。
课堂练习
1、下列物质中不属于烃的衍生物的是 ( )
CH3CH2OH
A、
B、
C、
D、
CH2 CH2
Cl
Cl
[CH2 CH2 ] n
A
课堂练习
2、下列化学式不表示官能团的是 ( )
OH
A、
B、
C、
D、
A
COOH
C C
课堂练习
3、下列有关乙醇说法错误的是 ( )
A、钠的密度比乙醇大,实验室可用乙醇保存金属钠
B、可用无水硫酸铜检验工业酒精中是否含水
C、乙醇不能萃取出溴水中的溴
D、分离乙醇和水常用蒸馏的方法
A
乙醇
一、物理性质
二、分子组成和结构
三、化学性质
1、分子式: 2、结构简式:
1、与钠反应:
2、氧化反应:1)燃烧
2)催化氧化
3)能使酸性高锰酸钾溶液褪色
课堂总结
四、概念识记
1、烃的衍生物:
2、官能团:
第七章 有机化合物
第 1 课时 乙醇
第 3 节 乙醇与乙酸
课程学习目标
掌握乙醇参加化学反应的断键机理
3
认识烃的衍生物、官能团等概念
2
认识乙醇的物理性质、分子组成和结构
1
核心素养
1、变化观念与平衡思想:通过对乙醇的分子结构和化学性
质的了解,理解烃的衍生物、官能团等概念。
2、证据推理与模型认知:通过对乙醇的结构及其主要性质
与应用的研究,认识有机物中羟基与其性质的关系。
3、科学探究与创新意识:通过完成乙醇与金属钠反应,乙
醇的催化氧化实验,了解科学探究的基本方法,培养学
生实验动手能力和探究水平。
导入
何以解忧,唯有杜康
酒的历史非常悠久,最早可以追溯到7000多年前的新石器时代,我国是最早掌握酿酒技术的国家之一。
酒的主要成分是什么?
乙醇
新课展示
乙醇
俗称:酒精
一、物理性质
乙醇是一种无色、有特殊香味的液体;
密度比水小,易挥发,与水以任意比互溶;
乙醇是一中有机溶剂,能够溶解多种有机物和无机物。
汽油,苯
I2 等
工业制备无水乙醇:加生石灰(CaO)蒸馏
二、分子组成
分子式:C2H6O
结构式:
C
O
H
H
H
C
H
H
H
结构简式:
CH3CH2OH 或 C2H5OH
羟基
空间填充模型
球棍模型
比较乙醇与乙烷结构式: 的特点?
C
H
H
H
C
H
H
H
我们把烃中的氢原子被羟基取代而成的化合物,叫做醇;被卤素原子取代而成的化合物,叫做卤代烃;
比如:一氯甲烷、1,2-二溴乙烷等卤代烃都属于烃的衍生物
乙醇可以看成是乙烷分子中的一个氢原子被羟基取代后的产物
像这样,烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物称为 烃的衍生物。
烃的衍生物
烃的衍生物和烃具有不同的性质
三、化学性质
【实验7-4】
在盛有少量无水乙醇的试管中,加入一小块新切的用滤纸吸干表面煤油的钠,在试管口迅速塞上带尖嘴导管的橡胶塞。用小试管收集气体并检验其纯度,然后点燃(如图7-19),再将干燥的小烧杯罩在火焰上,待烧杯壁上出现液滴后,迅速倒转烧杯,向其中加入少量澄清石灰水,观察现象,并与前面做过的水与钠反应的实验现象进行比较。
1、乙醇与钠反应
实验现象
乙醇与钠反应
① 钠沉入试管底部
② 钠仍为块状
③ 没有声音
④ 产生气泡,速率缓慢
反应
不剧烈
产生的气体可在空气中安静地燃烧,烧壁上有水滴生成,烧杯中
加入澄清的石灰水不变浑浊。
实验结论
说明产生的气体是 H2
ρ钠 > ρ乙醇
实验原理
2CH3CH2OH +2Na → 2CH3CH2ONa + H2↑
乙醇与钠反应
乙醇钠
断键机理:脱去羟基上的氢原子
反应类型: 置换反应 或者 取代反应
应用:此反应可检验—OH的存在,或者用来计算分子中—OH的数目
例如:某 1 mol 有机物分子与足量钠反应可产生 2 mol H2,求此有机
物分子中羟基的数目?
4 个
钠与乙醇、水反应的比较
钠与乙醇反应 钠与水反应
钠的位置
钠的形状
有无声音
有无气泡
剧烈程度
钠沉入乙醇底部
钠浮在水面上
钠仍为块状
钠溶化成小球
没有声音
发出嘶嘶的响声
有气泡产生
有气泡产生
反应剧烈
反应缓慢
为什么钠与乙醇反应缓慢
氢原子活泼性:酸>水>醇
官能团
思考:乙醇和乙烷性质相同吗?
有机化学反应主要发生在官能团上,官能团对有机物的性质起决定作用;即,具有相同的官能团,就具有相同的性质。
不相同,烃的衍生物和烃具有不同的性质
从分子结构分析,是因为取代氢原子的羟基对乙醇性质产生了影响,
像这样决定有机化合物特性的原子或原子团叫做 官能团 。
C
O
H
H
H
C
H
H
H
常见官能团:
碳碳双键
C
C
碳碳三键
C
C
卤素原子
Cl
新课展示
2CO2 +3H2O
C2H5OH + 3O2
点燃
1)乙醇在空气中燃烧
现象:产生淡蓝色火焰,同时放出大量热。
2、氧化反应
想一想:哪些物质燃烧时会产生淡蓝色火焰
H2
CH4
2)乙醇的催化氧化
【实验7-5】
向试管中加入少量乙醇,取一根铜丝,下端绕成螺旋状,在酒精灯上灼烧后插入乙醇,反复几次,注意观察反应现象,小心地闻试管中液体产生的气味。
在一定条件下,乙醇还能被氧化为其他产物
实验展示
实验现象
① 铜丝由红变黑再变红
② 产生有刺激性气味
实验分析
① 铜丝 红 → 黑 → 红
Cu
O2
CuO
Cu
乙醇
② 产生有刺激性气味,说明产生了新物质 乙醛
实验思考
铜丝在此反应中的作用是什么?
作催化剂
实验原理
2CH3CH2OH + O2 2CH3CHO + 2H2O
Cu / Ag
此反应中,说明乙醇具有 还原性
断键机理:脱去羟基上的氢原子和与羟基相连的碳原子上的一个氢
C
O
H
H
H
C
H
H
H
C
O
H
H
H
C
H
变化
思考:若与羟基相连的碳原子上没有氢,能不能发生催化氧化?
乙醛
C
O
H
H
H
C
H
分子式:C2H4O
结构式:
结构简式: CH3CHO
乙醛 分子中的 —CHO 叫做 醛基,是醛类物质的官能团。
在适当的条件下,乙醛可以继续被氧气氧化,最终生成乙酸。
2CH3CHO + O2 2CH3COOH
催化剂
3)乙醇还可以与酸性高锰酸钾溶液和酸性重铬酸钾溶液反应
乙酸遇到强氧化剂会被直接氧化成乙酸
如:
结论:乙醇能使酸性高锰酸钾溶液褪色;
使酸性重铬酸钾溶液由橙红色变为蓝绿色
CH3CH2OH CH3COOH
酸性高锰酸钾溶液
酸性重铬酸钾溶液
K2Cr2O7
Cr2(SO4)3
(橙红色)
(蓝绿色)
乙醇
交警常用此原理检测司机是否酒后驾车
四、乙醇的用途
乙醇可以用作燃料,还可用于生产医药、香料、化妆品、涂料等,医疗上常用 75% 的乙醇溶液作消毒剂。
课堂练习
1、下列物质中不属于烃的衍生物的是 ( )
CH3CH2OH
A、
B、
C、
D、
CH2 CH2
Cl
Cl
[CH2 CH2 ] n
A
课堂练习
2、下列化学式不表示官能团的是 ( )
OH
A、
B、
C、
D、
A
COOH
C C
课堂练习
3、下列有关乙醇说法错误的是 ( )
A、钠的密度比乙醇大,实验室可用乙醇保存金属钠
B、可用无水硫酸铜检验工业酒精中是否含水
C、乙醇不能萃取出溴水中的溴
D、分离乙醇和水常用蒸馏的方法
A
乙醇
一、物理性质
二、分子组成和结构
三、化学性质
1、分子式: 2、结构简式:
1、与钠反应:
2、氧化反应:1)燃烧
2)催化氧化
3)能使酸性高锰酸钾溶液褪色
课堂总结
四、概念识记
1、烃的衍生物:
2、官能团:
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
