4.4氢原子光谱和波尔的原子模型(共21张ppt)
文档属性
| 名称 | 4.4氢原子光谱和波尔的原子模型(共21张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 物理 | ||
| 更新时间 | 2022-04-26 00:00:00 | ||
图片预览






文档简介
(共21张PPT)
第四章 原子结构和波粒二象性
4.4 氢原子光谱和波尔的原子模型
阴极射线管
α粒子散射实验
枣糕模型
原子的核式结构
原子结构
原子的核式结构学说
1、在原子的中心有一个很小的核,叫做原子核。
2、原子的全部正电荷几乎全部质量都集中在原子核里。
3、带负电的电子在核外空间里绕着核旋转。4、电子在核外圆周运动过程中向外辐射电磁波。
5、电子在核外运动的轨道是连续的
α粒子的散射的实验使我们知道原子具有核式结构,
但是电子在核的周围怎样运动?这些还要通过其他事实才能认识。
早在17世纪,牛顿就发现了日光通过三棱镜后的色散现象,并把实验中得到的彩色光带叫做光谱
光 谱
氢 原 子 光 谱
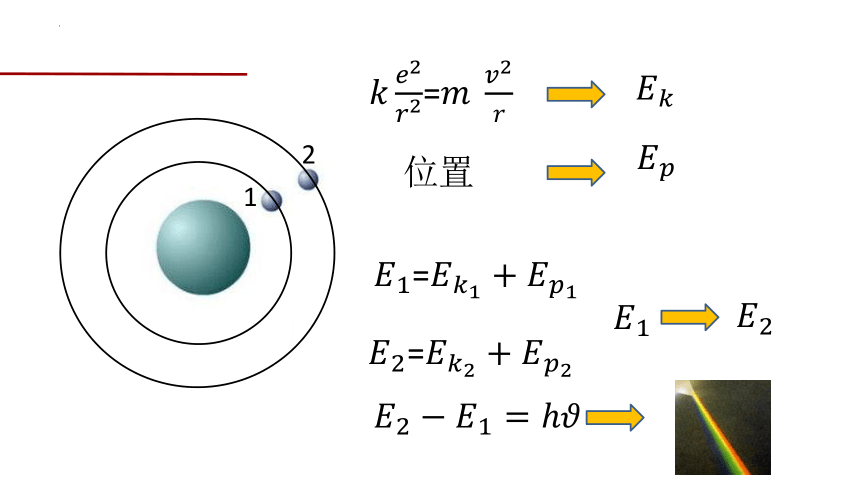
1
2
=
位置
=
=
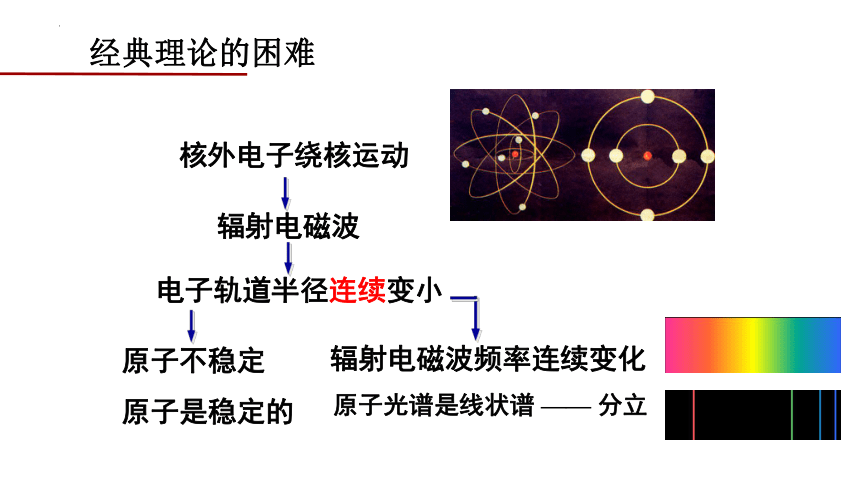
核外电子绕核运动
辐射电磁波
电子轨道半径连续变小
原子不稳定
辐射电磁波频率连续变化
原子是稳定的
原子光谱是线状谱 —— 分立
经典理论的困难
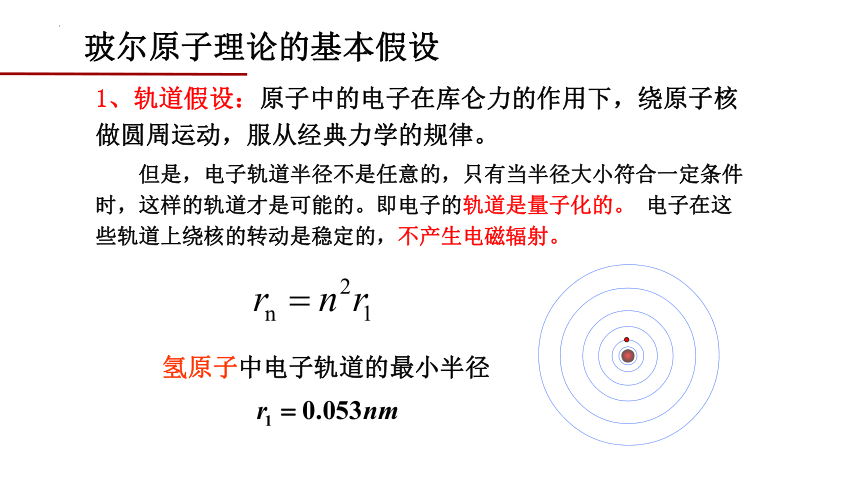
1、轨道假设:原子中的电子在库仑力的作用下,绕原子核做圆周运动,服从经典力学的规律。
玻尔原子理论的基本假设
氢原子中电子轨道的最小半径
但是,电子轨道半径不是任意的,只有当半径大小符合一定条件时,这样的轨道才是可能的。即电子的轨道是量子化的。 电子在这些轨道上绕核的转动是稳定的,不产生电磁辐射。
2、能级假设:当电子在不同轨道上运动时,原子处于不同状态,具有不同能量,所以原子能量也是量子化的。
玻尔原子理论的基本假设
氢原子在基态(第一能级)的能量:
这些量子化的能量值叫能级;原子中这些具有确定能量的稳定状态叫定态。
能量最低的状态叫基态,其他状态叫激发态。
3、跃迁假设:当电子从能量较高的定态轨道(设能量为Em)跃迁到能量较低的定态轨道(设能量为En,m>n)时,它辐射出一定频率的光子,光子的能量由这两种定态的能量差决定,即
玻尔原子理论的基本假设
反之,当电子吸收光子时会从较低的能量态跃迁到较高的能量态,吸收的光子的能量同样由两种定态的能量差决定。
(频率条件或辐射条件)
玻尔的原子模型
4 3 2 1
E4
E3
E2
E1
定态假设
跃迁假设
4 3 2 1
E4
E3
E2
E1
轨道假设
4 3 2 1
轨道半径:
能 量:
(n=1,2,3……)
式中r1 =0.53×10-10m 、E1=-13.6ev
玻尔理论对氢光谱的解释
氢原子中电子的可能轨道半径和相应的能量
频率条件
氢 原 子 光 谱
氢原子的光谱图
可见光区
特点
1、几种特定频率的光
2、光谱是分立的亮线
巴末耳的研究
巴末耳公式
巴末耳公式的推导
可见光光子的能量范围约为1.62eV~3.11eV
可见光 对应能级从n>3往n=2能级跃迁
(n=3,4,5,…),
α粒子散射实验
阴极射线管
枣糕模型
原子的核式结构
原子结构
轨道量子化
能量量子化
氢 原 子 光 谱
谢谢聆听
第四章 原子结构和波粒二象性
4.4 氢原子光谱和波尔的原子模型
阴极射线管
α粒子散射实验
枣糕模型
原子的核式结构
原子结构
原子的核式结构学说
1、在原子的中心有一个很小的核,叫做原子核。
2、原子的全部正电荷几乎全部质量都集中在原子核里。
3、带负电的电子在核外空间里绕着核旋转。4、电子在核外圆周运动过程中向外辐射电磁波。
5、电子在核外运动的轨道是连续的
α粒子的散射的实验使我们知道原子具有核式结构,
但是电子在核的周围怎样运动?这些还要通过其他事实才能认识。
早在17世纪,牛顿就发现了日光通过三棱镜后的色散现象,并把实验中得到的彩色光带叫做光谱
光 谱
氢 原 子 光 谱
1
2
=
位置
=
=
核外电子绕核运动
辐射电磁波
电子轨道半径连续变小
原子不稳定
辐射电磁波频率连续变化
原子是稳定的
原子光谱是线状谱 —— 分立
经典理论的困难
1、轨道假设:原子中的电子在库仑力的作用下,绕原子核做圆周运动,服从经典力学的规律。
玻尔原子理论的基本假设
氢原子中电子轨道的最小半径
但是,电子轨道半径不是任意的,只有当半径大小符合一定条件时,这样的轨道才是可能的。即电子的轨道是量子化的。 电子在这些轨道上绕核的转动是稳定的,不产生电磁辐射。
2、能级假设:当电子在不同轨道上运动时,原子处于不同状态,具有不同能量,所以原子能量也是量子化的。
玻尔原子理论的基本假设
氢原子在基态(第一能级)的能量:
这些量子化的能量值叫能级;原子中这些具有确定能量的稳定状态叫定态。
能量最低的状态叫基态,其他状态叫激发态。
3、跃迁假设:当电子从能量较高的定态轨道(设能量为Em)跃迁到能量较低的定态轨道(设能量为En,m>n)时,它辐射出一定频率的光子,光子的能量由这两种定态的能量差决定,即
玻尔原子理论的基本假设
反之,当电子吸收光子时会从较低的能量态跃迁到较高的能量态,吸收的光子的能量同样由两种定态的能量差决定。
(频率条件或辐射条件)
玻尔的原子模型
4 3 2 1
E4
E3
E2
E1
定态假设
跃迁假设
4 3 2 1
E4
E3
E2
E1
轨道假设
4 3 2 1
轨道半径:
能 量:
(n=1,2,3……)
式中r1 =0.53×10-10m 、E1=-13.6ev
玻尔理论对氢光谱的解释
氢原子中电子的可能轨道半径和相应的能量
频率条件
氢 原 子 光 谱
氢原子的光谱图
可见光区
特点
1、几种特定频率的光
2、光谱是分立的亮线
巴末耳的研究
巴末耳公式
巴末耳公式的推导
可见光光子的能量范围约为1.62eV~3.11eV
可见光 对应能级从n>3往n=2能级跃迁
(n=3,4,5,…),
α粒子散射实验
阴极射线管
枣糕模型
原子的核式结构
原子结构
轨道量子化
能量量子化
氢 原 子 光 谱
谢谢聆听
同课章节目录
- 第一章 分子动理论
- 1 分子动理论的基本内容
- 2 实验:用油膜法估测油酸分子的大小
- 3 分子运动速率分布规律
- 4 分子动能和分子势能
- 第二章 气体、固体和液体
- 1 温度和温标
- 2 气体的等温变化
- 3 气体的等压变化和等容变化
- 4 固体
- 5 液体
- 第三章 热力学定律
- 1 功、热和内能的改变
- 2 热力学第一定律
- 3 能量守恒定律
- 4 热力学第二定律
- 第四章 原子结构和波粒二象性
- 1 普朗克黑体辐射理论
- 2 光电效应
- 3 原子的核式结构模型
- 4 氢原子光谱和玻尔的原子模型
- 5 粒子的波动性和量子力学的建立
- 第五章 原子核
- 1 原子核的组成
- 2 放射性元素的衰变
- 3 核力与结合能
- 4 核裂变与核聚变
- 5 “基本”粒子
