浙教版科学九年级上第1章第二节探索酸的性质(第1课时)
文档属性
| 名称 | 浙教版科学九年级上第1章第二节探索酸的性质(第1课时) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2013-03-18 00:00:00 | ||
图片预览




文档简介
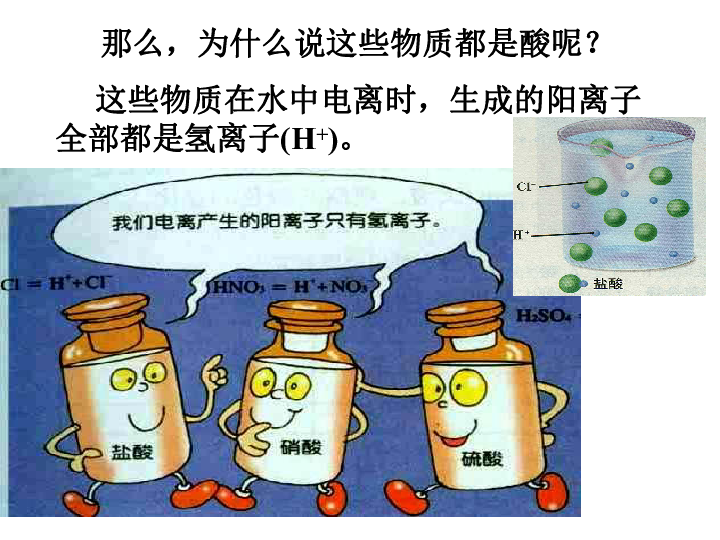
课件25张PPT。探索酸的性质看到这些,你会什么样的感觉?酸醋、放置时间过长的面包、杏、苹果、橘子等。溶液的酸性是由于其中含有一类特殊的物质——酸。食醋——醋酸,胃液——盐酸,柠檬、柑橘等水果中含有柠檬酸。 这些物质在水中电离时,生成的阳离子全部都是氢离子(H+)。那么,为什么说这些物质都是酸呢?盐酸的电离:HCl = H+ + Cl-H+H+H+H+H+H+盐酸:
硝酸:
硫酸:HCI = H + + CI-电离方程式:H NO3 = H + + NO3-H2SO4 = 2H + + SO 42-
电离通式:酸= H + + 酸根阴离子一.什么是酸:
在水中电离时,生成的阳离子全部都是氢离子(H+)的化合物。二.有哪些酸:
1、强酸:盐酸(HCl)、硫酸(H2SO4)、
硝酸(HNO3)
2、弱酸:醋酸(CH3COOH)、碳酸(H2co3)总结:酸碱指示剂pH试纸测物质的酸性?pH>7,碱性; pH =7,中性;pH<7,酸性。石蕊试液酚酞试液酚酞遇酸不变色,遇碱变红石蕊遇酸变红,遇碱变蓝1、用玻璃棒分别蘸取少许水、酸果汁、白醋、盐酸,点在pH试纸中部,观察试纸的颜色变化。
2、在白色点滴板的空穴(或小试管)里分别滴入几滴上述样品,再滴加2—3滴紫色石蕊试液,观察其颜色的变化,并将结果填入表中。实验 实验过程中物质的颜色变化蓝色紫色红色红色红色红色红色红色你能得出什么结论?石蕊遇酸变红1、下列物质不属于酸的是 ( )
A、HNO3 B、NaHCO3
C、H3PO4 D、HI
2、用简单的方法区别水和硫酸,并写出实验步骤。
3、思考:一位科学家在做研究时不小心将盐酸滴到了紫花上,紫花逐渐变红色。看到这么个现象,许多问题在他的脑子里涌现出来,如果你是那个科学家,你会有什么问题,你会有什么想法?B练习:酸的性质1.盐酸的性质在氢氧化钠溶液中滴入2滴紫色石蕊试液,溶液呈________色;再逐滴滴入盐酸,溶液颜色有什么变化?______________________。蓝色由蓝色逐渐变成紫色 HCI + NaOH = NaCI + H2O 酸 + 碱 〓 盐 + 水 【实验探究1】 胃酸过多的病人常服用一种叫“胃舒平”的药片来治疗,药片的主要成份是氢氧化铝,为什么能用它来治疗胃酸过多呢? 3 HCI + Al(OH)3 〓 AlCI3 + 3H2O 请用化学方程式表示: 酸 + 碱 〓 盐 + 水 【实验探究2】 a、把鸡蛋壳放入盛有盐酸的试管中,将燃着的火柴伸入试管口,你看到什么现象?
_________________________________.蛋壳表面产生气泡,燃着的木条伸入后会熄灭 2HCI + CaCO3 = CaCI2 + H2O + CO2↑ 酸 + 盐 = 新盐 + 新酸(碳酸)【实验探究2】澄清石灰水变浑浊 酸 + 盐 = 新盐 + 新酸(碳酸)b、碳酸钠和盐酸的反应,产生的气体通过澄清石灰水,观察现象?HCI + Na2CO3 = NaCI + H2O + CO2 ↑*? CO32-的检验:加盐酸,能产生使澄清石灰水变浑浊的气体(二氧化碳)
Ca(OH)2 + CO2 = CaCO3 ↓ + H2O【实验探究3】 a、向盛有一枚生锈的铁钉的试管中加入盐酸,振荡,过会儿观察现象?
_______________________________________. 铁锈消失,溶液变成黄色 6HCI + Fe2O3 = 2FeCI3+3H2O 盐酸 +金属氧化物= 盐 + 水【实验探究4】 上述探究实验3中,除了铁锈消失外,还可以观察到什么现象?___________________ 铁钉表面产生气泡提出问题: 气体是否是盐酸和金属铁反应生成的?建立假设:____________________________.实验验证: 2HCI + Fe = FeCI2 + H2↑酸 +金属 = 盐 + 氢气小结1、 酸能使紫色的石蕊变红,无色酚酞不变色。2、 酸 + 碱 〓 盐 + 水 3、酸 + 盐 = 新盐 + 新酸4、 盐酸 +金属氧化物= 盐 + 水5、酸 +金属 = 盐 + 氢气总结总结:
1、 酸能使指示剂变色
2、?能与碱反应生成盐和水
3、 能与某些金属氧化物反应生成盐和水
4、 能与某些金属反应生成盐和氢气
5、 能与盐反应生成新的盐和新的酸 谢谢观看
硝酸:
硫酸:HCI = H + + CI-电离方程式:H NO3 = H + + NO3-H2SO4 = 2H + + SO 42-
电离通式:酸= H + + 酸根阴离子一.什么是酸:
在水中电离时,生成的阳离子全部都是氢离子(H+)的化合物。二.有哪些酸:
1、强酸:盐酸(HCl)、硫酸(H2SO4)、
硝酸(HNO3)
2、弱酸:醋酸(CH3COOH)、碳酸(H2co3)总结:酸碱指示剂pH试纸测物质的酸性?pH>7,碱性; pH =7,中性;pH<7,酸性。石蕊试液酚酞试液酚酞遇酸不变色,遇碱变红石蕊遇酸变红,遇碱变蓝1、用玻璃棒分别蘸取少许水、酸果汁、白醋、盐酸,点在pH试纸中部,观察试纸的颜色变化。
2、在白色点滴板的空穴(或小试管)里分别滴入几滴上述样品,再滴加2—3滴紫色石蕊试液,观察其颜色的变化,并将结果填入表中。实验 实验过程中物质的颜色变化蓝色紫色红色红色红色红色红色红色你能得出什么结论?石蕊遇酸变红1、下列物质不属于酸的是 ( )
A、HNO3 B、NaHCO3
C、H3PO4 D、HI
2、用简单的方法区别水和硫酸,并写出实验步骤。
3、思考:一位科学家在做研究时不小心将盐酸滴到了紫花上,紫花逐渐变红色。看到这么个现象,许多问题在他的脑子里涌现出来,如果你是那个科学家,你会有什么问题,你会有什么想法?B练习:酸的性质1.盐酸的性质在氢氧化钠溶液中滴入2滴紫色石蕊试液,溶液呈________色;再逐滴滴入盐酸,溶液颜色有什么变化?______________________。蓝色由蓝色逐渐变成紫色 HCI + NaOH = NaCI + H2O 酸 + 碱 〓 盐 + 水 【实验探究1】 胃酸过多的病人常服用一种叫“胃舒平”的药片来治疗,药片的主要成份是氢氧化铝,为什么能用它来治疗胃酸过多呢? 3 HCI + Al(OH)3 〓 AlCI3 + 3H2O 请用化学方程式表示: 酸 + 碱 〓 盐 + 水 【实验探究2】 a、把鸡蛋壳放入盛有盐酸的试管中,将燃着的火柴伸入试管口,你看到什么现象?
_________________________________.蛋壳表面产生气泡,燃着的木条伸入后会熄灭 2HCI + CaCO3 = CaCI2 + H2O + CO2↑ 酸 + 盐 = 新盐 + 新酸(碳酸)【实验探究2】澄清石灰水变浑浊 酸 + 盐 = 新盐 + 新酸(碳酸)b、碳酸钠和盐酸的反应,产生的气体通过澄清石灰水,观察现象?HCI + Na2CO3 = NaCI + H2O + CO2 ↑*? CO32-的检验:加盐酸,能产生使澄清石灰水变浑浊的气体(二氧化碳)
Ca(OH)2 + CO2 = CaCO3 ↓ + H2O【实验探究3】 a、向盛有一枚生锈的铁钉的试管中加入盐酸,振荡,过会儿观察现象?
_______________________________________. 铁锈消失,溶液变成黄色 6HCI + Fe2O3 = 2FeCI3+3H2O 盐酸 +金属氧化物= 盐 + 水【实验探究4】 上述探究实验3中,除了铁锈消失外,还可以观察到什么现象?___________________ 铁钉表面产生气泡提出问题: 气体是否是盐酸和金属铁反应生成的?建立假设:____________________________.实验验证: 2HCI + Fe = FeCI2 + H2↑酸 +金属 = 盐 + 氢气小结1、 酸能使紫色的石蕊变红,无色酚酞不变色。2、 酸 + 碱 〓 盐 + 水 3、酸 + 盐 = 新盐 + 新酸4、 盐酸 +金属氧化物= 盐 + 水5、酸 +金属 = 盐 + 氢气总结总结:
1、 酸能使指示剂变色
2、?能与碱反应生成盐和水
3、 能与某些金属氧化物反应生成盐和水
4、 能与某些金属反应生成盐和氢气
5、 能与盐反应生成新的盐和新的酸 谢谢观看
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
