2021-2022学年度人教版化学九年级上册第三单元物质构成的奥秘专题测评试卷(word版含解析)
文档属性
| 名称 | 2021-2022学年度人教版化学九年级上册第三单元物质构成的奥秘专题测评试卷(word版含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 130.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-03 00:00:00 | ||
图片预览




文档简介
九年级上册第三单元物质构成的奥秘专题测评
考试时间:90分钟;命题人:化学教研组
考生注意:
1、本卷分第I卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分,考试时间90分钟
2、答卷前,考生务必用0.5毫米黑色签字笔将自己的姓名、班级填写在试卷规定位置上
3、答案必须写在试卷各个题目指定区域内相应的位置,如需改动,先划掉原来的答案,然后再写上新的答案;不准使用涂改液、胶带纸、修正带,不按以上要求作答的答案无效。
第I卷(选择题 30分)
一、单选题(10小题,每小题3分,共计30分)
1、用分子、原子的知识对下列现象进行解释,正确的是
A.水凝结成冰,说明水分子发生改变,产生了新的分子
B.大块石头碎成小块石头,说明分子可以被分裂
C.水银温度计受热汞柱上升,说明汞原子受热体积变大
D.墙内开花墙外香,说明分子在不断运动
2、下列相关实验现象及生活现象的描述中,错误的是
A.红磷在空气中燃烧,产生大量的白烟
B.铁片在空气中剧烈燃烧,火星四射
C.食物腐烂----分子并没有停止运动
D.湿衣服在阳光下比在阴凉处干得快----温度高,分子运动快
3、搭载北斗三号卫星导航系统的手机,在没有网络信号的情况下也可以精准导航,其中高精度铷原子钟起了重要作用。铷在元素周期表中的信息如图所示,下列说法正确的是
A.铷属于非金属元素 B.铷的元素符号为Rb
C.铷原子的中子数是37 D.铷的相对原子质量是85.47g
4、如图为四种原子的结构示意图,其中化学性质相似的一组是
A.①和② B.①和③ C.②和③ D.③和④
5、用分子的观点解释下列现象,错误的是
A.热胀冷缩——分子大小随温度变化改变
B.花香四溢——分子不停地运动
C.1滴水中大约有个水分子——分子很小
D.冰和水化学性质相同———分子构成相同
6、磷元素对生命活动具有重要意义,其相关信息如图所示。下列有关说法正确的是
A.属于金属元素 B.磷原子核外有16个电子
C.相对原子质量为30.97g D.每个磷原子中有16个中子
7、下列有关镍元素的说法不正确的是
A.原子序数是28 B.原子核内质子数为30
C.元素符号是Ni D.相对原子质量为58.69
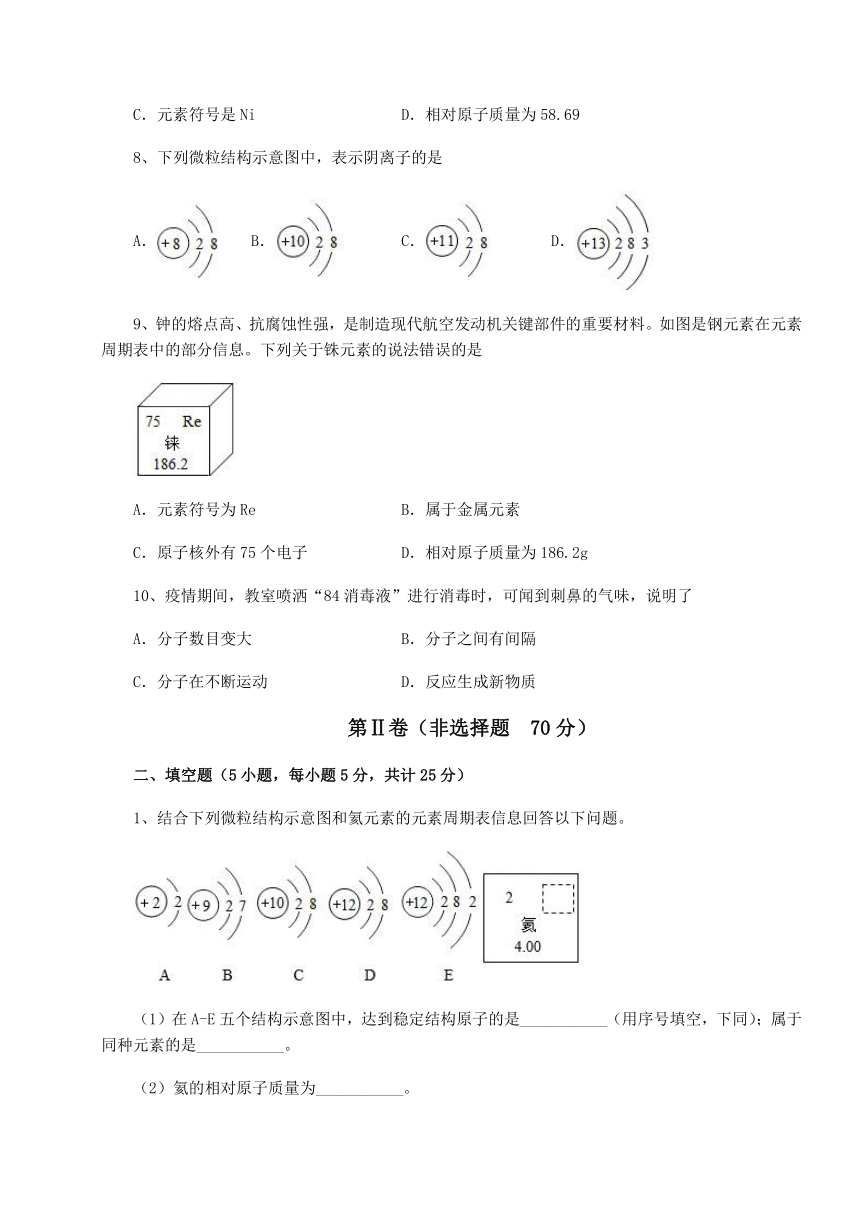
8、下列微粒结构示意图中,表示阴离子的是
A. B. C. D.
9、钟的熔点高、抗腐蚀性强,是制造现代航空发动机关键部件的重要材料。如图是钢元素在元素周期表中的部分信息。下列关于铢元素的说法错误的是
A.元素符号为Re B.属于金属元素
C.原子核外有75个电子 D.相对原子质量为186.2g
10、疫情期间,教室喷洒“84消毒液”进行消毒时,可闻到刺鼻的气味,说明了
A.分子数目变大 B.分子之间有间隔
C.分子在不断运动 D.反应生成新物质
第Ⅱ卷(非选择题 70分)
二、填空题(5小题,每小题5分,共计25分)
1、结合下列微粒结构示意图和氦元素的元素周期表信息回答以下问题。
(1)在A-E五个结构示意图中,达到稳定结构原子的是___________(用序号填空,下同);属于同种元素的是___________。
(2)氦的相对原子质量为___________。
(3)上述元素在周期表中处于同一周期是___________(用序号填空)
(4)碳-12原子质量为a,某原子的质量为b,则该原子的相对原子质量是___________。
2、下图是一些元素的粒子结构示意图和在元素周期表中的信息,请回答下列问题:
(1)锶元素的原子序数为______。
(2)锶元素它的原子的化学性质与A、B、C、D中的______(填序号,下同)相似,具有稳定结构的原子是______。
(3)图3所表示的粒子的化学符号是______。
3、核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题。
(1)在第三周期中,各原子结构的共同之处是___________ ;该周期中,各原子核外电子排布的变化规律是___________ 。
(2)硫元素和氧元素最本质的区别是它们原子的___________不同;硫元素和氧元素具有相似的化学性质,原因是它们原子的___________ 相同。
(3)写出核外电子排布与氖原子相同的阳离子___________ 。
4、下列是几种粒子的结构示意图,依图回答下列问题:
(1)D示意图中,x=__________,其所示元素属于__________(金属/非金属)元素。
(2)A、B、C、D、E中,在周期表中处于第二周期的是__________。
(3)B、D、E中,在化学反应中容易失去电子的是__________。
5、将①分子②原子③离子④质子⑤中子⑥电子等粒子名称填入下列空格中:
(1)化学反应中一定发生改变的是____________;
(2)构成物质的基本粒子是____________;
(3)构成原子的是__________;
(4)带电的粒子有___________。
三、计算题(3小题,每小题7分,共计21分)
1、某原子的质量是碳12原子质量的两倍。求这种原子的相对原子质量。
2、已知碳-12原子的质量是1.993×10-26kg,钠原子的相对原子质量为23,铁原子的质量为9.288×10-26kg。请填空或进行计算:
(注:第2、3小问写出计算过程并对钠原子质量计算结果保留三位小数)
(1)钠原子核内有____________个中子。
(2)一个钠原子的质量为多少?
(3)铁原子的相对原子质量是多少?
3、王者归“铼”,我国利用新技术发现并提纯了超级金属铼,制造出航空发动机核心部件。铼元素的部分信息如图。已知作为相对原子质量标准的一种碳原子的质量为2.0×10-26kg。
(1)铼元素位于元素周期表的第_________(填数字)周期。
(2)铼原子的中子数为________,x=_________。
(3)求铼元素一个原子的质量(写出简单的计算过程)。
四、实验探究(2小题,每小题12分,共计24分)
1、学习小组的同学在探究分子的性质,请你参与并完成相关的问题。
(进行实验)(如图)观察到的现象是B中溶液逐渐变为红色,结论为_______
(交流与讨论)有同学对B中溶液的变红提出了以下猜想:
猜想1:B中溶液变红也可能是B中溶液放置一段时间后,自动就会变红;
猜想2:大烧杯内壁附着的某种物质挥发出来使B中溶液变红。
(再次实验)请你选择其中一个猜想并设计实验进行验证。
实验操作 实验现象 实验结论
___________ ______ __________ ____
2、 “比较出真知”,比较是科学实验中常用的一种方法。小刚同学利用比较的方法探究得出了分子在不停地运动的结论。下面是他设计的实验:在第一步中他所观察到的现象是___;得出的结论是___.
进行第二步实验时,还应用到的一种仪器名称是___,他在滤纸上每间隔一段距离滴加一滴酚酞试液,那么,棉花上滴加的物质是___。放置一段时间后,他观察到的现象是____,由此,说明了氨分子在不停地运动。
(反思)分子和原子质量都很小,因此国际上采用相对原子质量的方式来进行相关计算。(已知作为相对原子质量标准的一种碳原子的质量为1.993×10-23kg)小华查阅资料发现了一个铝原子的质量为4.482x10-26kg请帮他计算铝原子的相对原子质量____
-参考答案-
一、单选题
1、D
【详解】
A、水凝结成冰,冰和水都是由水分子构成的,说明水分子不发生改变,没有产生了新的分子,选项A错误;
B、大块石头碎成小块石头,只是形状发生了改变,没有新物质生成,大块石头和小块石头中的分子没有改变,选项B错误;
C、水银是金属汞,是由汞原子直接构成的,温度计中的水银球受热体积膨胀是利用了汞原子的间隔受热变大,而不是体积变大,选项C错误;
D、墙内开花墙外香是因为分子在不停运动,向四周扩散,花香的分子运动到空气中,进入人们的鼻孔,闻到香味,选项D正确。
故选:D。
2、B
【详解】
A.红磷在空气中燃烧,产生大量的白烟,选项说法正确。
B.铁片在氧气中剧烈燃烧,火星四射,在空气中发红光,不燃烧,选项说法错误。
C.分子在永不停息的做无规则运动,食物腐烂后,分子并没有停止运动,选项说法正确。
D.温度越高,分子运动越快,因此湿衣服在阳光下比在阴凉处干得快,选项说法正确。
故选:B。
3、B
【分析】
元素周期表信息图中,元素名称的左上角的数字为元素的原子序数,右上角为元素符号,中间的汉字表示元素名称,下边是元素的相对原子质量。
【详解】
A、铷元素汉字名称中,有“钅”字旁可知,该元素属于金属元素,故选项错误;
B、伽的元素符号是Rb,故选项正确;
C、原子中,原子序数=质子数=核外电子数,故核外电子数为37,中子数不是37,故选项错误;
D、相对原子质量的单位是“1”,不是“g”,铷的相对原子质量为85. 47,故选项错误。
故选:B。
4、B
【详解】
原子最外层电子数相同,化学性质相似。最外层8个电子是相对稳定结构。但第一层就是最外层的,2个电子就是相对稳定结构。图中①③都是相对稳定结构。
综上所述:选择B。
5、A
【详解】
A、热胀冷缩是由于分子之间的间隔随着温度的变化而发生了变化,分子本身的大小不变,此选项表述不正确;
B、花香四溢是由于分子在不停地运动,花香分子运动到了鼻腔中,此选项表述正确;
C、1滴水中大约有 1.67×1021 个水分子,说明分子很小,此选项表述正确;
D、由分子构成的物质,分子是保持物质化学性质的最小微粒,冰和水化学性质相同是由于分子构成相同,此选项表述正确。
故选A。
6、D
【详解】
A:磷是“石”字旁,属于非金属元素。A错。
B:原子中核外电子数等于质子数,磷原子核外有15个电子。B错。
C:元素名称下面的数字表示相对原子质量,磷元素的相对原子质量为30.97。C错。
D:每个磷原子中有15个质子,相对原子质量为30.97≈31,所以每个磷原子中有31-15=16个中子。正确。
综上所述:选择D。
7、B
【详解】
A、根据元素周期表的信息可知,左上角的数字表示原子序数,镍的原子序数为28,故选项说法正确;
B、原子中原子序数=质子数=28,故选项说法不正确;
C、根据元素周期表的信息可知,右上角的字母表示元素符号,镍的元素符号是Ni,故选项说法正确;
D、根据元素周期表的信息可知,元素名称下方的数字表示相对原子质量,镍的相对原子质量为58.69,故选项说法正确。
故选B。
8、A
【分析】
质子带正电,电子带负电。
原子:核内质子数=核外电子数
阳离子:核内质子数>核外电子数
阴离子:核内质子数<核外电子数
【详解】
A. 核内质子数(8)<核外电子数(10),所以为阴离子。
B. 核内质子数(10)=核外电子数(10),所以为原子。
C. 核内质子数(11)>核外电子数(10),所以为阳离子。
D. 核内质子数(13)=核外电子数(13),所以为原子。
故选:A
9、D
【详解】
A、根据图示可知铼元素的元素符号为Re,故选项正确;
B、元素名称中带“钅”旁,所以该元素为金属元素,故选项正确;
C、原子序数=核电荷数=核外电子数,所以其原子核外有75个电子,故选项正确;
D、相对原子质量单位是“1”,不是“克",故选项错误。
故选D
【点睛】
10、C
【详解】
A、教室喷洒“84消毒液”进行消毒时,可闻到刺鼻的气味,是因为消毒水中含有特殊气味的分子运动到了空气中,,向四周扩散,使人们闻到刺鼻的气味,但分子数目不变,故选项不符合题意;
B、教室喷洒“84消毒液”进行消毒时,可闻到刺鼻的气味,与分子之间有间隔无关,故选项不符合题意;
C、教室喷洒“84消毒液”进行消毒时,可闻到刺鼻的气味,是因为消毒水中含有特殊气味的分子运动到了空气中,向四周扩散,使人们闻到刺鼻的气味,故选项符合题意;
D、教室喷洒“84消毒液”,没有新物质生成,属于物理变化,故选项不符合题意。
故选C。
二、填空题
1、
(1) AC DE
(2)4.00
(3)BC
(4)
【解析】
(1)
稳定结构即最外层电子数是8(只有一个电子层时,最外层是2)的微粒,所以ACD均是稳定结构,但D的质子数不等于电子数,所以D不是原子;同种元素质子数一定相同,DE质子数均为12,所以DE是同种元素,故填:AC;DE。
(2)
氦元素的元素符号为He,元素名称下面的数字表示相对原子质量,该元素的相对原子质量是4.00,故填:4.00。
(3)
原子的核外电子层数相同的位于同一周期,ABCE的质子数等于核外电子数,为原子,其中BC的电子层数相同,为同一周期,故填:BC。
(4)
相对原子质量,等于原子实际质量和碳12原子质量十二分之一的比值=,故填:。
2、
(1)38
(2) BD A
(3)Sr2+
【解析】
(1)
元素信息图中,左上角的数字就是元素的原子序数,由图可知,锶元素的原子序数为38,故填38。
(2)
由图可知,锶原子的最外层电子数为2,A、B、C、D四种微粒中,B、D的最外层电子数为2,在化学反应中溶液失去电子,与锶元素的原子的化学性质相同,虽然A微粒的原子最外层电子数也为2,但该原子既不容易失去电子,也不容易得到电子,与锶原子的化学性质不同,故填BD;
A原子的核外只有1个电子层,且该电子层的电子数为2,属于稳定结构,故填A。
(3)
由图可知,图3中的微粒的质子数为38,属于锶元素,核外电子数为36,是锶原子失去2个电子形成的带2个单位的正电荷的锶离子,其离子符号为,故填Sr2+。
3、
(1) 原子核外都有3个电子层 该周期中的原子从左到右,最外层电子数从1到8逐渐增加
(2) 质子数 最外层电子数
(3)Na+(或Mg2+、Al3+)
【解析】
(1)
同一周期中,各原子的核外电子层数相同,同一周期中的原子从左到右,最外层电子数从1到8逐渐增加。
(2)
元素是具有相同核电核数的一类原子的总称,硫元素和氧元素最本质的区别是它们原子核内的质子数相同;最外层电子数决定元素的化学性质,硫元素和氧元素具有相似的化学性质,原因是它们原子的最外层电子数相同。
(3)
阳离子带正电,氖原子的原子核外有2个电子层,一共有10个电子,故核外电子数是10个电子的带正电的阳离子可能是Na+(或Mg2+、Al3+)。
4、
(1) 13 金属
(2)B
(3)DE
【解析】
(1)
D示意图中,最外层电子数为3,则D属于原子,原子中核外电子数=原子质子数,,,质子数为13的元素为铝元素,铝元素属于金属元素;
(2)
原子中,原子核外电子层数=其所在的周期数;
A、原子核外电子层数=1,在元素周期表中处于第一周期;
B、原子核外电子层数=2,在元素周期表中处于第二周期;
C、C粒子对应的原子核外电子层数=3,在元素周期表中处于第三周期;
D、原子核外电子层数=3,在元素周期表中处于第三周期;
E、原子核外电子层数=3,在元素周期表中处于第三周期;
A、B、C、D、E中,在周期表中处于第二周期的是B;
(3)
最外层电子数小于4,在化学反应中容易失去电子,最外层电子数大于4,在化学反应中容易得到电子,B、D、E中,在化学反应中容易失去电子的是DE。
5、
(1)分子
(2)分子、原子、离子
(3)质子、中子、电子
(4)离子、质子、电子
【分析】
(1)
化学反应的本质是分子分裂成原子,原子重新组合成新的分子,所以化学变化中一定能改变的是分子,故填:分子;
(2)
分子、原子、离子都是构成物质的基本微粒,所以可以直接构成物质的粒子是分子、原子、离子,故填:分子、原子、离子;
(3)
原子是由质子、中子、电子构成,可知构成原子的是质子、中子、电子,故填:质子、中子、电子;
(4)
质子带正电,电子带负电,阴离子带负电荷,阳离子带正电荷,所以带电荷的粒子是离子、质子、电子,故填:离子、质子、电子。
三、计算题
1、解:设每个碳原子质量是aKg,则某原子质量为2aKg.
某原子的相对原子质量为:
答:该原子的相对原子质量是24。
【详解】
根据相对原子质量的定义进行计算,即以C-12原子质量的十二分之一作标准,其他原子质量与其相比较所得值,就是这种原子的相对原子质量,详解见答案。
2、
(1)12
(2)解:设一个钠原子的质量为x。
由题可知:碳-12原子的质量是1.993×10-26kg,钠原子的相对原子质量为23,有:
钠原子的相对原子质量为,
x=3.820×10-26kg
答:一个钠原子的质量为3.820×10-26kg。
(3)解:铁原子的相对原子质量为
答:铁原子的相对原子质量为56。
【分析】
(1)
根据相对原子质量=中子数+质子数,钠原子的相对原子质量为23,质子数为11,所以钠原子核内中子数=23-11=12,故填:12;
(2)
见答案(2)
(3)
见答案(3)
【点睛】
相对原子质量的理解并会计算某原子的相对原子质量。
3、
(1)6
(2) 111 13
(3)铼元素一个原子的质量为: 186×=3.1×10-25kg
答:铼元素一个原子的质量为:3.1×10-25kg。
【分析】
(1)
周期数等于核外电子层数,故铼元素位于元素周期表的第6周期,故填:6。
(2)
铼原子的中子数为186-75=111,x=75-2-8-18-32-2=13,故填:111;13。
(3)
见答案
四、实验探究
1、分子在不断地运动 取一烧杯,加入适量的水,再滴入几滴酚酞溶液,置于桌面上静置一段时间 溶液不变色 猜想1不成立 取一烧杯,加入适量的水,再滴入几滴酚酞溶液,用大烧杯罩住 溶液不变色 猜想2不成立
【详解】
进行实验:B中溶液逐渐变为红色,是因为氨水具有挥发性,氨气分子运动到A烧杯中溶于水形成氨水,氨水显碱性,说明了分子在不断地运动;
再次实验:证明一个猜想可采用对比实验,因此:
实验操作 实验现象 实验结论
取一烧杯,加入适量的水,再滴入几滴酚酞溶液,置于桌面上静置一段时间 溶液不变色 猜想1不成立
或
实验操作 实验现象 实验结论
取一烧杯,加入适量的水,再滴入几滴酚酞溶液,用大烧杯罩住 溶液不变色 猜想2不成立
2、A烧杯没有现象,B烧杯中液体变红 蒸馏水不能使酚酞试液变红,浓氨水能使酚酞试液变红 胶头滴管 浓氨水 滤纸条上的酚酞试液从右往左依次变红 铝原子的相对原子质量==27
【详解】
(1)A烧杯没有现象,B烧杯中液体变红,因为浓氨水显碱性,酚酞遇碱性溶液变红,蒸馏水显中性,酚酞与酸性和中性溶液不变色;蒸馏水不能使酚酞试液变红,浓氨水能使酚酞试液变红;
(2)取用少量液体时使用胶头滴管;棉花上滴加的物质是浓氨水,浓氨水有挥发性,滤纸条上的酚酞试液从右往左依次变红;
铝原子的相对原子质量==27
考试时间:90分钟;命题人:化学教研组
考生注意:
1、本卷分第I卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分,考试时间90分钟
2、答卷前,考生务必用0.5毫米黑色签字笔将自己的姓名、班级填写在试卷规定位置上
3、答案必须写在试卷各个题目指定区域内相应的位置,如需改动,先划掉原来的答案,然后再写上新的答案;不准使用涂改液、胶带纸、修正带,不按以上要求作答的答案无效。
第I卷(选择题 30分)
一、单选题(10小题,每小题3分,共计30分)
1、用分子、原子的知识对下列现象进行解释,正确的是
A.水凝结成冰,说明水分子发生改变,产生了新的分子
B.大块石头碎成小块石头,说明分子可以被分裂
C.水银温度计受热汞柱上升,说明汞原子受热体积变大
D.墙内开花墙外香,说明分子在不断运动
2、下列相关实验现象及生活现象的描述中,错误的是
A.红磷在空气中燃烧,产生大量的白烟
B.铁片在空气中剧烈燃烧,火星四射
C.食物腐烂----分子并没有停止运动
D.湿衣服在阳光下比在阴凉处干得快----温度高,分子运动快
3、搭载北斗三号卫星导航系统的手机,在没有网络信号的情况下也可以精准导航,其中高精度铷原子钟起了重要作用。铷在元素周期表中的信息如图所示,下列说法正确的是
A.铷属于非金属元素 B.铷的元素符号为Rb
C.铷原子的中子数是37 D.铷的相对原子质量是85.47g
4、如图为四种原子的结构示意图,其中化学性质相似的一组是
A.①和② B.①和③ C.②和③ D.③和④
5、用分子的观点解释下列现象,错误的是
A.热胀冷缩——分子大小随温度变化改变
B.花香四溢——分子不停地运动
C.1滴水中大约有个水分子——分子很小
D.冰和水化学性质相同———分子构成相同
6、磷元素对生命活动具有重要意义,其相关信息如图所示。下列有关说法正确的是
A.属于金属元素 B.磷原子核外有16个电子
C.相对原子质量为30.97g D.每个磷原子中有16个中子
7、下列有关镍元素的说法不正确的是
A.原子序数是28 B.原子核内质子数为30
C.元素符号是Ni D.相对原子质量为58.69
8、下列微粒结构示意图中,表示阴离子的是
A. B. C. D.
9、钟的熔点高、抗腐蚀性强,是制造现代航空发动机关键部件的重要材料。如图是钢元素在元素周期表中的部分信息。下列关于铢元素的说法错误的是
A.元素符号为Re B.属于金属元素
C.原子核外有75个电子 D.相对原子质量为186.2g
10、疫情期间,教室喷洒“84消毒液”进行消毒时,可闻到刺鼻的气味,说明了
A.分子数目变大 B.分子之间有间隔
C.分子在不断运动 D.反应生成新物质
第Ⅱ卷(非选择题 70分)
二、填空题(5小题,每小题5分,共计25分)
1、结合下列微粒结构示意图和氦元素的元素周期表信息回答以下问题。
(1)在A-E五个结构示意图中,达到稳定结构原子的是___________(用序号填空,下同);属于同种元素的是___________。
(2)氦的相对原子质量为___________。
(3)上述元素在周期表中处于同一周期是___________(用序号填空)
(4)碳-12原子质量为a,某原子的质量为b,则该原子的相对原子质量是___________。
2、下图是一些元素的粒子结构示意图和在元素周期表中的信息,请回答下列问题:
(1)锶元素的原子序数为______。
(2)锶元素它的原子的化学性质与A、B、C、D中的______(填序号,下同)相似,具有稳定结构的原子是______。
(3)图3所表示的粒子的化学符号是______。
3、核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题。
(1)在第三周期中,各原子结构的共同之处是___________ ;该周期中,各原子核外电子排布的变化规律是___________ 。
(2)硫元素和氧元素最本质的区别是它们原子的___________不同;硫元素和氧元素具有相似的化学性质,原因是它们原子的___________ 相同。
(3)写出核外电子排布与氖原子相同的阳离子___________ 。
4、下列是几种粒子的结构示意图,依图回答下列问题:
(1)D示意图中,x=__________,其所示元素属于__________(金属/非金属)元素。
(2)A、B、C、D、E中,在周期表中处于第二周期的是__________。
(3)B、D、E中,在化学反应中容易失去电子的是__________。
5、将①分子②原子③离子④质子⑤中子⑥电子等粒子名称填入下列空格中:
(1)化学反应中一定发生改变的是____________;
(2)构成物质的基本粒子是____________;
(3)构成原子的是__________;
(4)带电的粒子有___________。
三、计算题(3小题,每小题7分,共计21分)
1、某原子的质量是碳12原子质量的两倍。求这种原子的相对原子质量。
2、已知碳-12原子的质量是1.993×10-26kg,钠原子的相对原子质量为23,铁原子的质量为9.288×10-26kg。请填空或进行计算:
(注:第2、3小问写出计算过程并对钠原子质量计算结果保留三位小数)
(1)钠原子核内有____________个中子。
(2)一个钠原子的质量为多少?
(3)铁原子的相对原子质量是多少?
3、王者归“铼”,我国利用新技术发现并提纯了超级金属铼,制造出航空发动机核心部件。铼元素的部分信息如图。已知作为相对原子质量标准的一种碳原子的质量为2.0×10-26kg。
(1)铼元素位于元素周期表的第_________(填数字)周期。
(2)铼原子的中子数为________,x=_________。
(3)求铼元素一个原子的质量(写出简单的计算过程)。
四、实验探究(2小题,每小题12分,共计24分)
1、学习小组的同学在探究分子的性质,请你参与并完成相关的问题。
(进行实验)(如图)观察到的现象是B中溶液逐渐变为红色,结论为_______
(交流与讨论)有同学对B中溶液的变红提出了以下猜想:
猜想1:B中溶液变红也可能是B中溶液放置一段时间后,自动就会变红;
猜想2:大烧杯内壁附着的某种物质挥发出来使B中溶液变红。
(再次实验)请你选择其中一个猜想并设计实验进行验证。
实验操作 实验现象 实验结论
___________ ______ __________ ____
2、 “比较出真知”,比较是科学实验中常用的一种方法。小刚同学利用比较的方法探究得出了分子在不停地运动的结论。下面是他设计的实验:在第一步中他所观察到的现象是___;得出的结论是___.
进行第二步实验时,还应用到的一种仪器名称是___,他在滤纸上每间隔一段距离滴加一滴酚酞试液,那么,棉花上滴加的物质是___。放置一段时间后,他观察到的现象是____,由此,说明了氨分子在不停地运动。
(反思)分子和原子质量都很小,因此国际上采用相对原子质量的方式来进行相关计算。(已知作为相对原子质量标准的一种碳原子的质量为1.993×10-23kg)小华查阅资料发现了一个铝原子的质量为4.482x10-26kg请帮他计算铝原子的相对原子质量____
-参考答案-
一、单选题
1、D
【详解】
A、水凝结成冰,冰和水都是由水分子构成的,说明水分子不发生改变,没有产生了新的分子,选项A错误;
B、大块石头碎成小块石头,只是形状发生了改变,没有新物质生成,大块石头和小块石头中的分子没有改变,选项B错误;
C、水银是金属汞,是由汞原子直接构成的,温度计中的水银球受热体积膨胀是利用了汞原子的间隔受热变大,而不是体积变大,选项C错误;
D、墙内开花墙外香是因为分子在不停运动,向四周扩散,花香的分子运动到空气中,进入人们的鼻孔,闻到香味,选项D正确。
故选:D。
2、B
【详解】
A.红磷在空气中燃烧,产生大量的白烟,选项说法正确。
B.铁片在氧气中剧烈燃烧,火星四射,在空气中发红光,不燃烧,选项说法错误。
C.分子在永不停息的做无规则运动,食物腐烂后,分子并没有停止运动,选项说法正确。
D.温度越高,分子运动越快,因此湿衣服在阳光下比在阴凉处干得快,选项说法正确。
故选:B。
3、B
【分析】
元素周期表信息图中,元素名称的左上角的数字为元素的原子序数,右上角为元素符号,中间的汉字表示元素名称,下边是元素的相对原子质量。
【详解】
A、铷元素汉字名称中,有“钅”字旁可知,该元素属于金属元素,故选项错误;
B、伽的元素符号是Rb,故选项正确;
C、原子中,原子序数=质子数=核外电子数,故核外电子数为37,中子数不是37,故选项错误;
D、相对原子质量的单位是“1”,不是“g”,铷的相对原子质量为85. 47,故选项错误。
故选:B。
4、B
【详解】
原子最外层电子数相同,化学性质相似。最外层8个电子是相对稳定结构。但第一层就是最外层的,2个电子就是相对稳定结构。图中①③都是相对稳定结构。
综上所述:选择B。
5、A
【详解】
A、热胀冷缩是由于分子之间的间隔随着温度的变化而发生了变化,分子本身的大小不变,此选项表述不正确;
B、花香四溢是由于分子在不停地运动,花香分子运动到了鼻腔中,此选项表述正确;
C、1滴水中大约有 1.67×1021 个水分子,说明分子很小,此选项表述正确;
D、由分子构成的物质,分子是保持物质化学性质的最小微粒,冰和水化学性质相同是由于分子构成相同,此选项表述正确。
故选A。
6、D
【详解】
A:磷是“石”字旁,属于非金属元素。A错。
B:原子中核外电子数等于质子数,磷原子核外有15个电子。B错。
C:元素名称下面的数字表示相对原子质量,磷元素的相对原子质量为30.97。C错。
D:每个磷原子中有15个质子,相对原子质量为30.97≈31,所以每个磷原子中有31-15=16个中子。正确。
综上所述:选择D。
7、B
【详解】
A、根据元素周期表的信息可知,左上角的数字表示原子序数,镍的原子序数为28,故选项说法正确;
B、原子中原子序数=质子数=28,故选项说法不正确;
C、根据元素周期表的信息可知,右上角的字母表示元素符号,镍的元素符号是Ni,故选项说法正确;
D、根据元素周期表的信息可知,元素名称下方的数字表示相对原子质量,镍的相对原子质量为58.69,故选项说法正确。
故选B。
8、A
【分析】
质子带正电,电子带负电。
原子:核内质子数=核外电子数
阳离子:核内质子数>核外电子数
阴离子:核内质子数<核外电子数
【详解】
A. 核内质子数(8)<核外电子数(10),所以为阴离子。
B. 核内质子数(10)=核外电子数(10),所以为原子。
C. 核内质子数(11)>核外电子数(10),所以为阳离子。
D. 核内质子数(13)=核外电子数(13),所以为原子。
故选:A
9、D
【详解】
A、根据图示可知铼元素的元素符号为Re,故选项正确;
B、元素名称中带“钅”旁,所以该元素为金属元素,故选项正确;
C、原子序数=核电荷数=核外电子数,所以其原子核外有75个电子,故选项正确;
D、相对原子质量单位是“1”,不是“克",故选项错误。
故选D
【点睛】
10、C
【详解】
A、教室喷洒“84消毒液”进行消毒时,可闻到刺鼻的气味,是因为消毒水中含有特殊气味的分子运动到了空气中,,向四周扩散,使人们闻到刺鼻的气味,但分子数目不变,故选项不符合题意;
B、教室喷洒“84消毒液”进行消毒时,可闻到刺鼻的气味,与分子之间有间隔无关,故选项不符合题意;
C、教室喷洒“84消毒液”进行消毒时,可闻到刺鼻的气味,是因为消毒水中含有特殊气味的分子运动到了空气中,向四周扩散,使人们闻到刺鼻的气味,故选项符合题意;
D、教室喷洒“84消毒液”,没有新物质生成,属于物理变化,故选项不符合题意。
故选C。
二、填空题
1、
(1) AC DE
(2)4.00
(3)BC
(4)
【解析】
(1)
稳定结构即最外层电子数是8(只有一个电子层时,最外层是2)的微粒,所以ACD均是稳定结构,但D的质子数不等于电子数,所以D不是原子;同种元素质子数一定相同,DE质子数均为12,所以DE是同种元素,故填:AC;DE。
(2)
氦元素的元素符号为He,元素名称下面的数字表示相对原子质量,该元素的相对原子质量是4.00,故填:4.00。
(3)
原子的核外电子层数相同的位于同一周期,ABCE的质子数等于核外电子数,为原子,其中BC的电子层数相同,为同一周期,故填:BC。
(4)
相对原子质量,等于原子实际质量和碳12原子质量十二分之一的比值=,故填:。
2、
(1)38
(2) BD A
(3)Sr2+
【解析】
(1)
元素信息图中,左上角的数字就是元素的原子序数,由图可知,锶元素的原子序数为38,故填38。
(2)
由图可知,锶原子的最外层电子数为2,A、B、C、D四种微粒中,B、D的最外层电子数为2,在化学反应中溶液失去电子,与锶元素的原子的化学性质相同,虽然A微粒的原子最外层电子数也为2,但该原子既不容易失去电子,也不容易得到电子,与锶原子的化学性质不同,故填BD;
A原子的核外只有1个电子层,且该电子层的电子数为2,属于稳定结构,故填A。
(3)
由图可知,图3中的微粒的质子数为38,属于锶元素,核外电子数为36,是锶原子失去2个电子形成的带2个单位的正电荷的锶离子,其离子符号为,故填Sr2+。
3、
(1) 原子核外都有3个电子层 该周期中的原子从左到右,最外层电子数从1到8逐渐增加
(2) 质子数 最外层电子数
(3)Na+(或Mg2+、Al3+)
【解析】
(1)
同一周期中,各原子的核外电子层数相同,同一周期中的原子从左到右,最外层电子数从1到8逐渐增加。
(2)
元素是具有相同核电核数的一类原子的总称,硫元素和氧元素最本质的区别是它们原子核内的质子数相同;最外层电子数决定元素的化学性质,硫元素和氧元素具有相似的化学性质,原因是它们原子的最外层电子数相同。
(3)
阳离子带正电,氖原子的原子核外有2个电子层,一共有10个电子,故核外电子数是10个电子的带正电的阳离子可能是Na+(或Mg2+、Al3+)。
4、
(1) 13 金属
(2)B
(3)DE
【解析】
(1)
D示意图中,最外层电子数为3,则D属于原子,原子中核外电子数=原子质子数,,,质子数为13的元素为铝元素,铝元素属于金属元素;
(2)
原子中,原子核外电子层数=其所在的周期数;
A、原子核外电子层数=1,在元素周期表中处于第一周期;
B、原子核外电子层数=2,在元素周期表中处于第二周期;
C、C粒子对应的原子核外电子层数=3,在元素周期表中处于第三周期;
D、原子核外电子层数=3,在元素周期表中处于第三周期;
E、原子核外电子层数=3,在元素周期表中处于第三周期;
A、B、C、D、E中,在周期表中处于第二周期的是B;
(3)
最外层电子数小于4,在化学反应中容易失去电子,最外层电子数大于4,在化学反应中容易得到电子,B、D、E中,在化学反应中容易失去电子的是DE。
5、
(1)分子
(2)分子、原子、离子
(3)质子、中子、电子
(4)离子、质子、电子
【分析】
(1)
化学反应的本质是分子分裂成原子,原子重新组合成新的分子,所以化学变化中一定能改变的是分子,故填:分子;
(2)
分子、原子、离子都是构成物质的基本微粒,所以可以直接构成物质的粒子是分子、原子、离子,故填:分子、原子、离子;
(3)
原子是由质子、中子、电子构成,可知构成原子的是质子、中子、电子,故填:质子、中子、电子;
(4)
质子带正电,电子带负电,阴离子带负电荷,阳离子带正电荷,所以带电荷的粒子是离子、质子、电子,故填:离子、质子、电子。
三、计算题
1、解:设每个碳原子质量是aKg,则某原子质量为2aKg.
某原子的相对原子质量为:
答:该原子的相对原子质量是24。
【详解】
根据相对原子质量的定义进行计算,即以C-12原子质量的十二分之一作标准,其他原子质量与其相比较所得值,就是这种原子的相对原子质量,详解见答案。
2、
(1)12
(2)解:设一个钠原子的质量为x。
由题可知:碳-12原子的质量是1.993×10-26kg,钠原子的相对原子质量为23,有:
钠原子的相对原子质量为,
x=3.820×10-26kg
答:一个钠原子的质量为3.820×10-26kg。
(3)解:铁原子的相对原子质量为
答:铁原子的相对原子质量为56。
【分析】
(1)
根据相对原子质量=中子数+质子数,钠原子的相对原子质量为23,质子数为11,所以钠原子核内中子数=23-11=12,故填:12;
(2)
见答案(2)
(3)
见答案(3)
【点睛】
相对原子质量的理解并会计算某原子的相对原子质量。
3、
(1)6
(2) 111 13
(3)铼元素一个原子的质量为: 186×=3.1×10-25kg
答:铼元素一个原子的质量为:3.1×10-25kg。
【分析】
(1)
周期数等于核外电子层数,故铼元素位于元素周期表的第6周期,故填:6。
(2)
铼原子的中子数为186-75=111,x=75-2-8-18-32-2=13,故填:111;13。
(3)
见答案
四、实验探究
1、分子在不断地运动 取一烧杯,加入适量的水,再滴入几滴酚酞溶液,置于桌面上静置一段时间 溶液不变色 猜想1不成立 取一烧杯,加入适量的水,再滴入几滴酚酞溶液,用大烧杯罩住 溶液不变色 猜想2不成立
【详解】
进行实验:B中溶液逐渐变为红色,是因为氨水具有挥发性,氨气分子运动到A烧杯中溶于水形成氨水,氨水显碱性,说明了分子在不断地运动;
再次实验:证明一个猜想可采用对比实验,因此:
实验操作 实验现象 实验结论
取一烧杯,加入适量的水,再滴入几滴酚酞溶液,置于桌面上静置一段时间 溶液不变色 猜想1不成立
或
实验操作 实验现象 实验结论
取一烧杯,加入适量的水,再滴入几滴酚酞溶液,用大烧杯罩住 溶液不变色 猜想2不成立
2、A烧杯没有现象,B烧杯中液体变红 蒸馏水不能使酚酞试液变红,浓氨水能使酚酞试液变红 胶头滴管 浓氨水 滤纸条上的酚酞试液从右往左依次变红 铝原子的相对原子质量==27
【详解】
(1)A烧杯没有现象,B烧杯中液体变红,因为浓氨水显碱性,酚酞遇碱性溶液变红,蒸馏水显中性,酚酞与酸性和中性溶液不变色;蒸馏水不能使酚酞试液变红,浓氨水能使酚酞试液变红;
(2)取用少量液体时使用胶头滴管;棉花上滴加的物质是浓氨水,浓氨水有挥发性,滤纸条上的酚酞试液从右往左依次变红;
铝原子的相对原子质量==27
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
