第九单元溶液过关训练题-2021-2022学年九年级化学人教版下册(word版有答案)
文档属性
| 名称 | 第九单元溶液过关训练题-2021-2022学年九年级化学人教版下册(word版有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 89.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-03 00:00:00 | ||
图片预览

文档简介
2022年第九单元《溶液》过关训练题
附相对原子质量:H-1 C-12 N-14 O-16
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1、下列物质与水混合,不可能形成溶液的是( )
A.胆矾 B.纯碱 C.汽油 D.白醋
2、下列去“污”的方法中,利用了乳化原理的是( )
A.用洗涤剂除去餐具上的油脂 B.用酒精除去附着在试管内壁的碘
C.用汽油除去衣物上的油污 D.用热水除去附着在烧杯底部的硝酸钾
3、2021年7月,新冠病毒的变异体德尔塔病毒在整个欧洲大规模传播。75%的酒精可杀灭新冠病毒,酒精溶液中的溶剂是( )
A.乙醇 B.白醋 C.水 D.食盐
4、水是一种最常用的溶剂。下列做法或说法正确的是( )
A.用絮凝剂明矾可降低水的硬度
B.硝酸铵溶于水制成的冰袋可给高烧病人降温
C.天然水经过自然沉降、过滤、吸附,即得纯水
D.用 150mL 酒精和 50mL 蒸馏水混合配制成 200mL 的 75%的医用酒精
5、下列物质加入水中,能形成溶液并且温度不会发生明显改变的是( )
A.硝酸铵 B.牛奶 C.氢氧化钠 D.氯化钠
6、配制一定溶质质量分数的溶液,下列仪器不需要的是( )
A.量筒 B.胶头滴管
C.烧杯 D.漏斗
7、啤酒内溶有一定量的二氧化碳气体,打开瓶盖时,你会发现啤酒会喷出来。喝了啤酒后又会常常打嗝,这说明气体在水中的溶解度与压强和温度有关。下列关于气体溶解度的说法正确的是( )
A.压强减小,气体溶解度增大 B.压强增大,气体溶解度减小
C.温度升高,气体溶解度减小 D.温度降低,气体溶解度减小
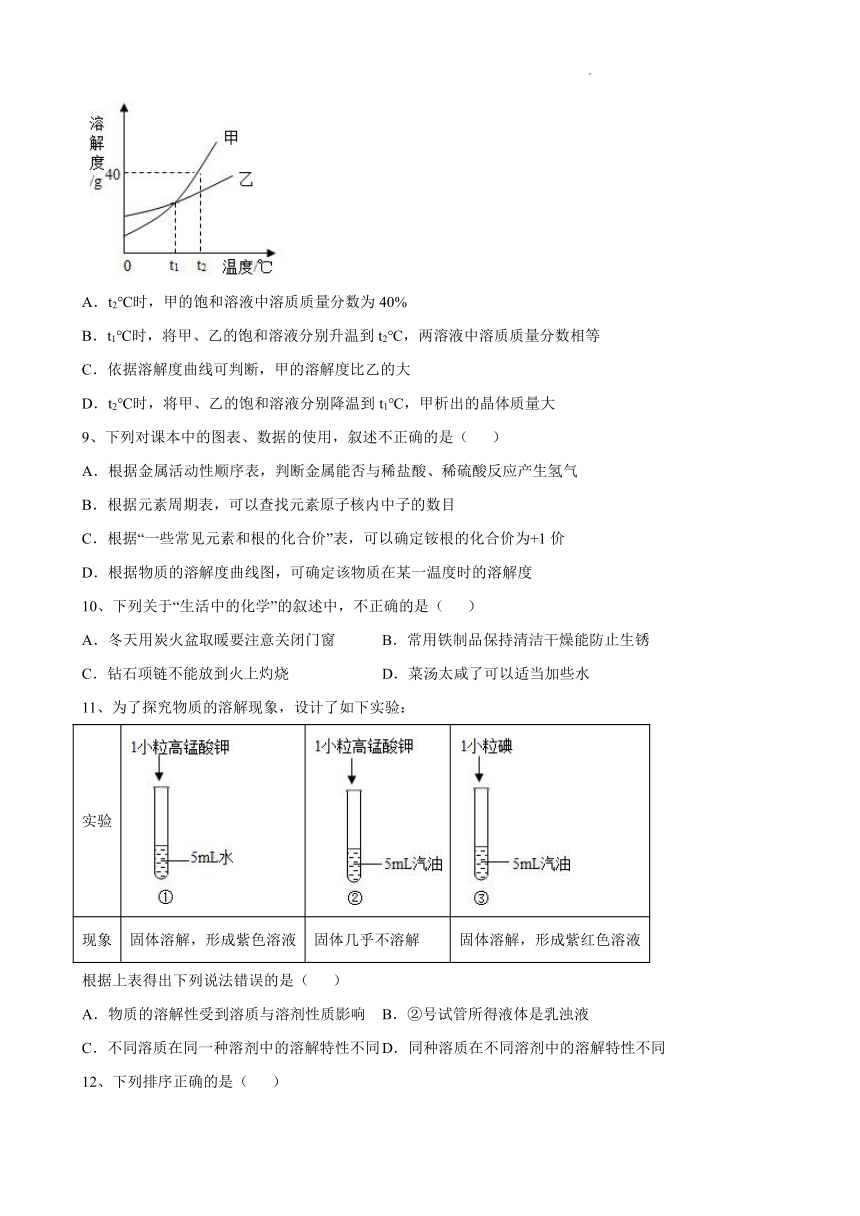
8、甲、乙的溶解度曲线如图所示(不考虑水的变化),下列说法正确的是( )
A.t2℃时,甲的饱和溶液中溶质质量分数为40%
B.t1℃时,将甲、乙的饱和溶液分别升温到t2℃,两溶液中溶质质量分数相等
C.依据溶解度曲线可判断,甲的溶解度比乙的大
D.t2℃时,将甲、乙的饱和溶液分别降温到t1℃,甲析出的晶体质量大
9、下列对课本中的图表、数据的使用,叙述不正确的是( )
A.根据金属活动性顺序表,判断金属能否与稀盐酸、稀硫酸反应产生氢气
B.根据元素周期表,可以查找元素原子核内中子的数目
C.根据“一些常见元素和根的化合价”表,可以确定铵根的化合价为+1价
D.根据物质的溶解度曲线图,可确定该物质在某一温度时的溶解度
10、下列关于“生活中的化学”的叙述中,不正确的是( )
A.冬天用炭火盆取暖要注意关闭门窗 B.常用铁制品保持清洁干燥能防止生锈
C.钻石项链不能放到火上灼烧 D.菜汤太咸了可以适当加些水
11、为了探究物质的溶解现象,设计了如下实验:
实验
现象 固体溶解,形成紫色溶液 固体几乎不溶解 固体溶解,形成紫红色溶液
根据上表得出下列说法错误的是( )
A.物质的溶解性受到溶质与溶剂性质影响 B.②号试管所得液体是乳浊液
C.不同溶质在同一种溶剂中的溶解特性不同 D.同种溶质在不同溶剂中的溶解特性不同
12、下列排序正确的是( )
A.溶解时放出的热量: B.氮元素的化合价:
C.地壳中元素含量: D.金属活动性顺序:
二、本大题包括5小题,共28分
13、阅读下列短文,回答问题。
“深海一号”能源站是由我国自主研发建造的全球首座10万吨级深水半潜式生产储油平台。2021年6月25日,该平台正式投产,标志着中国从装备技术到勘探开发能力全面实现从300来到1500米超深水的跨越。2022年2月13日,中国海洋石油集团有限公司对外宣布,该平台2021年6月25日正式投产以来,累计生产天然气超10亿立方米。在保供季为海南自贸港和粤港澳大湾区建设提供了重要清洁能源来源。
(1)天然气属于_______(填“可再生”或“不可再生”)能源,天然气的主要成分是甲烷(CH4),甲烷是由________(填“分子”、“原子”或“离子”)构成;已知甲烷中氢元素的化合价是+1,则碳元素的化合价是________。
(2)天然气之所以被称为清洁能源,是因为它完全燃烧时不产生污染物。请写出甲烷完全燃烧时的化学方程式________。
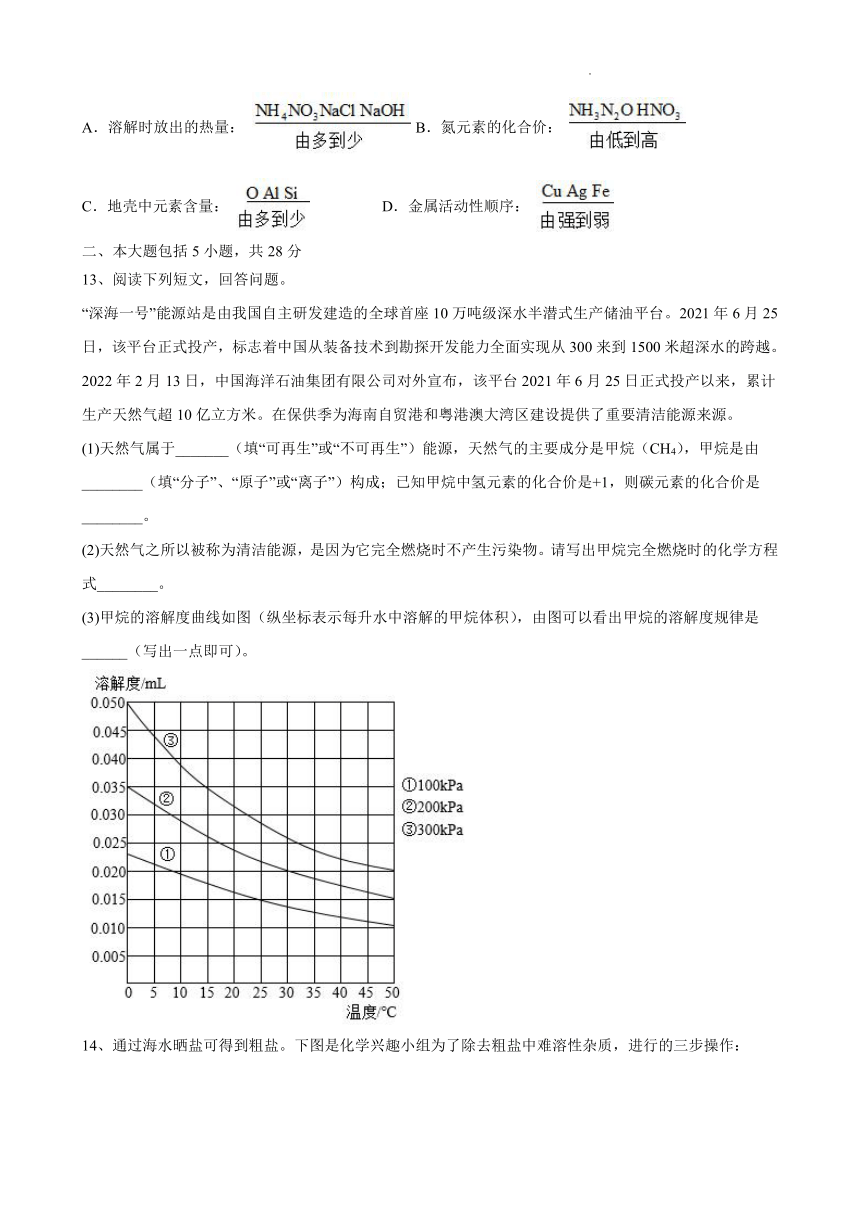
(3)甲烷的溶解度曲线如图(纵坐标表示每升水中溶解的甲烷体积),由图可以看出甲烷的溶解度规律是______(写出一点即可)。
14、通过海水晒盐可得到粗盐。下图是化学兴趣小组为了除去粗盐中难溶性杂质,进行的三步操作:
(1)三步操作的正确顺序是_________(填字母)。
(2)上述A、B操作中均使用了玻璃棒进行搅拌,其目的分别是:A:_________。B:_________。
(3)经过C操作后,发现滤液仍浑浊,可能的原因是_________(只写一条)。
(4)现有一瓶蒸馏水和一瓶稀氯化钠溶液,请用适当的化学方法把它们鉴别开,并完成实验报告。
实验步骤 实验现象 实验结论
_________。 _________。 _________。
15、工业上用电解食盐水的方法制取浓盐酸,分析下图回答有关问题。已知:氯气(Cl2)常温下为气体。
(1)写出反应①的化学方程式______;
(2)反应②的化学反应类型是______反应;
(3)制得的浓盐酸溶质质量分数为 35%(密度 1.15g/mL),要配制 70g 溶质质量分数为 10%的稀盐酸(不考虑挥发):
①需向盛有浓盐酸的烧杯中加______克水(水的密度 1g/mL);
②配制过程中需要用到的仪器有烧杯、量筒和______。
16、同学们在实验室用下图装置制取氧气。
(1)加热高锰酸钾时,试管口略向下倾斜的原因是 ______ 。
实验后,同学们发现沾有高锰酸钾的白抹布洗完晾干后变为棕褐色。
【查阅资料】草酸溶液能将棕褐色物质除去。
【提出问题】哪些因素能加快草酸除去棕褐色物质的速率?
【进行实验】
将均匀染有棕褐色的抹布剪成大小相同的小布条进行实验
实验 编号 实验1 20℃ 水 实验2 20℃ 0.5%草酸溶液 实验3 20℃ 0.25%草酸溶液 实验4 20℃ 0.125%草酸溶液 实验5 30℃ 0.25%草酸溶液 实验6 40℃ 0.25%草酸溶液
现象 颜色 没有褪去 70秒后 颜色褪去 98秒后 颜色褪去 150秒后 颜色褪去 51秒后 颜色褪去 40秒后 颜色褪去
【解释与结论】
(2)配制200g溶质质量分数为 0.5%的草酸溶液,需要草酸的质量为 ______ 。
(3)实验1的目的是 ______ 。
(4)证明升高温度能加快草酸除去棕褐色物质的速率,需要对比 ______ (填实验序号)。
(5)由实验2、3、4可以得出的结论是 ______ 。
【反思与评价】
(6)实验后,同学们查资料得知抹布上的棕褐色物质为二氧化锰,请你设计实验方案进行验证 ______ 。
17、某化学兴趣小组欲测定化学实验室内存放较久的过氧化氢溶液的溶质质量分数。他们取出该溶液68g,加入适量二氧化锰,生成氧气的质量与反应时间的关系如图所示。
(1)完全反应后生成氧气的质量为___________g。
(2)计算该过氧化氢溶液的溶质质量分数。(要求写出完整步骤)
参考答案
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1、C 2、A 3、C 4、B 5、D 6、D 7、C 8、B 9、B 10、A 11、B 12、B
二、本大题包括5小题,共28分
13、答案:(1) 不可再生 分子 -4
(2) CH4+2O2CO2+2H2O
(3)气压一定时,温度越高,甲烷的溶解度越小(或温度一定时,气压越大,甲烷的溶解度越大)
14、答案:(1)ACB
(2) 搅拌,加快溶解速率 搅拌,防止局部温度过高,造成液滴飞溅
(3)滤纸破损(或接滤液的烧杯不干净等)
(4) 各取两种溶液少许进行蒸干 一种有少量白色残留固体,另一种无残留固体 有固体残留的是氯化钠,无固体残留的是蒸馏水
15、答案:(1) 2NaCl+2H2O2NaOH+H2↑+Cl2↑
(2)化合
(3) 50 玻璃棒和胶头滴管
16、答案:(1)防止冷凝水回流,试管炸裂 (2)1g (3)空白对照,证明水不能使棕褐色布条褪色
(4)3、5、6 (5)其他条件相同时,草酸浓度增大能加快草酸除去棕褐色物质的速率
(6)取棕褐色布条放入试管中,加入过氧化氢溶液,观察是否产生气泡。或取少量二氧化锰粉末于试管中,加入草酸溶液,观察黑色固体是否逐渐消失
17.(1)1.6
(2)解:设68g过氧化氢溶液中含过氧化氢的质量为x。
该过氧化氢溶液的溶质质量分数
答:该过氧化氢溶液的溶质质量分数为5%。
附相对原子质量:H-1 C-12 N-14 O-16
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1、下列物质与水混合,不可能形成溶液的是( )
A.胆矾 B.纯碱 C.汽油 D.白醋
2、下列去“污”的方法中,利用了乳化原理的是( )
A.用洗涤剂除去餐具上的油脂 B.用酒精除去附着在试管内壁的碘
C.用汽油除去衣物上的油污 D.用热水除去附着在烧杯底部的硝酸钾
3、2021年7月,新冠病毒的变异体德尔塔病毒在整个欧洲大规模传播。75%的酒精可杀灭新冠病毒,酒精溶液中的溶剂是( )
A.乙醇 B.白醋 C.水 D.食盐
4、水是一种最常用的溶剂。下列做法或说法正确的是( )
A.用絮凝剂明矾可降低水的硬度
B.硝酸铵溶于水制成的冰袋可给高烧病人降温
C.天然水经过自然沉降、过滤、吸附,即得纯水
D.用 150mL 酒精和 50mL 蒸馏水混合配制成 200mL 的 75%的医用酒精
5、下列物质加入水中,能形成溶液并且温度不会发生明显改变的是( )
A.硝酸铵 B.牛奶 C.氢氧化钠 D.氯化钠
6、配制一定溶质质量分数的溶液,下列仪器不需要的是( )
A.量筒 B.胶头滴管
C.烧杯 D.漏斗
7、啤酒内溶有一定量的二氧化碳气体,打开瓶盖时,你会发现啤酒会喷出来。喝了啤酒后又会常常打嗝,这说明气体在水中的溶解度与压强和温度有关。下列关于气体溶解度的说法正确的是( )
A.压强减小,气体溶解度增大 B.压强增大,气体溶解度减小
C.温度升高,气体溶解度减小 D.温度降低,气体溶解度减小
8、甲、乙的溶解度曲线如图所示(不考虑水的变化),下列说法正确的是( )
A.t2℃时,甲的饱和溶液中溶质质量分数为40%
B.t1℃时,将甲、乙的饱和溶液分别升温到t2℃,两溶液中溶质质量分数相等
C.依据溶解度曲线可判断,甲的溶解度比乙的大
D.t2℃时,将甲、乙的饱和溶液分别降温到t1℃,甲析出的晶体质量大
9、下列对课本中的图表、数据的使用,叙述不正确的是( )
A.根据金属活动性顺序表,判断金属能否与稀盐酸、稀硫酸反应产生氢气
B.根据元素周期表,可以查找元素原子核内中子的数目
C.根据“一些常见元素和根的化合价”表,可以确定铵根的化合价为+1价
D.根据物质的溶解度曲线图,可确定该物质在某一温度时的溶解度
10、下列关于“生活中的化学”的叙述中,不正确的是( )
A.冬天用炭火盆取暖要注意关闭门窗 B.常用铁制品保持清洁干燥能防止生锈
C.钻石项链不能放到火上灼烧 D.菜汤太咸了可以适当加些水
11、为了探究物质的溶解现象,设计了如下实验:
实验
现象 固体溶解,形成紫色溶液 固体几乎不溶解 固体溶解,形成紫红色溶液
根据上表得出下列说法错误的是( )
A.物质的溶解性受到溶质与溶剂性质影响 B.②号试管所得液体是乳浊液
C.不同溶质在同一种溶剂中的溶解特性不同 D.同种溶质在不同溶剂中的溶解特性不同
12、下列排序正确的是( )
A.溶解时放出的热量: B.氮元素的化合价:
C.地壳中元素含量: D.金属活动性顺序:
二、本大题包括5小题,共28分
13、阅读下列短文,回答问题。
“深海一号”能源站是由我国自主研发建造的全球首座10万吨级深水半潜式生产储油平台。2021年6月25日,该平台正式投产,标志着中国从装备技术到勘探开发能力全面实现从300来到1500米超深水的跨越。2022年2月13日,中国海洋石油集团有限公司对外宣布,该平台2021年6月25日正式投产以来,累计生产天然气超10亿立方米。在保供季为海南自贸港和粤港澳大湾区建设提供了重要清洁能源来源。
(1)天然气属于_______(填“可再生”或“不可再生”)能源,天然气的主要成分是甲烷(CH4),甲烷是由________(填“分子”、“原子”或“离子”)构成;已知甲烷中氢元素的化合价是+1,则碳元素的化合价是________。
(2)天然气之所以被称为清洁能源,是因为它完全燃烧时不产生污染物。请写出甲烷完全燃烧时的化学方程式________。
(3)甲烷的溶解度曲线如图(纵坐标表示每升水中溶解的甲烷体积),由图可以看出甲烷的溶解度规律是______(写出一点即可)。
14、通过海水晒盐可得到粗盐。下图是化学兴趣小组为了除去粗盐中难溶性杂质,进行的三步操作:
(1)三步操作的正确顺序是_________(填字母)。
(2)上述A、B操作中均使用了玻璃棒进行搅拌,其目的分别是:A:_________。B:_________。
(3)经过C操作后,发现滤液仍浑浊,可能的原因是_________(只写一条)。
(4)现有一瓶蒸馏水和一瓶稀氯化钠溶液,请用适当的化学方法把它们鉴别开,并完成实验报告。
实验步骤 实验现象 实验结论
_________。 _________。 _________。
15、工业上用电解食盐水的方法制取浓盐酸,分析下图回答有关问题。已知:氯气(Cl2)常温下为气体。
(1)写出反应①的化学方程式______;
(2)反应②的化学反应类型是______反应;
(3)制得的浓盐酸溶质质量分数为 35%(密度 1.15g/mL),要配制 70g 溶质质量分数为 10%的稀盐酸(不考虑挥发):
①需向盛有浓盐酸的烧杯中加______克水(水的密度 1g/mL);
②配制过程中需要用到的仪器有烧杯、量筒和______。
16、同学们在实验室用下图装置制取氧气。
(1)加热高锰酸钾时,试管口略向下倾斜的原因是 ______ 。
实验后,同学们发现沾有高锰酸钾的白抹布洗完晾干后变为棕褐色。
【查阅资料】草酸溶液能将棕褐色物质除去。
【提出问题】哪些因素能加快草酸除去棕褐色物质的速率?
【进行实验】
将均匀染有棕褐色的抹布剪成大小相同的小布条进行实验
实验 编号 实验1 20℃ 水 实验2 20℃ 0.5%草酸溶液 实验3 20℃ 0.25%草酸溶液 实验4 20℃ 0.125%草酸溶液 实验5 30℃ 0.25%草酸溶液 实验6 40℃ 0.25%草酸溶液
现象 颜色 没有褪去 70秒后 颜色褪去 98秒后 颜色褪去 150秒后 颜色褪去 51秒后 颜色褪去 40秒后 颜色褪去
【解释与结论】
(2)配制200g溶质质量分数为 0.5%的草酸溶液,需要草酸的质量为 ______ 。
(3)实验1的目的是 ______ 。
(4)证明升高温度能加快草酸除去棕褐色物质的速率,需要对比 ______ (填实验序号)。
(5)由实验2、3、4可以得出的结论是 ______ 。
【反思与评价】
(6)实验后,同学们查资料得知抹布上的棕褐色物质为二氧化锰,请你设计实验方案进行验证 ______ 。
17、某化学兴趣小组欲测定化学实验室内存放较久的过氧化氢溶液的溶质质量分数。他们取出该溶液68g,加入适量二氧化锰,生成氧气的质量与反应时间的关系如图所示。
(1)完全反应后生成氧气的质量为___________g。
(2)计算该过氧化氢溶液的溶质质量分数。(要求写出完整步骤)
参考答案
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1、C 2、A 3、C 4、B 5、D 6、D 7、C 8、B 9、B 10、A 11、B 12、B
二、本大题包括5小题,共28分
13、答案:(1) 不可再生 分子 -4
(2) CH4+2O2CO2+2H2O
(3)气压一定时,温度越高,甲烷的溶解度越小(或温度一定时,气压越大,甲烷的溶解度越大)
14、答案:(1)ACB
(2) 搅拌,加快溶解速率 搅拌,防止局部温度过高,造成液滴飞溅
(3)滤纸破损(或接滤液的烧杯不干净等)
(4) 各取两种溶液少许进行蒸干 一种有少量白色残留固体,另一种无残留固体 有固体残留的是氯化钠,无固体残留的是蒸馏水
15、答案:(1) 2NaCl+2H2O2NaOH+H2↑+Cl2↑
(2)化合
(3) 50 玻璃棒和胶头滴管
16、答案:(1)防止冷凝水回流,试管炸裂 (2)1g (3)空白对照,证明水不能使棕褐色布条褪色
(4)3、5、6 (5)其他条件相同时,草酸浓度增大能加快草酸除去棕褐色物质的速率
(6)取棕褐色布条放入试管中,加入过氧化氢溶液,观察是否产生气泡。或取少量二氧化锰粉末于试管中,加入草酸溶液,观察黑色固体是否逐渐消失
17.(1)1.6
(2)解:设68g过氧化氢溶液中含过氧化氢的质量为x。
该过氧化氢溶液的溶质质量分数
答:该过氧化氢溶液的溶质质量分数为5%。
同课章节目录
