2021-2022学年度人教版化学九年级上册第三单元物质构成的奥秘综合测评试题(word版含解析)
文档属性
| 名称 | 2021-2022学年度人教版化学九年级上册第三单元物质构成的奥秘综合测评试题(word版含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 187.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-05 00:00:00 | ||
图片预览



文档简介
九年级上册第三单元物质构成的奥秘综合测评
考试时间:90分钟;命题人:化学教研组
考生注意:
1、本卷分第I卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分,考试时间90分钟
2、答卷前,考生务必用0.5毫米黑色签字笔将自己的姓名、班级填写在试卷规定位置上
3、答案必须写在试卷各个题目指定区域内相应的位置,如需改动,先划掉原来的答案,然后再写上新的答案;不准使用涂改液、胶带纸、修正带,不按以上要求作答的答案无效。
第I卷(选择题 30分)
一、单选题(10小题,每小题3分,共计30分)
1、水变成水蒸气的过程中,改变的是微粒的
A.大小 B.种类 C.间隙 D.化学性质
2、下列符号既可表示一种元素又可表示一个原子还能表示一种物质的是
A.H B.O2 C.Hg D.F
3、既可以表示一种物质,又可以表示一种元素,还能表示一个原子的符号是
A.Cu B.O C.Ca+ D.Cl-
4、按如图进行实验。滴有酚酞溶液的滤纸变红能说明
A.分子间有间隔 B.分子由原子构成
C.分子的体积小 D.分子在不断运动
5、在元素周期表中可寻找制备半导体材料的元素,位置关系如图,下列说法正确的是
A.硅的相对原子质量为14 B.镓属于非金属元素
C.锗与硅最外层电子数相同 D.砷的质子数为74.92
6、2021年5月22日,“祝融号”火星车安全驶离着陆平台,到达火星表面,开始巡视探测。锂离子蓄电池在“祝融号”供配电系统中起着十分重要的作用。在元素周期表中锂元素的某些信息如图所示,下列有关锂的说法不正确的是
A.锂属于金属元素 B.锂的元素符号为Li
C.锂的相对原子质量为6.941g D.锂原子核外有3个电子
7、如图所示为今年在三星堆遗址中发现的金面具残片,经测定该面具含金量约为85%。下列有关说法正确的是
A.金的元素符号为aU B.金容易被腐蚀
C.金单质由金原子构成 D.金的相对原子质量为197g
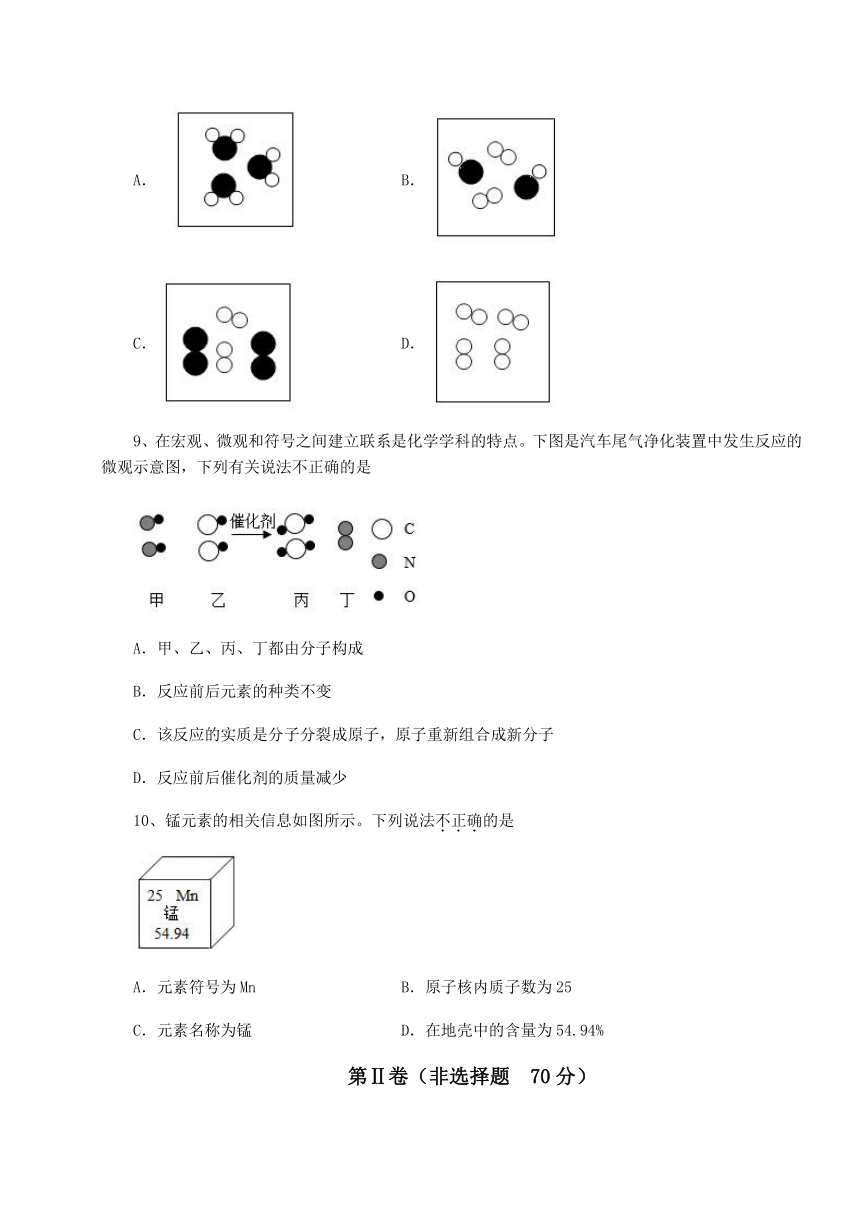
8、下图可以表示4个氧分子的是
A. B.
C. D.
9、在宏观、微观和符号之间建立联系是化学学科的特点。下图是汽车尾气净化装置中发生反应的微观示意图,下列有关说法不正确的是
A.甲、乙、丙、丁都由分子构成
B.反应前后元素的种类不变
C.该反应的实质是分子分裂成原子,原子重新组合成新分子
D.反应前后催化剂的质量减少
10、锰元素的相关信息如图所示。下列说法不正确的是
A.元素符号为Mn B.原子核内质子数为25
C.元素名称为锰 D.在地壳中的含量为54.94%
第Ⅱ卷(非选择题 70分)
二、填空题(5小题,每小题5分,共计25分)
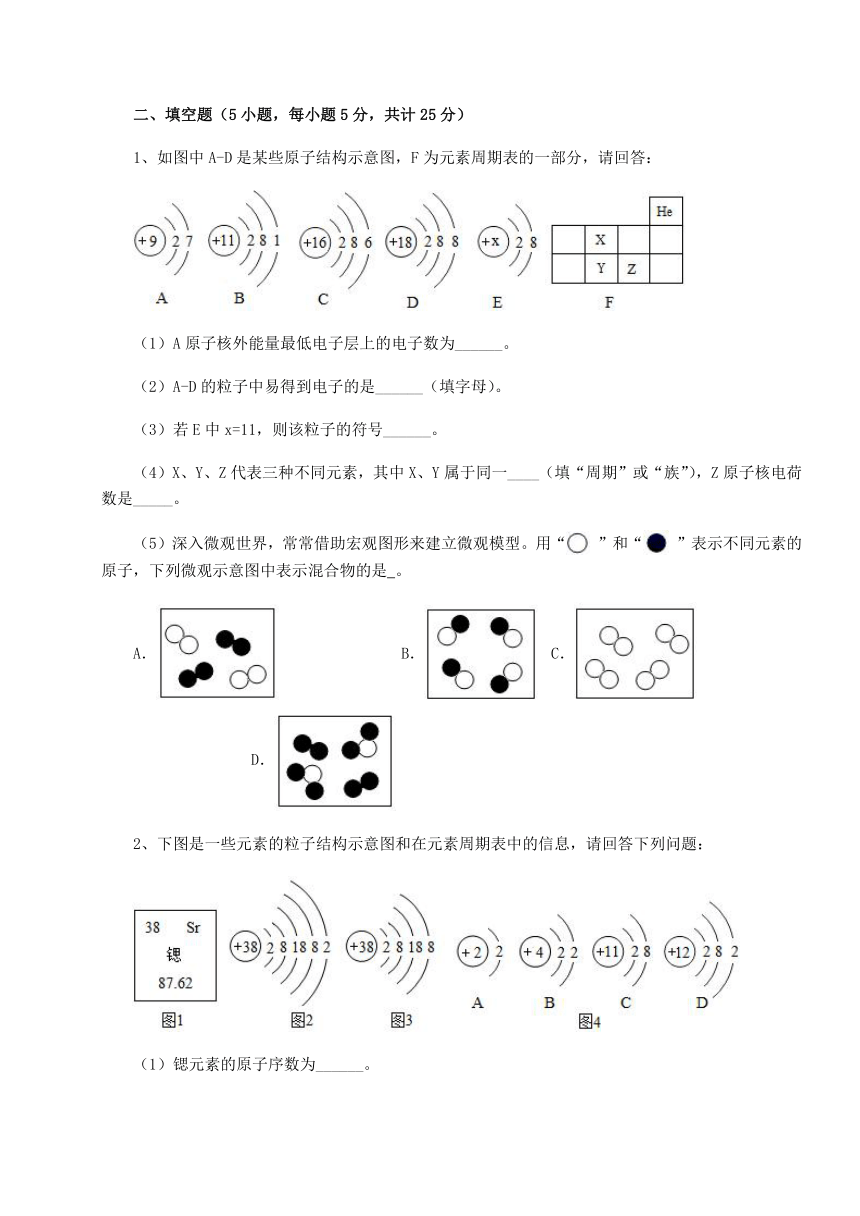
1、如图中A-D是某些原子结构示意图,F为元素周期表的一部分,请回答:
(1)A原子核外能量最低电子层上的电子数为______。
(2)A-D的粒子中易得到电子的是______(填字母)。
(3)若E中x=11,则该粒子的符号______。
(4)X、Y、Z代表三种不同元素,其中X、Y属于同一____(填“周期”或“族”),Z原子核电荷数是_____。
(5)深入微观世界,常常借助宏观图形来建立微观模型。用“ ”和“ ”表示不同元素的原子,下列微观示意图中表示混合物的是 。
A. B. C. D.
2、下图是一些元素的粒子结构示意图和在元素周期表中的信息,请回答下列问题:
(1)锶元素的原子序数为______。
(2)锶元素它的原子的化学性质与A、B、C、D中的______(填序号,下同)相似,具有稳定结构的原子是______。
(3)图3所表示的粒子的化学符号是______。
3、如图A是硒元素在周期表中的信息,B、C、D、E分别为四种粒子的结构示意图,请根据图中信息回答。
(1)硒元素的相对原子质量是______,属于______(填“金属”或“非金属”)元素。
(2)C所表示的元素的原子容易______(填“失去”或“得到”)电子。
(3)图中B、C、D、E四种粒子中属于同种元素的是______(填字母)。
(4)E所表示粒子的化学符号是______。
4、如图中A、B分别是某微粒的结构示意图,回答下列问题。
(1)若A微粒表示带2个单位正电荷的阳离子,则该离子的离子符号为___________;
(2)若B微粒表示某元素的原子,则y=___________,该原子在化学反应中容易___________(填“失去”或“得到”)电子。
5、元素Ca形成的粒子结构示意图如图所示。
(1)Ca属于______(填“金属”或“非金属”)元素。
(2)如图所表示的粒子的化学符号是_________。
(3)下图表示的微粒中,具有相对稳定结构的是________(填序号,下同),与Ca化学性质相似的是______。
三、计算题(3小题,每小题7分,共计21分)
1、若已知一个碳12原子的质量为5.4mkg,另一个R原子的相对原子质量为,R原子的质量为_____kg。
2、已知一个碳12原子的质量为1.993×10-26kg,一个氧原子的质量为2.657×10-26kg,求:
(1)氧原子的相对原子质量(结果保留整数);
(2)一个氧原子中有多少个中子?
3、已知碳12原子(原子核内有6个质子,6个中子)的质量为1.993×10﹣26kg,若A 原子的质量为4.4788×10﹣26kg。求:A原子的相对原子质量______(写出计算过程,结果保留整数)
四、实验探究(2小题,每小题12分,共计24分)
1、某同学设计了如下图所示的实验装置探究“分子的性质”,请回答下列问题:
[进行实验]图1是课本中某个探究实验,几分钟后该实验中可以看到的现象是______; 其中烧杯乙的作用________ ; 通过该实验可以得出或推到出一些结论:①分子在不断运动:②________(答一条即可)。
[实验改进]老师对图I所示的装置进行了改进(如图I所示),并进行了以下操作:
①取一长条形滤纸,等距离滴加无色酚酞试液;②将滴加了无色酚酞试液的长条形滤纸放入一洁净的试管中,并在试管口塞一团棉花;③向脱脂棉上滴加几滴浓氨水。
[分析讨论] (1)按照改进后的实验,几分钟后观察到的现象是____________。
(2)实验过程中若发现滤纸条没有变红而棉花变红,其可能原因是____________。
[拓展延伸]同学们经过讨论后认为,图1、图II所示装置虽能证明分子的性质,但不能证明影响分子性质的因素,于是又设计了如图Ⅲ所示的装置。
在U型管的两个管口分别放入卷成筒状的棉纱布,并用橡皮塞塞紧。用注射器吸取2mL酚酞溶液从橡皮塞慢慢注入棉纱布上,使其润湿,从另一管口插入吸取了浓氨水的注射器。按此方法再组装好另一套相同的装置,将其中- -套装置的下端放入热水中, 向两支U型管A、C处的棉纱上注入浓氨水,几分钟后看到的现象是_________, 该现象说明了__________。
[反思与评价]
(1)图Ⅲ所示的实验方法相对于图I所示的实验方法,具有哪些优点:
①_______________;②________________。
(2)为了得到可靠的结论,在图所示的实验中还应控制相同的变量有:
①____________;②_____________。
2、某兴趣小组探究分子的特性时做了以下实验。
探究一:研究温度对微粒运动速率的影响。
同学们进行图1所示实验时闻到氨气强烈的刺激性气味。于是对实验装置进行改进(如图2)。
(实验操作)
步骤一:向B、D、F三支试管中分别加入5mL的蒸馏水,各滴入1~2滴无色酚酞试液,振荡,观察溶液颜色;
步骤二:向A、E试管中分别加入2mL浓氨水,立即用带有橡皮塞的导管按图2连接好,并将E试管放置在盛有热水的烧杯中,观察几分钟。
(分析讨论)
(1)图1实验中能观察到湿润的酚酞试纸变红色。与图1实验相比,改进后实验的一个主要优点是______。
(2)改进后的实验中使用了F试管,作用是______。
(3)步骤二中将E试管放置在盛有热水的烧杯中,B、D试管中先出现颜色变化的是D试管,由此可得出温度对微粒运动速率的影响是______。
探究二:分子运动快慢与分子的质量有关
(查阅资料)
①浓氨水易挥发,挥发出氨气,浓盐酸易挥发,挥发出氯化氢气体;
②氨气和氯化氢反应生成氯化铵白色小颗粒;
③氯化氢分子质量大于氨气分子的质量。
(实验设计与探究)小花同学设计了如下图所示实验进行探究。
如图玻璃导管中产生大量白烟,而白烟较多较浓的点在C点,则说明______,分子运动越快。
-参考答案-
一、单选题
1、C
【详解】
水变成水蒸气的过程中,水分子的大小和种类均没变,水分子的化学性质也没变,只是分子之间的间隙变大了。故选C。
2、C
【详解】
A、表示氢元素;一个氢原子,不能表示物质,错误。
B、表示氧气,不能表示氧元素,不能表示一个氧原子,错误。
C、表示汞;汞元素;一个汞原子,正确。
D、表示氟元素;一个氟原子,不能表示物质,错误。
故选:C。
3、A
【详解】
A、Cu为金属,由原子构成,故符号Cu既可以表示一种物质,又可以表示一种元素,还能表示一个原子,正确;
B、氧气是由分子构成的物质,故符号O可以表示一种元素,还能表示一个原子,但不能表示一种物质,不符合题意;
C、Ca+为错误的离子符号,应写为Ca2+,不符合题意;
D、Cl-为氯离子的符号,也可表示一个氯离子,不符合题意。
故选A。
4、D
【详解】
浓氨水具有挥发性,从浓氨水中挥发出来的氨气分子在不断运动,运动到滴有酚酞溶液的滤纸上,溶于水形成氨水,呈碱性,使滴有酚酞溶液的滤纸变红;与分子间有间隔、分子由原子构成、分子的体积小无关。
故选D。
5、C
【分析】
元素周期表信息图中,元素名称的左上角的数字为元素的原子序数,右上角为元素符号,中间的汉字表示元素名称,下边是元素的相对原子质量。
【详解】
A、硅的相对原子质量为28.09,错误;
B、由汉字结构可知,镓属于金属元素,错误;
C、锗与硅属于同一主族,最外层电子数相同,正确;
D、砷的质子数=原子序数=33,错误。
故选C。
6、C
【详解】
A、根据元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名称是锂,带“钅”字旁,属于金属元素,故A正确;
B、锂的元素符号为Li,故B正确;
C、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为6. 941,相对原子质量单位是“1”,不是“克”,故C错误。
D、根据元素周期表中的一格可知,左上角的数字为3,表示原子序数为3,原子中原子序数等于核外电子数,故该原子核外有3个电子,故D正确;
故选C。
7、C
【详解】
A、书写元素符号时,由两个字母表示的元素符号,第二个字母必须小写,故金的元素符号为:Au,不符合题意;
B、金的化学性质稳定,不容易被锈蚀,不符合题意;
C、金是金属单质,是由金原子直接构成,符合题意;
D、相对原子质量是一个比值,单位为“1”,不是“g”,故金的相对原子质量为197,不符合题意。
故选C。
8、D
【详解】
A、 一个氧分子由两个氧原子构成,该图示中有3个相同的分子,但每个分子都是由两个“白”原子和一个“黑”原子构成,该图示可用来表示3个 分子,故A选项不符合题意;
B、该图示表示的物质由一种化合物和一种单质两种物质组成,属于混合物,氧气是纯净物,从微观方面看,该图示可以表示两个 分子和两个 分子混合在一起,不能表示4个氧分子,故B选项不符合题意;
C、该图示表示的物质由两种单质组成,属于混合物, 从微观方面看,该图示可以表示两个 分子和两个 分子混合在一起,不能表示4个氧分子,故C选项不符合题意;
D、该图示能表示四个相同的分子,且每个分子都由两个相同的原子构成,所以该图示能表示4个氧分子,故D选项符合题意;
故选D。
9、D
【详解】
A、由图可知,甲、乙、丙、丁都由分子构成,正确;
B、元素是质子数相同的一类原子,反应前后元素的种类不变,正确;
C、该反应的实质是分子分裂成原子,原子重新组合成新分子,正确;
D、反应前后催化剂的质量不变,错误。
故选D。
10、D
【分析】
图中可知信息为原子序数为25,元素符号为Mn,元素名称为锰,相对原子质量为54.94。
【详解】
A、由图示可知,右上角为元素符号为Mn,正确;
B、左上角为原子序数为25,正确;
C、元素名称为锰,正确;
D、相对原子质量为54.94,无法得知其在地壳中的含量,错误。
故选D。
二、填空题
1、
(1)2
(2)AC
(3)Na+
(4) 周期 17
(5)AD
【解析】
(1)
核外电子能量越低,离核越近;A原子核外能量最低电子层为第一层,该层上的电子数为2。
(2)
A-D的粒子A、C最外层电子数为7、6,均大于4,在化学反应中容易得到电子,故易得到电子的是AC。
(3)
若E中x=11,则该粒子为11号元素钠元素原子失去1个电子后形成的钠离子,符号为Na+。
(4)
由图可知,X、Y、Z代表三种不同元素,分别为O、S、Cl,其中X、Y为于同一横行,属于同一周期,Z为17号元素,原子中质子数=原子序数=核电荷数,故原子核电荷数是17。
(5)
A、为两种不同分子构成的混合物;
B、为同种分子构成的纯净物;
C、为同种分子构成的纯净物;
D、为两种不同分子构成的混合物;
故选AD。
2、
(1)38
(2) BD A
(3)Sr2+
【解析】
(1)
元素信息图中,左上角的数字就是元素的原子序数,由图可知,锶元素的原子序数为38,故填38。
(2)
由图可知,锶原子的最外层电子数为2,A、B、C、D四种微粒中,B、D的最外层电子数为2,在化学反应中溶液失去电子,与锶元素的原子的化学性质相同,虽然A微粒的原子最外层电子数也为2,但该原子既不容易失去电子,也不容易得到电子,与锶原子的化学性质不同,故填BD;
A原子的核外只有1个电子层,且该电子层的电子数为2,属于稳定结构,故填A。
(3)
由图可知,图3中的微粒的质子数为38,属于锶元素,核外电子数为36,是锶原子失去2个电子形成的带2个单位的正电荷的锶离子,其离子符号为,故填Sr2+。
3、
(1) 78.96 非金属
(2)失去
(3)B D
(4)Mg2+
【分析】
若核内质子数=核外电子数,则该粒子为原子;若核内质子数>核外电子数,则该粒子为阳离子;若核内质子数<核外电子数,则该粒子为阴离子。
在原子结构示意图中,最外层电子数>4,在化学反应中容易得到电子;最外层电子数<4,在化学反应中容易失去电子。
(1)
由硒元素在周期表中的信息可知,硒元素的相对原子质量是78.96,硒的偏旁为“石”字旁,属于非金属元素;故填:78.96;非金属。
(2)
由C的粒子结构示意图可知,最外层电子数为1<4,在化学反应中容易失去最外层的1个电子,达到稳定结构;故填:失去。
(3)
元素是具有相同质子数(核电荷数)的同一类原子的总称,由B、C、D、E四种粒子结构示意图可知,其中核内质子数相等的粒子是B和D,则说明B、D属于同种元素;故填:BD。
(4)
由E的粒子结构示意图可知,其核内质子数为12,为镁元素,核内质子数>核外电子数,则该粒子为镁离子,其离子符号为Mg2+;故填:Mg2+。
【点睛】
4、
(1)Mg2+
(2) 7 得到
【解析】
(1)
若A微粒表示带2个单位正电荷的阳离子,那么质子数比电子数大2,有12个质子,为12号元素镁元素,则该离子为镁离子,离子符号为Mg2+。
(2)
原子中质子数=电子数,B微粒表示某元素的原子,则y=17-2-8=7,该原子最外层有7个电子,大于4,在化学反应中容易得到电子。
5、
(1)金属
(2)Ca2+
(3) AC B
【分析】
(1)
Ca元素名称是钙,含“钅”旁,属于金属元素;
(2)
图示核外电子数为18,则是钙原子失去2个电子形成带2个单位正电荷的阳离子,表示为Ca2+;
(3)
最外层电子数为8(电子层数为1时,最外层电子数为2)时,表示的微粒具有相对稳定的结构,其中AC具有相对稳定的结构;最外层电子数相同,其化学性质相似,钙原子最外层电子数为2,AB最外层电子数均为2,但A表示的是He,只有1个电子层,属于稀有气体,所以与钙化学性质相似的是B。
【点睛】
三、计算题
1、
【详解】
解:已知一个碳12原子的质量为5.4mkg,另一个R原子的相对原子质量为,
所以可得:,
可得:R原子的质量=。
2、(1)相对原子质量==≈16
(2)中子数=相对原子质量-质子数=16-8=8
【详解】
见答案
3、已知碳-12原子的质量为1.993×10-26kg,A原子的质量为4.4788×10-26kg,A原子的相对原子质量为 ≈27
答:A原子的相对原子质量为27。
【分析】
相对原子质量是原子质量与碳12原子质量的十二分之一的比值;
【详解】
见答案。
四、实验探究
1、甲中的酚酞变红,乙中酚酞没有变红 对比实验(与甲对比或证明空气空气不能使酚酞变红) 氨水显碱性(或氨水能使酚酞变红等) (合理答案即可) 滤纸上的酚酞由右向左依次变红(没有提到依次或逐渐变红不给分) 将酚酞滴到了棉花上,氨水滴到了滤纸上 棉纱布D比棉纱布B先变红(只提到棉纱布变红不给分) 温度越高分子的运动速度越快(或分子的运动与温度有关) 减少污染(防止氨气污染空气或环保均可) 可以验证温度对分子运动的影响(合理答案即可) AC 两处注入的浓氨水的体积要相同 应同时向AC处的棉花上注入浓氨水(合理答案即可)
【详解】
解:[进行实验]图Ⅰ是课本中某个探究实验,几分钟后该实验中可以看到的现象是甲中的溶液变红色,其中烧杯乙的作用是对比,通过对比可知空气中的物质不能使酚酞试液变色,通过该实验可以得出或推到出一些结论是:①分子在不断运动;②氨水显碱性等;
[分析讨论](1)按照改进后的实验,氨分子是不断运动的,当运动到滤纸条上的酚酞试液中时,和其中的水结合生成氨水,从而使酚酞试液变红色,因此几分钟后观察到的现象是滤纸上的酚酞由右向左依次变红;
(2)实验过程中若发现滤纸条没有变红而棉花变红,其可能原因是将酚酞滴到棉花上,氨水滴到滤纸上,这是因为氨分子的相对分子质量远小于酚酞分子的相对分子质量,因此氨分子的运动速率远大于酚酞分子的运动速率;
[拓展延伸]按照图Ⅲ所示的装置进行操作,几分钟后看到的现象是棉纱布D比棉纱布B先变红,该现象说明了温度越高分子的运动速率越快;
[反思与评价](1)图Ⅲ所示的实验方法相对于图Ⅰ所示的实验方法,优点是:减少污染;节约药品;可以验证温度对分子运动的影响;
(2)为了得到可靠的结论,在图所示的实验中还应控制相同的变量有:AC 两处注入的浓氨水的体积要相同、应同时向AC处的棉花上注入相同体积的浓氨水、热水和冷水的体积相同等。
2、环保 对照实验 温度越高,分子的运动速率越快 分子质量越小
【详解】
探究一:分析讨论:(1)改进后的实验在密闭容器中进行,比较环保;
(2)改进后的实验中使用了F试管,作用是对照实验,证明不是空气中的成分使无色酚酞试液变红;
(3)步骤二中将E试管放置在盛有热水的烧杯中,B、D试管中先出现颜色变化的是D试管,说明温度越高,分子的运动速率越快;
探究二:实验设计与探究:浓氨水易挥发,挥发出氨气,浓盐酸易挥发,挥发出氯化氢气体;挥发出的氨分子和氯化氢分子不断运动,当氯化氢分子和氨分子相遇时,氨气和氯化氢反应生成氯化铵白色小颗粒,出现“白烟”,氯化氢分子质量大于氨气分子的质量,而白烟较多较浓的点在C点,说明分子质量越小,分子越快越快。
考试时间:90分钟;命题人:化学教研组
考生注意:
1、本卷分第I卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分,考试时间90分钟
2、答卷前,考生务必用0.5毫米黑色签字笔将自己的姓名、班级填写在试卷规定位置上
3、答案必须写在试卷各个题目指定区域内相应的位置,如需改动,先划掉原来的答案,然后再写上新的答案;不准使用涂改液、胶带纸、修正带,不按以上要求作答的答案无效。
第I卷(选择题 30分)
一、单选题(10小题,每小题3分,共计30分)
1、水变成水蒸气的过程中,改变的是微粒的
A.大小 B.种类 C.间隙 D.化学性质
2、下列符号既可表示一种元素又可表示一个原子还能表示一种物质的是
A.H B.O2 C.Hg D.F
3、既可以表示一种物质,又可以表示一种元素,还能表示一个原子的符号是
A.Cu B.O C.Ca+ D.Cl-
4、按如图进行实验。滴有酚酞溶液的滤纸变红能说明
A.分子间有间隔 B.分子由原子构成
C.分子的体积小 D.分子在不断运动
5、在元素周期表中可寻找制备半导体材料的元素,位置关系如图,下列说法正确的是
A.硅的相对原子质量为14 B.镓属于非金属元素
C.锗与硅最外层电子数相同 D.砷的质子数为74.92
6、2021年5月22日,“祝融号”火星车安全驶离着陆平台,到达火星表面,开始巡视探测。锂离子蓄电池在“祝融号”供配电系统中起着十分重要的作用。在元素周期表中锂元素的某些信息如图所示,下列有关锂的说法不正确的是
A.锂属于金属元素 B.锂的元素符号为Li
C.锂的相对原子质量为6.941g D.锂原子核外有3个电子
7、如图所示为今年在三星堆遗址中发现的金面具残片,经测定该面具含金量约为85%。下列有关说法正确的是
A.金的元素符号为aU B.金容易被腐蚀
C.金单质由金原子构成 D.金的相对原子质量为197g
8、下图可以表示4个氧分子的是
A. B.
C. D.
9、在宏观、微观和符号之间建立联系是化学学科的特点。下图是汽车尾气净化装置中发生反应的微观示意图,下列有关说法不正确的是
A.甲、乙、丙、丁都由分子构成
B.反应前后元素的种类不变
C.该反应的实质是分子分裂成原子,原子重新组合成新分子
D.反应前后催化剂的质量减少
10、锰元素的相关信息如图所示。下列说法不正确的是
A.元素符号为Mn B.原子核内质子数为25
C.元素名称为锰 D.在地壳中的含量为54.94%
第Ⅱ卷(非选择题 70分)
二、填空题(5小题,每小题5分,共计25分)
1、如图中A-D是某些原子结构示意图,F为元素周期表的一部分,请回答:
(1)A原子核外能量最低电子层上的电子数为______。
(2)A-D的粒子中易得到电子的是______(填字母)。
(3)若E中x=11,则该粒子的符号______。
(4)X、Y、Z代表三种不同元素,其中X、Y属于同一____(填“周期”或“族”),Z原子核电荷数是_____。
(5)深入微观世界,常常借助宏观图形来建立微观模型。用“ ”和“ ”表示不同元素的原子,下列微观示意图中表示混合物的是 。
A. B. C. D.
2、下图是一些元素的粒子结构示意图和在元素周期表中的信息,请回答下列问题:
(1)锶元素的原子序数为______。
(2)锶元素它的原子的化学性质与A、B、C、D中的______(填序号,下同)相似,具有稳定结构的原子是______。
(3)图3所表示的粒子的化学符号是______。
3、如图A是硒元素在周期表中的信息,B、C、D、E分别为四种粒子的结构示意图,请根据图中信息回答。
(1)硒元素的相对原子质量是______,属于______(填“金属”或“非金属”)元素。
(2)C所表示的元素的原子容易______(填“失去”或“得到”)电子。
(3)图中B、C、D、E四种粒子中属于同种元素的是______(填字母)。
(4)E所表示粒子的化学符号是______。
4、如图中A、B分别是某微粒的结构示意图,回答下列问题。
(1)若A微粒表示带2个单位正电荷的阳离子,则该离子的离子符号为___________;
(2)若B微粒表示某元素的原子,则y=___________,该原子在化学反应中容易___________(填“失去”或“得到”)电子。
5、元素Ca形成的粒子结构示意图如图所示。
(1)Ca属于______(填“金属”或“非金属”)元素。
(2)如图所表示的粒子的化学符号是_________。
(3)下图表示的微粒中,具有相对稳定结构的是________(填序号,下同),与Ca化学性质相似的是______。
三、计算题(3小题,每小题7分,共计21分)
1、若已知一个碳12原子的质量为5.4mkg,另一个R原子的相对原子质量为,R原子的质量为_____kg。
2、已知一个碳12原子的质量为1.993×10-26kg,一个氧原子的质量为2.657×10-26kg,求:
(1)氧原子的相对原子质量(结果保留整数);
(2)一个氧原子中有多少个中子?
3、已知碳12原子(原子核内有6个质子,6个中子)的质量为1.993×10﹣26kg,若A 原子的质量为4.4788×10﹣26kg。求:A原子的相对原子质量______(写出计算过程,结果保留整数)
四、实验探究(2小题,每小题12分,共计24分)
1、某同学设计了如下图所示的实验装置探究“分子的性质”,请回答下列问题:
[进行实验]图1是课本中某个探究实验,几分钟后该实验中可以看到的现象是______; 其中烧杯乙的作用________ ; 通过该实验可以得出或推到出一些结论:①分子在不断运动:②________(答一条即可)。
[实验改进]老师对图I所示的装置进行了改进(如图I所示),并进行了以下操作:
①取一长条形滤纸,等距离滴加无色酚酞试液;②将滴加了无色酚酞试液的长条形滤纸放入一洁净的试管中,并在试管口塞一团棉花;③向脱脂棉上滴加几滴浓氨水。
[分析讨论] (1)按照改进后的实验,几分钟后观察到的现象是____________。
(2)实验过程中若发现滤纸条没有变红而棉花变红,其可能原因是____________。
[拓展延伸]同学们经过讨论后认为,图1、图II所示装置虽能证明分子的性质,但不能证明影响分子性质的因素,于是又设计了如图Ⅲ所示的装置。
在U型管的两个管口分别放入卷成筒状的棉纱布,并用橡皮塞塞紧。用注射器吸取2mL酚酞溶液从橡皮塞慢慢注入棉纱布上,使其润湿,从另一管口插入吸取了浓氨水的注射器。按此方法再组装好另一套相同的装置,将其中- -套装置的下端放入热水中, 向两支U型管A、C处的棉纱上注入浓氨水,几分钟后看到的现象是_________, 该现象说明了__________。
[反思与评价]
(1)图Ⅲ所示的实验方法相对于图I所示的实验方法,具有哪些优点:
①_______________;②________________。
(2)为了得到可靠的结论,在图所示的实验中还应控制相同的变量有:
①____________;②_____________。
2、某兴趣小组探究分子的特性时做了以下实验。
探究一:研究温度对微粒运动速率的影响。
同学们进行图1所示实验时闻到氨气强烈的刺激性气味。于是对实验装置进行改进(如图2)。
(实验操作)
步骤一:向B、D、F三支试管中分别加入5mL的蒸馏水,各滴入1~2滴无色酚酞试液,振荡,观察溶液颜色;
步骤二:向A、E试管中分别加入2mL浓氨水,立即用带有橡皮塞的导管按图2连接好,并将E试管放置在盛有热水的烧杯中,观察几分钟。
(分析讨论)
(1)图1实验中能观察到湿润的酚酞试纸变红色。与图1实验相比,改进后实验的一个主要优点是______。
(2)改进后的实验中使用了F试管,作用是______。
(3)步骤二中将E试管放置在盛有热水的烧杯中,B、D试管中先出现颜色变化的是D试管,由此可得出温度对微粒运动速率的影响是______。
探究二:分子运动快慢与分子的质量有关
(查阅资料)
①浓氨水易挥发,挥发出氨气,浓盐酸易挥发,挥发出氯化氢气体;
②氨气和氯化氢反应生成氯化铵白色小颗粒;
③氯化氢分子质量大于氨气分子的质量。
(实验设计与探究)小花同学设计了如下图所示实验进行探究。
如图玻璃导管中产生大量白烟,而白烟较多较浓的点在C点,则说明______,分子运动越快。
-参考答案-
一、单选题
1、C
【详解】
水变成水蒸气的过程中,水分子的大小和种类均没变,水分子的化学性质也没变,只是分子之间的间隙变大了。故选C。
2、C
【详解】
A、表示氢元素;一个氢原子,不能表示物质,错误。
B、表示氧气,不能表示氧元素,不能表示一个氧原子,错误。
C、表示汞;汞元素;一个汞原子,正确。
D、表示氟元素;一个氟原子,不能表示物质,错误。
故选:C。
3、A
【详解】
A、Cu为金属,由原子构成,故符号Cu既可以表示一种物质,又可以表示一种元素,还能表示一个原子,正确;
B、氧气是由分子构成的物质,故符号O可以表示一种元素,还能表示一个原子,但不能表示一种物质,不符合题意;
C、Ca+为错误的离子符号,应写为Ca2+,不符合题意;
D、Cl-为氯离子的符号,也可表示一个氯离子,不符合题意。
故选A。
4、D
【详解】
浓氨水具有挥发性,从浓氨水中挥发出来的氨气分子在不断运动,运动到滴有酚酞溶液的滤纸上,溶于水形成氨水,呈碱性,使滴有酚酞溶液的滤纸变红;与分子间有间隔、分子由原子构成、分子的体积小无关。
故选D。
5、C
【分析】
元素周期表信息图中,元素名称的左上角的数字为元素的原子序数,右上角为元素符号,中间的汉字表示元素名称,下边是元素的相对原子质量。
【详解】
A、硅的相对原子质量为28.09,错误;
B、由汉字结构可知,镓属于金属元素,错误;
C、锗与硅属于同一主族,最外层电子数相同,正确;
D、砷的质子数=原子序数=33,错误。
故选C。
6、C
【详解】
A、根据元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名称是锂,带“钅”字旁,属于金属元素,故A正确;
B、锂的元素符号为Li,故B正确;
C、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为6. 941,相对原子质量单位是“1”,不是“克”,故C错误。
D、根据元素周期表中的一格可知,左上角的数字为3,表示原子序数为3,原子中原子序数等于核外电子数,故该原子核外有3个电子,故D正确;
故选C。
7、C
【详解】
A、书写元素符号时,由两个字母表示的元素符号,第二个字母必须小写,故金的元素符号为:Au,不符合题意;
B、金的化学性质稳定,不容易被锈蚀,不符合题意;
C、金是金属单质,是由金原子直接构成,符合题意;
D、相对原子质量是一个比值,单位为“1”,不是“g”,故金的相对原子质量为197,不符合题意。
故选C。
8、D
【详解】
A、 一个氧分子由两个氧原子构成,该图示中有3个相同的分子,但每个分子都是由两个“白”原子和一个“黑”原子构成,该图示可用来表示3个 分子,故A选项不符合题意;
B、该图示表示的物质由一种化合物和一种单质两种物质组成,属于混合物,氧气是纯净物,从微观方面看,该图示可以表示两个 分子和两个 分子混合在一起,不能表示4个氧分子,故B选项不符合题意;
C、该图示表示的物质由两种单质组成,属于混合物, 从微观方面看,该图示可以表示两个 分子和两个 分子混合在一起,不能表示4个氧分子,故C选项不符合题意;
D、该图示能表示四个相同的分子,且每个分子都由两个相同的原子构成,所以该图示能表示4个氧分子,故D选项符合题意;
故选D。
9、D
【详解】
A、由图可知,甲、乙、丙、丁都由分子构成,正确;
B、元素是质子数相同的一类原子,反应前后元素的种类不变,正确;
C、该反应的实质是分子分裂成原子,原子重新组合成新分子,正确;
D、反应前后催化剂的质量不变,错误。
故选D。
10、D
【分析】
图中可知信息为原子序数为25,元素符号为Mn,元素名称为锰,相对原子质量为54.94。
【详解】
A、由图示可知,右上角为元素符号为Mn,正确;
B、左上角为原子序数为25,正确;
C、元素名称为锰,正确;
D、相对原子质量为54.94,无法得知其在地壳中的含量,错误。
故选D。
二、填空题
1、
(1)2
(2)AC
(3)Na+
(4) 周期 17
(5)AD
【解析】
(1)
核外电子能量越低,离核越近;A原子核外能量最低电子层为第一层,该层上的电子数为2。
(2)
A-D的粒子A、C最外层电子数为7、6,均大于4,在化学反应中容易得到电子,故易得到电子的是AC。
(3)
若E中x=11,则该粒子为11号元素钠元素原子失去1个电子后形成的钠离子,符号为Na+。
(4)
由图可知,X、Y、Z代表三种不同元素,分别为O、S、Cl,其中X、Y为于同一横行,属于同一周期,Z为17号元素,原子中质子数=原子序数=核电荷数,故原子核电荷数是17。
(5)
A、为两种不同分子构成的混合物;
B、为同种分子构成的纯净物;
C、为同种分子构成的纯净物;
D、为两种不同分子构成的混合物;
故选AD。
2、
(1)38
(2) BD A
(3)Sr2+
【解析】
(1)
元素信息图中,左上角的数字就是元素的原子序数,由图可知,锶元素的原子序数为38,故填38。
(2)
由图可知,锶原子的最外层电子数为2,A、B、C、D四种微粒中,B、D的最外层电子数为2,在化学反应中溶液失去电子,与锶元素的原子的化学性质相同,虽然A微粒的原子最外层电子数也为2,但该原子既不容易失去电子,也不容易得到电子,与锶原子的化学性质不同,故填BD;
A原子的核外只有1个电子层,且该电子层的电子数为2,属于稳定结构,故填A。
(3)
由图可知,图3中的微粒的质子数为38,属于锶元素,核外电子数为36,是锶原子失去2个电子形成的带2个单位的正电荷的锶离子,其离子符号为,故填Sr2+。
3、
(1) 78.96 非金属
(2)失去
(3)B D
(4)Mg2+
【分析】
若核内质子数=核外电子数,则该粒子为原子;若核内质子数>核外电子数,则该粒子为阳离子;若核内质子数<核外电子数,则该粒子为阴离子。
在原子结构示意图中,最外层电子数>4,在化学反应中容易得到电子;最外层电子数<4,在化学反应中容易失去电子。
(1)
由硒元素在周期表中的信息可知,硒元素的相对原子质量是78.96,硒的偏旁为“石”字旁,属于非金属元素;故填:78.96;非金属。
(2)
由C的粒子结构示意图可知,最外层电子数为1<4,在化学反应中容易失去最外层的1个电子,达到稳定结构;故填:失去。
(3)
元素是具有相同质子数(核电荷数)的同一类原子的总称,由B、C、D、E四种粒子结构示意图可知,其中核内质子数相等的粒子是B和D,则说明B、D属于同种元素;故填:BD。
(4)
由E的粒子结构示意图可知,其核内质子数为12,为镁元素,核内质子数>核外电子数,则该粒子为镁离子,其离子符号为Mg2+;故填:Mg2+。
【点睛】
4、
(1)Mg2+
(2) 7 得到
【解析】
(1)
若A微粒表示带2个单位正电荷的阳离子,那么质子数比电子数大2,有12个质子,为12号元素镁元素,则该离子为镁离子,离子符号为Mg2+。
(2)
原子中质子数=电子数,B微粒表示某元素的原子,则y=17-2-8=7,该原子最外层有7个电子,大于4,在化学反应中容易得到电子。
5、
(1)金属
(2)Ca2+
(3) AC B
【分析】
(1)
Ca元素名称是钙,含“钅”旁,属于金属元素;
(2)
图示核外电子数为18,则是钙原子失去2个电子形成带2个单位正电荷的阳离子,表示为Ca2+;
(3)
最外层电子数为8(电子层数为1时,最外层电子数为2)时,表示的微粒具有相对稳定的结构,其中AC具有相对稳定的结构;最外层电子数相同,其化学性质相似,钙原子最外层电子数为2,AB最外层电子数均为2,但A表示的是He,只有1个电子层,属于稀有气体,所以与钙化学性质相似的是B。
【点睛】
三、计算题
1、
【详解】
解:已知一个碳12原子的质量为5.4mkg,另一个R原子的相对原子质量为,
所以可得:,
可得:R原子的质量=。
2、(1)相对原子质量==≈16
(2)中子数=相对原子质量-质子数=16-8=8
【详解】
见答案
3、已知碳-12原子的质量为1.993×10-26kg,A原子的质量为4.4788×10-26kg,A原子的相对原子质量为 ≈27
答:A原子的相对原子质量为27。
【分析】
相对原子质量是原子质量与碳12原子质量的十二分之一的比值;
【详解】
见答案。
四、实验探究
1、甲中的酚酞变红,乙中酚酞没有变红 对比实验(与甲对比或证明空气空气不能使酚酞变红) 氨水显碱性(或氨水能使酚酞变红等) (合理答案即可) 滤纸上的酚酞由右向左依次变红(没有提到依次或逐渐变红不给分) 将酚酞滴到了棉花上,氨水滴到了滤纸上 棉纱布D比棉纱布B先变红(只提到棉纱布变红不给分) 温度越高分子的运动速度越快(或分子的运动与温度有关) 减少污染(防止氨气污染空气或环保均可) 可以验证温度对分子运动的影响(合理答案即可) AC 两处注入的浓氨水的体积要相同 应同时向AC处的棉花上注入浓氨水(合理答案即可)
【详解】
解:[进行实验]图Ⅰ是课本中某个探究实验,几分钟后该实验中可以看到的现象是甲中的溶液变红色,其中烧杯乙的作用是对比,通过对比可知空气中的物质不能使酚酞试液变色,通过该实验可以得出或推到出一些结论是:①分子在不断运动;②氨水显碱性等;
[分析讨论](1)按照改进后的实验,氨分子是不断运动的,当运动到滤纸条上的酚酞试液中时,和其中的水结合生成氨水,从而使酚酞试液变红色,因此几分钟后观察到的现象是滤纸上的酚酞由右向左依次变红;
(2)实验过程中若发现滤纸条没有变红而棉花变红,其可能原因是将酚酞滴到棉花上,氨水滴到滤纸上,这是因为氨分子的相对分子质量远小于酚酞分子的相对分子质量,因此氨分子的运动速率远大于酚酞分子的运动速率;
[拓展延伸]按照图Ⅲ所示的装置进行操作,几分钟后看到的现象是棉纱布D比棉纱布B先变红,该现象说明了温度越高分子的运动速率越快;
[反思与评价](1)图Ⅲ所示的实验方法相对于图Ⅰ所示的实验方法,优点是:减少污染;节约药品;可以验证温度对分子运动的影响;
(2)为了得到可靠的结论,在图所示的实验中还应控制相同的变量有:AC 两处注入的浓氨水的体积要相同、应同时向AC处的棉花上注入相同体积的浓氨水、热水和冷水的体积相同等。
2、环保 对照实验 温度越高,分子的运动速率越快 分子质量越小
【详解】
探究一:分析讨论:(1)改进后的实验在密闭容器中进行,比较环保;
(2)改进后的实验中使用了F试管,作用是对照实验,证明不是空气中的成分使无色酚酞试液变红;
(3)步骤二中将E试管放置在盛有热水的烧杯中,B、D试管中先出现颜色变化的是D试管,说明温度越高,分子的运动速率越快;
探究二:实验设计与探究:浓氨水易挥发,挥发出氨气,浓盐酸易挥发,挥发出氯化氢气体;挥发出的氨分子和氯化氢分子不断运动,当氯化氢分子和氨分子相遇时,氨气和氯化氢反应生成氯化铵白色小颗粒,出现“白烟”,氯化氢分子质量大于氨气分子的质量,而白烟较多较浓的点在C点,说明分子质量越小,分子越快越快。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
