2013届高三化学题型专题复习专题三 有机综合题
文档属性
| 名称 | 2013届高三化学题型专题复习专题三 有机综合题 |

|
|
| 格式 | zip | ||
| 文件大小 | 590.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2013-03-26 00:00:00 | ||
图片预览

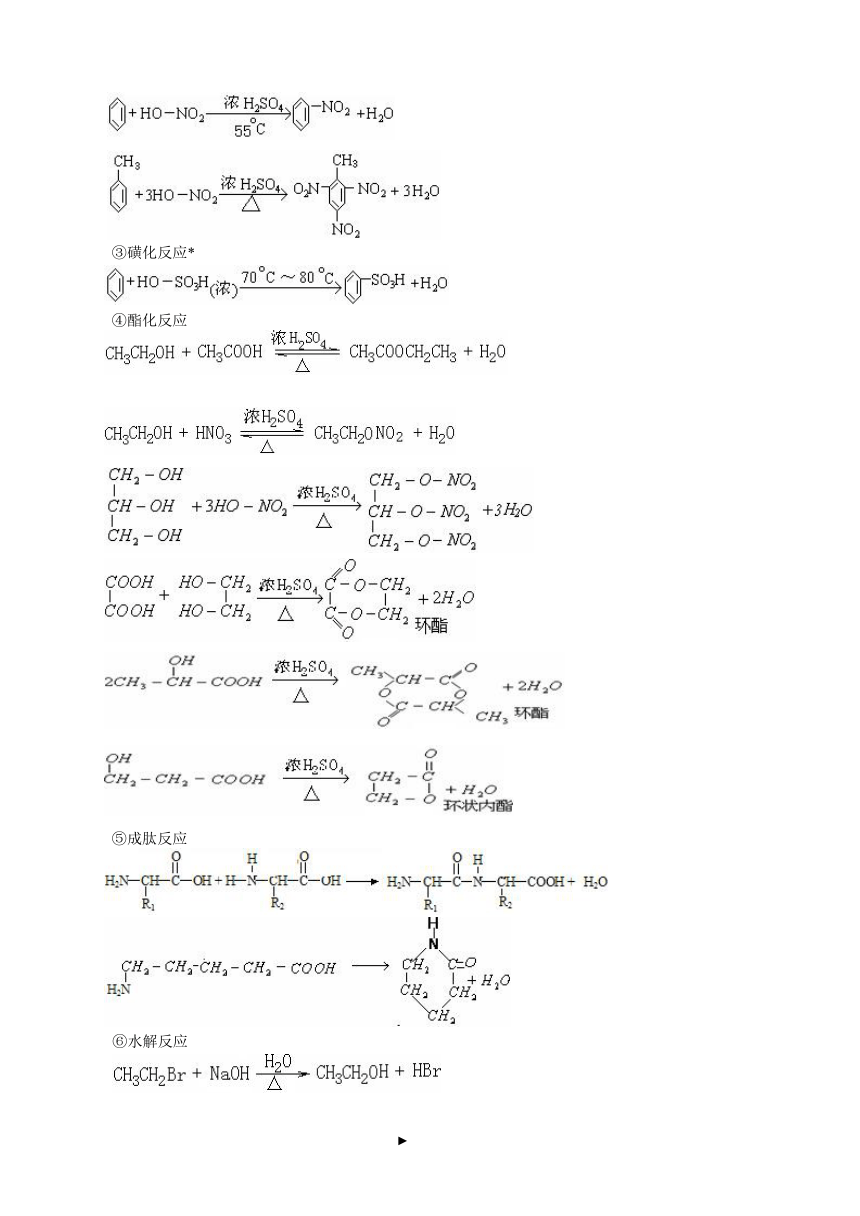



文档简介
2013届高三化学题型专题复习
专题三 有机综合题
【考点梳理】
1. 《2013年江苏省高考化学考试说明》中“考试范围和内容”之“有机化合物及其应用”:⑴了解测定有机化合物组成和结构的一般方法。⑵知道有机化合物中碳的成键特征,并能认识手性碳原子。⑶了解常见有机化合物中的官能团,能正确表示简单有机化合物的结构。能根据有机化合物的命名规则命名简单的有机化合物。⑷了解有机化合物存在同分异构现象(不包括立体异构),能判断并正确书写简单有机化合物的同分异构体的结构简式。⑸了解加成、取代、消去、加聚和缩聚等有机反应的特点,能判断典型有机反应的类型。⑹掌握烃(烷烃、烯烃、炔烃和芳香烃)及其衍生物(卤代烃、醇、酚、醛、羧酸、酯)的组成、结构特点和主要性质。能利用不同类型有机化合物之间的转化关系设计合理路线合成简单有机化合物。⑺知道天然气、液化石油气和汽油的主要成分及其应用。⑻了解糖类、油脂、氨基酸和蛋白质的组成、结构特点和主要性质,认识化学科学在生命科学发展中的重要作用。⑼知道简单合成高分子的单体、链节和聚合度,了解合成高分子的性能及其在高新技术领域中的应用。⑽认识有机化合物在生产、生活中的作用和对环境、健康产生的影响。
2.结合考试说明和江苏高考有机综合题的命题要求,学生必须掌握的主要知识储备:
⑴质谱图、红外光谱图、核磁共振氢谱图的解读,不饱和度的理解与应用(注意分子中出现氮原子时的变化),有机物燃烧分析(注意烃与烃的含氧衍生物的燃烧通式的应用以及烃与烃的含氧衍生物的混合物完全燃烧的规律的理解)
⑵有机物中原子的成键特征:碳原子总是形成4个键(关注手性碳原子问题),氮、磷原子总是形成3个键,氧、硫原子总是形成2个键,氢、卤素原子总是形成1个键。
⑶有机物分子中原子共直线、共平面问题:①几个基本模型:C2H2的立体结构,C2H4的立体结构,C6H6的立体结构,④HCHO的立体结构,CH4的立体结构,NH3的立体结构。
⑷熟悉选修5表1-1中给出的有机化合物中的常见官能团的结构和名称,能熟悉键线式、熟练书写有机物的结构简式(注意原子之间的结合方式),能以烷烃的系统命名为基础命名简单的有机化合物。
⑸了解有机化合物存在的典型的同分异构现象(不包括立体异构),如官能团异构,位置异构,碳链异构。以此为基础能熟练对有机综合题流程图中某一中学未见的简单有机物根据题目要求正确书写出结构简式或确定符合条件的同分异构体的数目。
⑹掌握烃(烷烃、烯烃、炔烃和芳香烃)及其衍生物(卤代烃、醇、酚、醛、羧酸、酯)的组成、结构特点和主要性质。并能根据加成、取代、消去、加聚和缩聚等有机反应的特点,能判断典型有机反应的类型。简单归纳如下:
Ⅰ 取代反应:有机物分子中的某些原子或原子团被其它(现成的)原子或原子团所代替的反应。
①卤代反应
……
②硝化反应
③磺化反应*
④酯化反应
⑤成肽反应
⑥水解反应
⑦其它反应
Ⅱ 加成反应:有机物分子中双键(或三键)两端的碳原子(或其它原子)与其它原子或原子团直接结合生成新的化合物的反应。
①与H2加成
+3H2
CH2OH(CHOH)4CHO+H2CH2OH(CHOH)4CH2OH
②与X2加成
③与HX加成
④与H2O加成
Ⅲ 消去反应:有机物化合物在适当的条件下,从一个小分子(如水、卤化氢等分子)而生成不饱和(双键或叁键)的化合物的反应。
Ⅳ 聚合反应:相对分子量较小的化合物彼此结合成相对分子质量较大的化合 物的反应。
①加聚反应:一种或多种不饱和的化合物通过不饱和键的相互加成而形成高分子化合物的反应。
②缩聚反应:单体间相互反应而生成高分子化合物,同时还生成小分子(如水、氨等)的反应
Ⅴ 氧化还原反应:
①有机物的燃烧反应:
②有机物的催化氧化:
③有机物被其它氧化剂氧化:
A.银氨溶液:
CH2OH(CHOH)4CHO+2Ag(NH3)2OH CH2OH(CHOH)4COONH4+3NH3+2Ag↓+H2O
B.新制的Cu(OH)2悬浊液:
CH2OH(CHOH)4CHO+2Cu(OH)2+NaOHCH2OH(CHOH)4COONa+Cu2O+3H2O
C.酸性KMnO4溶液:含碳碳双键、碳碳叁键的有机物,苯的同系物,醇,醛,酚等。
D.溴水:CH3CHO+Br2+H2O→CH3COOH+2HBr
⑺有机合成中链或环的改变,是有机合成流程中亘古不变的话题,如果在考前有所了解,考试时遇到类似的问题学生会有亲近的感觉。
①重氮甲烷()在加热或光照时分解成N2和碳烯(), ,碳烯()与烯烃或苯环能起加成反应,生成有三元环的化合物:。
②在一定条件下,不饱和烃分子可以进行自身加成反应。例如: 。
③在一定条件下卤代烃可以发生下列反应:R—X+2Na+R—X→R—R+2NaX。
④Grignard试剂的合成方法是:RX+MgRMgX(Grignard试剂)。生成的卤代烃基镁与具有羰基结构的化合物(醛、酮等)发生反应,再水解就能合成各种指定结构的醇:
⑤羟醛缩合反应:,。
⑥醛和酮之间也可以相互加成,如。
⑦将羧酸的碱金属盐溶液用惰性电极电解可得到烃类化合物,例如:
⑧。
⑨。……
⑻官能团的保护和恢复是有机合成中常常绕不过的坎,还是让学生先睹为快吧!
①碳碳双键的保护及恢复:与HBr发生加成反应,将双键转化为单键,防止被氧化,再通过卤代烃的消去反应解除保护;或者先与Br2发生加成反应,将双键转化为单键,防止被氧化,再通过在Zn存在的情况下将单键转化为双键解除保护。
②醇羟基的保护及恢复:成醚保护或者成酯保护。
③酚羟基的保护及恢复:
基本原理:
酚甲醚对碱稳定,对酸不稳定。
④醛基(酮基)的保护及恢复:
?基本原理:
缩醛(酮)或环状缩醛(酮)对碱Grignard试剂,金属氢化物等稳定,但对酸不稳定。
⑤羧基的保护及恢复
基本原理:。
⑥氨基的保护及恢复:
基本原理:。
3.有机综合题全面体现了考试说明中的“素养和能力要求”。学生需要在理解化学科学的基础上,敏捷、准确地获取试题所给的相关信息,与已有的不同类型有机化合物之间的转化关系等知识整合,在分析评价的基础上应用新信息,设计合理路线合成简单有机化合物,并能用合成路线图正确的表达化学问题解决的过程和结果。
【真题再现】
1.(2008年江苏卷,19)(12分)苯噁布洛芬是一种消炎镇痛的药物。它的工业合成路线如下:
请回答下列问题:
⑴A长期暴露在空气中会变质,其原因是 ▲ 。
⑵有A到B的反应通常在低温时进行。温度升高时,多硝基取代副产物会增多。下列二硝基取代物中,最可能生成的是 ▲ 。(填字母)
a. b. c. d.
⑶在E的下列同分异构体中,含有手性碳原子的分子是 ▲ 。(填字母)
a. b.
c. d.
⑷F的结构简式 ▲ 。
⑸D的同分异构体H是一种α-氨基酸,H可被酸性KMnO4溶液氧化成对苯二甲酸,则H的结构简式是 ▲ 。高聚物L由H通过肽键连接而成,L的结构简式是 ▲ 。
【参考答案】
⑴酚类化合物易被空气中的O2氧化
⑵a
⑶ac
⑷
⑸ 或
2. (2009年江苏卷,19)(14分)多沙唑嗪盐酸盐是一种用于治疗高血压的药物。多唑嗪的合成路线如下:
⑴写出D中两种含氧官能团的名称: ▲ 和 ▲ 。
⑵写出满足下列条件的D的一种同分异构体的结构简式 ▲ 。
①苯的衍生物,且苯环上的一取代产物只有两种;②与Na2CO3溶液反应放出CO2气体;③水解后的产物才能与FeCl3溶液发生显色反应。
⑶E→F的反应中还可能生成一种有机副产物,该副产物的结构简式为 ▲ 。
⑷由F制备多沙唑嗪的反应中要加入试剂X(C10H10N3O2Cl),X的结构简式为 ▲ 。
⑸苯乙酸乙酯是一种常见的合成香料。请设计合理方案以苯甲醛和乙醇为原料合成苯乙酸乙酯(用合成路线流程图表示,并注明反应条件)。
提示:①R—Br+NaCN→R—CN+NaBr;
②合成过程中无机试剂任选;
③合成路线流程图示例如下:
【参考答案】
2. (2010年江苏卷,19)(14分)阿立哌唑(A)是一种新的抗精神分裂症药物,可由化合物B、C、D在有机溶剂中通过以下两条路线合成得到。
线路一:
线路二:
⑴E的结构简式为 ▲ 。
⑵由C、D生成化合物F的反应类型是 ▲ 。
⑶合成F时还可能生成一种相对分子质量为285的副产物G,G的结构简式为 ▲ 。
⑷H属于α-氨基酸,与B的水解产物互为同分异构体。H能与FeCl3溶液发生显色反应,且苯环上的一氯代物只有2种。写出两种满足上述条件的H的结构简式: ▲ 。
⑸已知:,写出由C制备化合物的合成路
线流程图(无机试剂任选)。合成路线流程图示例如下:
【参考答案】
⑴
⑵取代反应
⑶
⑷
⑸
(凡合理答案均可)
4. (2011年江苏卷,17)(15分)敌草胺是一种除草剂。它的合成路线如下:
回答下列问题:
⑴在空气中久置,A由无色转变为棕色,其原因是 ▲ 。
⑵C分子中有2个含氧官能团,分别为 ▲ 和 ▲ 填官能团名称)。
⑶写出同时满足下列条件的C的一种同分异构体的结构简式: ▲ 。
①能与金属钠反应放出H2;②是萘()的衍生物,且取代基都在同一个苯环上;③可发生水解反应,其中一种水解产物能发生银镜反应,另一种水解产物分子中有5种不同化学环境的氧。
⑷若C不经提纯,产物敌草胺中将混有少量副产物E(分子式为C23H18O3),E是一种酯。E的结构简式为 ▲ 。
⑸已知:,写出以苯酚和乙醇为原料制备的合成路线流程图(无机试剂任用)。合成路线流程图例如下:
【参考答案】
⑴A被空气中的O2氧化
⑵羟基 醚键
⑶
⑷
⑸
5. (2012年江苏卷,17)(15分)化合物H是合成药物盐酸沙格雷酯的重要中间体,其合成路线如下:
⑴化合物A的含氧官能团为 ▲ 和 ▲ (填官能团的名称)。
⑵反应①→⑤中属于取代反应的是 ▲ (填序号)。
⑶写出同时满足下列条件的B的一种同分异构体的结构简式 ▲ 。
I.分子含有两个苯环;II.分子有7个不同化学环境的氢;III.不能与FeCl3溶液发生显色反应,但水解产物之一能发生此反应。
⑷实现D→E的转化中,加入化合物X能发生银镜反应,X的结构简式 ▲ 。
⑸已知:。化合物是合成抗癌药物美发伦的中间体,请写出以和为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
【参考答案】
⑴羟基 醛基
⑵①③⑤
⑶ 或
⑷
⑸
【命题趋势】
1.从近5年的江苏高考卷来看,有机综合题的命制十分稳定。基础部分和选择题交叉考查有机物的组成、官能团的名称和典型的化学性质、反应类型;中等难度部分考查对流程图的识读、理解,要求正确书写流程图中的部分中间产物或者副产物的结构简式;较难部分考查某种中间产物的给定条件的同分异构体的结构简式的书写(连续5年)和合成路线图(连续4年)。
2.近2年的高考试卷获得了较好的评价,正常情况下,2013年的江苏高考卷的有机综合题应该和2011年、2012年相似。
【典型错误】
从2012年江苏高考阅卷及2013届学情调研和“一模”阅卷情况看,学生在有机综合部分的典型错误如下,需要引起足够的重视,防患于未然!
1. 官能团的结构与名称不能对号入座。如“一模”考试中不少学生将“醛基”写成了“羰基”、“酯基”、“酮基”;错别字现象不能容忍,如“一模”考试中出现了“醚健”、“荃基”等。
2.对典型有机反应类型的特点理解不到位,无法准确判断反应的类型。如2012年江苏高考中,对要求判断的几个简单的反应的反应类型出现了漏选和错选;“一模”考试中有学生将A→B的反应类型写成了“消去反应”。
3.有机物的结构简式书写不规范、甚至错误者比比皆是。无论是2012年江苏高考还是“一模”考试中,不少学生书写的苯环的键线式严重变形、“开口笑”或者“出头露角”,碳原子上结合的氢原子个数写错。“一模”考试中,部分学生不注意原子之间的结合方式,将“HCOOCH2CH2-”写成了“-CH2CH2COOH”。
4.缺乏必要的采集信息的能力,对给定条件的同分异构体的确定无法全面把握,顾此失彼。
5.合成路线图没有正确的思路,乱写一气,或者思路正确但化学用语表达不正确导致不得分,尤其是反应条件的选择错误而扣分更为可惜。
【思路方法】
有机综合题是II卷中学生比较好得分的试题之一,“授之以鱼不如授之以渔”,教给学生合适的应对方略,将能拿的分稳稳妥妥的拿到手,争取多拿分!
1.快速通读试题,粗略了解大致要求。此时不对流程图做过多的纠缠,注意题目中另给的已知信息和问题中隐含的相关信息。
2.精心分析流程图,重点关注在不同条件下旧键的断裂和新键的形成方式,可以根据题目的要求对某些中间步骤“一笑而过”。但也要学会敏锐地比对获取信息。
3.稳稳妥妥将基础分拿到手,避免低级失误。如错别字等,也不要用教材中没有出现的名词来代替教材中的专有名词,如“酮基”、“醚基”等。
4.科学把握每一条信息,获得同时满足条件的同分异构体的结构简式。
5.比较目标产物和原料之间的差异,综合中学所学烃和烃的衍生物之间的相互转化关系和题目中的相关信息,包括已知流程图中的相关信息,设计合理的合成路线流程图。 并做科学的表达,尤其是结构简式的书写和反应条件的正确性(告诉学生题目中所给条件是第一位的,其次是书本上所给条件,尽可能不要出现一定条件),防止功亏一篑。
6.不同的学生,要做不同的合理取舍,拿自己该拿的分、能拿的分,不能顾此失彼、因小失大。
【拓展练习】
(15分)物质I的合成路线如下:
已知:
⑴A→B的反应类型为 ▲ ,F中的含氧官能团的名称为 ▲ 和 ▲ 。
⑵满足下列条件的C的同分异构体的结构简式有 ▲ 种。
①苯的衍生物,且苯环上的一氯取代产物只有一种;②苯环上有四个取代基,其中三个为甲氧基(-OCH3),其在苯环上位置与C相同;③含—COO—基团;④与NaOH溶液反应时,1mol 该同分异构体 最多消耗1 mol NaOH。
⑶物质D的结构简式为 ▲ 。
⑷写出F→G的化学方程式 ▲ 。
⑸结合题给相关信息,请写出以甲苯、HCONH2为原料合成的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:。
提示:①; ②;③
【参考答案】
⑴取代反应(1分),醚键(1分)、羧基(1分)
⑵3(3分)
⑶(2分)
⑷+ HCONH2+2H2O(2分)
⑸(5分)
专题三 有机综合题
【考点梳理】
1. 《2013年江苏省高考化学考试说明》中“考试范围和内容”之“有机化合物及其应用”:⑴了解测定有机化合物组成和结构的一般方法。⑵知道有机化合物中碳的成键特征,并能认识手性碳原子。⑶了解常见有机化合物中的官能团,能正确表示简单有机化合物的结构。能根据有机化合物的命名规则命名简单的有机化合物。⑷了解有机化合物存在同分异构现象(不包括立体异构),能判断并正确书写简单有机化合物的同分异构体的结构简式。⑸了解加成、取代、消去、加聚和缩聚等有机反应的特点,能判断典型有机反应的类型。⑹掌握烃(烷烃、烯烃、炔烃和芳香烃)及其衍生物(卤代烃、醇、酚、醛、羧酸、酯)的组成、结构特点和主要性质。能利用不同类型有机化合物之间的转化关系设计合理路线合成简单有机化合物。⑺知道天然气、液化石油气和汽油的主要成分及其应用。⑻了解糖类、油脂、氨基酸和蛋白质的组成、结构特点和主要性质,认识化学科学在生命科学发展中的重要作用。⑼知道简单合成高分子的单体、链节和聚合度,了解合成高分子的性能及其在高新技术领域中的应用。⑽认识有机化合物在生产、生活中的作用和对环境、健康产生的影响。
2.结合考试说明和江苏高考有机综合题的命题要求,学生必须掌握的主要知识储备:
⑴质谱图、红外光谱图、核磁共振氢谱图的解读,不饱和度的理解与应用(注意分子中出现氮原子时的变化),有机物燃烧分析(注意烃与烃的含氧衍生物的燃烧通式的应用以及烃与烃的含氧衍生物的混合物完全燃烧的规律的理解)
⑵有机物中原子的成键特征:碳原子总是形成4个键(关注手性碳原子问题),氮、磷原子总是形成3个键,氧、硫原子总是形成2个键,氢、卤素原子总是形成1个键。
⑶有机物分子中原子共直线、共平面问题:①几个基本模型:C2H2的立体结构,C2H4的立体结构,C6H6的立体结构,④HCHO的立体结构,CH4的立体结构,NH3的立体结构。
⑷熟悉选修5表1-1中给出的有机化合物中的常见官能团的结构和名称,能熟悉键线式、熟练书写有机物的结构简式(注意原子之间的结合方式),能以烷烃的系统命名为基础命名简单的有机化合物。
⑸了解有机化合物存在的典型的同分异构现象(不包括立体异构),如官能团异构,位置异构,碳链异构。以此为基础能熟练对有机综合题流程图中某一中学未见的简单有机物根据题目要求正确书写出结构简式或确定符合条件的同分异构体的数目。
⑹掌握烃(烷烃、烯烃、炔烃和芳香烃)及其衍生物(卤代烃、醇、酚、醛、羧酸、酯)的组成、结构特点和主要性质。并能根据加成、取代、消去、加聚和缩聚等有机反应的特点,能判断典型有机反应的类型。简单归纳如下:
Ⅰ 取代反应:有机物分子中的某些原子或原子团被其它(现成的)原子或原子团所代替的反应。
①卤代反应
……
②硝化反应
③磺化反应*
④酯化反应
⑤成肽反应
⑥水解反应
⑦其它反应
Ⅱ 加成反应:有机物分子中双键(或三键)两端的碳原子(或其它原子)与其它原子或原子团直接结合生成新的化合物的反应。
①与H2加成
+3H2
CH2OH(CHOH)4CHO+H2CH2OH(CHOH)4CH2OH
②与X2加成
③与HX加成
④与H2O加成
Ⅲ 消去反应:有机物化合物在适当的条件下,从一个小分子(如水、卤化氢等分子)而生成不饱和(双键或叁键)的化合物的反应。
Ⅳ 聚合反应:相对分子量较小的化合物彼此结合成相对分子质量较大的化合 物的反应。
①加聚反应:一种或多种不饱和的化合物通过不饱和键的相互加成而形成高分子化合物的反应。
②缩聚反应:单体间相互反应而生成高分子化合物,同时还生成小分子(如水、氨等)的反应
Ⅴ 氧化还原反应:
①有机物的燃烧反应:
②有机物的催化氧化:
③有机物被其它氧化剂氧化:
A.银氨溶液:
CH2OH(CHOH)4CHO+2Ag(NH3)2OH CH2OH(CHOH)4COONH4+3NH3+2Ag↓+H2O
B.新制的Cu(OH)2悬浊液:
CH2OH(CHOH)4CHO+2Cu(OH)2+NaOHCH2OH(CHOH)4COONa+Cu2O+3H2O
C.酸性KMnO4溶液:含碳碳双键、碳碳叁键的有机物,苯的同系物,醇,醛,酚等。
D.溴水:CH3CHO+Br2+H2O→CH3COOH+2HBr
⑺有机合成中链或环的改变,是有机合成流程中亘古不变的话题,如果在考前有所了解,考试时遇到类似的问题学生会有亲近的感觉。
①重氮甲烷()在加热或光照时分解成N2和碳烯(), ,碳烯()与烯烃或苯环能起加成反应,生成有三元环的化合物:。
②在一定条件下,不饱和烃分子可以进行自身加成反应。例如: 。
③在一定条件下卤代烃可以发生下列反应:R—X+2Na+R—X→R—R+2NaX。
④Grignard试剂的合成方法是:RX+MgRMgX(Grignard试剂)。生成的卤代烃基镁与具有羰基结构的化合物(醛、酮等)发生反应,再水解就能合成各种指定结构的醇:
⑤羟醛缩合反应:,。
⑥醛和酮之间也可以相互加成,如。
⑦将羧酸的碱金属盐溶液用惰性电极电解可得到烃类化合物,例如:
⑧。
⑨。……
⑻官能团的保护和恢复是有机合成中常常绕不过的坎,还是让学生先睹为快吧!
①碳碳双键的保护及恢复:与HBr发生加成反应,将双键转化为单键,防止被氧化,再通过卤代烃的消去反应解除保护;或者先与Br2发生加成反应,将双键转化为单键,防止被氧化,再通过在Zn存在的情况下将单键转化为双键解除保护。
②醇羟基的保护及恢复:成醚保护或者成酯保护。
③酚羟基的保护及恢复:
基本原理:
酚甲醚对碱稳定,对酸不稳定。
④醛基(酮基)的保护及恢复:
?基本原理:
缩醛(酮)或环状缩醛(酮)对碱Grignard试剂,金属氢化物等稳定,但对酸不稳定。
⑤羧基的保护及恢复
基本原理:。
⑥氨基的保护及恢复:
基本原理:。
3.有机综合题全面体现了考试说明中的“素养和能力要求”。学生需要在理解化学科学的基础上,敏捷、准确地获取试题所给的相关信息,与已有的不同类型有机化合物之间的转化关系等知识整合,在分析评价的基础上应用新信息,设计合理路线合成简单有机化合物,并能用合成路线图正确的表达化学问题解决的过程和结果。
【真题再现】
1.(2008年江苏卷,19)(12分)苯噁布洛芬是一种消炎镇痛的药物。它的工业合成路线如下:
请回答下列问题:
⑴A长期暴露在空气中会变质,其原因是 ▲ 。
⑵有A到B的反应通常在低温时进行。温度升高时,多硝基取代副产物会增多。下列二硝基取代物中,最可能生成的是 ▲ 。(填字母)
a. b. c. d.
⑶在E的下列同分异构体中,含有手性碳原子的分子是 ▲ 。(填字母)
a. b.
c. d.
⑷F的结构简式 ▲ 。
⑸D的同分异构体H是一种α-氨基酸,H可被酸性KMnO4溶液氧化成对苯二甲酸,则H的结构简式是 ▲ 。高聚物L由H通过肽键连接而成,L的结构简式是 ▲ 。
【参考答案】
⑴酚类化合物易被空气中的O2氧化
⑵a
⑶ac
⑷
⑸ 或
2. (2009年江苏卷,19)(14分)多沙唑嗪盐酸盐是一种用于治疗高血压的药物。多唑嗪的合成路线如下:
⑴写出D中两种含氧官能团的名称: ▲ 和 ▲ 。
⑵写出满足下列条件的D的一种同分异构体的结构简式 ▲ 。
①苯的衍生物,且苯环上的一取代产物只有两种;②与Na2CO3溶液反应放出CO2气体;③水解后的产物才能与FeCl3溶液发生显色反应。
⑶E→F的反应中还可能生成一种有机副产物,该副产物的结构简式为 ▲ 。
⑷由F制备多沙唑嗪的反应中要加入试剂X(C10H10N3O2Cl),X的结构简式为 ▲ 。
⑸苯乙酸乙酯是一种常见的合成香料。请设计合理方案以苯甲醛和乙醇为原料合成苯乙酸乙酯(用合成路线流程图表示,并注明反应条件)。
提示:①R—Br+NaCN→R—CN+NaBr;
②合成过程中无机试剂任选;
③合成路线流程图示例如下:
【参考答案】
2. (2010年江苏卷,19)(14分)阿立哌唑(A)是一种新的抗精神分裂症药物,可由化合物B、C、D在有机溶剂中通过以下两条路线合成得到。
线路一:
线路二:
⑴E的结构简式为 ▲ 。
⑵由C、D生成化合物F的反应类型是 ▲ 。
⑶合成F时还可能生成一种相对分子质量为285的副产物G,G的结构简式为 ▲ 。
⑷H属于α-氨基酸,与B的水解产物互为同分异构体。H能与FeCl3溶液发生显色反应,且苯环上的一氯代物只有2种。写出两种满足上述条件的H的结构简式: ▲ 。
⑸已知:,写出由C制备化合物的合成路
线流程图(无机试剂任选)。合成路线流程图示例如下:
【参考答案】
⑴
⑵取代反应
⑶
⑷
⑸
(凡合理答案均可)
4. (2011年江苏卷,17)(15分)敌草胺是一种除草剂。它的合成路线如下:
回答下列问题:
⑴在空气中久置,A由无色转变为棕色,其原因是 ▲ 。
⑵C分子中有2个含氧官能团,分别为 ▲ 和 ▲ 填官能团名称)。
⑶写出同时满足下列条件的C的一种同分异构体的结构简式: ▲ 。
①能与金属钠反应放出H2;②是萘()的衍生物,且取代基都在同一个苯环上;③可发生水解反应,其中一种水解产物能发生银镜反应,另一种水解产物分子中有5种不同化学环境的氧。
⑷若C不经提纯,产物敌草胺中将混有少量副产物E(分子式为C23H18O3),E是一种酯。E的结构简式为 ▲ 。
⑸已知:,写出以苯酚和乙醇为原料制备的合成路线流程图(无机试剂任用)。合成路线流程图例如下:
【参考答案】
⑴A被空气中的O2氧化
⑵羟基 醚键
⑶
⑷
⑸
5. (2012年江苏卷,17)(15分)化合物H是合成药物盐酸沙格雷酯的重要中间体,其合成路线如下:
⑴化合物A的含氧官能团为 ▲ 和 ▲ (填官能团的名称)。
⑵反应①→⑤中属于取代反应的是 ▲ (填序号)。
⑶写出同时满足下列条件的B的一种同分异构体的结构简式 ▲ 。
I.分子含有两个苯环;II.分子有7个不同化学环境的氢;III.不能与FeCl3溶液发生显色反应,但水解产物之一能发生此反应。
⑷实现D→E的转化中,加入化合物X能发生银镜反应,X的结构简式 ▲ 。
⑸已知:。化合物是合成抗癌药物美发伦的中间体,请写出以和为原料制备该化合物的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
【参考答案】
⑴羟基 醛基
⑵①③⑤
⑶ 或
⑷
⑸
【命题趋势】
1.从近5年的江苏高考卷来看,有机综合题的命制十分稳定。基础部分和选择题交叉考查有机物的组成、官能团的名称和典型的化学性质、反应类型;中等难度部分考查对流程图的识读、理解,要求正确书写流程图中的部分中间产物或者副产物的结构简式;较难部分考查某种中间产物的给定条件的同分异构体的结构简式的书写(连续5年)和合成路线图(连续4年)。
2.近2年的高考试卷获得了较好的评价,正常情况下,2013年的江苏高考卷的有机综合题应该和2011年、2012年相似。
【典型错误】
从2012年江苏高考阅卷及2013届学情调研和“一模”阅卷情况看,学生在有机综合部分的典型错误如下,需要引起足够的重视,防患于未然!
1. 官能团的结构与名称不能对号入座。如“一模”考试中不少学生将“醛基”写成了“羰基”、“酯基”、“酮基”;错别字现象不能容忍,如“一模”考试中出现了“醚健”、“荃基”等。
2.对典型有机反应类型的特点理解不到位,无法准确判断反应的类型。如2012年江苏高考中,对要求判断的几个简单的反应的反应类型出现了漏选和错选;“一模”考试中有学生将A→B的反应类型写成了“消去反应”。
3.有机物的结构简式书写不规范、甚至错误者比比皆是。无论是2012年江苏高考还是“一模”考试中,不少学生书写的苯环的键线式严重变形、“开口笑”或者“出头露角”,碳原子上结合的氢原子个数写错。“一模”考试中,部分学生不注意原子之间的结合方式,将“HCOOCH2CH2-”写成了“-CH2CH2COOH”。
4.缺乏必要的采集信息的能力,对给定条件的同分异构体的确定无法全面把握,顾此失彼。
5.合成路线图没有正确的思路,乱写一气,或者思路正确但化学用语表达不正确导致不得分,尤其是反应条件的选择错误而扣分更为可惜。
【思路方法】
有机综合题是II卷中学生比较好得分的试题之一,“授之以鱼不如授之以渔”,教给学生合适的应对方略,将能拿的分稳稳妥妥的拿到手,争取多拿分!
1.快速通读试题,粗略了解大致要求。此时不对流程图做过多的纠缠,注意题目中另给的已知信息和问题中隐含的相关信息。
2.精心分析流程图,重点关注在不同条件下旧键的断裂和新键的形成方式,可以根据题目的要求对某些中间步骤“一笑而过”。但也要学会敏锐地比对获取信息。
3.稳稳妥妥将基础分拿到手,避免低级失误。如错别字等,也不要用教材中没有出现的名词来代替教材中的专有名词,如“酮基”、“醚基”等。
4.科学把握每一条信息,获得同时满足条件的同分异构体的结构简式。
5.比较目标产物和原料之间的差异,综合中学所学烃和烃的衍生物之间的相互转化关系和题目中的相关信息,包括已知流程图中的相关信息,设计合理的合成路线流程图。 并做科学的表达,尤其是结构简式的书写和反应条件的正确性(告诉学生题目中所给条件是第一位的,其次是书本上所给条件,尽可能不要出现一定条件),防止功亏一篑。
6.不同的学生,要做不同的合理取舍,拿自己该拿的分、能拿的分,不能顾此失彼、因小失大。
【拓展练习】
(15分)物质I的合成路线如下:
已知:
⑴A→B的反应类型为 ▲ ,F中的含氧官能团的名称为 ▲ 和 ▲ 。
⑵满足下列条件的C的同分异构体的结构简式有 ▲ 种。
①苯的衍生物,且苯环上的一氯取代产物只有一种;②苯环上有四个取代基,其中三个为甲氧基(-OCH3),其在苯环上位置与C相同;③含—COO—基团;④与NaOH溶液反应时,1mol 该同分异构体 最多消耗1 mol NaOH。
⑶物质D的结构简式为 ▲ 。
⑷写出F→G的化学方程式 ▲ 。
⑸结合题给相关信息,请写出以甲苯、HCONH2为原料合成的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:。
提示:①; ②;③
【参考答案】
⑴取代反应(1分),醚键(1分)、羧基(1分)
⑵3(3分)
⑶(2分)
⑷+ HCONH2+2H2O(2分)
⑸(5分)
同课章节目录
