化学:第2章《元素与物质世界》复习课件(鲁科版必修1)
文档属性
| 名称 | 化学:第2章《元素与物质世界》复习课件(鲁科版必修1) |  | |
| 格式 | zip | ||
| 文件大小 | 288.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2013-03-29 06:32:46 | ||
图片预览



文档简介
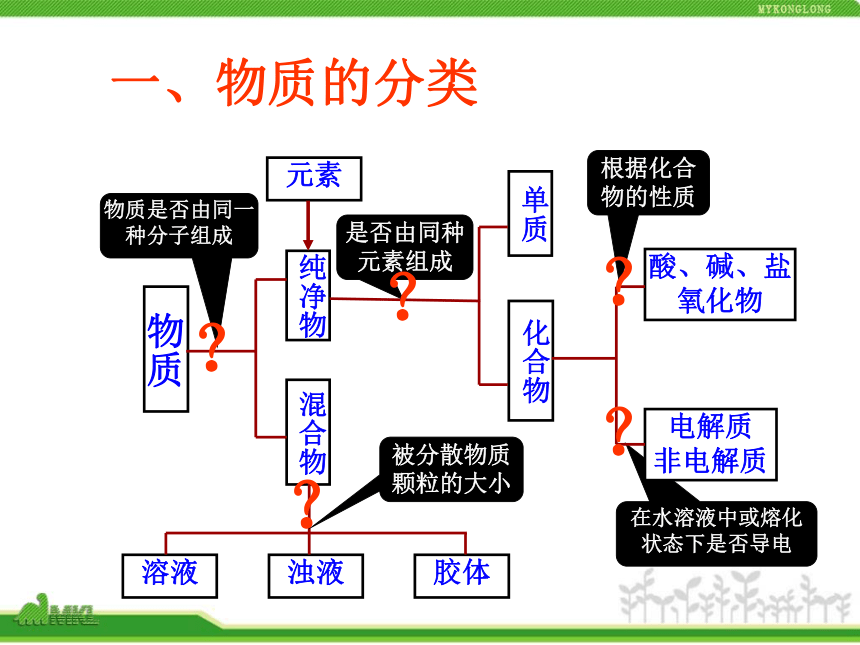
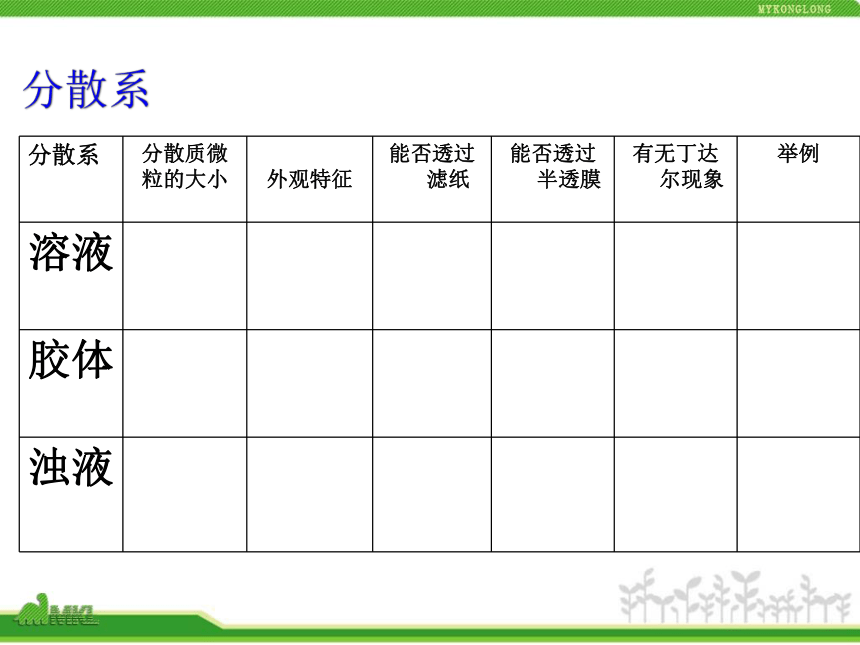
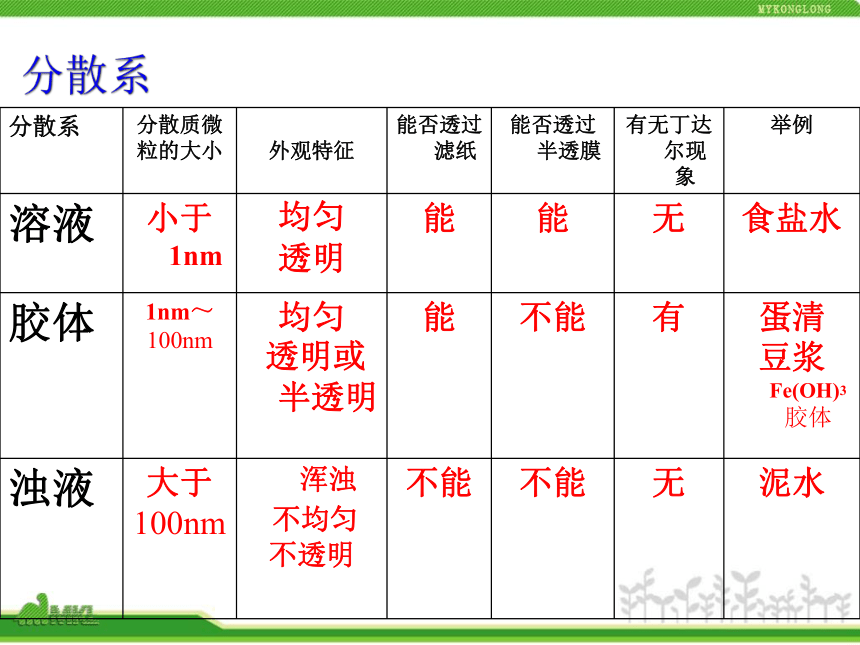
课件18张PPT。第二章 元素与物质世界根据化合物的性质在水溶液中或熔化状态下是否导电一、物质的分类物质是否由同一种分子组成是否由同种元素组成被分散物质颗粒的大小????? 分散系 分散系(1)在物质的分类中,下列属于同一范畴的物质
是( )
①NaCl ②(NH4)2SO4 ③ NH3·H2O ④KOH
⑤ Fe(OH)3 ⑥HNO3
A. ③④⑤ B. ①③⑥ C. ②③⑤ D. ②③⑥
(2)下列关于胶体的叙述不正确的是 ( )
A. 利用电泳现象可以区别溶液和胶体
B. 胶体都可以发生丁达尔现象
C. 胶体粒子的大小都在1nm-100nm之间
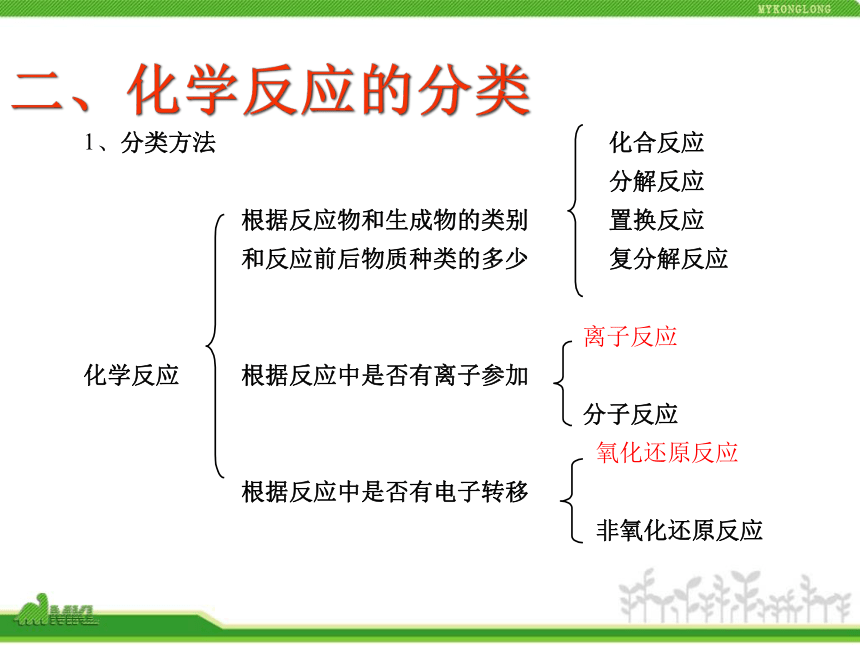
D. 氢氧化铁胶体在电场作用下向正极移动 AA D二、化学反应的分类 2.离子反应
(1)定义:有离子参加的一类反应。
(2)发生条件(复分解类型):生成难溶物、
生成难电离物、生成挥发性物质。
(3)表示方法——离子方程式书写方法离子方程式特点1)下列离子方程式正确的是( )
A. 碳酸钙与盐酸反应:
CaCO3 +2H+=Ca2+ +H2O +CO2 ↑
B. 锌与盐酸反应:
Zn +2H+ +2Cl- =Zn2++2Cl- + H2 ↑
C. 氯化铁溶液与氢氧化钠溶液反应:
Fe3+ +3OH- = Fe(OH)3 ↓
D. Cl2 通入FeCl2 溶液
Cl2 +Fe2+ = 2Cl-+ Fe3+AC2)下列离子方程式正确的是 ( )
A. 澄清石灰水与稀盐酸反应:
Ca(OH)2 + 2H+=Ca2+ +2H2O
B. 钠与水反应:
Na +2H2O = Na+ +2OH- +H2 ↑
C. 铜片插入硝酸银溶液中:
Cu + Ag+= Cu2+ +Ag
D. 大理石溶于醋酸的反应:
CaCO3 + 2CH3COOH= Ca2++2CH3COO-
+CO2↑+H2O D3)下列离子方程式中正确的是( )
A. 小苏打溶液与稀硫酸混合
CO32- + 2H + =CO2 ↑ +H2O
B. 大理石溶液与醋酸
CaCO3 + 2H+ =Ca2+ +CO2 ↑ +H2O
C. 硫酸亚铁溶液与过氧化氢溶液混合
Fe2+ +2H2O2 +4H+ = Fe3+ + 4H2O
D. 氨水与醋酸溶液反应
NH3·H2O + CH3COOH = CH3COO-+
NH4+ +H2O D3. 氧化还原反应
(1)特征:元素的化合价发生变化
(2)实质:电子转移
(3)概念和关系
化合价升高 →失e- → 发生氧化反应 →做还原剂 →被氧化→生成氧化产物
化合价降低 →得e- → 发生还原反应 →做氧化剂 →被还原→生成还原产物
(4)电子转移的表示方法:1.下列有关氧化还原反应的叙述正确的是( )
A. 肯定有一种元素被氧化,另一种元素被还原
B. 在反应中不一定所有元素的化合价都发生变化
C. 置换反应一定属于氧化还原反应
D. 化合反应和复分解反应不可能有氧化还原反应练 习BC2.已知X2、Y2、Z2、W2四种物质的氧化能力为:W2>Z2 >X2 >Y2,下列氧化还原反应能发生的是( )
A .2NaW+ Z2 =2NaZ + W2
B. 2NaX + Z2 =2NaZ +X2
C. 2NaY + W2 =2NaW + Y2
D. 2NaZ +X2 =2NaX +Z2
3.亚硝酸(HNO2)既可做氧化剂又可做还原剂,当它在反应中做氧化剂时,可能生成的产物是( )
A. N2 B. N2O3 C. NH4+ D. NO2 BCAC4. 硫代硫酸钠(Na2S2O3)可作为脱氯剂,如Na2S2O3 和氯气反应,可将氯气完全转化为CI- 从而消除氯气对环境的污染,则在该反应中S2O32-不能转化为( )
A. S2- B. SO2 C. S D. SO42-
5. 法医常用“马氏试砷法”来证明是否为砒霜(As2O3)中毒。方法是:用锌.盐酸与被检验试样混和,若有砒霜,则发生反应生成砷化氢、氯化锌。下列对这一反应的叙述中,正确的是( )
A. 盐酸做氧化剂 B. 砒霜做氧化剂
C. 锌和盐酸做还原剂 D. 盐酸做还原剂ACB三、铁及其化合物的氧化性和还原性
1.Fe的还原性:与Cl2、O2 、H+、Cu2+、Fe3+ 等反
应,表现了铁较活泼的化学性质。
2.Fe3+的氧化性:
Fe3+具有较强的氧化性,可以将Fe Cu Zn
KI等氧化,而本身被还原为Fe2+.
3.Fe2+的氧化性和还原性:
①氧化性:Fe2+可以被Zn还原。
②还原性:Fe2+可以被Cl2 O2 KMnO4
HNO3等 氧化。[小结] “铁三角”H+ Cu2+ Fe3+ Zn H2 CO Zn H2 CO Cl2 HNO3Fe Cu Zn I- SO2 Cl2 HNO3 H2O2 KMnO4(1)下列叙述正确的是( )
A. 含最高价元素的化合物,一定具有强
的氧化性
B. 阳离子只有氧化性,阴离子只有还原性
C. 失电子多的还原剂,还原性就强
D. 在化学反应中,某元素由化合态变为游
离态,此元素可能被氧化,也可能被还原
(2)除去FeCl2溶液中的少量FeCl3 ,可加入
____________;除去FeCl3溶液中的少量
FeCl2 ,可加入___________,除去FeCl2溶
液中的少量CuCl2,可加入__________。D铁粉氯水铁粉(3) 已知铜在常温下能被HNO3 溶解。反应方程式为:
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO↑ +4H2O
1)请将上述反应改成离子方程式
_________________________________ ,
2)上述反应中,氧化剂是_________,氧化产物是__________。HNO3 没有全部参加氧化还原反应,没有参加氧化还原反应的硝酸占参加反应的全部硝酸的_____。
Cu(NO3)23Cu + 8H++2NO3- = 3Cu2++ 2NO↑+4H2O
HNO33/4
是( )
①NaCl ②(NH4)2SO4 ③ NH3·H2O ④KOH
⑤ Fe(OH)3 ⑥HNO3
A. ③④⑤ B. ①③⑥ C. ②③⑤ D. ②③⑥
(2)下列关于胶体的叙述不正确的是 ( )
A. 利用电泳现象可以区别溶液和胶体
B. 胶体都可以发生丁达尔现象
C. 胶体粒子的大小都在1nm-100nm之间
D. 氢氧化铁胶体在电场作用下向正极移动 AA D二、化学反应的分类 2.离子反应
(1)定义:有离子参加的一类反应。
(2)发生条件(复分解类型):生成难溶物、
生成难电离物、生成挥发性物质。
(3)表示方法——离子方程式书写方法离子方程式特点1)下列离子方程式正确的是( )
A. 碳酸钙与盐酸反应:
CaCO3 +2H+=Ca2+ +H2O +CO2 ↑
B. 锌与盐酸反应:
Zn +2H+ +2Cl- =Zn2++2Cl- + H2 ↑
C. 氯化铁溶液与氢氧化钠溶液反应:
Fe3+ +3OH- = Fe(OH)3 ↓
D. Cl2 通入FeCl2 溶液
Cl2 +Fe2+ = 2Cl-+ Fe3+AC2)下列离子方程式正确的是 ( )
A. 澄清石灰水与稀盐酸反应:
Ca(OH)2 + 2H+=Ca2+ +2H2O
B. 钠与水反应:
Na +2H2O = Na+ +2OH- +H2 ↑
C. 铜片插入硝酸银溶液中:
Cu + Ag+= Cu2+ +Ag
D. 大理石溶于醋酸的反应:
CaCO3 + 2CH3COOH= Ca2++2CH3COO-
+CO2↑+H2O D3)下列离子方程式中正确的是( )
A. 小苏打溶液与稀硫酸混合
CO32- + 2H + =CO2 ↑ +H2O
B. 大理石溶液与醋酸
CaCO3 + 2H+ =Ca2+ +CO2 ↑ +H2O
C. 硫酸亚铁溶液与过氧化氢溶液混合
Fe2+ +2H2O2 +4H+ = Fe3+ + 4H2O
D. 氨水与醋酸溶液反应
NH3·H2O + CH3COOH = CH3COO-+
NH4+ +H2O D3. 氧化还原反应
(1)特征:元素的化合价发生变化
(2)实质:电子转移
(3)概念和关系
化合价升高 →失e- → 发生氧化反应 →做还原剂 →被氧化→生成氧化产物
化合价降低 →得e- → 发生还原反应 →做氧化剂 →被还原→生成还原产物
(4)电子转移的表示方法:1.下列有关氧化还原反应的叙述正确的是( )
A. 肯定有一种元素被氧化,另一种元素被还原
B. 在反应中不一定所有元素的化合价都发生变化
C. 置换反应一定属于氧化还原反应
D. 化合反应和复分解反应不可能有氧化还原反应练 习BC2.已知X2、Y2、Z2、W2四种物质的氧化能力为:W2>Z2 >X2 >Y2,下列氧化还原反应能发生的是( )
A .2NaW+ Z2 =2NaZ + W2
B. 2NaX + Z2 =2NaZ +X2
C. 2NaY + W2 =2NaW + Y2
D. 2NaZ +X2 =2NaX +Z2
3.亚硝酸(HNO2)既可做氧化剂又可做还原剂,当它在反应中做氧化剂时,可能生成的产物是( )
A. N2 B. N2O3 C. NH4+ D. NO2 BCAC4. 硫代硫酸钠(Na2S2O3)可作为脱氯剂,如Na2S2O3 和氯气反应,可将氯气完全转化为CI- 从而消除氯气对环境的污染,则在该反应中S2O32-不能转化为( )
A. S2- B. SO2 C. S D. SO42-
5. 法医常用“马氏试砷法”来证明是否为砒霜(As2O3)中毒。方法是:用锌.盐酸与被检验试样混和,若有砒霜,则发生反应生成砷化氢、氯化锌。下列对这一反应的叙述中,正确的是( )
A. 盐酸做氧化剂 B. 砒霜做氧化剂
C. 锌和盐酸做还原剂 D. 盐酸做还原剂ACB三、铁及其化合物的氧化性和还原性
1.Fe的还原性:与Cl2、O2 、H+、Cu2+、Fe3+ 等反
应,表现了铁较活泼的化学性质。
2.Fe3+的氧化性:
Fe3+具有较强的氧化性,可以将Fe Cu Zn
KI等氧化,而本身被还原为Fe2+.
3.Fe2+的氧化性和还原性:
①氧化性:Fe2+可以被Zn还原。
②还原性:Fe2+可以被Cl2 O2 KMnO4
HNO3等 氧化。[小结] “铁三角”H+ Cu2+ Fe3+ Zn H2 CO Zn H2 CO Cl2 HNO3Fe Cu Zn I- SO2 Cl2 HNO3 H2O2 KMnO4(1)下列叙述正确的是( )
A. 含最高价元素的化合物,一定具有强
的氧化性
B. 阳离子只有氧化性,阴离子只有还原性
C. 失电子多的还原剂,还原性就强
D. 在化学反应中,某元素由化合态变为游
离态,此元素可能被氧化,也可能被还原
(2)除去FeCl2溶液中的少量FeCl3 ,可加入
____________;除去FeCl3溶液中的少量
FeCl2 ,可加入___________,除去FeCl2溶
液中的少量CuCl2,可加入__________。D铁粉氯水铁粉(3) 已知铜在常温下能被HNO3 溶解。反应方程式为:
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO↑ +4H2O
1)请将上述反应改成离子方程式
_________________________________ ,
2)上述反应中,氧化剂是_________,氧化产物是__________。HNO3 没有全部参加氧化还原反应,没有参加氧化还原反应的硝酸占参加反应的全部硝酸的_____。
Cu(NO3)23Cu + 8H++2NO3- = 3Cu2++ 2NO↑+4H2O
HNO33/4
