专题3第一单元脂肪烃的性质及应用-——课后训练(word版 含解析)
文档属性
| 名称 | 专题3第一单元脂肪烃的性质及应用-——课后训练(word版 含解析) |
|
|
| 格式 | docx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-05-09 00:00:00 | ||
图片预览




文档简介
专题3第一单元脂肪烃的性质及应用
一、选择题(共16题)
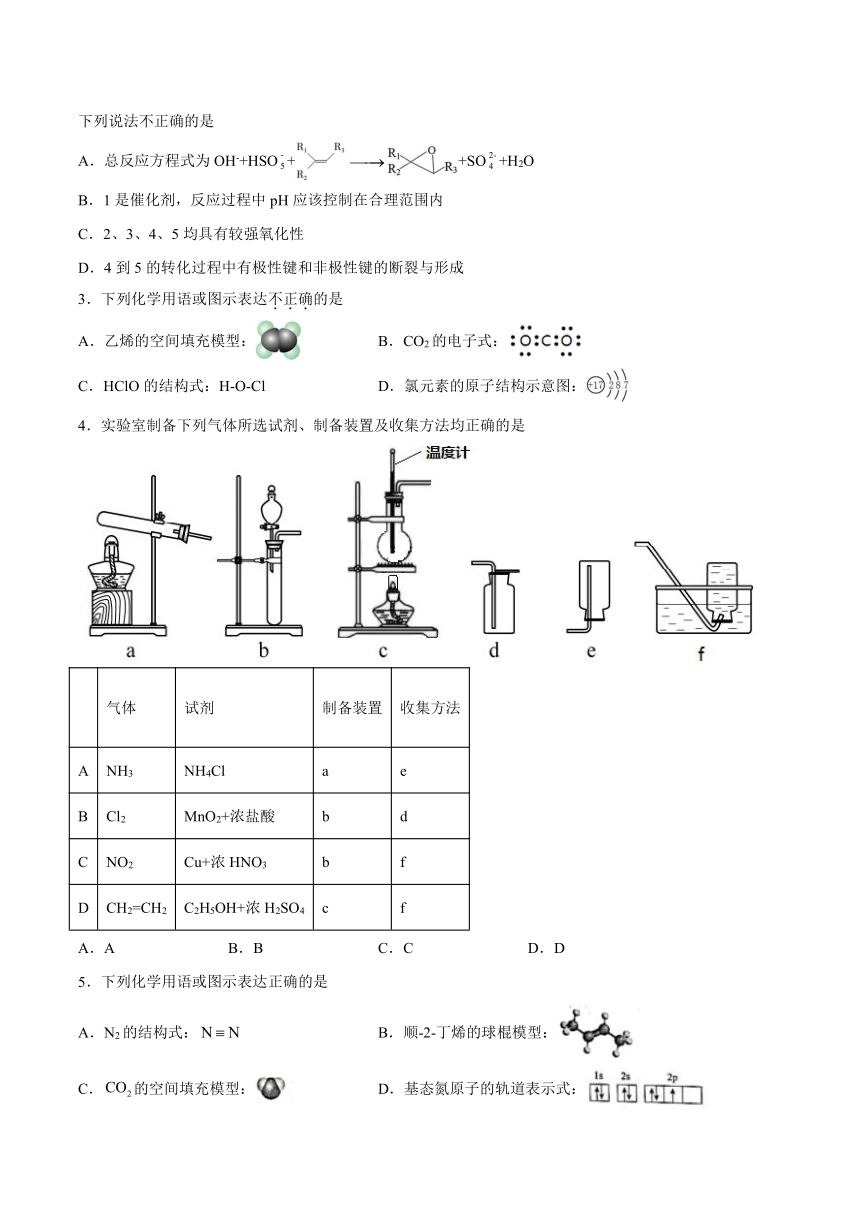
1.已知反-2-丁烯转化为顺-2-丁烯反应如下,,和随温度变化的曲线如图。下列有关该反应的说法正确的是
A.反-2-丁烯与顺-2-丁烯互为位置异构体
B.温度变化对的影响程度小于对的影响程度
C.正反应的活化能大于逆反应的活化能
D.顺-2-丁烯比反-2-丁烯稳定
2.烯烃不对称环氧化在药物合成中应用广泛,如图为手性酮催化的烯烃不对称环氧化反应的机理图(部分产物未写出):
下列说法不正确的是
A.总反应方程式为OH-+HSO++SO+H2O
B.1是催化剂,反应过程中pH应该控制在合理范围内
C.2、3、4、5均具有较强氧化性
D.4到5的转化过程中有极性键和非极性键的断裂与形成
3.下列化学用语或图示表达不正确的是
A.乙烯的空间填充模型: B.CO2的电子式:
C.HClO的结构式:H-O-Cl D.氯元素的原子结构示意图:
4.实验室制备下列气体所选试剂、制备装置及收集方法均正确的是
气体 试剂 制备装置 收集方法
A NH3 NH4Cl a e
B Cl2 MnO2+浓盐酸 b d
C NO2 Cu+浓HNO3 b f
D CH2=CH2 C2H5OH+浓H2SO4 c f
A.A B.B C.C D.D
5.下列化学用语或图示表达正确的是
A.N2的结构式: B.顺-2-丁烯的球棍模型:
C.的空间填充模型: D.基态氮原子的轨道表示式:
6.DHA(二十二碳六烯酸)俗称脑黄金,是神经系统细胞生长及维持的一种主要成分。下列有关该物质的说法中正确的是
A.分子式为 B.能使酸性高锰酸钾溶液褪色
C.1molDHA完全燃烧消耗26mol D.1molDHA最多与7mol发生加成反应
7.已知烯烃(RCH=CHR')臭氧化反应时C=C键发生断裂,被氧化成RCHO和R'CHO。下列烯烃发生臭氧化反应有甲醛生成的是
A. B.
C. D.
8.①正丁烷;②异丁烷;③正戊烷;④异戊烷;⑤新戊烷;⑥丙烷,物质的沸点由高到低的排列顺序是
A.③>④>⑤>①>②>⑥ B.③>④>⑤>②>①>⑥
C.④>③>⑤>①>②>⑥ D.⑥>③>⑤>①>②>④
9.高聚物A在生物医学上有广泛应用。以N—乙烯基吡咯烷酮(NVP)和甲基丙烯酸β—羟乙酯(HEMA)为原料合成路线如图:
下列说法正确的是
A.HEMA具有顺反异构
B.1mol高聚物A可以与2molNaOH反应
C.NVP分子式为C6H9NO
D.HEMA和NVP通过缩聚反应生成高聚物A
10.用如图所示装置能制备下列干燥的气体,且能控制反应的发生和停止的是(甲、乙、丙表示加入的试剂,部分夹持装置省略)
选项 气体 甲 乙 丙
A Cl2 浓盐酸 二氧化锰 氯化钙
B CO2 稀硫酸 石灰石 五氧化二磷
C C2H2 饱和食盐水 电石 碱石灰
D H2 稀硫酸 锌粒 碱石灰
A.A B.B C.C D.D
11.瞬时胶粘剂“502”主要成分为氰基丙烯酸乙酯,结构简式如图所示。下列说法错误的是
A.氰基丙烯酸乙酯无色、无味、无毒性
B.氰基能深入蛋白质内部与蛋白质端基的氨基、羧基形成氢键
C.氰基丙烯酸乙酯能发生加聚反应
D.第一电离能:
12.下列“类比”结果不正确的是
A.PH3分子的空间构型为三角锥形,则NCl3分子的空间构型也为三角锥形
B.FeS+H2SO4=FeSO4+H2S↑,则CuS+H2SO4 = CuSO4+H2S↑
C.NH3的水溶液显碱性,则甲胺(CH3NH2)的水溶液也显碱性
D.CaC2与水反应生成乙炔,则Mg2C3与水反应生成丙炔
13.已知丙烯与HCl发生加成反应有两种可能,如图1所示;其中丙烯加H+的位能曲线图如图2所示。下列说法错误的是
A.生成①的过程所需活化能较低,速率快
B.过渡态(Ⅰ)比过渡态(Ⅱ)稳定
C.碳碳双键易断裂,能与HBr、H2O等发生加成反应
D.丙烯与HCl发生加成反应,主要生成产物④
14.下列“类比”合理的是
A.Cu在Cl2中燃烧生成CuCl2,则Fe在Cl2中燃烧生成FeCl2
B.电解熔融NaCl生成Na和Cl2,则电解熔融AlCl3生成Al和Cl2
C.根据较强酸可以制取较弱酸的规律,推出CO2通入Na2SiO3溶液中能生成H2SiO3
D.氮气因三键而性质稳定,故乙炔也因三键而性质稳定
15.已知X、Y、Z、W是原子序数依次增大的短周期主族元素,位于三个不同的周期。由X、Y、Z组成的某有机物常用于合成高分子化合物,其结构如下图所示。W原子的最外层电子数比Z多。相关说法正确的是
A.该有机物不能使酸性溶液退色
B.Y、Z、W可以组成各原子均满足8电子稳定结构的某种微粒
C.Z的氢化物熔点一定高于Y的氢化物
D.氧化物对应水化物的酸性:W一定比Z强
16.设为阿伏伽德罗常数的值。下列叙述错误的是
A.10 g 60%的乙酸水溶液中含有的氧原子总数为
B.1 L 溶液中含有的数目为
C.72 g与FeO的混合物中含有的阴离子总数为
D.与在光照条件下反应,当消耗1 mol时,生成HCl的数目为
二、综合题
17.有机物X的合成流程图如图:
已知:
①醛类物质能发生银镜反应
②+
(1)化合物B中官能团的名称____。
(2)A生成B的反应类型为____,A生成B的化学方程式____。
(3)化合物C的名称是____。
(4)化合物D的化学式为____,在一定条件下能与H2O发生加成反应,试写出所有可能产物的结构简式____。
(5)符合下列条件的X的同分异构体有____种。(不考虑立体异构)
a.含有六元环结构
b.六元环上有两个取代基,分别连接在不同碳上
c.能发生银镜反应
18.有机物的合成流程图如下:
(1)化合物B中官能团的名称_______。
(2)A生成B的反应类型为_______,A生成B的化学方程式_______。
(3)化合物A能发生加聚反应合成一种塑料,该塑料的结构简式为_______。
(4)化合物G的一氯取代产物有_______种。(不考虑立体异构)
(5)化合物D的化学式为_______,在一定条件下能与发生加成反应,试写出所有可能产物的结构简式_______。
19.回答下列问题:
I.煤的综合利用,是推进能源革命的重要方向。
请回答下列问题:
(1)煤经过操作X可获得出炉煤气 焦炭 煤焦油等产品,操作X的名称是___________。
(2)出炉煤气中含有丙烯(),医用口罩中对阻挡病毒起关键作用的是熔喷布(主要原料是聚丙烯),由丙烯在一定条件下制取聚丙烯的化学方程式是___________。
(3)焦炭与水蒸气反应生成合成气,进而可制备乙二醇(),乙二醇与乙醇___________(填“是”或“不是”)同系物。
(4)出炉煤气和煤焦油中都含有苯,用苯制取溴苯的化学方程式是___________。
II.乙酸环己酯是一种香料,可用于配制苹果、香蕉等果香型香精。一种制备乙酸环己酯的合成路线如下:
回答下列问题:
(5)由石油获得E的生产工艺称为___________。
(6)G中官能团名称是_______,在反应①~④中,原子利用率理论上可达100%的是_____(填序号)。
(7)X是E的同系物,其相对分子质量比E大42,X可能的结构有_____种,其中含3个的X结构简式为____________。
20.某烃A0.2mol在氧气中充分燃烧后,生成化合物B、C各1.2mol,试回答:
(1)烃A的分子式是___。
(2)若取一定量的烃A充分燃烧后,生成B、C各3mol,则有___g的A参加了反应,燃烧时消耗标准状况下的氧气___L。
(3)若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯代物只有一种,则烃A的结构简式是___。
(4)若烃A能使溴水褪色,在催化剂作用下与H2发生加成反应后生成C(CH3)3CH2CH3,则A的结构简式为__。
(5)若烃A能使溴水褪色,且分子中所有碳原子共平面,则A的结构简式为___。
(6)比A少2个碳原子的A的烯烃的同系物的同分异构体共有___种。
21.Ⅰ.现有下列六种烃:① ② ③乙烷④戊烷⑤ ⑥
(1)用系统命名法命名有机物①____,②③④⑤四种物质按它们的沸点由高到低的顺序排列____(填序号),⑥的二氯代物有____种。
(2)Ⅱ.聚氯乙烯,简称PVC,是一种在建筑材料、工业制品等方面广泛应用的通用塑料,若以乙炔(CH≡CH)为原料合成聚氯乙烯,流程如图。
CH≡CHPVC
乙炔与①反应的有机反应类型为____,②的官能团名称为____。写出由②生成PVC的反应方程式____。
(3)异戊二烯是重要的有机化工原料,其结构简式为CH2=C(CH3)CH=CH2,它与溴水反应最多可以得到____种产物。若烃X与异戊二烯具有相同的分子式,与Br2/CCl4反应后得到3—甲基—1,1,2,2—四溴丁烷,则烃X的结构简式为____。
22.回答下列问题:
(1)邻羟基苯甲酸俗名水杨酸,其结构简式为,水杨酸的同分异构体中有一类物质属于酚类,但不属于酯类也不属于酸类,则它的结构中除了羟基之外,必定还有的官能团的电子式_______,这类物质的结构式共有_______种。
(2)某炔烃与足量的氢气催化加成得到烷烃,且烷烃满足的条件:①主链含5个碳原子②两个支链:一个甲基、一个乙基。则该炔烃可能有_______种结构。
(3)现有一种共轭二烯烃(分子中含有两个相隔一个单键的碳碳双键的烯烃叫共轭二烯烃)A。A与足量H2充分反应后得到烃B。B的结构简式如图所示。不考虑顺反异构体的情况下,A的可能结构有_______种。
23.由4个碳原子结合形成的5种有机化合物(氢原子没有画出),如图所示。
(1)在如图所示的有机化合物中,碳原子与碳原子之间不仅可以形成碳碳单键,还可以形成____和____;不仅可以形成____,还可以形成碳环。
(2)写出上述五种物质的结构简式和分子式:
a.____;____;
b.___;____;
c.____;____;
d.____;____;
e._____;___。
24.写出下列各烷烃的分子式。
(1)烷烃A在同温同压下蒸气的密度是H2的50倍____。
(2)烷烃B的分子中含有200个氢原子____。
(3)1L烷烃C的蒸气完全燃烧时,生成同温同压下16L的水蒸气____。
(4)分子中含有22个共价键的烷烃D____。
(5)0.1mol烷烃E完全燃烧,消耗标准状况下的O211.2L____。
(6)室温下相对分子质量最大的气态直链烷烃F____。
参考答案:
1.C
【详解】
A.反-2-丁烯与顺-2-丁烯互为顺反异构体,A错误;
B.由图可知,的斜率更大,受温度影响更大,温度变化对的影响程度大于对的影响程度,B错误;
C.图中曲线的斜率代表活化能,正反应的斜率更大,活化能更大,C正确;
D.由C分析可知,正反应的活化能更大,则反应为吸热反应,生成物能量大于反应物能,故反-2-丁烯比顺-2-丁烯稳定,D错误;
故选C。
2.B
【详解】
A.由图示可知:进入的微粒是反应物,出来的微粒是生成物,总反应方程式可用该式表示,A正确;
B.根据图示可知1是中间产物,不是催化剂,B错误;
C.根据2、3、4、5表示的物质微粒可知:其中都含有双氧链-O-O-,因此均具有较强氧化性,C正确;
D.根据图示可知:在4到5的转化过程中有S-O极性键的断裂与形成,也有O-O非极性键的断裂与形成,因此转化关系中有极性键和非极性键的断裂与形成,D正确;
故合理选项是B。
3.B
【详解】
CO2的电子式为:,故答案为:B。
4.D
【详解】
A.制备氨气应选用氯化铵和氢氧化钙固体,只用氯化铵无法制得氨气,A错误;
B.浓盐酸与二氧化锰需要加热才能反应生成氯气,制备装置应选用c,B错误;
C.NO2会和水反应,不能用排水法收集,C错误;
D.乙醇与浓硫酸共热至170℃发生消去反应制取乙烯,所以制备装置选c,乙烯难溶于水,可以用排水法收集,D正确;
综上所述答案为D。
5.A
【详解】
A.结构式是指用一根短线表示一对共用电子对的式子,则N2的结构式为:,A正确;
B.由于碳碳双键两端的甲基分别位于双键平面的两侧,则是反-2-丁烯的球棍模型,B错误;
C.已知CO2是直线形分子,故的空间填充模型为:,C错误;
D.根据洪特规则及特例可知,基态氮原子的轨道表示式为:,D错误;
故答案为:A。
6.B
【详解】
A.分子式为,A错误;
B.二十二碳六烯酸中含有碳碳双键,能使酸性高锰酸钾溶液褪色,B正确;
C.+29O222CO2+16H2O,1molDHA完全燃烧消耗29mol,C错误;
D.1molDHA最多与6mol发生加成反应,因为1mol该物质含有6mol碳碳双键,D错误;
答案选B。
7.B
【详解】
A.结合题目已知信息可知,发生臭氧化反应时,生成CH3CHO和CH3CH2CH2CHO,没有甲醛生成,A错误;
B.结合题目已知信息可知,发生臭氧化反应时,生成HCHO和CH3CH2CH2CHO,有甲醛生成,B正确;
C.结合题目已知信息可知,发生臭氧化反应时,生成CH3CHO和OHCCHO,没有甲醛生成,C错误;
D.结合题目已知信息可知,发生臭氧化反应时,生成CH3CH2CHO,没有甲醛生成,D错误;
答案选B。
8.A
【详解】
烷烃中碳原子数越多,沸点越大,则有沸点:丙烷<丁烷<戊烷,碳原子数相同的烷烃,支链越多,沸点越低,则有沸点:异丁烷<正丁烷,新戊烷<异戊烷<正戊烷,综上分析,沸点由高到低的排列顺序为:正戊烷>异戊烷>新戊烷>正丁烷>异丁烷>丙烷,即③>④>⑤>①>②>⑥,答案选A。
9.C
【详解】
A.HEMA中连接双键的C原子上有相同的原子,故不具有顺反异构,A错误;
B.高聚物A含有酯基可以在碱性条件下水解,1mol高聚物A可以水解出1mol-COOH与1molNaOH反应,B错误;
C.根据结构式可知,NVP分子式为C6H9NO,C正确;
D.HEMA和NVP通过加聚反应生成高聚物A,D错误;
答案选C。
10.D
【详解】
A.二氧化锰和浓盐酸制取氯气需要加热,故不选A;
B.硫酸钙微溶于水,不能用石灰石和稀硫酸制取CO2,故不选B;
C.电石和水反应剧烈,生成微溶于水的氢氧化钙,堵塞多孔隔板,不能用该装置制备乙炔,故不选C;
D.锌和稀硫酸反应生成硫酸锌和氢气,属于固液不加热制备气体,该装置能控制反应的发生和停止,故选D;
选D。
11.A
【详解】
A.氰基丙烯酸乙酯无色透明,有刺激性气味,液态有毒,固化后毒性降低,故A错误;
B.氰基中N原子有孤对电子,可深入蛋白质内部与蛋白质端基的氨基、羧基提供的氢原子形成氢键,故B正确;
C.氰基丙烯酸乙酯存在碳碳双键、碳氮三键等,能发生加聚反应,故C正确;
D.由于N的2p轨道有3个电子,属于半充满,结构稳定很难失去电子,故第一电离能:N>O>C,故D正确;
答案选A。
12.B
【详解】
A.PH3分子中P原子价层电子对个数= 3+=4,所以磷原子采用sp3杂化,空间构型为三角锥形,NCl3中价层电子对个数 =3+=4,所以原子杂化方式是sp3,空间构型为三角锥形,故A正确;
B.CuS与硫酸不反应,故B错误;
C.甲胺和液氨相似,其水溶液显溶碱性,其电离方程式为CH3NH2+H2O +OH-,故C正确;
D.CaC2与水发生反应:CaC2+2H2O=Ca(OH)2+C2H2↑,Mg2C3的结构与CaC2的结构相似,则Mg2C3与水反应的方程式为:Mg2C3+4H2O=2Mg(OH)2+C3H4↑,反应生成丙炔,故D正确;
故选:B。
13.D
【详解】
A. 活化能越低,越易反应,生成①的过程所需活化能较低,速率快,故A正确;
B. 能量越低越稳定,过渡态(Ⅰ)比过渡态(Ⅱ)稳定,故B正确;
C. 碳碳双键不稳定,易发生加成反应,碳碳双键易断裂,能与HBr、H2O等发生加成反应,故C正确;
D. 活化能越低,越易反应,丙烯与HCl发生加成反应,主要生成产物③,故D错误;
故选D。
14.C
【详解】
A.Cl2氧化性强,可以把变价金属氧化为高价态,因此Cl2与Cu点燃产生CuCl2,与Fe反应产生FeCl3,A错误;
B.NaCl是离子化合物,电解熔融NaCl生成Na和Cl2;而AlCl3是共价化合物,在液体时仍然是物质分子,不含自由移动的离子,因此不能通过电解方法冶炼AlCl3生成Al和Cl2,B错误;
C.CO2溶于水反应产生H2CO3,由于酸性:H2CO3>H2SiO3,所以CO2通入Na2SiO3溶液中能发生反应生成H2SiO3,C正确;
D.氮气分子中含有的氮氮三键结合牢固,因而性质稳定,而乙炔分子中含有的碳碳三键结合不牢固,容易发生加成反应、氧化反应,因而性质活泼,D错误;
故合理选项是C。
15.B
【详解】
A.该有机物中含有碳碳双键能使酸性KMnO4溶液退色,A错误;
B.有分析可知Y为C、Z为N、W为S或Cl,可以组成各原子均满足8电子稳定结构的可以是(SCN)2或为CSCl2,B正确;
C.Z为N可以形成NH3为简单气态氢化物,Y为C可以形成CH4,为简单气态氢化物,NH3存在分子间氢键,熔沸点比甲烷的高,但是C还可以形成以苯等许多的烃类,苯就氨的熔沸点高了,C错误;
D.W为S或Cl,Z为N,W最高价氧化物对应水化物的酸性一定Z的最高价氧化物对应水化物的酸性强,H2SO4和HClO4二者酸性大于HNO3,但是H2SO3和HClO的酸性比HNO3的酸性弱,D错误;
故选B。
16.A
【详解】
A.根据选项所给数据,换算CH3COOH为0.1mol,其中氧原子有0.2mol,但选项有文字陷阱,重点在“溶液”,溶剂水也含氧原子,故氧原子总量应大于0.2NA,描述错误,符合题意;
B.Cl-不水解,故其物质的量为3×0.1mol/L×1L=0.3mol,描述正确,不符题意;
C.CaO2和FeO的摩尔质量均为72g/mol,所以72g混合物物质的量为1mol,CaO2中过氧根是一个阴离子,所以混合物中阴离子总数是NA,描述正确,不符题意;
D.CH4与Cl2反应时,Cl2分子中一个氯原子参与生成有机物,另一个氯原子生成HCl分子,当有1molCl2参与反应时,生成HCl为1mol,描述正确,不符题意;
综上,本题选A。
17.(1)碳碳双键、碳氯键
(2) 取代反应 CH2=CH—CH3+Cl2CH2=CH—CH2Cl+HCl
(3)1,3—丁二烯
(4) C7H11Cl 、
(5)6
【分析】
CH2=CH-CH3与氯气发生取代反应生成CH2=CH-CH2Cl;CH2=CH-CH2Cl与C反应生成,则C为CH2=CH-CH=CH2;与反应生成;与氢气发生加成反应生成;再经过一系列反应得到。
(1)
B为CH2=CH-CH2Cl,含有的官能团为:碳碳双键、碳氯键;
(2)
CH2=CH-CH3与氯气发生取代反应生成CH2=CH-CH2Cl,反应的化学方程式为:CH2=CH—CH3+Cl2CH2=CH—CH2Cl+HCl;
(3)
化合物C为CH2=CH-CH=CH2,名称为1,3—丁二烯;
(4)
化合物D为,化学式为C7H11Cl,有碳碳双键,一定条件下与水发生加成反应,产物可能为:或;
(5)
X的分子式为C9H16O,其同分异构体含有六元环结构、六元环上有两个取代基,分别连接在不同碳上、能发生银镜反应,说明有醛基,则可能的取代基为-CH3和-CH2CHO,位于六元环的邻、间、对位共3种,也可能为-CH2CH3和-CHO,位于六元环的邻、间、对位共3种,总共6种同分异构体。
18.(1)碳碳双键、碳氯键
(2) 取代反应
(3)
(4)7
(5) 、
【分析】
A生成B是发生一氯取代,B和C发生加成反应得到D,则C的结构简式为:CH2=CH-CH=CH2,D中碳碳双键和氢气发生加成反应得到E为,E发生取代反应生成F,碳碳三键和1mol H2发生加成反应得到G,G和水发生加成反应得到,再催化氧化得到;
(1)
化合物B中官能团的名称:碳碳双键、碳氯键;
(2)
A生成B的反应类型为取代反应,化学方程式为:;
(3)
化合物A能发生加聚反应,碳碳双键断裂得到高聚物,结构简式为;
(4)
化合物G共有7种不同化学状态的H原子,故化合物G的一氯取代产物共7种;
(5)
化合物D的化学式为,在一定条件下碳碳双键能与发生加成反应,可能产物的结构简式有、。
19.(1)干馏
(2)n
(3)不是
(4)
(5)石油裂解
(6) 羧基 ②③
(7) 5
【分析】
煤经过操干馏可获得出炉煤气、焦炭、煤焦油等产品;丙烯在一定条件下可发生聚合反应制得聚丙烯;同系物结构相似,在分子组成上相差若干个CH2原子团;苯和液溴在催化剂的条件下发生反应生成溴苯和溴化氢;苯和液溴在催化剂作用下发生取代反应生成溴苯,溴苯和氢气发生加成反应生成C,C和NaOH溶液加热发生水解反应生成环己醇,石油裂解得到乙烯,乙烯和水在一定条件下发生加成反应生成乙醇,乙醇在酸性高锰酸钾作用下发生氧化反应生成乙酸,乙酸和环己醇发生酯化反应生成乙酸环己酯。
(1)
将煤隔绝空气加强热可获得出炉煤气、焦炭、煤焦油等产品,操作X的名称是干馏,故答案为:干馏;
(2)
丙烯在一定条件下发生聚合反应制取聚丙烯的化学方程式是:n ;
(3)
焦炭与水蒸气反应生成合成气,进而可制备乙二醇,乙二醇与乙醇结构不相似,不是同系物,故答案为:不是;
(4)
出炉煤气和煤焦油中都含有苯,用苯在铁催化作用下制取溴苯的化学方程式是:;
(5)
反应①是苯和液溴在催化剂作用下发生取代反应,所用试剂是Fe粉、液溴,由石油获得乙烯的生产工艺称为石油裂解;
(6)
F(乙醇)在酸性高锰酸钾作用下发生氧化反应生成G(乙酸),G中官能团名称是羧基,在反应①~④中,①④是取代反应,②③是加成反应,因此原子利用率理论上可达100%的是②③;故答案为:羧基;②③;
(7)
X是E的同系物,其相对分子质量比E大42,则X分子式为C5H10,X可能的结构有,,,,共5种,其中含3个的X结构简式为。
20.(1)C6H12
(2) 42 100.8
(3)
(4)C(CH3)3CH = CH2
(5)(CH3)2C=C(CH3)2
(6)3
【分析】
假设该烃的化学式为CxHy,则根据燃烧通式:CxHy+(x+)O2xCO2+H2O,结合0.2mol烃A在氧气中充分燃烧后,生成化合物B、C各1.2mol,解得:x=6,y=12,故烃A的分子式为C6H12,据此分析解题。
(1)
由分析可知,烃A的化学式为C6H12,故答案为:C6H12;
(2)
根据反应方程式进行计算如下:,解得:m=42g,V=100.8L,故答案为:42;100.8;
(3)
若烃A不能使溴水褪色说明分子中不含有碳碳双键,则A为环烷烃,但在一定条件下能与氯气发生取代反应,其一氯代物只有一种,故A为环己烷,则烃A的结构简式是,故答案为:;
(4)
若烃A能使溴水褪色,说明烃A中含有碳碳双键,在催化剂作用下与H2发生加成反应后生成C(CH3)3CH2CH3,根据碳原子的四价结构可知,A的结构简式为C(CH3)3CH = CH2,故答案为:C(CH3)3CH = CH2;
(5)
若烃A能使溴水褪色,说明烃A中含有碳碳双键,且分子中所有碳原子共平面,故A的结构简式为(CH3)2C=C(CH3)2,故答案为:(CH3)2C=C(CH3)2;
(6)
比A少2个碳原子的A的烯烃的同系物即为丁烯,故其的同分异构体共有1-丁烯、2-丁烯和2-甲基-1-丙烯3种,故答案为:3。
21.(1) 3,3,6-三甲基辛烷 ④②⑤③ 3
(2) 加成反应 碳碳双键、碳氯键 nCH2=CHCl
(3) 4 CH≡CCH(CH3)2
【解析】
(1)
对①编号,系统命名法命名为3,3,6-三甲基辛烷,分子组成相似,相对分子质量越大,熔沸点越高,碳原子数相同时,支链越多,沸点越低,故沸点由高到低的顺序是:④②⑤③;⑥的二氯代物有取代在同一边上、在同一面的对角、在体的对角共3种;
(2)
PVC为聚氯乙烯,逆推可知②为氯乙烯,则乙炔与HCl发生加成反应得到,因此乙炔与①反应的有机反应类型为加成反应,②为CH2=CHCl,官能团名称为碳碳双键、碳氯键,由CH2=CHCl发生加聚反应生成PVC的反应方程式为nCH2=CHCl;
(3)
CH2=C(CH3)CH=CH2与1mol溴水发生加成反应可以得到产物有:、、,与2mol溴水反应得到,共4种产物;3—甲基—1,1,2,2—四溴丁烷结构为,说明加成反应都发生在1和2号碳上,则为碳碳三键,则烃X的结构简式为CH≡CCH(CH3)2。
22.(1) 6
(2)2
(3)6
【解析】
(1)
其同分异构体属于酚类,则含有酚羟基,但不属于酯类也不属于酸类,根据不饱和度可知还含有醛基,醛基的电子式为,根据O原子的数目可知,其同分异构体中含两个酚羟基、一个醛基,若两个酚羟基处于邻位,醛基有2种位置,若酚羟基处于间位,醛基3种位置,若两个酚羟基处于对位,醛基只有一种位置,可能的结构简式有6种;
(2)
烷烃满足的条件:①主链含5个碳原子,则炔烃中主链上也有5个原子,②两个支链:一个甲基、一个乙基,则炔烃中乙基只能位于3号碳上,所以可能的结构有、,共2种;
(3)
当相连的两个碳原子上都至少有一个氢原子时,可以由双键加成得到,根据B的结构简式可知A可能的结构有:、、、、、,共6种。
23.(1) 碳碳双键 碳碳三键 碳链
(2) CH3CH(CH3)CH3 C4H10 C4H8 CH3CH=CHCH3 C4H8 CH≡C—CH2—CH3 C4H6 C4H8
【解析】
(1)
由图示可知,碳原子与碳原子之间不仅可以形成碳碳单键,还可以形成碳碳双键(如图b、c)、碳碳三键(如图d),不仅可以形成碳链(如图a、b、c、d),还可以形成碳环。
(2)
由图示可知,a为烷烃,其结构简式为:CH3CH(CH3)CH3,分子式为:C4H10;b为单烯烃,其结构简式为:,分子式为:C4H8;c为单烯烃,其结构简式为:CH3CH=CHCH3,分子式为:C4H8;d为单炔烃,其结构简式为:CH≡C—CH2—CH3,分子式为:C4H6;e为环烷烃,其结构简式为:,分子式为:C4H8。
24.(1)C7H16
(2)C99H200
(3)C15H32
(4)C7H16
(5)C3H8
(6)C4H10
【分析】
烷烃的通式为CnH2n+2;
(1)
烷烃A在同温同压下蒸气的密度是H2的50倍,则A的相对分子质量为50×2=100,则12n+(2n+2)=10,n=7,化学式为C7H16;
(2)
烷烃B的分子中含有200个氢原子,则2n+2=200,n=99,化学式为C99H200;
(3)
1L烷烃C的蒸气完全燃烧时,生成同温同压下16L的水蒸气,相同条件下气体体积比等于物质的量比,则1个C分子中含有氢原子的数目为16×2=32,则n=15,化学式为C15H32;
(4)
烷烃CnH2n+2中共价键的数目为3n+1,分子中含有22个共价键的烷烃D,则n=7,化学式为C7H16;
(5)
1mol烷烃CnH2n+2完全燃烧消耗O2的物质的量为,0.1mol烷烃E完全燃烧,消耗标准状况下的O211.2L,O2的物质的量11.2L÷22.4L/mol=0.5mol,则1molE完全燃烧消耗O2的物质的量为5mol,,n=3,化学式为C3H8;
(6)
室温下相对分子质量最大的气态直链烷烃F为正丁烷,化学式为C4H10。
一、选择题(共16题)
1.已知反-2-丁烯转化为顺-2-丁烯反应如下,,和随温度变化的曲线如图。下列有关该反应的说法正确的是
A.反-2-丁烯与顺-2-丁烯互为位置异构体
B.温度变化对的影响程度小于对的影响程度
C.正反应的活化能大于逆反应的活化能
D.顺-2-丁烯比反-2-丁烯稳定
2.烯烃不对称环氧化在药物合成中应用广泛,如图为手性酮催化的烯烃不对称环氧化反应的机理图(部分产物未写出):
下列说法不正确的是
A.总反应方程式为OH-+HSO++SO+H2O
B.1是催化剂,反应过程中pH应该控制在合理范围内
C.2、3、4、5均具有较强氧化性
D.4到5的转化过程中有极性键和非极性键的断裂与形成
3.下列化学用语或图示表达不正确的是
A.乙烯的空间填充模型: B.CO2的电子式:
C.HClO的结构式:H-O-Cl D.氯元素的原子结构示意图:
4.实验室制备下列气体所选试剂、制备装置及收集方法均正确的是
气体 试剂 制备装置 收集方法
A NH3 NH4Cl a e
B Cl2 MnO2+浓盐酸 b d
C NO2 Cu+浓HNO3 b f
D CH2=CH2 C2H5OH+浓H2SO4 c f
A.A B.B C.C D.D
5.下列化学用语或图示表达正确的是
A.N2的结构式: B.顺-2-丁烯的球棍模型:
C.的空间填充模型: D.基态氮原子的轨道表示式:
6.DHA(二十二碳六烯酸)俗称脑黄金,是神经系统细胞生长及维持的一种主要成分。下列有关该物质的说法中正确的是
A.分子式为 B.能使酸性高锰酸钾溶液褪色
C.1molDHA完全燃烧消耗26mol D.1molDHA最多与7mol发生加成反应
7.已知烯烃(RCH=CHR')臭氧化反应时C=C键发生断裂,被氧化成RCHO和R'CHO。下列烯烃发生臭氧化反应有甲醛生成的是
A. B.
C. D.
8.①正丁烷;②异丁烷;③正戊烷;④异戊烷;⑤新戊烷;⑥丙烷,物质的沸点由高到低的排列顺序是
A.③>④>⑤>①>②>⑥ B.③>④>⑤>②>①>⑥
C.④>③>⑤>①>②>⑥ D.⑥>③>⑤>①>②>④
9.高聚物A在生物医学上有广泛应用。以N—乙烯基吡咯烷酮(NVP)和甲基丙烯酸β—羟乙酯(HEMA)为原料合成路线如图:
下列说法正确的是
A.HEMA具有顺反异构
B.1mol高聚物A可以与2molNaOH反应
C.NVP分子式为C6H9NO
D.HEMA和NVP通过缩聚反应生成高聚物A
10.用如图所示装置能制备下列干燥的气体,且能控制反应的发生和停止的是(甲、乙、丙表示加入的试剂,部分夹持装置省略)
选项 气体 甲 乙 丙
A Cl2 浓盐酸 二氧化锰 氯化钙
B CO2 稀硫酸 石灰石 五氧化二磷
C C2H2 饱和食盐水 电石 碱石灰
D H2 稀硫酸 锌粒 碱石灰
A.A B.B C.C D.D
11.瞬时胶粘剂“502”主要成分为氰基丙烯酸乙酯,结构简式如图所示。下列说法错误的是
A.氰基丙烯酸乙酯无色、无味、无毒性
B.氰基能深入蛋白质内部与蛋白质端基的氨基、羧基形成氢键
C.氰基丙烯酸乙酯能发生加聚反应
D.第一电离能:
12.下列“类比”结果不正确的是
A.PH3分子的空间构型为三角锥形,则NCl3分子的空间构型也为三角锥形
B.FeS+H2SO4=FeSO4+H2S↑,则CuS+H2SO4 = CuSO4+H2S↑
C.NH3的水溶液显碱性,则甲胺(CH3NH2)的水溶液也显碱性
D.CaC2与水反应生成乙炔,则Mg2C3与水反应生成丙炔
13.已知丙烯与HCl发生加成反应有两种可能,如图1所示;其中丙烯加H+的位能曲线图如图2所示。下列说法错误的是
A.生成①的过程所需活化能较低,速率快
B.过渡态(Ⅰ)比过渡态(Ⅱ)稳定
C.碳碳双键易断裂,能与HBr、H2O等发生加成反应
D.丙烯与HCl发生加成反应,主要生成产物④
14.下列“类比”合理的是
A.Cu在Cl2中燃烧生成CuCl2,则Fe在Cl2中燃烧生成FeCl2
B.电解熔融NaCl生成Na和Cl2,则电解熔融AlCl3生成Al和Cl2
C.根据较强酸可以制取较弱酸的规律,推出CO2通入Na2SiO3溶液中能生成H2SiO3
D.氮气因三键而性质稳定,故乙炔也因三键而性质稳定
15.已知X、Y、Z、W是原子序数依次增大的短周期主族元素,位于三个不同的周期。由X、Y、Z组成的某有机物常用于合成高分子化合物,其结构如下图所示。W原子的最外层电子数比Z多。相关说法正确的是
A.该有机物不能使酸性溶液退色
B.Y、Z、W可以组成各原子均满足8电子稳定结构的某种微粒
C.Z的氢化物熔点一定高于Y的氢化物
D.氧化物对应水化物的酸性:W一定比Z强
16.设为阿伏伽德罗常数的值。下列叙述错误的是
A.10 g 60%的乙酸水溶液中含有的氧原子总数为
B.1 L 溶液中含有的数目为
C.72 g与FeO的混合物中含有的阴离子总数为
D.与在光照条件下反应,当消耗1 mol时,生成HCl的数目为
二、综合题
17.有机物X的合成流程图如图:
已知:
①醛类物质能发生银镜反应
②+
(1)化合物B中官能团的名称____。
(2)A生成B的反应类型为____,A生成B的化学方程式____。
(3)化合物C的名称是____。
(4)化合物D的化学式为____,在一定条件下能与H2O发生加成反应,试写出所有可能产物的结构简式____。
(5)符合下列条件的X的同分异构体有____种。(不考虑立体异构)
a.含有六元环结构
b.六元环上有两个取代基,分别连接在不同碳上
c.能发生银镜反应
18.有机物的合成流程图如下:
(1)化合物B中官能团的名称_______。
(2)A生成B的反应类型为_______,A生成B的化学方程式_______。
(3)化合物A能发生加聚反应合成一种塑料,该塑料的结构简式为_______。
(4)化合物G的一氯取代产物有_______种。(不考虑立体异构)
(5)化合物D的化学式为_______,在一定条件下能与发生加成反应,试写出所有可能产物的结构简式_______。
19.回答下列问题:
I.煤的综合利用,是推进能源革命的重要方向。
请回答下列问题:
(1)煤经过操作X可获得出炉煤气 焦炭 煤焦油等产品,操作X的名称是___________。
(2)出炉煤气中含有丙烯(),医用口罩中对阻挡病毒起关键作用的是熔喷布(主要原料是聚丙烯),由丙烯在一定条件下制取聚丙烯的化学方程式是___________。
(3)焦炭与水蒸气反应生成合成气,进而可制备乙二醇(),乙二醇与乙醇___________(填“是”或“不是”)同系物。
(4)出炉煤气和煤焦油中都含有苯,用苯制取溴苯的化学方程式是___________。
II.乙酸环己酯是一种香料,可用于配制苹果、香蕉等果香型香精。一种制备乙酸环己酯的合成路线如下:
回答下列问题:
(5)由石油获得E的生产工艺称为___________。
(6)G中官能团名称是_______,在反应①~④中,原子利用率理论上可达100%的是_____(填序号)。
(7)X是E的同系物,其相对分子质量比E大42,X可能的结构有_____种,其中含3个的X结构简式为____________。
20.某烃A0.2mol在氧气中充分燃烧后,生成化合物B、C各1.2mol,试回答:
(1)烃A的分子式是___。
(2)若取一定量的烃A充分燃烧后,生成B、C各3mol,则有___g的A参加了反应,燃烧时消耗标准状况下的氧气___L。
(3)若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯代物只有一种,则烃A的结构简式是___。
(4)若烃A能使溴水褪色,在催化剂作用下与H2发生加成反应后生成C(CH3)3CH2CH3,则A的结构简式为__。
(5)若烃A能使溴水褪色,且分子中所有碳原子共平面,则A的结构简式为___。
(6)比A少2个碳原子的A的烯烃的同系物的同分异构体共有___种。
21.Ⅰ.现有下列六种烃:① ② ③乙烷④戊烷⑤ ⑥
(1)用系统命名法命名有机物①____,②③④⑤四种物质按它们的沸点由高到低的顺序排列____(填序号),⑥的二氯代物有____种。
(2)Ⅱ.聚氯乙烯,简称PVC,是一种在建筑材料、工业制品等方面广泛应用的通用塑料,若以乙炔(CH≡CH)为原料合成聚氯乙烯,流程如图。
CH≡CHPVC
乙炔与①反应的有机反应类型为____,②的官能团名称为____。写出由②生成PVC的反应方程式____。
(3)异戊二烯是重要的有机化工原料,其结构简式为CH2=C(CH3)CH=CH2,它与溴水反应最多可以得到____种产物。若烃X与异戊二烯具有相同的分子式,与Br2/CCl4反应后得到3—甲基—1,1,2,2—四溴丁烷,则烃X的结构简式为____。
22.回答下列问题:
(1)邻羟基苯甲酸俗名水杨酸,其结构简式为,水杨酸的同分异构体中有一类物质属于酚类,但不属于酯类也不属于酸类,则它的结构中除了羟基之外,必定还有的官能团的电子式_______,这类物质的结构式共有_______种。
(2)某炔烃与足量的氢气催化加成得到烷烃,且烷烃满足的条件:①主链含5个碳原子②两个支链:一个甲基、一个乙基。则该炔烃可能有_______种结构。
(3)现有一种共轭二烯烃(分子中含有两个相隔一个单键的碳碳双键的烯烃叫共轭二烯烃)A。A与足量H2充分反应后得到烃B。B的结构简式如图所示。不考虑顺反异构体的情况下,A的可能结构有_______种。
23.由4个碳原子结合形成的5种有机化合物(氢原子没有画出),如图所示。
(1)在如图所示的有机化合物中,碳原子与碳原子之间不仅可以形成碳碳单键,还可以形成____和____;不仅可以形成____,还可以形成碳环。
(2)写出上述五种物质的结构简式和分子式:
a.____;____;
b.___;____;
c.____;____;
d.____;____;
e._____;___。
24.写出下列各烷烃的分子式。
(1)烷烃A在同温同压下蒸气的密度是H2的50倍____。
(2)烷烃B的分子中含有200个氢原子____。
(3)1L烷烃C的蒸气完全燃烧时,生成同温同压下16L的水蒸气____。
(4)分子中含有22个共价键的烷烃D____。
(5)0.1mol烷烃E完全燃烧,消耗标准状况下的O211.2L____。
(6)室温下相对分子质量最大的气态直链烷烃F____。
参考答案:
1.C
【详解】
A.反-2-丁烯与顺-2-丁烯互为顺反异构体,A错误;
B.由图可知,的斜率更大,受温度影响更大,温度变化对的影响程度大于对的影响程度,B错误;
C.图中曲线的斜率代表活化能,正反应的斜率更大,活化能更大,C正确;
D.由C分析可知,正反应的活化能更大,则反应为吸热反应,生成物能量大于反应物能,故反-2-丁烯比顺-2-丁烯稳定,D错误;
故选C。
2.B
【详解】
A.由图示可知:进入的微粒是反应物,出来的微粒是生成物,总反应方程式可用该式表示,A正确;
B.根据图示可知1是中间产物,不是催化剂,B错误;
C.根据2、3、4、5表示的物质微粒可知:其中都含有双氧链-O-O-,因此均具有较强氧化性,C正确;
D.根据图示可知:在4到5的转化过程中有S-O极性键的断裂与形成,也有O-O非极性键的断裂与形成,因此转化关系中有极性键和非极性键的断裂与形成,D正确;
故合理选项是B。
3.B
【详解】
CO2的电子式为:,故答案为:B。
4.D
【详解】
A.制备氨气应选用氯化铵和氢氧化钙固体,只用氯化铵无法制得氨气,A错误;
B.浓盐酸与二氧化锰需要加热才能反应生成氯气,制备装置应选用c,B错误;
C.NO2会和水反应,不能用排水法收集,C错误;
D.乙醇与浓硫酸共热至170℃发生消去反应制取乙烯,所以制备装置选c,乙烯难溶于水,可以用排水法收集,D正确;
综上所述答案为D。
5.A
【详解】
A.结构式是指用一根短线表示一对共用电子对的式子,则N2的结构式为:,A正确;
B.由于碳碳双键两端的甲基分别位于双键平面的两侧,则是反-2-丁烯的球棍模型,B错误;
C.已知CO2是直线形分子,故的空间填充模型为:,C错误;
D.根据洪特规则及特例可知,基态氮原子的轨道表示式为:,D错误;
故答案为:A。
6.B
【详解】
A.分子式为,A错误;
B.二十二碳六烯酸中含有碳碳双键,能使酸性高锰酸钾溶液褪色,B正确;
C.+29O222CO2+16H2O,1molDHA完全燃烧消耗29mol,C错误;
D.1molDHA最多与6mol发生加成反应,因为1mol该物质含有6mol碳碳双键,D错误;
答案选B。
7.B
【详解】
A.结合题目已知信息可知,发生臭氧化反应时,生成CH3CHO和CH3CH2CH2CHO,没有甲醛生成,A错误;
B.结合题目已知信息可知,发生臭氧化反应时,生成HCHO和CH3CH2CH2CHO,有甲醛生成,B正确;
C.结合题目已知信息可知,发生臭氧化反应时,生成CH3CHO和OHCCHO,没有甲醛生成,C错误;
D.结合题目已知信息可知,发生臭氧化反应时,生成CH3CH2CHO,没有甲醛生成,D错误;
答案选B。
8.A
【详解】
烷烃中碳原子数越多,沸点越大,则有沸点:丙烷<丁烷<戊烷,碳原子数相同的烷烃,支链越多,沸点越低,则有沸点:异丁烷<正丁烷,新戊烷<异戊烷<正戊烷,综上分析,沸点由高到低的排列顺序为:正戊烷>异戊烷>新戊烷>正丁烷>异丁烷>丙烷,即③>④>⑤>①>②>⑥,答案选A。
9.C
【详解】
A.HEMA中连接双键的C原子上有相同的原子,故不具有顺反异构,A错误;
B.高聚物A含有酯基可以在碱性条件下水解,1mol高聚物A可以水解出1mol-COOH与1molNaOH反应,B错误;
C.根据结构式可知,NVP分子式为C6H9NO,C正确;
D.HEMA和NVP通过加聚反应生成高聚物A,D错误;
答案选C。
10.D
【详解】
A.二氧化锰和浓盐酸制取氯气需要加热,故不选A;
B.硫酸钙微溶于水,不能用石灰石和稀硫酸制取CO2,故不选B;
C.电石和水反应剧烈,生成微溶于水的氢氧化钙,堵塞多孔隔板,不能用该装置制备乙炔,故不选C;
D.锌和稀硫酸反应生成硫酸锌和氢气,属于固液不加热制备气体,该装置能控制反应的发生和停止,故选D;
选D。
11.A
【详解】
A.氰基丙烯酸乙酯无色透明,有刺激性气味,液态有毒,固化后毒性降低,故A错误;
B.氰基中N原子有孤对电子,可深入蛋白质内部与蛋白质端基的氨基、羧基提供的氢原子形成氢键,故B正确;
C.氰基丙烯酸乙酯存在碳碳双键、碳氮三键等,能发生加聚反应,故C正确;
D.由于N的2p轨道有3个电子,属于半充满,结构稳定很难失去电子,故第一电离能:N>O>C,故D正确;
答案选A。
12.B
【详解】
A.PH3分子中P原子价层电子对个数= 3+=4,所以磷原子采用sp3杂化,空间构型为三角锥形,NCl3中价层电子对个数 =3+=4,所以原子杂化方式是sp3,空间构型为三角锥形,故A正确;
B.CuS与硫酸不反应,故B错误;
C.甲胺和液氨相似,其水溶液显溶碱性,其电离方程式为CH3NH2+H2O +OH-,故C正确;
D.CaC2与水发生反应:CaC2+2H2O=Ca(OH)2+C2H2↑,Mg2C3的结构与CaC2的结构相似,则Mg2C3与水反应的方程式为:Mg2C3+4H2O=2Mg(OH)2+C3H4↑,反应生成丙炔,故D正确;
故选:B。
13.D
【详解】
A. 活化能越低,越易反应,生成①的过程所需活化能较低,速率快,故A正确;
B. 能量越低越稳定,过渡态(Ⅰ)比过渡态(Ⅱ)稳定,故B正确;
C. 碳碳双键不稳定,易发生加成反应,碳碳双键易断裂,能与HBr、H2O等发生加成反应,故C正确;
D. 活化能越低,越易反应,丙烯与HCl发生加成反应,主要生成产物③,故D错误;
故选D。
14.C
【详解】
A.Cl2氧化性强,可以把变价金属氧化为高价态,因此Cl2与Cu点燃产生CuCl2,与Fe反应产生FeCl3,A错误;
B.NaCl是离子化合物,电解熔融NaCl生成Na和Cl2;而AlCl3是共价化合物,在液体时仍然是物质分子,不含自由移动的离子,因此不能通过电解方法冶炼AlCl3生成Al和Cl2,B错误;
C.CO2溶于水反应产生H2CO3,由于酸性:H2CO3>H2SiO3,所以CO2通入Na2SiO3溶液中能发生反应生成H2SiO3,C正确;
D.氮气分子中含有的氮氮三键结合牢固,因而性质稳定,而乙炔分子中含有的碳碳三键结合不牢固,容易发生加成反应、氧化反应,因而性质活泼,D错误;
故合理选项是C。
15.B
【详解】
A.该有机物中含有碳碳双键能使酸性KMnO4溶液退色,A错误;
B.有分析可知Y为C、Z为N、W为S或Cl,可以组成各原子均满足8电子稳定结构的可以是(SCN)2或为CSCl2,B正确;
C.Z为N可以形成NH3为简单气态氢化物,Y为C可以形成CH4,为简单气态氢化物,NH3存在分子间氢键,熔沸点比甲烷的高,但是C还可以形成以苯等许多的烃类,苯就氨的熔沸点高了,C错误;
D.W为S或Cl,Z为N,W最高价氧化物对应水化物的酸性一定Z的最高价氧化物对应水化物的酸性强,H2SO4和HClO4二者酸性大于HNO3,但是H2SO3和HClO的酸性比HNO3的酸性弱,D错误;
故选B。
16.A
【详解】
A.根据选项所给数据,换算CH3COOH为0.1mol,其中氧原子有0.2mol,但选项有文字陷阱,重点在“溶液”,溶剂水也含氧原子,故氧原子总量应大于0.2NA,描述错误,符合题意;
B.Cl-不水解,故其物质的量为3×0.1mol/L×1L=0.3mol,描述正确,不符题意;
C.CaO2和FeO的摩尔质量均为72g/mol,所以72g混合物物质的量为1mol,CaO2中过氧根是一个阴离子,所以混合物中阴离子总数是NA,描述正确,不符题意;
D.CH4与Cl2反应时,Cl2分子中一个氯原子参与生成有机物,另一个氯原子生成HCl分子,当有1molCl2参与反应时,生成HCl为1mol,描述正确,不符题意;
综上,本题选A。
17.(1)碳碳双键、碳氯键
(2) 取代反应 CH2=CH—CH3+Cl2CH2=CH—CH2Cl+HCl
(3)1,3—丁二烯
(4) C7H11Cl 、
(5)6
【分析】
CH2=CH-CH3与氯气发生取代反应生成CH2=CH-CH2Cl;CH2=CH-CH2Cl与C反应生成,则C为CH2=CH-CH=CH2;与反应生成;与氢气发生加成反应生成;再经过一系列反应得到。
(1)
B为CH2=CH-CH2Cl,含有的官能团为:碳碳双键、碳氯键;
(2)
CH2=CH-CH3与氯气发生取代反应生成CH2=CH-CH2Cl,反应的化学方程式为:CH2=CH—CH3+Cl2CH2=CH—CH2Cl+HCl;
(3)
化合物C为CH2=CH-CH=CH2,名称为1,3—丁二烯;
(4)
化合物D为,化学式为C7H11Cl,有碳碳双键,一定条件下与水发生加成反应,产物可能为:或;
(5)
X的分子式为C9H16O,其同分异构体含有六元环结构、六元环上有两个取代基,分别连接在不同碳上、能发生银镜反应,说明有醛基,则可能的取代基为-CH3和-CH2CHO,位于六元环的邻、间、对位共3种,也可能为-CH2CH3和-CHO,位于六元环的邻、间、对位共3种,总共6种同分异构体。
18.(1)碳碳双键、碳氯键
(2) 取代反应
(3)
(4)7
(5) 、
【分析】
A生成B是发生一氯取代,B和C发生加成反应得到D,则C的结构简式为:CH2=CH-CH=CH2,D中碳碳双键和氢气发生加成反应得到E为,E发生取代反应生成F,碳碳三键和1mol H2发生加成反应得到G,G和水发生加成反应得到,再催化氧化得到;
(1)
化合物B中官能团的名称:碳碳双键、碳氯键;
(2)
A生成B的反应类型为取代反应,化学方程式为:;
(3)
化合物A能发生加聚反应,碳碳双键断裂得到高聚物,结构简式为;
(4)
化合物G共有7种不同化学状态的H原子,故化合物G的一氯取代产物共7种;
(5)
化合物D的化学式为,在一定条件下碳碳双键能与发生加成反应,可能产物的结构简式有、。
19.(1)干馏
(2)n
(3)不是
(4)
(5)石油裂解
(6) 羧基 ②③
(7) 5
【分析】
煤经过操干馏可获得出炉煤气、焦炭、煤焦油等产品;丙烯在一定条件下可发生聚合反应制得聚丙烯;同系物结构相似,在分子组成上相差若干个CH2原子团;苯和液溴在催化剂的条件下发生反应生成溴苯和溴化氢;苯和液溴在催化剂作用下发生取代反应生成溴苯,溴苯和氢气发生加成反应生成C,C和NaOH溶液加热发生水解反应生成环己醇,石油裂解得到乙烯,乙烯和水在一定条件下发生加成反应生成乙醇,乙醇在酸性高锰酸钾作用下发生氧化反应生成乙酸,乙酸和环己醇发生酯化反应生成乙酸环己酯。
(1)
将煤隔绝空气加强热可获得出炉煤气、焦炭、煤焦油等产品,操作X的名称是干馏,故答案为:干馏;
(2)
丙烯在一定条件下发生聚合反应制取聚丙烯的化学方程式是:n ;
(3)
焦炭与水蒸气反应生成合成气,进而可制备乙二醇,乙二醇与乙醇结构不相似,不是同系物,故答案为:不是;
(4)
出炉煤气和煤焦油中都含有苯,用苯在铁催化作用下制取溴苯的化学方程式是:;
(5)
反应①是苯和液溴在催化剂作用下发生取代反应,所用试剂是Fe粉、液溴,由石油获得乙烯的生产工艺称为石油裂解;
(6)
F(乙醇)在酸性高锰酸钾作用下发生氧化反应生成G(乙酸),G中官能团名称是羧基,在反应①~④中,①④是取代反应,②③是加成反应,因此原子利用率理论上可达100%的是②③;故答案为:羧基;②③;
(7)
X是E的同系物,其相对分子质量比E大42,则X分子式为C5H10,X可能的结构有,,,,共5种,其中含3个的X结构简式为。
20.(1)C6H12
(2) 42 100.8
(3)
(4)C(CH3)3CH = CH2
(5)(CH3)2C=C(CH3)2
(6)3
【分析】
假设该烃的化学式为CxHy,则根据燃烧通式:CxHy+(x+)O2xCO2+H2O,结合0.2mol烃A在氧气中充分燃烧后,生成化合物B、C各1.2mol,解得:x=6,y=12,故烃A的分子式为C6H12,据此分析解题。
(1)
由分析可知,烃A的化学式为C6H12,故答案为:C6H12;
(2)
根据反应方程式进行计算如下:,解得:m=42g,V=100.8L,故答案为:42;100.8;
(3)
若烃A不能使溴水褪色说明分子中不含有碳碳双键,则A为环烷烃,但在一定条件下能与氯气发生取代反应,其一氯代物只有一种,故A为环己烷,则烃A的结构简式是,故答案为:;
(4)
若烃A能使溴水褪色,说明烃A中含有碳碳双键,在催化剂作用下与H2发生加成反应后生成C(CH3)3CH2CH3,根据碳原子的四价结构可知,A的结构简式为C(CH3)3CH = CH2,故答案为:C(CH3)3CH = CH2;
(5)
若烃A能使溴水褪色,说明烃A中含有碳碳双键,且分子中所有碳原子共平面,故A的结构简式为(CH3)2C=C(CH3)2,故答案为:(CH3)2C=C(CH3)2;
(6)
比A少2个碳原子的A的烯烃的同系物即为丁烯,故其的同分异构体共有1-丁烯、2-丁烯和2-甲基-1-丙烯3种,故答案为:3。
21.(1) 3,3,6-三甲基辛烷 ④②⑤③ 3
(2) 加成反应 碳碳双键、碳氯键 nCH2=CHCl
(3) 4 CH≡CCH(CH3)2
【解析】
(1)
对①编号,系统命名法命名为3,3,6-三甲基辛烷,分子组成相似,相对分子质量越大,熔沸点越高,碳原子数相同时,支链越多,沸点越低,故沸点由高到低的顺序是:④②⑤③;⑥的二氯代物有取代在同一边上、在同一面的对角、在体的对角共3种;
(2)
PVC为聚氯乙烯,逆推可知②为氯乙烯,则乙炔与HCl发生加成反应得到,因此乙炔与①反应的有机反应类型为加成反应,②为CH2=CHCl,官能团名称为碳碳双键、碳氯键,由CH2=CHCl发生加聚反应生成PVC的反应方程式为nCH2=CHCl;
(3)
CH2=C(CH3)CH=CH2与1mol溴水发生加成反应可以得到产物有:、、,与2mol溴水反应得到,共4种产物;3—甲基—1,1,2,2—四溴丁烷结构为,说明加成反应都发生在1和2号碳上,则为碳碳三键,则烃X的结构简式为CH≡CCH(CH3)2。
22.(1) 6
(2)2
(3)6
【解析】
(1)
其同分异构体属于酚类,则含有酚羟基,但不属于酯类也不属于酸类,根据不饱和度可知还含有醛基,醛基的电子式为,根据O原子的数目可知,其同分异构体中含两个酚羟基、一个醛基,若两个酚羟基处于邻位,醛基有2种位置,若酚羟基处于间位,醛基3种位置,若两个酚羟基处于对位,醛基只有一种位置,可能的结构简式有6种;
(2)
烷烃满足的条件:①主链含5个碳原子,则炔烃中主链上也有5个原子,②两个支链:一个甲基、一个乙基,则炔烃中乙基只能位于3号碳上,所以可能的结构有、,共2种;
(3)
当相连的两个碳原子上都至少有一个氢原子时,可以由双键加成得到,根据B的结构简式可知A可能的结构有:、、、、、,共6种。
23.(1) 碳碳双键 碳碳三键 碳链
(2) CH3CH(CH3)CH3 C4H10 C4H8 CH3CH=CHCH3 C4H8 CH≡C—CH2—CH3 C4H6 C4H8
【解析】
(1)
由图示可知,碳原子与碳原子之间不仅可以形成碳碳单键,还可以形成碳碳双键(如图b、c)、碳碳三键(如图d),不仅可以形成碳链(如图a、b、c、d),还可以形成碳环。
(2)
由图示可知,a为烷烃,其结构简式为:CH3CH(CH3)CH3,分子式为:C4H10;b为单烯烃,其结构简式为:,分子式为:C4H8;c为单烯烃,其结构简式为:CH3CH=CHCH3,分子式为:C4H8;d为单炔烃,其结构简式为:CH≡C—CH2—CH3,分子式为:C4H6;e为环烷烃,其结构简式为:,分子式为:C4H8。
24.(1)C7H16
(2)C99H200
(3)C15H32
(4)C7H16
(5)C3H8
(6)C4H10
【分析】
烷烃的通式为CnH2n+2;
(1)
烷烃A在同温同压下蒸气的密度是H2的50倍,则A的相对分子质量为50×2=100,则12n+(2n+2)=10,n=7,化学式为C7H16;
(2)
烷烃B的分子中含有200个氢原子,则2n+2=200,n=99,化学式为C99H200;
(3)
1L烷烃C的蒸气完全燃烧时,生成同温同压下16L的水蒸气,相同条件下气体体积比等于物质的量比,则1个C分子中含有氢原子的数目为16×2=32,则n=15,化学式为C15H32;
(4)
烷烃CnH2n+2中共价键的数目为3n+1,分子中含有22个共价键的烷烃D,则n=7,化学式为C7H16;
(5)
1mol烷烃CnH2n+2完全燃烧消耗O2的物质的量为,0.1mol烷烃E完全燃烧,消耗标准状况下的O211.2L,O2的物质的量11.2L÷22.4L/mol=0.5mol,则1molE完全燃烧消耗O2的物质的量为5mol,,n=3,化学式为C3H8;
(6)
室温下相对分子质量最大的气态直链烷烃F为正丁烷,化学式为C4H10。
